艾滋病、梅毒、乙肝实验室检测技术教材
- 格式:docx
- 大小:269.51 KB
- 文档页数:12

艾滋病实验室检测技术课件.一、教学内容本节课将围绕《艾滋病实验室检测技术》展开教学,具体内容包括教材第十二章第二节,详细讨论艾滋病病毒的检测方法、实验原理、操作步骤以及结果判读等。
二、教学目标1. 让学生掌握艾滋病病毒的实验室检测方法,了解各种检测技术的优缺点。
2. 培养学生独立进行实验室检测操作的能力,提高实验结果的准确性。
3. 使学生认识到艾滋病检测在防控艾滋病传播中的重要性,增强社会责任感。
三、教学难点与重点教学难点:艾滋病病毒实验室检测技术的操作步骤和结果判读。
教学重点:艾滋病病毒的实验室检测方法及其优缺点。
四、教具与学具准备1. 教具:PPT课件、实验室检测设备、试剂等。
2. 学具:实验报告册、笔、计算器等。
五、教学过程1. 实践情景引入通过展示一组艾滋病病毒感染者的数据,让学生思考如何准确检测艾滋病病毒,引出本节课的教学内容。
2. 理论知识讲解(1)介绍艾滋病病毒的生物学特性,让学生了解病毒检测的必要性。
(2)讲解艾滋病病毒实验室检测的主要方法,包括抗体检测、抗原检测、核酸检测等。
(3)分析各种检测技术的优缺点,指导学生根据实际情况选择合适的检测方法。
3. 例题讲解以一道实验室检测艾滋病病毒的题目为例,讲解操作步骤和结果判读。
4. 随堂练习让学生独立完成一道实验室检测题目,巩固所学知识。
5. 实验操作演示现场演示实验室检测操作步骤,让学生直观地了解实验过程。
6. 结果判读与分析指导学生如何判读实验结果,分析实验数据,得出结论。
六、板书设计1. 艾滋病实验室检测技术2. 内容:(1)艾滋病病毒检测方法(2)实验室检测操作步骤(3)结果判读与分析七、作业设计1. 作业题目:(1)简述艾滋病病毒实验室检测的主要方法。
(2)操作步骤:以抗体检测为例,描述实验室检测艾滋病病毒的具体操作步骤。
2. 答案:(1)艾滋病病毒实验室检测主要方法有抗体检测、抗原检测、核酸检测等。
(2)操作步骤:①采集样本。

实验室艾滋、梅毒和乙肝相应项目的标准化操作程序实验室是进行各类病原微生物检测的重要场所,包括艾滋病、梅毒和乙肝等项目的标准化操作程序也是实验室工作的核心。
标准化操作程序的制定,旨在确保实验室工作的准确性、可靠性和连续性,最大程度地减少误差和风险。
下面将详细介绍实验室艾滋病、梅毒和乙肝项目的标准化操作程序。
一、艾滋病检测项目的标准化操作程序:1.标本采集:按照规定的采样方法采集血液标本,包括静脉血和采血盒采集的血液。
2.样本处理:收到标本后,首先检查样本标签和申请单上的信息是否一致,然后进行样本分装和保存,确保样本的完整性和稳定性。
3.样本检测:使用艾滋病抗体检测试剂盒进行检测。
按照检测试剂的说明书,将样本和试剂按照比例混合并孵育一定时间,然后进行洗涤和显色。
4.结果判断:根据试剂盒的说明书,根据显色反应的强度和比色卡提供的判断标准,判断样本阴阳性。
5.结果记录和报告:将检测结果记录在检验记录中,并生成相应的实验报告,确保结果能够及时准确地传达给临床医生。
二、梅毒检测项目的标准化操作程序:1.标本采集:按照规定的采样方法采集血液标本,包括静脉血和采血盒采集的血液。
2.样本处理:收到标本后,首先检查样本标签和申请单上的信息是否一致,然后进行样本分装和保存,确保样本的完整性和稳定性。
3.样本检测:使用梅毒抗体检测试剂盒进行检测。
按照检测试剂的说明书,将样本和试剂按照比例混合并孵育一定时间,然后进行洗涤和显色。
4.结果判断:根据试剂盒的说明书,根据显色反应的强度和比色卡提供的判断标准,判断样本阴阳性。
5.结果记录和报告:将检测结果记录在检验记录中,并生成相应的实验报告,确保结果能够及时准确地传达给临床医生。
三、乙肝检测项目的标准化操作程序:1.标本采集:按照规定的采样方法采集血液标本,包括静脉血和采血盒采集的血液。
2.样本处理:收到标本后,首先检查样本标签和申请单上的信息是否一致,然后进行样本分装和保存,确保样本的完整性和稳定性。

2024年梅毒患者梅毒检测课件一、教学内容本节课内容选自《医学检验技术》第十章第一节“梅毒的实验室检测”,详细内容包括梅毒病原学、传播途径、临床表现、实验室检测方法及梅毒检测的注意事项。
二、教学目标1. 掌握梅毒病原学、传播途径和临床表现。
2. 熟悉梅毒实验室检测方法及操作步骤。
3. 了解梅毒检测的注意事项,提高实验操作安全意识。
三、教学难点与重点难点:梅毒实验室检测方法及操作步骤。
重点:梅毒病原学、传播途径、临床表现和实验室检测注意事项。
四、教具与学具准备1. 教具:梅毒病原体模型、PPT课件、实验操作视频。
2. 学具:实验手册、实验器材(梅毒检测试剂盒、手套、口罩等)。
五、教学过程1. 导入:通过一个实践情景,引入梅毒检测的重要性。
情景:2024年,某地发现一名梅毒患者,需要对其进行梅毒检测。
2. 新课内容讲解:a) 梅毒病原学、传播途径和临床表现b) 梅毒实验室检测方法(如:暗视野显微镜检查、免疫印迹法等)c) 梅毒检测的注意事项3. 例题讲解:讲解一道梅毒检测的例题,分析解题思路。
4. 随堂练习:让学生进行梅毒检测方法的操作练习。
六、板书设计1. 梅毒病原学、传播途径、临床表现2. 梅毒实验室检测方法暗视野显微镜检查免疫印迹法3. 梅毒检测注意事项七、作业设计1. 作业题目:某患者疑似梅毒感染,请根据所学知识,为其设计一套梅毒检测方案。
答案:梅毒检测方案:(1)暗视野显微镜检查:取患者皮损处分泌物,进行暗视野显微镜检查,观察梅毒螺旋体。
(2)免疫印迹法:取患者血清,进行免疫印迹法检测,观察梅毒特异性抗体。
2. 课后反思及拓展延伸1. 梅毒检测中,如何避免假阳性和假阴性的发生?2. 除了实验室检测,还有哪些方法可以辅助诊断梅毒?3. 针对梅毒患者,如何进行有效治疗和预防?通过本节课的学习,希望学生能够掌握梅毒检测的基本知识,提高实验操作技能,为未来的医学检验工作打下坚实基础。
重点和难点解析1. 梅毒实验室检测方法及操作步骤2. 梅毒检测注意事项3. 作业设计中的梅毒检测方案一、梅毒实验室检测方法及操作步骤1. 暗视野显微镜检查:此方法主要用于检测梅毒早期感染。

2024年梅毒实验室检测技术课件一、教学内容本节课我们将学习2024年梅毒实验室检测技术,内容涉及《临床微生物学》教材第十二章第二节:梅毒病原学及其实验室诊断方法。
详细内容包括梅毒螺旋体的生物学特性、梅毒的传播途径、实验室检测技术的原理、操作步骤以及结果判读。
二、教学目标1. 掌握梅毒螺旋体的生物学特性和传播途径。
2. 了解梅毒实验室检测技术的种类、原理及操作步骤。
3. 能够正确判读梅毒实验室检测结果,并给出合理的诊断建议。
三、教学难点与重点难点:梅毒实验室检测技术的操作步骤及结果判读。
重点:梅毒螺旋体的生物学特性、传播途径以及实验室检测技术的种类和原理。
四、教具与学具准备1. 教具:多媒体教学设备、PPT课件、梅毒实验室检测操作视频。
2. 学具:笔记本、教材、笔。
五、教学过程1. 导入:通过展示梅毒病例,引起学生对梅毒实验室检测技术的重视。
2. 理论讲解:1) 梅毒螺旋体的生物学特性和传播途径。
2) 梅毒实验室检测技术的种类、原理及操作步骤。
3. 实践操作演示:播放梅毒实验室检测操作视频,让学生了解实际操作过程。
4. 例题讲解:讲解梅毒实验室检测结果判读的实例,让学生掌握判读方法。
5. 随堂练习:发放梅毒实验室检测结果判读练习题,让学生巩固所学知识。
六、板书设计1. 梅毒螺旋体的生物学特性和传播途径。
2. 梅毒实验室检测技术的种类、原理及操作步骤。
3. 梅毒实验室检测结果判读方法。
七、作业设计1. 作业题目:1) 请简述梅毒螺旋体的生物学特性和传播途径。
2) 请列举三种梅毒实验室检测技术,并简要说明其原理。
病例1:TPHA(+)、RPR(+)、VDRL(+)病例2:TPHA()、RPR(+)、VDRL(+)4) 请谈谈你对梅毒实验室检测技术的认识。
2. 答案:1) 梅毒螺旋体是一种革兰氏阴性细菌,主要通过性接触、母婴传播等途径传播。
2) 三种梅毒实验室检测技术:TPHA(梅毒螺旋体血凝试验)、RPR(快速血浆反应素试验)、VDRL(性病研究实验室试验)。




艾梅乙的临床实验室检查一、艾滋病艾滋病的诊断必须根据流行病学接触史、临床表现和实验室检查结果,综合分析。
无论处于哪一期的HIV感染,都必须要有抗HIV抗体阳性或HIV抗原阳性的实验室诊断为依据。
HIV的实验室检测方法包括:抗体检测、抗原检测、病毒分离培养、病毒核酸检测、病毒载量检测。
我国现阶段HIV实验室检测主要为HIV抗体检测,HIV抗体检测需要通过初筛和确认实验。
HIV初筛试验可以选择酶联免疫吸附试验(ELISA)、明胶颗粒凝集实验(PA)、免疫荧光法(IF)、免疫酶法(IE)、乳胶凝集实验(LA),还有临床普遍应用的快速诊断试剂。
初筛实验结果阳性后在做确认实验。
常用的确认实验为免疫印迹法。
确认试验阳性才能确定为HIV感染。
1、初筛试验由于系统性红斑狼疮和风湿病者体内的自身抗体和HIV-1型的某些抗原决定簇有交叉反应性,不同厂家及同一厂家不同批次试剂的敏感性和特异性村存在一定差异,故初筛试验呈阳性。
对初筛呈阳性反应的样品用原有试剂和另外一种不同原理或不同厂家的筛查试剂重复检测,如两种试剂复测均呈阴性反应,则报告HIV抗体阴性;如均呈阳性反应,或一阴一阳,需送艾滋病确认实验室进行确认(1)胶体金(或胶体硒)快速试验:以硝酸纤维膜为载体,区别在于不用酶标记抗体,而代之以红色的胶体金(或胶体硒)A蛋白,用渗滤法作为洗涤方法。
试剂稳定,可室温长期保存。
试验时不需任何设备,迅速、简便、特异性较好,敏感性约相当于中度敏感的ELISA,适用于应急检测、门诊急诊个体检测。
一般可在10~30min内判读结果。
(2)是酶联免疫试验(ELISA):目前国内外主要使用第三代(双抗原夹心法)试剂,少数使用第二代试剂。
血源筛查仍以第三代ELISA为主,国际上有些国家和地区已将线性免疫酶测定(第四代ELISA试剂)用于血源筛查。
第四代ELISA试剂是最近发展起来的HIV 抗原抗体联合测定试剂,可同时检测P24抗原和抗HIV-1/2抗体。


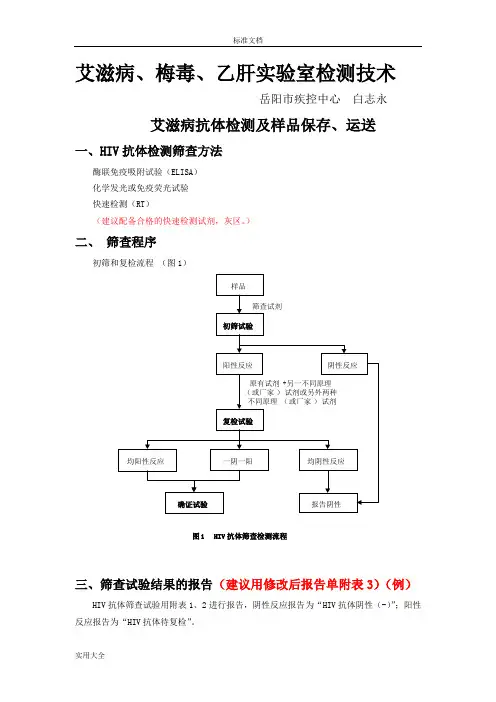
艾滋病、梅毒、乙肝实验室检测技术岳阳市疾控中心白志永艾滋病抗体检测及样品保存、运送一、HIV抗体检测筛查方法酶联免疫吸附试验(ELISA)化学发光或免疫荧光试验快速检测(RT)(建议配备合格的快速检测试剂,灰区。
)二、筛查程序初筛和复检流程(图1)图1 HIV抗体筛查检测流程三、筛查试验结果的报告(建议用修改后报告单附表3)(例)HIV抗体筛查试验用附表1、2进行报告,阴性反应报告为“HIV抗体阴性(-)”;阳性反应报告为“HIV抗体待复检”。
四、 HIV感染产妇所生儿童HIV抗体检测策略及流程1、适用范围HIV感染产妇所生婴幼儿;已满18个月的婴幼儿,其母亲HIV感染状态不详,儿童出现H IV相关临床表现,临床怀疑HIV感染的儿童。
2、检测程序图4 艾滋病感染产妇所生儿童HIV抗体检测流程五、样品的保存、运送1、样品的保存用于抗体和抗原检测的血清或血浆样品,短期(1周)内进行检测的可存放于2~8℃,一周以上应存放于-20℃以下。
2、样品的运送(例)(1)应符合生物安全要求;(2)应采用三层容器对样品进行包装。
第一层容器:直接装样品,应防渗漏。
样品应置于带盖的试管内。
在试管的周围应垫有缓冲吸水材料,以免碰碎。
第二层容器:容纳并保护第一层容器,可以装若干个第一层容器。
要求不易破碎、带盖、防渗漏、容器的材料要易于消毒处理。
第三层容器:容纳并保护第二层容器的运输用外层包装箱。
外面要贴上醒目的标签、联系方式,还应易于消毒。
(3) 用于抗体检测的血清和血浆样品应在冻存条件下运送。
质量控制一、艾滋病抗体检测的统计学室内质量控制1、试剂盒内部对照即试剂盒提供的阳性和阴性对照血清。
用于判断实验的有效性,不能作为室内质控品使用,内部对照结果无效,必须重新试验。
2、室内质控品为非试剂盒组份的外部质控品,是为了监控检测的重复性而设置的,包括强阳性、弱阳性和阴性质控血清。
也可以只设置一个弱阳性质控,以该试剂盒临界值(Cut-off)的2~3倍为宜。
2024年《梅毒检测》课件一、教学内容本节课我们将学习2024年版《梅毒检测》教材的第五章“实验室诊断技术”,具体内容包括梅毒病原体的生物学特性、实验室检测方法、结果判读及其临床意义。
二、教学目标1. 了解梅毒病原体的基本生物学特性,掌握梅毒的实验室检测方法。
2. 能够正确解读梅毒检测报告,并分析其与临床的关系。
3. 培养学生的实验室操作技能和生物安全意识。
三、教学难点与重点难点:梅毒检测方法的原理及其操作步骤。
重点:快速血浆反应素试验(RPR)和梅毒螺旋体颗粒凝集试验(TPPA)的原理与操作。
四、教具与学具准备1. 教具:梅毒检测教学PPT、实验操作视频、检测仪器和试剂。
2. 学具:实验服、手套、口罩、显微镜、试管、滴管等。
五、教学过程1. 实践情景引入(5分钟)通过展示梅毒病例,引发学生对梅毒检测的兴趣。
2. 理论讲解(10分钟)介绍梅毒病原体的生物学特性。
讲解梅毒实验室检测方法,如RPR和TPPA。
3. 例题讲解(10分钟)通过例题,讲解如何解读梅毒检测报告。
4. 随堂练习(10分钟)学生分组讨论,分析梅毒检测报告案例。
5. 实验操作演示与练习(15分钟)播放实验操作视频,教师示范操作步骤。
学生分组进行实验操作练习。
六、板书设计1. 梅毒病原体生物学特性2. 梅毒实验室检测方法RPRTPPA3. 检测报告解读七、作业设计1. 作业题目:描述RPR和TPPA的原理和操作步骤。
解读给定梅毒检测报告,分析其临床意义。
2. 答案:RPR和TPPA的原理和操作步骤描述。
梅毒检测报告解读及临床意义分析。
八、课后反思及拓展延伸1. 课后反思:关注学生的学习情况,及时给予指导和反馈。
2. 拓展延伸:探讨梅毒检测新技术的发展趋势。
研究梅毒检测在我国的防控策略和实施情况。
重点和难点解析1. 梅毒实验室检测方法的原理及其操作步骤。
2. 实验操作演示与练习过程中的安全注意事项。
3. 检测报告的解读及临床意义分析。
艾滋病、梅毒、乙肝实验室检测技术岳阳市疾控中心白志永艾滋病抗体检测及样品保存、运送一、HIV抗体检测筛查方法酶联免疫吸附试验(ELISA)化学发光或免疫荧光试验快速检测(RT)(建议配备合格的快速检测试剂,灰区。
)二、筛查程序初筛和复检流程(图1)样品筛查试剂初筛试验阳性反应阴性反应原有试剂+另一不同原理(或厂家)试剂或另外两种不同原理(或厂家)试剂复检试验均阳性反应一阴一阳均阴性反应确证试验报告阴性图1 HIV抗体筛查检测流程三、筛查试验结果的报告(建议用修改后报告单附表3)(例)HIV抗体筛查试验用附表1、2进行报告,阴性反应报告为“HIV抗体阴性(-)”;阳性反应报告为“HIV抗体待复检”。
四、 HIV感染产妇所生儿童HIV抗体检测策略及流程1、适用范围HIV感染产妇所生婴幼儿;已满18个月的婴幼儿,其母亲HIV感染状态不详,儿童出现H IV相关临床表现,临床怀疑HIV感染的儿童。
2、检测程序图4 艾滋病感染产妇所生儿童HIV抗体检测流程五、样品的保存、运送1、样品的保存用于抗体和抗原检测的血清或血浆样品,短期(1周)内进行检测的可存放于2~8℃,一周以上应存放于-20℃以下。
2、样品的运送(例)(1)应符合生物安全要求;(2)应采用三层容器对样品进行包装。
第一层容器:直接装样品,应防渗漏。
样品应置于带盖的试管内。
在试管的周围应垫有缓冲吸水材料,以免碰碎。
第二层容器:容纳并保护第一层容器,可以装若干个第一层容器。
要求不易破碎、带盖、防渗漏、容器的材料要易于消毒处理。
第三层容器:容纳并保护第二层容器的运输用外层包装箱。
外面要贴上醒目的标签、联系方式,还应易于消毒。
(3) 用于抗体检测的血清和血浆样品应在冻存条件下运送。
质量控制一、艾滋病抗体检测的统计学室内质量控制1、试剂盒内部对照即试剂盒提供的阳性和阴性对照血清。
用于判断实验的有效性,不能作为室内质控品使用,内部对照结果无效,必须重新试验。
2、室内质控品为非试剂盒组份的外部质控品,是为了监控检测的重复性而设置的,包括强阳性、弱阳性和阴性质控血清。
也可以只设置一个弱阳性质控,以该试剂盒临界值(Cut-off)的2~3倍为宜。
作用:判断该批临床样品检测的有效性,每次实验必须包含室内质控品,其结果无效,必须重新试验。
二、 统计室内质控的主要表示方法—建立质控图最常用的质控图是Levey-Jennings 利维詹宁斯质控图,下面以ELISA 方法检测HIV 抗体为例,描述建立质控图步骤:1、建立质控图参数一般采用在不同批次检测取得至少20个数据,以建立一个临时性的均值和标准差a 、算术平均值():Σx= ── nb 、标准差(s ):是描述样品与均数之间离散程度的一个指标s 计算公式为:─────── ∑( x n - )2s = ─────── n-1c 、变异系数(cv ):scv = ──- × 100 %2、绘制质控图(a )在常规条件下,对同一批血清连续测定20次(天)或以上,获得一组S/CO 值,求均数()和标准差(s ), 超出2s 或3s 的数据不应删除。
(b )将均值()和标准差(s )分别在质控框架图中标示出来。
以S/CO 值作纵座标(Y 轴),每一批次试验作横座标(x 轴),绘制质控图。
(c )从第21次起,将每次质控血清的检测结果依次点入该质控框架图中,检验进入质控状态。
x x x xx x3、质控规则及其使用质控规则的使用应检出随机误差和系统误差,目前有许多质控规则,常用的是12S 和13S规则。
(a )告警(12S ):当外部质控品的S/CO 值超出+2s 范围时,系统处于告警状态,应予注意,是否可以继续检测需要进一步观察。
若将12S 做失控标准,有较高的假失控概率,所以一般不采用。
(b )失控(13S ):当外部质控品的S/CO 值超出+3s 范围时,系统处于失控状态,本次实验结果不能被接受,可能是系统误差、随机误差或外部质控品 稳定性下降所致。
(c )漂移:连续几次(3~5次)外部质控品的S/CO 值都落在均值的一侧则称为漂移,提示实验条件发生了较大的变化。
(d )趋势:连续几次(5~7次)外部质控品的S/CO 值几乎按一个方向分布时称为趋势,通常由参数的缓慢改变引起。
艾滋病实验室生物安全一、HIV 的生物危害第一类、第二类病原微生物统称为高致病性病原微生物。
人类免疫缺陷病毒(HIV )属第二类病原微生物,是高致病性病原微生物。
二、HIV 相关检测的生物安全级别HIV 抗体检测应在符合Ⅱ级生物安全实验室(BSL-2)要求的艾滋病检测实验室中进行。
三、生物安全保证措施1、建立安全制度艾滋病检测实验室应建立下列安全制度(1) 实验室的安全工作制度或安全标准操作程序(S-SOP )。
(2) 意外事故处理预案,主要是生物安全意外事故。
(3) 信息安全及保密制度:(例) 2、培训和管理 3、个人保健和防护 4、安全操作5、实验室的清洁和消毒工作完毕应对工作台面消毒,推荐用0.1~0.2%的次氯酸溶液消毒;用消毒液清洗后要干燥20min 以上;操作过程中如有样品、检测试剂外溅,应及时消毒。
如有大量高浓度的传染性液体溅出,在清洁之前应先用1%的次氯酸钠溶液浸泡,然后戴上手套擦净。
离心样品时要使用密闭的罐和密封头,防止离心时液体溢出或在超/高速离心时形成气溶胶。
x x四、污染物处理1、艾滋病实验室产生的所有废弃物,包括不再需要的样品、培养物和其它物品,均应视为感染性废弃物,应置于专用的密封防漏容器中,安全运至消毒室,经高压消毒后再进行处理或废弃。
2、艾滋病检测实验室常用的消毒方法(1 )物理消毒方法a 高压蒸汽消毒,121℃,保持15~20min;b 干燥空气烘箱消毒(干烤消毒),140℃,保持2~3h。
(2)化学消毒方法含氯消毒剂(次氯酸钠,含有效氯2000~5000mg/L)、75%乙醇、2%戊二醛(3)艾滋病检测实验室物品常用的消毒方法a、废弃物缸:5000mg/L 次氯酸钠。
b、生物安全柜工作台面和仪器表面:75%乙醇。
c、溢出物:5000mg/L次氯酸钠。
d、污染的台面和器具:2000mg/L 次氯酸钠,也可以用过氧化氢或过氧乙酸。
器械可用2%戊二醛消毒。
艾滋病检测实验室质量管理一、范围艾滋病检测实验室质量管理包括质量保证、质量控制和质量评价二、质量保证1、人员培训检测技术人员需经过上岗培训和在岗持续培训。
筛查实验室技术人员至少每2年1次。
2、环境条件艾滋病抗体筛查实验室的设置及其建筑、设施、设备必须符合《全国艾滋病检测工作管理办法》的要求。
HCV,HBV及梅毒等血清学检测在满足实验室管理要求和保证生物安全的条件下,可以与HIV检测共享空间和设备,应避免交叉污染。
3、样品采集、运送和处理4、检测方法和试剂的选择5、设备维护与校准6、实验耗材7、文件和文件管理8、标准操作程序(SOP)筛查实验室SOP文件包括:(1)样品的接收、登记、处理、保存和运输;(2)检测方法和步骤;(3)试剂使用和保存;(4)仪器的使用维护和校准;(5)质量控制要求及程序;(6)结果解释与报告;(7)保密程序;(8)实验室数据、相关文件记录与保存;(9)不确定样品追踪和处理;(10)实验室安全防护及实验室的清理和消毒;(11)标题和编号;(12)编写和修订日期;(13)编写和修订人员姓名;(14)方法、目的和应用范围;(15)检测设备;(16)试剂及有效期;(17)安全防护相关步骤;(18)结果的解释和报告;(19)附录,包括相关的附加文件如标准表格、设备和试剂盒说明书等。
9 、实验原始记录表(附表4)10、结果报告11、样品登记和保存三、质量控制四、质量评价包括内部质量评价和外部质量评价。
1、内部质量评价2、外部质量评价筛查实验室应参加省级职能工作考核和PT。
3、职能工作考核现场评价内容,筛查实验室现场评价应包括:实验室人员组成及其职责分工;实验室分区、布局、恒温设施;仪器设备及其使用、校准记录;质量保证文件、实验室SOP文件及原始记录;实验室的安全防护措施,安全用品及安全规程;消毒与污物处理方法及设施;HIV检测资料数据库的建设、存档、备份、安全和保密;样品保存和安全;开展的HIV检测项目和检测试剂等。
梅毒、乙肝检测要点一、梅毒螺旋体感染人体后出现两种抗体,特异体抗体和非特异性抗体。
特异性抗体(TPHA):为lgM,这种抗体一旦产生,终身是阳性。
灵敏度高、特异性强非特异性抗体(反应素 RPR):为lgA与lgM的混合物,随病情发展而变化。
可与正常生物组织中的类脂抗原发生非特异性结合。
二、梅毒特异性抗体检测:用于证实试验,即使患者已经经过充分的治疗,IgG抗体仍保持阳性所以不能用以观察疗效、复发及再感染。
方法有:TP-ELISA酶联免疫法、TPPA。
梅毒非特异性抗体检测:用于梅毒诊断疗效观察和对复发或再感染的监测。
方法有:性病实验室试验(又称VDRL试验)、快速血浆反应素(RPR)试验、梅毒甲苯胺红不加热血清试验(TRUST)、世界卫生组织推荐用RPR等方法进行过筛试验,出现阳性者再用TPHA等方法进行确认试验。
三、梅毒滴度测定使用仪器:水平旋转仪转速:100转/min 室温四、乙肝定性:检测方法同艾滋病筛查。
五、乙肝定量:乙肝病毒DNA检测特点:灵敏度高、易出现假阳性、数据波动大要点:合理分区、防止污染。
附表1HIV抗体筛查报告REPORT OF HIV ANTIBODY SCREENING TESTING秘密编号:PRINTED BY CHINESE CENTER FORDISEASE CONTROL AND PREVENTION 中国疾病预防控制中心制订附表2HIV抗体复检检测单秘密编号中国疾病预防控制中心制订附表3HIV抗体复检检测单样品受理号:编号:岳阳市疾病预防控制中心YYCDC附表4ELISA法原始记录(HIV抗体检测)样品数量:标本类型:血清使用试剂:HIV 1/2 生产厂家:有效期:批号:检测项目:HIV抗体检测检测依据:《全国艾滋病检测技术规范》2009版使用设备:酶标仪编号0304037 洗板机编号0304047培养箱编号0304046 生物安全柜编号0304049移液器实验条件:孵育温度:37℃测量波长:450nm 参考波长:620nm试剂配制:洗涤液500 ml,其他:操作步骤:见试剂说明书。
1 2 3 4 5 6 7 8 9 10 11 12结果见酶标仪读数打印纸。
结果分析:共份呈阳性反应,需要(复检□,确认□);其余均为阴性反应。
检验日期:年月日检验者:复核者:。