高一化学必修一钠及其化合物的习题
- 格式:doc
- 大小:224.50 KB
- 文档页数:7

《钠及其化合物》测试题及参考答案1、下列关于钠的说法不正确的是()A、金属钠与氧气反应,条件不同产物不同B、金属钠着火可用水扑灭C、少量的钠可保存在煤油中D、钠的化学性质活泼,可从CuSO4溶液中置换出Cu2、将一小块金属钠放在石棉网上加热燃烧,下列实验现象描述正确的是()①金属钠先熔化②在空气中燃烧,产生黄色火花③燃烧后生成白色固体④燃烧火焰为黄色⑤燃烧后生成淡黄色粉末状物质A、①②B、①②③C、①④D、①④⑤3、金属钠长期放置于空气中,最后应变为()A、Na2O B Na2O2 C NaOH D Na2CO34、为维持人体内电解平衡,人在大量出汗后应及时补充的离子是()A. Mg2+B. Ca2+C. Na+D. Fe3+5、下列关于金属钠的叙述中,说法正确的是()A、金属钠可以保存在少量水中B、钠在空气中燃烧,产物是Na2OC、钠是银白色金属,硬度大,熔点高D、.Na、K合金可作原子反应堆的导热剂6、下列金属单质中,能从CuSO4溶液中置换出铜的是()A、汞B、银C、钠D、铁7、下列实验操作正确的是()A、向盛水的烧杯中投入黄豆粒大小的钠块,观察现象B、将钠保存在汽油中C、将一小块钠放在石棉网上加热,观察现象D、用手掰开一块金属钠,观察钠的颜色。
8、将少量金属钠放入盛有CuSO4溶液的烧杯中,剧烈反应,有蓝色沉淀及无色气体产生。
则烧杯中发生的反应是( )①2Na+CuSO4====Na2SO4+Cu;②Cu+2H2O====Cu(OH)2↓+H2↑;③2Na+H2O====2NaOH+H2↑;④2NaOH+CuSO4====Cu(OH)2↓+Na2SO4A. ①B. ①②C. ③④D. ①③9、将金属钠投入到硫酸铜溶液中,产物是()A.NaOH和H2 B.Cu(OH)2、Na2SO4、 H2C.Cu和 Na2SO4 D.H2SO4、 Cu(OH)2、、 Na2SO410、下列六种物质:①Na2O ②Na2O2③NaCl ④Na2CO3溶液⑤NaOH ⑥NaHCO3,其中不能与CO2反应的是 ( )A.①④B.②③C.③⑥D.⑤⑥11、下列各组中的两种物质作用时,反应条件(温度、反应物用量)改变,不会引起产物种类改变的是 ( )A. Na和O2B. NaOH和CO2C. Na2O2和CO2D. C和O212、在实验探究活动中,下列属于实验报告内容的是()①实验目的②仪器和试剂③实验现象④结论及解释⑤实验步骤A、①②③B、②③⑤C、①③④D、全部13、金属钠着火,能用来灭火的是()A、水B、湿抹布C、泡沫灭火器D、干沙14、将2.3克钠放入100克水中,生成的溶液中溶质的质量分数为( )A、等于2.3%B、等于4%C、大于2.3%小于4%D、大于4%15、查阅资料发现,金属钠不仅能与氧气和水反应,还能与多种其他物质发生反应,其中包括与酒精在常温下反应。

2.1钠及其化合物(同步练习)一、单选题1.关于钠元素的单质及其化合物的叙述不正确的是()A.钠为银白色,质软,熔点相对较低,密度比水小B.大量的钠着火时可以用沙土扑灭,少量的钠应保存在煤油中C.金属钠在空气中长期放置,最终变为碳酸钠D.取一块金属钠放在燃烧匙里加热,观察到金属钠熔化,燃烧后得到白色固体2.2019年诺贝尔化学奖颁给几位在锂离子电池研发领域做出贡献的科学家,锂单质化学性质与钠类似,活泼性比钠略差。
它的密度为0.534g/cm3,锂元素的焰色为紫红色,将绿豆大的锂投入水中,下列实验现象合理的有()①锂沉入水中②锂浮在水面上③水中不会有大量气泡④反应后在水中加入几滴石蕊试液,溶液变红⑤反应剧烈,发出紫红色火焰⑥锂四处游动A.②⑥B.①③C.②③⑤D.②④⑤⑥3.下列离子方程式正确的是()A.Na与CuSO4溶液的反应:2Na+Cu2+=Cu+2Na+B.向澄清石灰水中滴加少量NaHCO3溶液:Ca2++OH−+HCO3−=CaCO3+H2O C.制备Fe(OH)3胶体:Fe3++3H2O=Fe(OH)3↓+3H+D.酸性KMnO4溶液和双氧水混合:2MnO4−+5H2O2=2Mn2++5O2↑+6OH−+ 2H2O4.下列有关钠及其化合物的性质与用途具有对应关系的是()A.NaHCO3受热易分解,可用于制膨松剂B.Na2O2呈淡黄色,可用于消防员呼吸面具中的供氧剂C.氢氧化钠具有强碱性,可用作干燥剂D.碳酸钠显碱性,可以用于制抗酸药物5.部分含Na或含Cu物质的分类与相应化合价关系如图所示。
下列推断合理的是()A.Na与CuSO4溶液的反应:2Na+Cu2+=Cu+2Na+B.能与H2O反应生成c的物质只有bC.存在c→d→e的转化D.若b能与H2O反应生成c和O2,则b是碱性氧化物6.钠、氯元素及其化合物十分重要。
海水中蕴含着丰富的氯元素,主要以氯化钠、氯化镁等氯化物形式存在。
人们通过物理方法和化学方法可以制得多种钠、氯化工产品,这些产品广泛地应用于生产生活中。

2.1 钠及其化合物 课时作业2024-2025学年高一上学期化学人教版(2019)必修第一册一、单选题1.2023年国庆节,南昌以天空为幕,以烟花为笔,举办了一场盛大的“风景这边独好”国庆烟花晚会。
璀敁的焰火点亮了南昌的夜空,惊艳了无数国人。
这与高中化学中“焰色试验”知识相关,下列说法中正确的是A .焰色试验是化学变化B .利用焰色试验可区分NaCl 与23Na CO 固体C .焰色试验均应透过蓝色钴玻璃观察D .用稀盐酸清洗做焰色试验的铂丝2.下列物质中,可用于呼吸面具供氧剂的是A .2SOB .2NOC .22Na OD .23Al O3.化学与我们日常生产、生活及环境密切相关,下列说法不正确的是( )A .当光线透过树叶间的缝隙射入密林中时,可以观察到丁达尔效应B .当火灾现场存放有大量金属钠时,可以用水来灭火C .节日燃放的五彩缤纷的烟花,所呈现的就是锂、钠、钾、钡等金属元素的焰色D .目前很多自来水厂用2Cl 来杀菌、消毒,我们偶尔闻到的自来水散发出来的刺激性气味就是余氯的气味4.向滴有酚酞溶液的水中加入一块绿豆大的钠,下列实验现象描述错误的是A .钠沉入水底B .钠熔成小球C .发出“嘶嘶”声音D .溶液变红5.英国化学家汉弗里·戴维在十九世纪初通过电解的方式获得金属钠的单质,下列有关金属钠的性质描述,错误的是( )A .金属钠性质活泼,一般保存在煤油中B .Na 的金属性强,可从硫酸铜溶液中置换出铜C .金属钠可用刀切割,说明其硬度较小D .使用后多余的金属钠应放回试剂瓶中6.当温度恒定时,一定量的饱和NaOH 溶液中加入少量22Na O 固体,下列说法正确的是( )A.溶液的质量不变B.溶液中的Na 数目增多C.溶质的质量分数变大D.溶液的碱性不变7.化学改善人类的生活,创造美好的世界。
下列生产生活情境中涉及的化学原理错误的是()选项生产生活情境化学原理A国庆节天安门广场燃放烟花,色彩绚丽利用了某些金属的焰色试验B用氯化铁溶液刻蚀覆铜板制作印刷电路板铜与FeCl3发生置换反应C水果罐头中常添加适量抗坏血酸(即维生素C)抗坏血酸有抗氧化作用D秸秆、餐厨垃圾等进行密闭发酵提供燃料发酵过程中产生CH4 A.A B.B C.C D.D8.下列关于钠的叙述不正确的是A.钠是硬度很大的银白色金属B.钠燃烧时,发出黄色的火焰C.钠在空气中燃烧时,生成淡黄色固体D.钠原子的最外层电子数为19.焰色试验过程中铂丝的清洗和灼烧与钾焰色试验的观察两项操作如图所示,下列说法正确的是()A.铂丝也可用稀硫酸来清洗B.某溶液进行焰色试验火焰呈黄色,则表明待测液中一定含有Na+,可能含有K+C.焰色试验是化学变化D.所有金属及其化合物灼烧时火焰均有颜色10.有关Na2O和Na2O2的比较,下列叙述正确的是()A.Na2O和Na2O2都是钠的氧化物,都是碱性氧化物B.Na2O和Na2O2都是易溶于水且能与水反应的白色固体C.Na2O2在和H2O的反应中既是氧化剂又是还原剂D.Na2O中阴、阳离子的个数比为1:2,Na2O2中阴、阳离子的个数比为1:111.下列有关钠及其化合物的性质与用途具有对应关系的是()O应,可用作高压钠灯A.Na易与2NaHCO受热易分解,可用作抗酸药B.3Na O具有漂白性,可用作供氧剂C.22Na CO溶液显碱性,可用于清洗油污D.2312.下列物质性质与用途具有对应关系的是Na O呈淡黄色,可用作供氧剂A.22B.NaCl熔点较高,可用于制取NaOHNa CO溶液呈碱性,可用于除油污C.23NaHCO易分解,可用于治疗胃酸过多D.313.下列关于钠的叙述中,错误的是()A.通常情况下钠是固体,密度比水的小B.钠在自然界中以游离态(单质)存在C.钠在空气中燃烧生成过氧化钠D.金属钠着火时应该用干燥的沙土灭火14.下列实验操作过程中,观察不到金属Na光亮银白色的是()A.取出长期保存在煤油中的Na B.Na投入水中C.用小刀将Na切开D.Na在空气中加热15.焰火“脚印”“笑脸”“五环”,让北京奥运会开幕式更加辉煌、浪漫,这与高中化学中“焰色试验”知识相关。
钠及其化合物(习题)1.钠作为一种重要原料,可用于制造许多在国防工业上有重要用途的金属。
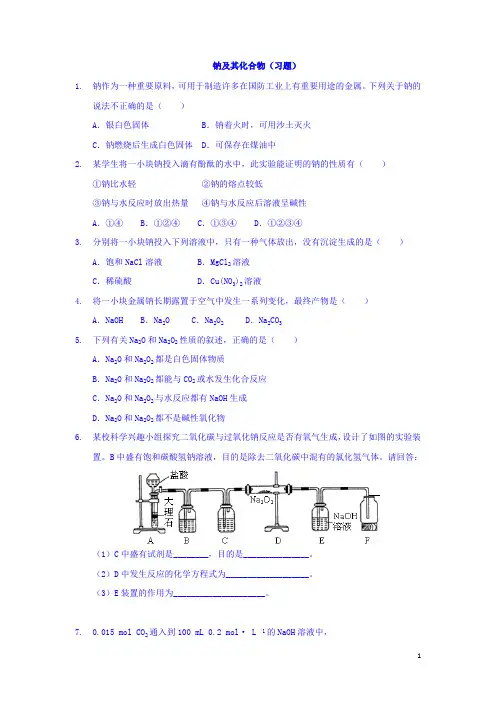
下列关于钠的说法不正确的是()A.银白色固体 B.钠着火时,可用沙土灭火C.钠燃烧后生成白色固体 D.可保存在煤油中2.某学生将一小块钠投入滴有酚酞的水中,此实验能证明的钠的性质有()①钠比水轻②钠的熔点较低③钠与水反应时放出热量④钠与水反应后溶液呈碱性A.①④ B.①②④ C.①③④ D.①②③④3.分别将一小块钠投入下列溶液中,只有一种气体放出,没有沉淀生成的是()A.饱和NaCl溶液 B.MgCl2溶液C.稀硫酸 D.Cu(NO3)2溶液4.将一小块金属钠长期露置于空气中发生一系列变化,最终产物是()A.NaOH B.Na2O C.Na2O2 D.Na2CO35.下列有关Na2O和Na2O2性质的叙述,正确的是()A.Na2O和Na2O2都是白色固体物质B.Na2O和Na2O2都能与CO2或水发生化合反应C.Na2O和Na2O2与水反应都有NaOH生成D.Na2O和Na2O2都不是碱性氧化物6.某校科学兴趣小组探究二氧化碳与过氧化钠反应是否有氧气生成,设计了如图的实验装置。
B中盛有饱和碳酸氢钠溶液,目的是除去二氧化碳中混有的氯化氢气体。
请回答:(1)C中盛有试剂是________,目的是_______________。
(2)D中发生反应的化学方程式为___________________。
(3)E装置的作用为_____________________。
7.0.015 mol CO2通入到100 mL 0.2 mol· L 1的NaOH溶液中,所得溶液中CO32 和HCO3 的物质的量浓度之比是________。
8.下列有关Na2CO3和NaHCO3的说法中,正确的是()A.热稳定性:Na2CO3<NaHCO3B.相同温度下在水中的溶解度:Na2CO3<NaHCO3C.等质量的两种固体,分别与过量盐酸反应,生成CO2的质量相等D.向等物质的量的Na2CO3粉末与NaHCO3粉末中分别加入适量相同浓度的稀盐酸,后者的反应更剧烈9.现有25 mL 2 mol·L 1的Na2CO3溶液和75 mL 1 mol·L 1的稀盐酸,进行以下两种操作:①将Na2CO3溶液缓缓滴加到稀盐酸中,②将稀盐酸缓缓滴加到Na2CO3溶液中。

第三章:钠及其化合物专题练习钠的性质1.下列盛放物质的方法错误的是A.将金属钠保存在煤油中。
B.少量的白磷可保存在水中。
C.纯碱溶液用带磨口玻璃瓶塞的试剂瓶保存。
D.硝酸银溶液盛放在棕色试剂瓶中。
2.金属钠长期暴露在空气中,它的最终产物是:( )A.Na2O2B.NaOHC.Na2CO3D.NaHCO33.将一小块金属钠投入到硫酸铜溶液中,得到的主要产物是:( )A.Cu和CuSO4 B.Cu(OH)2、Na2SO4和H2C.Cu、Na2SO4和 H2D.Cu、Cu(OH)2、Na2SO4和 H24.试管中装有煤油和水的混合物,静置后放入一小块金属钠,可下列说法不正确的是A.观察到金属钠在煤油和水的界面附近上下往复运动。
B.反应一段时间煤油会燃烧。
C.上下运动是由于该金属与水反应产生气体。
D.若是向水中加入酚酞溶液,则溶液变红色。
5、下列属于钠离子性质的是A、极易被氧化B、有银白色金属光泽C、能置换CaCl2溶液中的Ca D、焰色反应为黄色6.将一小块钠投入盛5mL澄清石灰水的试管里,不可能观察到的现象是( )A.钠熔成小球并在液面上滚动B.有气体产生C.溶液底部有银白色物质生成D.溶液变浑浊7.钠与水反应时的现象与钠的下列性质无关的是()A.钠的熔点低 B.钠的密度小C.钠的硬度小 D.钠有强还原性8、将金属钠分别投入下列物质的水溶液中,生成白色沉淀的是A、HClB、K2SO4C、CuCl2D、Ca(HCO3)29.将4.6g金属钠投入到95.4g水中,所得溶液中溶质的质量分数:A.等于4.6%B. 等于8%C.小于8%D.大于8%10.将ag钠投入bg水中(水过量),反应后所得溶液中溶质的质量分数是( )A.a/(a+b) ×100%B.40a/(a+b) ×100%C.20a/(a+b) ×100%D.40a/(22a+23b) ×100%11.写出钠和下列物质反应的化学反应方程式及离子方程式:(1)、氧气(2)、氯化铁溶液(3)、碳酸氢钠溶液钠的化合物――碳酸钠和碳酸氢钠1.有四种含钠的化合物W、X、Y、Z,根据下列变化推断与W、X、Y、Z的分子式对应的一组是 ( )W→X+CO2↑+H2O Z+CO2→X+O2↑ Z十H20→Y十O2↑2X+Ca(OH)2→Y+CaCO 3↓A.Na 2C03、NaHC03、NaOH 、Na 202B.NaOH 、Na 202、Na 2C03、NaHC03C.NaHC03、NaC03、NaOH 、Na 202D.NaHC03、Na 2C03、Na 202、NaOH 2、关于NaHCO 3性质的说法正确的是A.只能与酸反应,不能与碱反应B.医疗可用于冶疗胃酸过多C.与足量的酸反应时放出的CO 2比等质量的Na 2CO 3要少D.同温度时,碳酸氢钠的溶解度大于碳酸钠的溶解度。

第三章第一节一、选择题1.将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体(粉末),下列有关叙述不正确的是() A.表面迅速变暗是因为钠与空气中的氧气反应生成了氧化钠B.“出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液C.最后变成碳酸钠粉末D.该过程的所有化学反应均为氧化还原反应2.“神舟七号”宇航员翟志刚成功完成中国历史上首次太空行走,使中国成为第三个独立掌握出舱活动技术的国家。
宇航员出舱时,呼吸所需的氧气主要来自太空服中的呼吸面具。
下列物质在一定条件下均能产生氧气,其中最适宜用于呼吸面具中供氧的是() A.HNO3B.H2O2C.KClO3D.Na2O23.(2009·巢湖模拟)在25℃,101 kPa下由HCHO(g)、H2和CO组成的混合气体共6.72 g,其相对氢气的密度为14,将该气体与2.24 L氧气(标准状况)充分反应后的产物通过足量的Na2O2粉末,使Na2O2粉末增重的质量为() A.等于6.72 g B.小于6.72 gC.大于6.72 g D.无法计算4.(2009·蚌埠模拟)有关苏打和小苏打的叙述正确的是() A.等质量的苏打、小苏打分别与足量稀硫酸反应,小苏打产生的二氧化碳多B.等质量的苏打、小苏打分别与足量的同种盐酸反应,小苏打消耗的盐酸多C.向小苏打溶液中滴入氢氧化钡溶液无沉淀,而苏打溶液中滴入氢氧化钡溶液出现沉淀D.苏打和小苏打都既能与酸反应又能与氢氧化钠反应5.为除去括号内的杂质,所选用的试剂或方法不正确的是() A.Na2CO3溶液(NaHCO3),选用适量NaOH溶液B.NaHCO3溶液(Na2CO3),通入过量的CO2气体C.Na2O2粉末(Na2O),将混合物在空气中加热D.Na2SO4溶液(Na2CO3),加入适量的H2SO4溶液6.(2009·湖北重点中学模拟)Cs是稳定的核电荷数最大的碱金属元素,下列关于铯及其化合物的叙述,正确的是() A.铯与冷水反应十分平缓并生成H2B.铯与硫酸反应,生成CsSO4与H2C.铯的氧化物可直接与水反应生成CsOHD.铯在空气中燃烧生成Cs2O7.在一定条件下,将钠与氧气反应的生成物1.5 g溶于水,所得溶液恰好能被80 mL 浓度为0.50 mol/L的HCl溶液中和,则该生成物的成分是() A.Na2O B.Na2O2C.Na2O和Na2O2D.Na2O2和NaO28.(2009·济宁模拟)由Na2O2、Na2CO3、NaHCO3、NaCl固体中的某几种组成的混合物,向混合物中加入足量的盐酸,有气体放出,将放出的气体通入足量的NaOH溶液后,气体体积有所减少,若将上述混合物在空气中充分加热,也有气体放出,下列判断正确的是() A.混合物中一定含有Na2O2、NaHCO3B.混合物中一定不含有Na2CO3和NaClC.混合物一定不含有Na2O2和NaClD.混合物中一定含有Na2O2、Na2CO3、NaHCO39.取一支大试管,加入20 mL饱和澄清石灰水(ρ=1.6 g·cm-3),再加入5 mL苯(ρ=0.87g·cm -3),静置后缓慢加入黄豆粒大小的钠块(ρ=0.97 g·cm -3)。

2.1 钠及其化合物 同步练习题一、选择题1.下列有关碳酸钠和碳酸氢钠的叙述正确的是 A .二者均不稳定,易分解生成气体B .等浓度等体积二份溶液都滴入2滴酚酞,3NaHCO 溶液颜色深C .碳酸氢钠的溶解度大于碳酸钠D .等质量的二种固体分别与足量盐酸反应,3NaHCO 产生气体多 2.下列物质不能通过化合反应生成的是 A .FeCl 2B .CuC .()3Fe OHD .NaHCO 33.下列物质的俗称不正确的是 A .2Ca(OH) 熟石灰 B .3NaHCO 苏打 C .NaOH 烧碱D .3CH COOH 醋酸4.下列关于钠的叙述中,不正确的是 A .钠燃烧时发出黄色的火焰 B .钠具有很强的还原性 C .钠燃烧时生成氧化钠D .钠通常保存在煤油中 5.在下列实验过程中,出现的“异常”现象的解释,不正确的是A .金属钠投入到硫酸铜溶液中,生成黑色沉淀物,是因为金属钠置换出金属铜B .过氧化钠加入到含有酚酞的水中,溶液变红再变无色,可能有强氧化性物质生成C .过量的二氧化碳通入澄清石灰水中,溶液变浑浊再变澄清,说明最终生成可以溶于水的盐D .在氯化亚铁的溶液中,滴加氢氧化钠溶液,先有白色沉淀,随后变灰绿色再变红褐色,说明氢氧化亚铁易被空气中的氧气氧化6.下列关于金属钠及其化合物的说法不正确...的是 A .钠切开后,光亮的表面迅速变暗,是因为生成了Na 2O B .向饱和Na 2CO 3溶液中通入足量二氧化碳有碳酸氢钠晶体析出 C .石蕊试液中加入过氧化钠粉末溶液先变蓝后褪色D .氧化钠与过氧化钠都能与水反应生成碱,因此他们都是碱性氧化物 7.表示下列反应的离子方程式错误的是A .Na 2O 2加入H 218O 中:2Na 2O 2+2H 218O=4Na ++4OH -+18O 2↑B .FeSO 4酸性溶液中加入H 2O 2:2Fe 2++H 2O 2+2H +=2Fe 3++2H 2OC .用过量氨水吸收工业尾气中的SO 2:2NH 3·H 2O+SO 2=2NH 4++SO 23-+H 2OD .Cl 2和水反应:Cl 2+H 2O=H ++C1-+HClO8.下表中,对陈述Ⅰ、Ⅰ的正确性及两者间是否具有因果关系的判断都正确的是A .AB .BC .CD .D二、非选择题 9.碳酸钠(Na 2CO 3)(1)碳酸钠是白色固体,俗称_______,_______于水;电离方程式_______。

钠及钠的化合物练习可能用到的相对原子质量:H 1 O 16 Na 23 Fe 56 Al 27一、单项选择题(本题包括12小题,每小题4分,共48分。
)1.将金属Cu投入金属A的盐溶液中,观察到Cu的表面出现银白色物质;金属B投入稀硫酸中,观察到B的表面有气泡产生。
下列关于金属A、B、Cu活动性的叙述正确的是() A.B>Cu>A B.A>Cu>B C.B>A>Cu D.A>B>Cu2.下列叙述正确的是()A.钠与氧气反应时,产物是由O2的用量决定的B.铝箔在空气中受热可以熔化且会发生剧烈燃烧C.金属与非金属发生反应时,被氧化的一定是金属D.铁丝不论在空气中还是在纯氧中都不会燃烧3.等质量的两份铝分别与适量的稀H2SO4和NaOH溶液完全反应,若消耗两溶液的体积相同,则稀H2SO4与NaOH溶液的物质的量浓度之比为()A.3∶2 B.2∶3 C.2∶1 D.1∶24.将11.5 g钠、9 g铝、28 g铁分别投入200 mL 1 mol·L-1的盐酸中,下列正确的是() A.铁与盐酸反应产生的气体比钠多 B.钠与盐酸反应最剧烈,产生的气体最多C.反应结束时产生的气体一样多 D.铝与盐酸反应的速率仅次于钠,但产生的气体最多5.将2.3 g钠投放到97.7 g水中,所得溶液中溶质的质量分数为()A.2.3% B.小于2.3% C.4% D.大于4%6.某学习小组进行了如下左图所示的实验,实验后组员之间的交流不合理的是()A.甲同学认为试管b中收集到的气体可点燃,且产生淡蓝色火焰B.乙同学认为试管a中生成的黑色固体可能为四氧化三铁C.丙同学认为将少量还原性铁粉放入试管中,加适量的水,加热也可实现该反应D.丁同学认为用盐酸溶解固体生成物所得溶液有颜色7.将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol·L-1的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如上右图所示,则下列说法错误的是()A.反应时,Na、Mg、Al均过量 B.x=2.24C.钠的物质的量为0.2 mol D.曲线b表示Mg与盐酸的反应8.实验:用脱脂棉包住0.2 g Na2O2粉末,放在石棉网上,在脱脂棉上滴加几滴水,可以观察到脱脂棉剧烈燃烧起来。

2.1 钠及其化合物 同步测试2024-2025学年高一上学期化学人教版(2019)必修第一册一、单选题1.下列关于金属钠的叙述中,正确的是 ( )A .钠在空气中的缓慢氧化与其在空气中点燃的产物都一样B .钠能与CuSO 4溶液发生置换反应生成CuC .将金属钠与水反应后的溶液中通入适量氯气后,溶液中含有两种溶质D .Na 2O 2与H 2O 反应是一个置换反应,有单质O 2产生2.下面关于金属钠的描述正确的是A .少量钠应保存在水中B .钠离子具有较强的还原性C .钠很软,在新材料领域没有用途D .钠的化学性质很活泼,在自然界里不能以游离态存在3.下列对实验的评价正确的是( )A .实验测得熔融NaCl 能导电,说明NaCl 属于电解质B .向久置的Na 2O 2粉末中滴加稀盐酸,产生无色气体,说明Na 2O 2已变质C .向某溶液中滴加AgNO 3溶液,产生白色沉淀,该溶液中一定有Cl -D .向KI -淀粉溶液中滴加氯水,溶液变蓝,说明氧化性:I 2>Cl 24.下列关于过氧化钠的说法中,错误的是( )A .化学式为Na 2O 2B .白色固体C .能与H 2O 反应D .能与CO 2反应5.下列化学名词正确的是( )A .焦炭B .硫黄C .风化D .饱合6.将一粒绿豆大小的金属钠,投入硫酸铜溶液的烧杯中,下列实验现象错误的是( )A .溶液中有蓝色沉淀生成B .反应放出热量,发出嘶嘶声C .钠熔成一个闪亮的小球,并在液面上向各方向迅速游动最后消失D .有红色物质生成7.下列有关23Na CO 和3NaHCO 的叙述正确的是( )A .均可用作食用碱和工业用碱B .23Na CO 俗称小苏打,3NaHCO 俗称苏打C .常温下,23Na CO 的溶解度比3NaHCO 的溶解度小D .与足量盐酸反应得到等量的2CO 时,消耗3NaHCO 的质量比23Na CO 多8.化学处处呈现美。
下列描述涉及的化学知识不正确的是( )A .茉莉花的芳香扑鼻而来,体现了分子是运动的B .晨雾中的光束如梦如幻,是丁达尔效应带来的美景C .甲烷分子为正四面体结构,四个氢原子完美对称D .烟花燃放时呈现出五彩缤纷的火花,是锂、钠、铜等金属被氧化所致9.焰色实验过程中,铂丝的清洗和灼烧与钾焰色实验的观察两项操作如图所示,下列叙述中错误的是( )A .每次实验中都要先将铂丝灼烧到火焰颜色,再蘸取被检验物质B .钾的焰色实验要透过蓝色钴玻璃观察C .焰色实验是某种金属元素灼烧时所具有的特殊颜色,是化学变化D .没有铂丝可用无锈铁丝代替进行实验10.以不同类别物质间的转化为线索,认识钠及其化合物。

2.1 钠及其化合物 同步练习题一、选择题1.化学让生活更美好,下列说法错误的是 A .甲醇可用作汽车燃料 B .苯酚溶液常用于皮肤消毒C .碳酸氢铵可用作食品膨松剂D .氢化的植物油可用来生产人造奶油2.在大试管内将足量3NaHCO 加热到200℃,将产生的混合气体通入到盛有1.87g2Na O和22Na O 的密闭容器中,待2Na O和22Na O 全部反应后,得到标准状况下224mL2O 再将反应后密闭容器内的固体部溶于水配成100mL 。
下列说法正确的是 A .2Na O 和22Na O 均为碱性氧化物B .3NaHCO 加热分解为23Na CO ,所以其碱性比23Na CO 强C .反应过程中总共转移0.04mol 电子D .配成的100mL 溶液中()Na 0.5mol /L c +=3.一次性鉴别等浓度的3KNO 、HCl 、23Na CO 溶液,下列方法不可行的是 A .焰色试验 B .测定各溶液pH C .滴加3AgNO 溶液D .滴加()32Ba HCO 溶液4.下列关于钠及其化合物的叙述中,正确的是A .钠元素在自然界中都以化合物的形式存在,是因为金属钠具有很强的氧化性B .过氧化钠要密封保存,是因为过氧化钠露置于空气中会发生反应变质C .金属钠保存在煤油中,是因为钠的密度比煤油的密度小D .钠可与硫酸铜溶液反应得到铜,是因为钠的性质比铜活泼 5.关于下列诗句或谚语,说法合理的是A .“滴水石穿、绳锯木断”前者包含化学变化,而后者包含物理变化B .“雨过天晴云破处,这般颜色做将来。
”所描述的瓷器青色,来自氧化铁C .“日照澄州江雾开”诗句中描述的丁达尔现象是因为胶体粒子本身发光D .“纷纷灿烂如星陨,霍霍喧逐似火攻。
”诗中涉及的焰色试验属于化学变化 6.下列化学实验室中的实验操作正确的是 A .用带有橡胶塞的棕色细口瓶盛装4KMnO 溶液 B .将实验剩余的钠块小心地放入垃圾桶中 C .用漏斗向燃着的酒精灯中添加少量酒精D .稀释浓硫酸时应将浓硫酸沿烧杯内壁缓缓注入水中并用玻璃棒不断搅拌 7.下列俗名不正确的是 A .纯碱:Na 2CO 3 B .苛性钠:NaOH C .苏打:NaHCO 3D .熟石灰:Ca(OH)28.下列关于22Na O 的说法中,不正确...的是A .是淡黄色固体B .氧元素的化合价为-2价C .能与水发生反应D .可在潜水艇中作为氧气的来源二、填空题9.判断下列关于22Na O 的叙述是否正确,若不正确,指出其错误之处。

《第一节钠及其化合物》同步训练(答案在后面)一、单项选择题(本大题有16小题,每小题3分,共48分)1、钠(Na)是周期表中的一种金属元素,以下关于钠的描述正确的是:A、钠的原子序数为11,位于第三周期ⅠA族。
B、钠的电子排布为2, 8, 1,具有一个未成对电子。
C、钠的原子量为22.99,位于金属活动性顺序表的中间位置。
D、钠在空气中燃烧会产生白色固体,即氧化钠(Na2O)。
2、钠与水反应的现象与下列哪种物质与水反应的现象相似?A、K(钾)与水B、Cu(铜)与水C、Na2O2(过氧化钠)与水D、Al(铝)与水3、实验室里用金属钠与氯气反应制备氯化钠,反应的化学方程式为Na + Cl2 = ()A. NaClB. 2NaClC. 2NaCl2D. NaCl24、将金属钠投入足量的水中,发生的化学反应可以表示为:A、2Na + 2H2O → 2NaOH + H2↑B、Na + H2O → NaOH + H2↑C、4Na + 2H2O → 4NaOH + 3H2↑D、Na + 3H2O → NaOH + 2H2↑5、下列关于钠的性质描述错误的是:A. 钠是一种银白色的金属,质地柔软。
B. 钠在空气中容易氧化,表面形成一层氧化膜。
C. 钠可以与水剧烈反应,放出氢气并放出大量热量。
D. 钠的熔点和沸点都很高,且在室温下呈固态。
E. 钠的密度比水小,所以在与水反应时会浮在水面上。
6、下列关于钠的描述,正确的是:A、钠在常温下为固态,不易与其他物质发生反应。
B、钠的熔点较高,不易熔化。
C、钠在空气中燃烧生成氧化钠。
D、钠与水反应生成氢气和氢氧化钠。
7、下列关于钠及其化合物的叙述正确的是()A. 钠在空气中燃烧生成氧化钠B. 钠在高温下可与二氧化碳反应生成金属碳化钠C. 过氧化钠与水反应生成氢氧化钠和氧气D. 碳酸钠的热稳定性比碳酸氢钠强8、下列关于钠的性质叙述不正确的是:A、钠是一种活泼的金属,在空气中能够自燃。
2.1《钠及其化合物》练习含答案一、选择题(单选题,共14个小题,每小题4分,共56分)1、金属钠是一种活泼金属,除了具有金属的一般性质外,还具有自己的特性。
下列关于钠的叙述中,正确的是()A.钠是银白色金属,熔点低,硬度大B.钠放置在空气中,会迅速被氧化而生成淡黄色的氧化钠C.在氧气中加热时,金属钠剧烈燃烧,发出黄色火焰D.金属钠着火可以用泡沫灭火器或用干燥的沙土灭火解析A中,钠的硬度小,可用小刀切割;B中,放置在空气中,钠被缓慢氧化生成白色Na2O;D中,钠着火时生成Na2O2,泡沫灭火器释放的泡沫中有CO2、H2O会与Na和Na2O2反应生成H2、O2,故不能用泡沫灭火器灭火。
答案C2、将一块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗―→“出汗”―→变成白色固体(粉末),下列有关叙述中正确的是()A.表面迅速变暗是因为钠与空气中的氧气反应生成了过氧化钠B.“出汗”是因为生成的氢氧化钠吸收空气中的H2O在表面形成了溶液C.最后变成碳酸氢钠粉末D.该过程中的所有化学反应均为氧化还原反应解析钠露置在空气中表面迅速变暗,是因为Na与O2反应生成了Na2O,A项错误;Na2O与水反应生成NaOH,NaOH又吸收空气中的H2O和CO2,生成Na2CO3·10H2O,Na2CO3·10H2O逐渐风化脱水,最后变成Na2CO3粉末,B正确;该过程中只有钠的氧化是氧化还原反应,C错误,应该是碳酸钠,碳酸氢钠不稳定,D项错误。
答案B3、下列叙述中正确的是()A.过氧化钠是淡黄色固体,久置于空气中变成白色氢氧化钠固体B.过氧化钠中阴阳离子比例为1∶2C.用过氧化钠漂白织物、麦秆等日久又逐渐变成黄色D.Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物解析过氧化钠久置于空气中变成白色碳酸钠固体,A错误;过氧化钠漂白是由于它的氧化性将有色物质永久漂白,C错误;碱性氧化物与酸反应生成盐和水,Na2O2与酸反应生成盐、水和氧气,不是碱性氧化物,属于过氧化物,D错误。
钠及其化合物的性质与应用1.下列物质的俗名与其化学式、用途都相符的是( )A.烧碱、Na2CO3、制玻璃B.小苏打、NaHCO3、治疗胃酸过多C.苏打、NaOH、造纸 D.食盐、NaCl、化肥2.下列有关钠的叙述中,错误的是()A.钠的还原性很强,可以用来冶炼金属钛、锆、铌等B.钠的化学性质非常活泼,钠和氧气在不同条件下反应可生成不同的物质C.钠可以把铁从氯化铁溶液中置换出来D.钠的质地软,可用小刀切割,可以保存在煤油中3.钠与水反应时的现象与钠的下列性质无关的是()A.钠的熔点低B.钠的密度小 C.钠的硬度小D.有强还原性4. 取一块金属钠放在燃烧匙里加热,下列实验现象:①金属熔化;②在空气中燃烧,放出黄色火花;③燃烧后得白色固体;④燃烧时火焰为黄色;⑤燃烧后生成淡黄色固体物质。
描述正确的是( )A.①② B.①②③ C.①④⑤ D.④⑤5.将一小块钠投入下列溶液时,既能产生气体又会出现沉淀的是()A.稀H2SO4 B.氢氧化钠溶液 C.硫酸钠溶液 D.氯化镁溶液6.把4.6 g钠投入到95.6 g水中,发生化学反应。
假设水无蒸发现象,所得溶液中溶质的质量分数是( )A.4.6% B.7.7% C.8.0% D.10%7.一定量的Na、Mg、Al分别与足量的盐酸反应,放出氢气的质量之比为1:2:3,则Na、Mg、Al三种金属的物质的量之比为()A.1:1:1 B.4:2:1 C.2:3:4 D.3:3:48.等质量的两块钠,第一块在足量氧气中加热,第二块在足量氧气(常温)中充分反应,则下列说法正确的是( )A.第一块钠失去电子多 B.两块钠失去电子一样多C.第二块钠的反应产物质量较大 D.两块钠的反应产物质量一样大9.下列物质的俗名与其化学式、用途都相符的是( )A.烧碱、Na2CO3、制玻璃B.小苏打、NaHCO3、治疗胃酸过多C.苏打、NaOH、造纸 D.食盐、NaCl、化肥10.106 g Na2CO3和84 g NaHCO3分别与足量的盐酸溶液反应,其中()A.Na2CO3放出的CO2多 B.NaHCO3放出的CO2多C.Na2CO3消耗的盐酸多 D.NaHCO3消耗的盐酸多11.下列化合物与小苏打溶液反应,没有气体或沉淀生成的是()A.烧碱 B.硫酸氢钠C.氢氧化钡D.稀盐酸12.可用于判断碳酸氢钠粉末中混有碳酸钠的实验方法是()A.加热时有无气体放出 B.滴加盐酸时有无气泡放出C.溶于水后滴加澄清石灰水,有白色沉淀生成D.溶于水后滴加BaCl2稀溶液,有白色沉淀生成13.下列关于碳酸氢钠的叙述,不正确的是()A.碳酸氢钠固体受热分解为碳酸钠B.碳酸氢钠溶液中加入氯化钙溶液,立即产生沉淀C.碳酸氢钠溶液中加入少量澄清石灰水,反应为:NaHCO3+Ca(OH)2=NaOH+CaCO3↓+H2O D.碳酸氢钠溶液中加入过量澄清石灰水,反应为:2NaHCO3+Ca(OH)2=Na2CO3+CaCO3↓+2H2O 14.加热4.2g小苏打,直到再没有气体放出为止,剩余固体物质的质量为( )A.1.68g B.2.65g C.3.36g D.5.3g15.有相同质量的两份NaHCO3粉末,第一份加入足量盐酸,笫二份先加热使其完全分解再加足量同质量分数的盐酸,则两者所消耗的盐酸中氯化氢的质量比为()A.2:1 B.1:1 C.1:2 D.4:216.物质A是由A元素组成的单质,将其在酒精灯火焰上灼烧,火焰呈黄色。
2.1钠及其化合物一、单选题1.下列有关钠的描述中错误的是( )A .钠可以保存在煤油中,说明钠的密度比煤油的大且钠不与煤油发生反应B .实验时钠需用镊子夹取,用后剩余的钠不能放回试剂瓶中C .新切开的钠放置在空气中会迅速被氧化D .钠能与氯化钠溶液发生化学反应2.下列关于Na 2O 和Na 2O 2的说法中,错误的是( ) A .Na 2O 与Na 2O 2中的阴阳离子比均为1:2B .Na 2O 2可在呼吸面具或潜水艇中作为氧气的来源C .钠放置在空气中,会迅速被氧化而生成白色的氧化钠D .Na 2O 2与Na 2O 都能与水反应生成碱,都属于碱性氧化物 3.下列有关钠的说法错误的是( )A .钠露置于空气的过程中有氢氧化钠生成B .取用金属钠要用镊子夹取,且剩下的金属钠应放回原试剂瓶C .金属钠在空气中的燃烧实验,应近距离俯视坩埚以便观察更仔细D .火灾现场若有大量活泼金属时,需用干燥的沙土4.钠的下列性质中与钠和水反应时的现象无关的是( ) A .钠的熔点较低 B .钠的密度小于水的 C .钠能导电 D .钠的金属活动性强 5.下列有关钠的取用方法、保存及存在形式的描述正确的是( ) A .实验中,取用少量的金属钠可用手直接取 B .实验室中,钠通常保存在煤油或石蜡油中C .实验后剩余的金属钠要丢入垃圾桶,不能放回原试剂瓶中D .钠在自然界中主要以化合态形式存在,少量以游离态形式存在 6.钠与水反应的现象与钠的下列性质无关的是( ) A .钠的熔点 B .钠的密度 C .钠的硬度 D .钠的还原性 7.化学与生产、生活、科技息息相关。
下列说法错误的是( ) A .过氧化钠常用作呼吸面具的供氧剂B .医用酒精能灭菌消毒是因为乙醇具有强氧化性C .常温下,可用铁制容器储运浓硫酸或浓硝酸D .明矾[KAl(SO 4)2⋅12H 2O]在水中能形成Al(OH)3胶体,可用作净水剂 8.下列关于金属钠的叙述不正确的是( ) A .具有很强的还原性 B .燃烧时生成氧化钠 C .燃烧时发出黄色的火焰 D .与水反应时,钠浮在水面上方 9.下列物质中,常温下不能与金属钠反应的是( ) A .煤油 B .水 C .稀硫酸 D .氯气 10.下列叙述正确的是①Na 2O 与Na 2O 2都能和水反应生成碱,它们都是碱性氧化物②Na 2O 与CO 2发生化合反应生成Na 2CO 3,Na 2O 2与CO 2发生置换反应生成O 2 ③Na 2O 是淡黄色物质,Na 2O 2是白色物质 ④Na 2O 2可作供氧剂,而Na 2O 不可 A .都正确B .①③④C .②③⑤D .④11.钠与水反应的实验过程如图①、②、③所示,下列有关说法错误的是( )A .图②中钠熔成小球,说明钠与水反应放热且钠的熔点低B .图③中滴加酚酞试液后溶液变红,说明有碱性物质生成C .钠与水反应的离子方程式为: 2Na+2H 2O= 2Na + +2OH -+H 2↑D .实验过程中切取一块绿豆大的钠后,将剩余的钠放入废液缸中 12.在蒸发皿中放一小块钠,加热至熔化时,用玻璃棒蘸取少量无水CuSO 4与熔化的钠接触,瞬间产生耀眼的火花,同时有红色物质生成。
高一化学《钠及其化合物》练习题及答案1. 下列物质中,属于元素的是()A. 水B. 氧气C. 醋酸D. 糖答案:B2. 下列物质中,不属于化合物的是()A. 水B. 氧气C. 乙醇D. 纸答案:B3. 下列物质中,属于混合物的是()A. 铁B. 空气C. 酒精D. 橡皮答案:B4. 下列物质中,属于纯净物的是()A. 空气B. 水C. 石墨D. 酒精答案:C5. 下列物质中,属于化合物的是()A. 空气B. 水C. 铁D. 石墨答案:B6. 下列物质中,属于气体的是()A. 铁B. 水C. 氧气D. 酒精答案:C7. 下列物质中,属于液体的是()A. 二氧化碳B. 氧气C. 石墨D. 乙醇答案:D8. 下列物质中,属于固体的是()A. 二氧化碳B. 氧气C. 水D. 酒精答案:C9. 下列物质中,属于有机物的是()A. 水B. 空气C. 石墨D. 乙醇答案:D10. 下列物质中,属于无机物的是()A. 石墨B. 氧气C. 酒精D. 糖答案:B11. 下列物质中,属于金属的是()A. 氧气B. 水C. 铁D. 石墨答案:C12. 下列物质中,属于非金属的是()A. 铁B. 氧气C. 铜D. 锡答案:B13. 下列物质中,属于半金属的是()A. 硫B. 铁C. 铜D. 锡答案:A14. 下列物质中,属于碱金属的是()A. 钠B. 铜C. 铁D. 锡答案:A15. 下列物质中,属于碱土金属的是()A. 钠B. 镁C. 铁D. 锡答案:B16. 下列物质中,属于卤素的是()A. 钠B. 氯气C. 铁D. 锡答案:B17. 下列物质中,属于惰性气体的是()A. 氢气B. 氧气C. 氮气D. 氦气答案:D18. 下列物质中,属于碳酸盐的是()A. 石灰石B. 金刚石C. 石墨D. 石膏答案:A19. 下列物质中,属于硫酸盐的是()A. 石灰石B. 石膏C. 石墨D. 石英答案:B20. 下列物质中,属于氯化物的是()A. 石灰石B. 石膏C. 石墨D. 氯气答案:D21. 下列物质中,属于铁系物质的是()A. 铁B. 钠C. 铜D. 锡答案:A22. 下列物质中,属于铜系物质的是()A. 铁B. 钠C. 铜D. 锡答案:C23. 下列物质中,属于铝系物质的是()A. 铁B. 钠C. 铜D. 铝答案:D24. 下列物质中,属于硅系物质的是()A. 铁B. 钠C. 铜D. 石英答案:D25. 下列物质中,属于氧化物的是()A. 水B. 氧气C. 酒精D. 乙酸答案:B26. 下列物质中,属于酸的是()A. 碳酸B. 硫酸C. 氢氧化钠D. 氯化铁答案:B27. 下列物质中,属于碱的是()A. 碳酸B. 硫酸C. 氢氧化钠D. 氯化铁答案:C28. 下列物质中,属于盐的是()A. 碳酸B. 硫酸C. 氢氧化钠D. 氯化铁答案:D29. 下列物质中,属于单质的是()A. 水B. 氧气C. 二氧化碳D. 酒精答案:B30. 下列物质中,属于分子化合物的是()A. 水B. 钠氯化合物C. 氯气D. 铁答案:A31. 下列物质中,属于离子化合物的是()A. 水B. 钠氯化合物C. 氯气D. 铁答案:B32. 下列物质中,属于均相混合物的是()A. 空气B. 铁C. 水D. 沙子答案:A33. 下列物质中,属于异相混合物的是()A. 空气B. 铁C. 水D. 沙子答案:D34. 下列物质中,属于溶液的是()A. 水B. 氧气C. 二氧化碳D. 酒精答案:A35. 下列物质中,属于悬浮液的是()A. 水B. 氧气C. 二氧化碳D. 沙子答案:D36. 下列物质中,属于乳浊液的是()A. 水B. 氧气C. 二氧化碳D. 牛奶答案:D37. 下列物质中,属于胶体的是()A. 水B. 氧气C. 二氧化碳D. 胶水答案:D38. 下列物质中,属于溶解度大的是()A. 水B. 酒精C. 油D. 盐答案:A39. 下列物质中,属于溶解度小的是()A. 水B. 酒精C. 油D. 盐答案:C40. 下列物质中,属于氧化剂的是()A. 氧气B. 氯气C. 碳酸D. 硫酸答案:A41. 下列物质中,属于还原剂的是()A. 氧气B. 氯气C. 金属D. 碳酸答案:C42. 下列物质中,属于强酸的是()A. 硫酸B. 醋酸C. 碳酸D. 磷酸答案:A43. 下列物质中,属于强碱的是()A. 氢氧化钠B. 氢氧化铜C. 氢氧化铁D. 氢氧化铝答案:A44. 下列物质中,属于弱酸的是()A. 醋酸B. 硫酸C. 磷酸D. 氢氧化铝答案:A45. 下列物质中,属于弱碱的是()A. 氢氧化铜B. 氢氧化铁C. 氢氧化铝D. 氢氧化钠答案:C46. 下列物质中,属于酸性氧化物的是()A. 氧气B. 二氧化碳C. 三氧化硫D. 氯气答案:C47. 下列物质中,属于碱性氧化物的是()A. 氧气B. 二氧化碳C. 氢氧化钠D. 氯气答案:C48. 下列物质中,属于中性氧化物的是()A. 氧气B. 二氧化碳C. 三氧化硫D. 一氧化碳答案:B49. 下列物质中,属于酸的盐的是()A. 碳酸钙B. 硫酸钠C. 氢氧化钠D. 氯化钠答案:B50. 下列物质中,属于碱的盐的是()A. 碳酸钙B. 硫酸钠C. 氢氧化钠D. 氯化钠答案:C51. 下列物质中,属于中性盐的是()A. 碳酸钙B. 硫酸钠C. 氢氧化钠D. 氯化钠答案:D52. 下列物质中,属于酸碱指示剂的是()A. 酚酞B. 甲基橙C. 甲基红D. 亚甲基蓝答案:A53. 下列物质中,属于强还原剂的是()A. 氢气B. 氯气C. 金属D. 氧气答案:A54. 下列物质中,属于强氧化剂的是()A. 氢气B. 氯气C. 金属D. 氧气答案:B55. 下列物质中,属于化学反应中的产物的是()A. 反应物B. 催化剂C. 溶剂D. 产物答案:D56. 下列物质中,属于化学反应中的反应物的是()A. 反应物B. 催化剂C. 溶剂D. 产物答案:A57. 下列物质中,属于化学反应中的催化剂的是()A. 反应物B. 催化剂C. 溶剂D. 产物答案:B58. 下列物质中,属于化学反应中的溶剂的是()A. 反应物B. 催化剂C. 溶剂D. 产物答案:C59. 下列物质中,属于化学反应的条件的是()A. 反应物B. 催化剂C. 温度D. 产物答案:C60. 下列物质中,属于化学反应的类型的是()A. 合成反应B. 分解反应C. 燃烧反应D. 酸碱反应答案:D61. 下列物质中,属于酸的性质的是()A. 有酸味B. 呈红色C. 能使蓝色石蕊变红D. 能使红色石蕊变绿答案:C62. 下列物质中,属于碱的性质的是()A. 有碱味B. 呈蓝色C. 能使蓝色石蕊变红D. 能使红色石蕊变绿答案:D63. 下列物质中,属于中性物质的是()A. 水B. 酒精C. 糖D. 食盐答案:A64. 下列物质中,属于氧化还原反应的是()A. 酸碱反应B. 氧化反应C. 分解反应D. 合成反应答案:B65. 下列物质中,属于酸碱反应的是()A. 酸碱反应B. 氧化反应C. 分解反应D. 合成反应答案:A66. 下列物质中,属于分解反应的是()A. 酸碱反应B. 氧化反应C. 分解反应D. 合成反应答案:C67. 下列物质中,属于合成反应的是()A. 酸碱反应B. 氧化反应C. 分解反应D. 合成反应答案:D68. 下列物质中,属于单纯物质的是()A. 水B. 酒精C. 糖D. 食盐答案:A69. 下列物质中,属于化合物的是()A. 水B. 酒精C. 石墨D. 铁答案:A70. 下列物质中,属于混合物的是()A. 水B. 钠C. 铁D. 石墨答案:A1. 钠的原子序数是23,其电子排布为1s²2s²2p⁶3s¹。
高一化学钠及其化合物试题答案及解析1.欲除去Na2CO3固体中的NaHCO3杂质,可采取的方法是()A.加水溶解后过滤B.配成溶液后通入足量的CO2气体C.将固体加热D.先加足量盐酸后过滤【答案】C【解析】 NaHCO3不稳定,加热时分解生成Na2CO3,所以可用加热固体的方法除去Na2CO3固体中的NaHCO3杂质,题中A、B、D为溶液,不利于固体的除杂,并且Na2CO3、NaHCO3都溶于水,不能用过滤的方法分离;配成溶液后通入足量的CO2气体,Na2CO3生成NaHCO3,不符合除杂的要求;Na2CO3、NaHCO3都与盐酸反应,也不能用于除杂。
【考点】碳酸钠的性质与应用2. NaCl是一种化工原料,可以制备一系列物质(见下图)。
下列说法正确的是()A.25℃,NaHCO3在水中的溶解度比Na2CO3的大B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应D.上图所示转化反应都是氧化还原反应【答案】B【解析】 25℃,NaHCO3在水中的溶解度比Na2CO3的小,A项错误;石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂,B项正确;常温下干燥的Cl2能用钢瓶贮存,但是铁点燃时可以与氯气反应,C项错误;图中生成碳酸氢钠和碳酸氢钠分解的反应都不是氧化还原反应,D项错误。
【考点】碳酸钠的性质与应用3.向盛有少量过氧化钠的试管中加入少量水,对实验现象描述错误的是()A.反应剧烈进行B.产生大量气泡,该气体使带火星的木条复燃C.试管底部发热D.反应后即向试管中加2滴酚酞,振荡,溶液呈红色【答案】D【解析】过氧化钠能与水剧烈反应生成氧气和氢氧化钠,该反应为放热反应;该反应剧烈进行,产生大量气泡,故A正确;产生大量氧气使带火星的木条复燃,故B正确;该反应为放热反应,试管底部发热,故C正确;反应生成了氢氧化钠,氢氧化钠能使酚酞溶液变红色,过氧化钠具有漂白性,随后溶液褪色,故D错误。
《钠及其化合物》练习题1. 一块外表已被氧化为Na2O的钠块,将其投入100g水中,产生H2,则被氧化的钠是()A.B.C.D.2. 金属钫(Fr)天然存在极微,它的21个已经知道同位素都具有放射性,它是碱金属元素中最重的元素。
依照在周期表中的位置预言其性质,其中不正确的选项()A.在碱金属元素中,它具有最大的原子半径B.在空气中燃烧时生成化学式为Fr2O的氧化物C.氧化物的水化物的化学式为FrOH,它应属于强碱D.其单质常温下跟水反响比钠剧烈3. 某物质灼烧时,焰色反响为黄色,以下推断正确的选项()A.该物质一定是钠的化合物B.该物质一定是含钠元素C.该物质一定是金属钠D.可确定该物质中不含钾元素4. 向紫色石蕊试液中参加过量的Na2O2粉末,振荡,观察不到的现象是()A.有大量气泡产生B.溶液颜色先变为蓝色C.最后溶液褪色D.最后溶液变为蓝色5. 以下关于“焰色反响”的理解正确的选项()A.只有金属单质才有焰色反响B.只有金属化合物才有焰色反响C.只有某些金属或其化合物才有焰色反响D.只有金属离子才有焰色反响6. 在烧杯中参加水和苯(密度/cm3,不与钠反响)各50mL,将一小粒金属钠(密度/cm3)投入烧杯中,观察到的现象可能是A.钠在水层中反响并四处游动B.钠停留在苯层中不发生反响C.钠在苯的液面上反响并四处游动D.钠在苯与水的交界处反响并可能做上、下跳动7. 泡沫灭火器内装的药液之一是NaHCO3饱和溶液,而不选用更廉价的Na2CO3饱和溶液,其缘故是①质量一样的两种钠盐,NaHCO3与足量酸反响产生的CO2比Na2CO3多②产生一样体积(同温、同压)的CO2,耗费的量NaHCO3比Na2CO3少③NaHCO3与酸反响比Na2CO3快得多④NaHCO3比Na2CO3稳定,便于长期保存A.只有①③B.只有②③C.①②③D.①②③④8. 将一定量的金属钠放入一定物质的量浓度的NaOH溶液中,反响完成后,NaOH溶液的物质的量浓度A.增大B.不能确定C.减少D.不变9. Na2CO3俗名纯碱,下面是对纯碱采纳不同分类方法,其中不正确的选项()A.纯碱是碱 B.纯碱是正盐 C.纯碱是钠盐 D.纯碱是碳酸盐10. 以下金属在一定条件下可以与水反响,且生成金属氧化物是()A.K B.Mg C.Fe D.Cu11. 在烧杯中加一些水,滴入几滴酚酞溶液,然后把一小块钠放入水中,从这个实验过程观察到的反响现象中,不可能得出的结论是()A.钠比拟柔软B.钠与水反响生成碱C.钠与水反响放热D.钠与水反响放出气体12. 某研究性学习小组在整理实验室化学试剂时,发觉一盛有无色溶液的试剂瓶,标签破损,如以下图。
第7课时钠及其化合物A组基础题组1.(2016浙江温州月考)下列叙述正确的是()A.钠在空气中燃烧生成Na2O比NaHCO3稳定,NaHCO3比Na2CO3易溶于水C.用铂丝蘸取某溶液进行焰色反应,火焰呈黄色,说明该溶液中一定存在Na+,不存在K+D.将Na投入NH4Cl溶液中可生成两种气体2.(2016湖北宜昌月考)下列各组中的两种物质作用,反应条件(温度或者反应物用量)改变,不会引起产物种类改变的是()%和O2和CO2和CO2和NaOH3.(2015黑龙江哈尔滨月考)钠与水反应时的现象与钠的下列性质无关的是()A.钠的密度小B.钠的熔点低C.钠的硬度小D.钠有强还原性4.(2016河南安阳一中月考)化学知识在生产和生活中有着重要的应用。
下列说法中正确的是()①钠的还原性很强,可以用来冶炼金属钛、钽、铌、锆等②K、Na合金可作原子反应堆的导热剂③明矾常用作消毒剂④Na2O2既可作呼吸面具中O2的来源,又可漂白织物、麦秆、羽毛等(⑤碳酸钠在医疗上是治疗胃酸过多的一种药剂⑥发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔A.①②③④B.①②④⑥C.①②③④⑥D.①②③④⑤⑥5.(2015广东广州模拟)等质量的钠进行下列实验,其中生成氢气最多的是()A.将钠投入到足量水中B.将钠用铝箔包好并刺一些小孔,再放入足量的水中C.将钠放入足量稀硫酸中D.将钠放入足量稀盐酸中<6.(2015山东潍坊模拟)关于NaHCO3性质的有关叙述正确的是()A.只能与强酸反应,不能与强碱反应B.医疗上可用于治疗胃酸过多C.与足量的酸反应时放出的CO2比等质量的Na2CO3要少D.同温度时,NaHCO3的溶解度>Na2CO3的溶解度7.(2015湖南常德月考)如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应。
已知钠及其氧化物的物质的量均为mol,水的质量为100 g。
下列说法正确的是()A.反应③最多能产生mol O2~B.反应①的离子方程式为Na+2H2O Na++2OH-+H2↑中阴阳离子数目之比为1∶1D.①、②、③充分反应后所得溶液中溶质的质量分数从大到小:①>②>③8.(2015黑龙江黑河月考)将mol Na分别投入到盛有100 mL水、100 mL 1 mol/L盐酸、100 mL1 mol/L硫酸铜溶液的X、Y、Z三个烧杯中,下列有关说法错误的是()A.三个烧杯中一定均会发生的离子反应有:2Na+2H2O2Na++2OH-+H2↑B.三个烧杯中钠均在液面上剧烈反应,相比而言,X烧杯中的反应平缓些烧杯中一定会有沉淀生成,但沉淀不是单质铜,D.三个烧杯中生成氢气的物质的量相同9.(2015河南南阳模拟)如图所示实验装置用于验证某些物质的性质。
在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。
试回答下列问题:(1)在A试管内发生反应的化学方程式是。
(2)B装置的作用是。
(3)在双球干燥管内发生反应的化学方程式为,该反应中氧化剂为,氧化产物为,每有1 mol Na2O2发生反应,转移电子数目为。
(4)双球干燥管内观察到的实验现象是;上述实验现象说明。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是。
:B组提升题组10.(2016湖北襄阳四校期中)下列各组物质相互混合反应后,最终有白色沉淀生成的是()①金属钠投入到FeCl3溶液中②过量NaOH溶液和明矾溶液混合③少量Ca(OH)2投入过量NaHCO3溶液中④向AlCl3溶液中滴入NaHCO3溶液⑤向饱和Na2CO3溶液中通入足量CO2:A.①③④⑤B.只有①④C.只有②③D.只有③④⑤11.(2015河北衡水模拟)将等物质的量的①Na②Na2O③Na2O2④NaOH⑤Na2CO3露置于空气中,最后质量变化由小到大的顺序是()A.⑤<④<③<①<②B.②<①<③<④<⑤C.⑤<④<②=③<①D.⑤<③<④<②<①12.(2014北京理综,9,6分)下列解释事实的方程式不正确...的是()A.测mol/L氨水的pH为11:NH3·H2O N+OH-B.将Na块放入水中,产生气体:2Na+2H2O2NaOH+H2↑C.用CuCl2溶液做导电实验,灯泡发光:CuCl2Cu2++2Cl-片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O2Al+3H2↑】13.(2015安徽阜阳模拟)过氧化钠具有强氧化性,遇木炭、铝粉等还原性物质时可燃烧。
下列有关说法不正确的是()与CO2反应时,Na2O2是氧化剂,CO2是还原剂mol过氧化钠中阴离子数目为N AC.过氧化钠与木炭、铝粉反应时,过氧化钠均表现出强氧化性D.过氧化钠与二氧化硫反应时可生成硫酸钠14.(2015河南安阳模拟)某实验小组欲探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。
于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(1)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。
A受热分解的化学方程式为。
(2)称取两种固体各2 g,分别加入两个小烧杯中,再各加10 mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复至室温,向所得溶液中各滴入2滴酚酞溶液。
^①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论。
②同学们在两烧杯中还观察到以下现象。
其中,属于盛放Na2CO3的烧杯中出现的现象的是(填字母序号)。
a.溶液温度下降b.溶液温度升高c.滴入酚酞后呈浅红色d.滴入酚酞后呈红色(3)如图所示,在气密性良好的装置Ⅰ和Ⅱ中分别放入药品,将气球内的固体同时倒入试管中。
①两试管中均产生气体,(填“Ⅰ”或“Ⅱ”)的反应程度更为剧烈。
②反应结束后,气球均有膨胀,恢复至室温,下列说法正确的是。
、a.装置Ⅰ的气球体积较大b.装置Ⅱ的气球体积较大c.生成气体的体积根据盐酸计算d.生成气体的体积根据固体计算(4)同学们将两种固体分别配制成mol·L-1的溶液,设计如下方案并对反应现象作出预测:实验方案预测现象预测依据|操作1:向2 mL Na2CO3溶液中滴加1mL mol·L-1CaCl2溶液有白色沉淀Na2CO3溶液中的C浓度较大,能与CaCl2发生反应(写离子方程式)操作2:向2 mL NaHCO3溶液中滴加1 mL mol·L-1CaCl2溶液无白色沉淀NaHCO3溶液中的C浓度很小,不能与CaCl2反应实际实验后,发现操作2的现象与预测有差异:产生白色沉淀和气体。
则该条件下,NaHCO3溶液与CaCl2溶液反应的离子方程式为。
答案全解全析¥A组基础题组A项,钠在空气中燃烧生成过氧化钠,错误;B项,Na2CO3比NaHCO3易溶于水,错误;C项,用铂丝蘸取某溶液进行焰色反应,火焰呈黄色,说明该溶液中一定存在Na+,不能确定是否存在K+,错误;D项,钠和水反应生成氢氧化钠和氢气,氢氧化钠和氯化铵反应有氨气放出,所以将Na投入NH4Cl溶液中可生成两种气体,正确。
A项,钠和氧气反应,在常温时生成氧化钠,在点燃或者加热条件下生成过氧化钠,故A不符合题意;B项,氢氧化钠与二氧化碳反应,二氧化碳不足时生成碳酸钠,二氧化碳过量时生成碳酸氢钠,故B不符合题意;C 项,过氧化钠与二氧化碳反应生成碳酸钠和氧气,故C符合题意;D项,氯化铝和少量氢氧化钠溶液反应生成氯化钠和氢氧化铝白色沉淀,和过量氢氧化钠溶液反应时,生成氯化钠和偏铝酸钠,故D不符合题意。
A项,钠的密度比水小,所以钠浮在水面上,故A不符合题意;B项,钠与水反应放热,钠的熔点低,所以看到钠熔化成小球,故B不符合题意;C项,硬度大小与反应现象无关,故C符合题意;D项,钠有强还原性,所以与水反应剧烈,故D不符合题意。
③明矾不能用作消毒剂,可用作净水剂,故错误;⑤碳酸钠碱性较强,所以不能用来治疗胃酸过多,碳酸氢钠在医疗上是治疗胃酸过多的一种药剂,故错误。
将等质量的钠投入水、稀硫酸、稀盐酸中,放出氢气的量相等;将钠用铝箔包好并刺一些小孔,再放入足量的水中,首先是钠与水反应生成NaOH和氢气,其次是铝与NaOH溶液反应生成氢气,故生成氢气最多。
A项,NaHCO3可与酸反应,如与盐酸反应生成二氧化碳、氯化钠和水,也可与碱反应,如与氢氧化钠反应生成碳酸钠和水,故A错误;B项,碳酸氢钠和盐酸反应,可用于中和胃酸,故B正确;C项,等质量的碳酸钠、碳酸氢钠,n(NaHCO3)>n(Na2CO3),分别与足量的酸反应,NaHCO3生成的二氧化碳多,故C错误;D项,常温下溶剂均为水时,Na2CO3较NaHCO3易溶,故D错误。
A项,反应③为2Na2O2+2H2O4NaOH+O2↑,根据方程式知,最多产生mol O2,故A正确;B项,反应①的离子方程式为2Na+2H2O2Na++2OH-+H2↑,故B错误;C项,过氧化钠中阴离子是,所以阴阳离子数目之比为1∶2,故C错误;D项,①、②、③充分反应后所得溶液中溶质的质量分数从大到小为①<②=③,故D错误。
、A项,钠投入溶液中,发生反应的实质是钠与酸或水电离产生的氢离子反应,钠与盐酸反应的实质为2Na+2H+2Na++H2↑,故A错误;B项,X、Y、Z三种溶液中,氢离子浓度由大到小的顺序为Y>Z>X,氢离子浓度越大,反应越剧烈,水中氢离子浓度最小,所以反应最缓和,故B正确;C项,钠与硫酸铜溶液反应,化学方程式为2Na+2H2O2NaOH+H2↑、2NaOH+CuSO4Cu(OH)2↓+Na2SO4,故C正确;D项,依据得失电子守恒可知,相同物质的量的钠失去电子数相同,生成氢气的量相同,故D正确。
9.答案(1)2NaHCO 3Na2CO3+H2O+CO2↑(2)吸收气体中的水蒸气(或干燥CO2)(3)2Na2O2+2CO22Na2CO3+O2Na2O2O2N A(或×1023)(4)淡黄色的Na2O2逐渐转变为白色粉末,点燃的蚊香燃烧更加剧烈CO2与Na2O2反应有O2生成(5)点燃的蚊香逐渐熄灭解析(1)A试管中发生的是加热碳酸氢钠固体生成碳酸钠、水和二氧化碳的反应,反应的化学方程式为2NaHCO3Na2CO3+H2O+CO2↑。
(2)B中盛的浓硫酸起到吸收水蒸气、干燥二氧化碳气体的作用。
(3)过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO22Na2CO3+O2。
(4)过氧化钠是淡黄色固体,随反应进行变为白色固体碳酸钠,反应生成的氧气具有助燃性,蚊香燃烧更剧烈。
(5)氧化钠和二氧化碳反应生成碳酸钠,无氧气生成,在二氧化碳环境中蚊香逐渐熄灭。