生活中常见的盐(1)
- 格式:ppt
- 大小:1.71 MB
- 文档页数:30



考点生活中常见的盐(完整版)实用资料(可以直接使用,可编辑完整版实用资料,欢迎下载)考点:生活中常见的盐一、基本考点考点1.生活中常见的盐(1)氯化钠(NaCl):①俗名:食盐。
②存在:在自然界中分布很广,存在于海水、盐湖、盐井、盐矿中。
③用途:a. 调味品,b. 配制生理盐水,c. 工业原料,d. 工业上用来做原料制取碳酸钠、氢氧化钠、氯气、盐酸等,e. 农业上用氯化钠溶液来选种等。
(2)碳酸钠(Na 2CO 2):俗名:纯碱、苏打;用途:用于生产玻璃、造纸、纺织、洗涤剂。
(3)碳酸氢钠(NaHCO 3):俗名:小苏打;用途:在食品工业上用作食品添加剂,在医疗上是治疗胃酸过多的一种药剂。
(4)碳酸钙(CaCO 3):它是大理石或石灰石的主要成分;用途:用作建筑材料及补钙剂。
考点2.盐的化学性质和复分解反应(1)盐的化学性质:①盐与金属反应生成另一种金属和另一种盐;如Zn+CuSO 4==ZnSO 4+Cu 。
②盐和酸反应生成另一种盐和另一种酸;如:BaCl 2+H 2SO 4==BaSO 4↓+2HCl 。
③盐和碱反应生成另一种盐和另一种碱;如:CuSO 4+2NaOH==Cu(OH)2↓+Na 2SO 4。
④盐和盐反应生成两种新盐;如:NaCl+AgNO 3==AgCl ↓+NaNO 3。
(3)复分解反应:①定义:两种化合物相互交换成分生成另外两种化合物的反应叫复分解反应。
如NaOH+HCl==NaCl+H 2O 。
②发生的条件:酸、碱、盐之间并不是都能发生反应,只有当两种化合物相互交换成分,有沉淀、水或气体生成时,复分解反应才能发生。
考点3.粗盐提纯粗盐中含有较多的可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等),可以通过过滤的方法把不溶于液体的固体物质跟液体分离。
过滤时,液体穿过滤纸上的小孔,而固态物质留在滤纸上,从而使固体和液体分离。
粗盐提纯时,把粗盐溶解在水里,经过过滤,把泥沙等杂质从食盐水中除去,然后再通过蒸发结晶,得到食盐晶体。

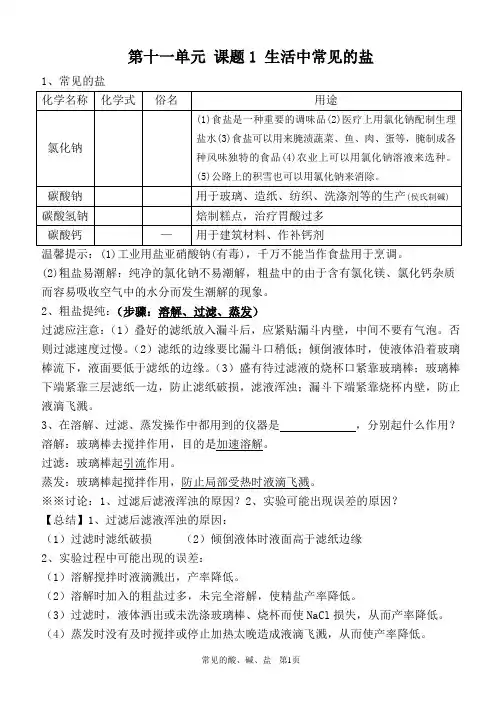
第十一单元课题1 生活中常见的盐1、常见的盐温馨提示:(1)工业用盐亚硝酸钠(有毒),千万不能当作食盐用于烹调。
(2)粗盐易潮解:纯净的氯化钠不易潮解,粗盐中的由于含有氯化镁、氯化钙杂质而容易吸收空气中的水分而发生潮解的现象。
2、粗盐提纯:(步骤:溶解、过滤、蒸发)过滤应注意:(1)叠好的滤纸放入漏斗后,应紧贴漏斗内壁,中间不要有气泡。
否则过滤速度过慢。
(2)滤纸的边缘要比漏斗口稍低;倾倒液体时,使液体沿着玻璃棒流下,液面要低于滤纸的边缘。
(3)盛有待过滤液的烧杯口紧靠玻璃棒;玻璃棒下端紧靠三层滤纸一边,防止滤纸破损,滤液浑浊;漏斗下端紧靠烧杯内壁,防止液滴飞溅。
3、在溶解、过滤、蒸发操作中都用到的仪器是,分别起什么作用?溶解:玻璃棒去搅拌作用,目的是加速溶解。
过滤:玻璃棒起引流作用。
蒸发:玻璃棒起搅拌作用,防止局部受热时液滴飞溅。
※※讨论:1、过滤后滤液浑浊的原因?2、实验可能出现误差的原因?【总结】1、过滤后滤液浑浊的原因:(1)过滤时滤纸破损(2)倾倒液体时液面高于滤纸边缘2、实验过程中可能出现的误差:(1)溶解搅拌时液滴溅出,产率降低。
(2)溶解时加入的粗盐过多,未完全溶解,使精盐产率降低。
(3)过滤时,液体洒出或未洗涤玻璃棒、烧杯而使NaCl损失,从而产率降低。
(4)蒸发时没有及时搅拌或停止加热太晚造成液滴飞溅,从而使产率降低。
4、盐的化学性质:【务必掌握】(1)盐+金属→新盐+新金属(置换反应) 如:Fe + CuSO4——Cu + AgNO3——(2)盐+酸→新盐+新酸(复分解反应)如:HCl + BaCO3——H 2SO4+ BaCl2——Na2CO3+ H2SO4——HCl + AgNO3——H 2SO4+ MgCO3——(3)盐+碱→新盐+新碱(复分解反应) (前提:反应物均可溶)如:K2CO3+ Ca(OH)2——MgSO4 + Ba(OH)2——FeCl3+ NaOH ——Cu(NO3)2+ KOH ——Al2(SO4)3+ NaOH ——(NH4)2SO4+ Ca(OH)2——(4)盐+盐→另两种盐(复分解反应) (前提:反应物均可溶)如:Na2CO3+ Ca(NO3)2——BaCl2 + AgNO3——Ba(NO3)2+ K2SO4——K 2CO3+ Fe(NO3)2——MgSO4 + Na2CO3——判断下列反应能否发生,能反应的完成化学方程式:① Zn + FeSO4——② Cu + AgCl ——③ NaCl + CuSO4——④ Na2CO3+ Ca(OH)2——⑤ BaCl2 + Na2CO3——⑥ CuCl2 + H2SO4——⑦ CaCO3 + BaCl2——⑧ BaSO4+ HCl ——⑨ Na2CO3+ Cu(OH)2——⑩Na2CO3+ BaCl2——5、复分解反应(1)定义:由________________互相交换成分,生成_________________的反应。



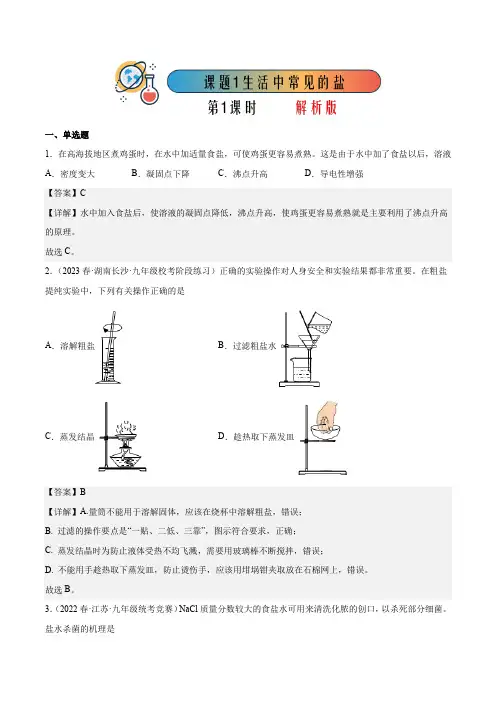
一、单选题1.在高海拔地区煮鸡蛋时,在水中加适量食盐,可使鸡蛋更容易煮熟。
这是由于水中加了食盐以后,溶液A.密度变大B.凝固点下降C.沸点升高D.导电性增强【答案】C【详解】水中加入食盐后,使溶液的凝固点降低,沸点升高,使鸡蛋更容易煮熟就是主要利用了沸点升高的原理。
故选C。
2.(2023春·湖南长沙·九年级校考阶段练习)正确的实验操作对人身安全和实验结果都非常重要。
在粗盐提纯实验中,下列有关操作正确的是A.溶解粗盐B.过滤粗盐水C.蒸发结晶D.趁热取下蒸发皿【答案】B【详解】A.量筒不能用于溶解固体,应该在烧杯中溶解粗盐,错误;B. 过滤的操作要点是“一贴、二低、三靠”,图示符合要求,正确;C. 蒸发结晶时为防止液体受热不均飞溅,需要用玻璃棒不断搅拌,错误;D. 不能用手趁热取下蒸发皿,防止烫伤手,应该用坩埚钳夹取放在石棉网上,错误。
故选B。
3.(2022春·江苏·九年级统考竞赛)NaCl质量分数较大的食盐水可用来清洗化脓的创口,以杀死部分细菌。
盐水杀菌的机理是A.病毒无法在盐水的环境中生存B.NaCl质量分数较大的盐水能溶解细菌C.NaCl质量分数较大的盐水的pH较小,细菌无法存活D.盐水中的NaCl的质量分数大于细菌的细胞液中的,使细菌因失水而死亡【答案】D【分析】NaCl质量分数较大的食盐水可用来清洗化脓的创口,以杀死部分细菌,是因为浓盐水溶质质量分数大于细菌内细胞液中溶质质量分数,使细菌失水死亡。
【详解】A、有些病毒不能在盐水中生存,有个别耐盐病毒可以在盐水中生存,故该项说法错误;B、盐水不能溶解细菌,而是因为浓盐水溶质质量分数大于细菌内细胞液中溶质质量分数,使细菌失水死亡,故该项说法错误;C、NaCl质量分数较大的盐水显中性,pH为7,有个别耐盐病毒可以在盐水中生存,故该项说法错误;D、盐水中的NaCl的质量分数大于细菌的细胞液中的溶质质量分数,细菌会因失水而死亡,达到杀菌作用,故该项说法正确。


初三化学:生活中常见的盐一、氯化钠(NaCl )↓性质氯化钠的熔点、沸点较高。
纯净的氯化钠不潮解,粗盐因含有少量的氯化镁、氯化钙等杂质,能吸收空气中的水分而潮解。
↓制法由于氯化钠的溶解度随温度的影响不大,故可以使用蒸发结晶法将氯化钠析出。
工业上用海水或盐井水晒盐,盐湖水煮盐等方法,使氯化钠成晶体析出。
↓分类氯化钠属于盐,但是盐类中大多数是有毒的,如亚硝酸钠、硫酸铜等。
氯化钠是少数可以食用的盐。
↓用途氯化钠在生活中可作为调味品。
医疗上使用的生理盐水是0.9%的氯化钠溶液。
农业上用10%—16%的氯化钠溶液来选种。
交通上,将氯化钠撒在积雪的路面上,可使路面上的积雪消融,减少事故的发生。
工业上用氯化钠作为原料制取碳酸钠、氢氧化钠、氯气、盐酸等化工产品。
↓粗盐的提纯步骤:溶解、过滤、蒸发、计算产率。
注意的问题:1.过滤时应遵循“一贴、二低、三靠”的基本原则。
2.过滤之前的溶液应静置一会儿,以免不溶物堵住滤纸的小孔,影响过滤的速度及效果。
3.过滤后的溶液如果仍浑浊,应查找原因,在过滤一次。
4.蒸发时应不断搅拌,以免溶液受热不均匀造成液滴飞溅。
5.当蒸发皿中出现较多固体时,应停止加热,利用蒸发皿的余热使滤液蒸干。
6.粗盐提纯的每一步操作中,玻璃棒的作用为:加速溶解、使液体均匀受热、转移固体。
过滤食盐水 蒸发食盐水二、碳酸钙、碳酸钠、碳酸氢钠↓碳酸钙(CaCO 3)碳酸钙大量应用于建筑业。
天然存在的石灰石、大理石的主要成分是碳酸钙。
碳酸钙也可以作为补钙剂等。
氯化钠晶体↓碳酸钠(Na2CO3)碳酸钠俗称纯碱、苏打。
为白色粉末,易溶于水。
虽然碳酸钠的溶液呈碱性,但碳酸钠属于盐。
碳酸钠广泛用于制玻璃、纺织、造纸和洗涤剂等工业生产中。
在蒸馒头前加入一些碳酸钠,可以中和发酵过程中产生的酸性物质。
↓碳酸氢钠(NaHCO3)碳酸氢钠俗称小苏打,是白色粉末,易溶于水,水溶液呈碱性。
碳酸氢钠是发酵粉的主要成分,也可以制治疗胃酸过多的药品。
常见的盐一、知识点知识点1、生活中常见的盐1.生活中常见的盐:有氯化钠、碳酸钠、碳酸氢钠、碳酸钙等。
亚硝酸钠(NaNO2)是一种工业用盐,外观和食盐相似,有毒。
2.粗盐提纯的主要步骤:溶解、过滤、蒸发。
3.碳酸根离子的检验:含CO32-(HCO3-)的化合物,遇到酸会反应放出能使澄清的石灰水变浑浊的二氧化碳气体。
利用此反应可以检验盐的组成中是否含有CO32-离子(或HCO3-)。
【要点诠释】1.组成里含有碳酸根离子的盐统称为碳酸盐,如Na2CO3、K2CO3、BaCO3、CaCO3等,它们与盐酸反应都会生成使澄清石灰水变浑浊的二氧化碳气体。
2.含有碳酸根离子的盐和某些物质反应生成不溶于水的固体,这一类反应有时也可以用来鉴别碳酸盐。
例如:Na2CO3 + Ca(OH)2=CaCO3↓+ 2NaOH知识点2、复分解反应发生的条件复分解反应发生的条件:当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
【要点诠释】1.复分解反应属于基本反应类型,其特点为AB+CD=AD+CB。
2.复分解反应发生的三个条件中,只要具备其中一个,反应就可以进行,不必三个条件都具备。
知识点3、盐的化学性质不同种类的盐其化学性质也有所不同。
对于其共性总结如下表所示:盐与酸反应、盐与碱反应、盐与盐反应都属于复分解反应,盐与金属反应属于置换反应。
二、精选练习题知识点1 生活中常见的盐【典例】1.用符合要求的物质的序号填空。
①氯化钠②小苏打③二氧化碳④熟石灰(1)可用于治疗胃酸过多的是。
(2)可用于改良酸性土壤的是。
2.在河边有A、B、C、D四家工厂向河中排放废水,每个工厂的废水中含有NaOH、HCl、MgCl2、Na2CO3四种物质中的一种.某中学环保小组对该河流的污染状况进行检测,发现:A处河水能使紫色石蕊试液变蓝色;F处河水出现白色浑浊;E处河水有大量气泡产生.试推断:(1)A工厂排放的废水中含有的污染物是;(2)C工厂排放的废水中含有的污染物是;(3)E处发生反应的化学方程式为:.【变式训练】1.服用可溶性的钡盐可使人中毒.医疗水用X射线检查胃肠疾病时,可作为“钡餐”让病人服用的是()A.BaCl2B.Ba(OH)2C.BaCO3D.BaSO42.酸、碱、盐在工农业生产和日常生活中应用广泛.下列做法错误的是()A.用石灰乳与硫酸铜溶液配制农药波尔多液B.用稀盐酸除去铁制品表面的铁锈C.用食盐水除去水壶中的水垢D.用NaOH溶液洗涤石油产品中残留的硫酸3.下列物质俗称小苏打的是()A.碳酸钠B.碳酸氢钠C.氢氧化钠D.硫酸钠4.食盐、食醋、纯碱均是家庭厨房中常用的物质,利用这些物质,我能够完成的实验是()①检验自来水中是否含有氯离子;②除去热水瓶中的水垢;③区分食盐和纯碱;④检验鸡蛋壳中是否含有碳酸盐。