吡格列酮杂质总结经验分享
- 格式:pdf
- 大小:318.94 KB
- 文档页数:3
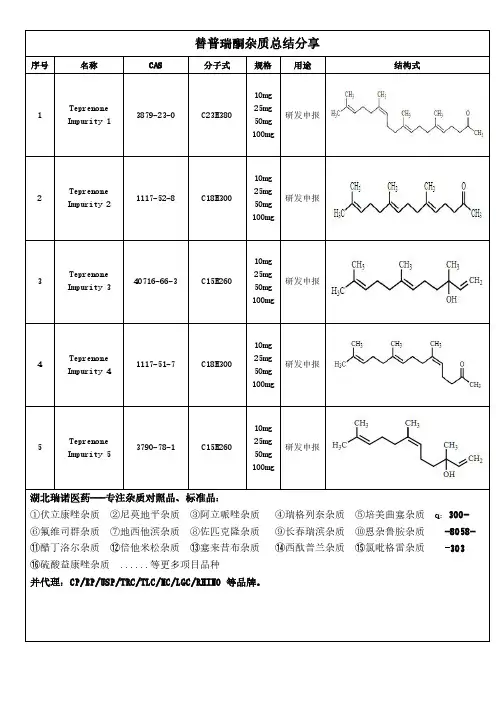
替普瑞酮杂质总结分享
序号
名称
CAS
分子式
规格
用途
结构式
1
Teprenone Impurity 1
3879-23-0C23H38O
10mg 25mg 50mg 100mg
研发申报
2
Teprenone Impurity 2
1117-52-8C18H30O
10mg 25mg 50mg 100mg
研发申报
3
Teprenone Impurity 3
40716-66-3C15H26O
10mg 25mg 50mg 100mg
研发申报
4
Teprenone Impurity 4
1117-51-7C18H30O
10mg 25mg 50mg 100mg
研发申报
5
Teprenone Impurity 5
3790-78-1C15H26O
10mg 25mg 50mg 100mg
研发申报
湖北瑞诺医药---专注杂质对照品、标准品:①伏立康唑杂质②尼莫地平杂质③阿立哌唑杂质④瑞格列奈杂质⑤培美曲塞杂质q:300-
⑥氟维司群杂质⑦地西他滨杂质⑧佐匹克隆杂质⑨长春瑞滨杂质⑩恩杂鲁胺杂质-8058-⑪醋丁洛尔杂质⑫倍他米松杂质
⑬塞来昔布杂质
⑭西酞普兰杂质
⑮氯吡格雷杂质
-303
⑯硫酸益康唑杂质......等更多项目品种
并代理:CP/EP/USP/TRC/TLC/MC/LGC/RHINO 等品牌。


什么是基因毒性杂质对于基因毒性杂质的定义主要是指:在以DNA 反应物质为主要研究对象的体内/ 体外试验中,如果发现它们对DNA 有潜在的破坏性,那可称之为基因毒性。
对没有进行体内实验的情况下,也可以根据关联系做一些相关的体外实验去评估该物质在体内的毒性。
如果没有关联评估的,体外基因毒性物质经常被考虑为假定的体内诱变剂和致癌剂。
GUIDELINE ON THE LIMITS OF GENOTOXIC IMPURITIES ( EMEA/CHMP/QWP/251344/2006 )基因毒性杂质的风险按照目前的法规来说,(体内)基因毒性物质在任何摄入量水平上对DNA 都有潜在的破坏性,这种破坏可能导致肿瘤的产生。
因此,对于基因毒性致癌物,不能说“不存在明显的阀值,或是任何的摄入水平都具有致癌的风险”。
可接受风险的摄入量对于那些可以与DNA 进行反应的化合物,由于在较低的剂量时机体保护机制可以有效的运行,按照摄入量由高到低所造成的影响进行线性推断是很困难的。
目前,对于一个给定诱变剂,我们很难从实验方面证明它的基因毒性存在一个阀值。
特别是对某些化合物,它们可以与非DNA 靶点进行反应,或一些潜在的突变剂,在与关键靶位结合之前就迅速失去了毒性。
由于缺乏支持基因毒性阀值存在的有力证据,而使得我们很难界定一个安全的服用量。
所以有必要采取一个新观点:确定一个可接受其风险的摄入量。
可接受其风险的摄入量即毒理学阈值一般通用的被定义为Threshold of Toxicological Concern (TTC)。
具体含义为:一个“ 1.5ug/day ”的TTC 值,即相当于每天摄入1.5ug 的基因毒性杂质,被认为对于大多数药品来说是可以接受的风险(一生中致癌的风险小于100000 分之1 )。
按照这个阀值,可以根据预期的每日摄入量计算出活性药物中可接受的杂质水平。
在特定的条件下一些基因毒性杂质也可以有较高的阈值。



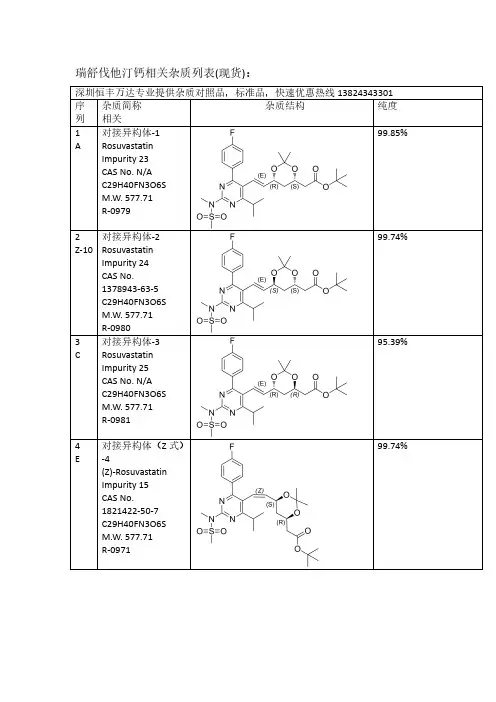
瑞舒伐他汀钙相关杂质列表(现货):深圳恒丰万达专业提供杂质对照品,标准品,快速优惠热线138****3301序列杂质简称相关杂质结构纯度1A 对接异构体-1RosuvastatinImpurity 23CAS No.N/A C29H40FN3O6S M.W.577.71R-097999.85%2Z-10对接异构体-2RosuvastatinImpurity 24CAS No.1378943-63-5C29H40FN3O6S M.W.577.71R-098099.74%3C 对接异构体-3RosuvastatinImpurity 25CAS No.N/A C29H40FN3O6S M.W.577.71R-098195.39%4E对接异构体(Z 式)-4(Z)-Rosuvastatin Impurity 15CAS No.1821422-50-7C29H40FN3O6S M.W.577.71R-097199.74%5Q对接光降解-1CAS No.N/A C29H40FN3O6S M.W.577.71R-099099.31%6P对接光降解-2CAS No.N/A C29H40FN3O6S M.W.577.71R-099299.69%7I丙酮加合物CAS No.N/A C32H46FN3O7S M.W.635.7998.23%8Z-12对接脱氟CAS No.N/AC29H41N3O6S M.W.559.72R-099399.46%9Z-16双键环氧脱丙酮叉CAS No.N/AC29H40FN3O7S M.W.593.7199.18%10B脱丙酮叉异构体-1ent-Rosuvastatin tert-Butyl Ester CAS No.615263-60-0C26H36FN3O6S M.W.537.65R-091899.90%11Z-11脱丙酮叉异构体-2(3S,5S)-Rosuvastatintert-Butyl Ester CAS No.2185805-16-5C26H36FN3O6S M.W.537.65R-097699.66%12D 脱丙酮叉异构体-3(3R,5R)-tert-ButylRosuvastatin (Rosuvastatin Impurity)CAS No.2162136-65-2C26H36FN3O6S M.W.537.65R-0911100%13F 脱丙酮叉异构体(Z 式)-4CAS No.1821422-51-8C26H36FN3O6S M.W.537.65R-099699.44%14S脱丙酮叉光降解-1CAS No.N/A C26H36FN3O6S M.W.537.65R-098999.61%15R脱丙酮叉光降解-2CAS No.N/A C26H36FN3O6S M.W.537.65R-099199.20%16J丙酮加合物脱丙酮叉Rosuvastatin EP Impurity A CAS No.1714147-49-5C29H42FN3O7S M.W.595.72R-099799.65%17Z-13无氟脱丙酮叉CAS No.N/AC26H37N3O6S M.W.519.65R-099599.17%18Z-255-甲氧基脱叉杂质RosuvastatinImpurity 42CAS No.N/A C27H38FN3O6S M.W.551.67R-0910098.80%19Z-263-甲氧基脱叉杂质RosuvastatinImpurity 47CAS No.N/A C27H38FN3O6S M.W.551.67R-0910598.65%203,5-二甲氧基脱叉杂质Rosuvastatin Impurity 44CAS No.N/A C28H40FN3O6S M.W.565.70R-0910698%21G钙盐异构体-1Rosuvastatin EP Impurity G Calcium Salt CAS No.1242184-42-4(free acid)C22H27FN3O6S.1/2Ca M.W.480.5420.0499.88%22Z-1钙盐异构体-2(3S,5S)Rosuvastatin Calcium Salt CAS No.1584149-34-7(free acid)C22H27FN3O6S.1/2Ca M.W.480.5420.04R-091598.15%23H钙盐异构体-3Rosuvastatin EP Impurity B Calcium Salt(3R,5R)-Rosuvastatin Calcium Salt CAS No.1422515-55-61094100-06-7(free acid)C22H27FN3O6S.1/2Ca M.W.480.5420.04R-091296.13%24V钙盐异构体(Z 式)-4Rosuvastatin Z-Isomer Calcium Salt CAS No.1444772-08-01445208-17-2(free acid)C22H27FN3O6S.1/2Ca M.W.480.5420.0499.51%25Z-245-甲氧基钠盐CAS No.N/AC23H29FN3NaO6S M.W.517.5599.50%26Z-273-甲氧基钠盐CAS No.N/AC23H29FN3NaO6S M.W.517.5596.83%27Z-293,5-二甲氧基钠盐CAS No.N/AC24H31FN3NaO6S M.W.531.5797.78%28U钙盐异构体光降解-5RosuvastatinImpurity 1Calcium Salt CAS No.854898-49-0854898-48-9(free acid)C22H27FN3O6S.1/2Ca M.W.480.5420.0499.75%29T 钙盐异构体光降解-6RosuvastatinImpurity 2Calcium Salt CAS No.854898-50-3854898-53-6(free base)C22H27FN3O6S.1/2Ca M.W.480.5420.0499.83%30Z-18钠盐异构体光降解-7(混合物)RosuvastatinImpurity 1Calcium SaltCAS No.N/A C22H27FN3O6S.1/2Ca M.W.480.5420.04R-093499.16%31Z-20钙盐异构体光降解-8Rosuvastatin Impurity CAS No.N/A C22H26FN3O6S M.W.479.5296.69%32Z-14钙盐无氟DesfluoroRosuvastatin Calcium Salt CAS No.N/A847849-66-5(acid)C22H28N3O6S.1/2Ca M.W.462.5420.04R-099499.78%33K 丙酮加合物钙盐Rosuvastatin EPImpurity A Calcium Salt CAS No.1714147-47-31715120-13-0(free acid)C25H33FN3O7S.1/2Ca M.W.538.6120.04R-092599.46%34M 内酯Rosuvastatin EPImpurity D CAS No.503610-43-3C22H26FN3O5S M.W.463.52R-09199.46%35N 内酯异构体CAS No.N/AC22H26FN3O5S M.W.463.5299.46%36内酯异构体CAS No.N/A C22H26FN3O5S M.W.463.5297%37Z-283-甲氧基内酯CAS No.N/AC23H28FN3O5S M.W.477.5598.97%38L5-氧代Rosuvastatin EP Impurity C freed acid CAS No.1620823-61-1(sodium salt)1422619-13-3(acid)C22H26FN3O6S M.W.479.5297.92%39Z-63-氧代3-Oxo Rosuvastatin Sodium Salt CAS No.1346606-28-71346747-49-6(acid)C22H25FN3O6S.Na M.W.478.5222.99R-091798.61%40O内酯脱水Rosuvastatin2,6-Diene Lactone Impurity CAS No.1246665-85-9C22H24FN3O4S M.W.445.5299.36%R-094141Z-44,6-二烯Rosuvastatin4,6-Diene Impurity CAS No.1422954-13-9C22H26FN3O5S M.W.463.53R-092795.44%42Z-152,6-二烯CAS NO.1422954-12-8(free acid)C22H26FN3O5S R-092695.70%43Z-8脱甲基二钠盐(体内代谢产物)N-Desmethyl Rosuvastatin Disodium Salt CAS No.371775-74-5(free base)C21H24FN3O6S.2Na M.W.465.50222.99R-09598.87%44W光降解内酯CAS No.854898-47-8C22H26FN3O5S M.W.463.5299.80%45X 光降解内酯CAS No.854898-46-7C22H26FN3O5S M.W.463.5297.84%46Z-2Z 式异构体内酯CAS No.N/A C22H26FN3O5S M.W.463.5296.52%47Z-9脱甲基内酯(体内代谢产物)N-Desmethyl Rosuvastatin Lactone CAS:1797419-58-9C21H24FN3O5S M.W.449.5097.42%48Z-7基因毒性杂质(体内代谢产物)Rosuvastatin Impurity 28CAS No.N/A C22H28FN3O7S M.W.497.54R-098498.94%49Z-5母核烯醛(工艺相关杂质)CAS No.890028-66-7C18H20FN3O3S M.W.377.4398.85%50Z-42母核无氟膦盐CAS No.N/A C34H35BrN3O2PS M.W.660.6099.14%51Y 本体脱丙酮叉CAS No.N/A C26H36FN3O6S M.W.537.6599.74%更多其他项目:雷西纳德,阿格列汀,依鲁替尼,唑吡坦,利奈唑胺,西他沙星,沙丁胺醇,罗替戈汀,丙戊酸钠,左乙拉西坦,西格列汀,特地唑胺,帕瑞昔布钠,帕布昔利布,赛乐西帕,伏硫西汀,曲格列汀,米拉贝隆,沙芬酰胺,达泊西汀,吡格列酮,达泊西汀,吉非替尼,去甲肾上素,阿昔洛韦,文拉法辛,普拉洛芬,普拉克索,曲唑酮,茚达特罗,阿扎胞苷,酮替芬,依折麦布,西那卡塞,氨曲南,替诺福韦,厄多司坦,孤法辛,雷贝拉唑,阿法替尼,依达拉奉,帕利哌酮,达比加群酯,鲁拉西酮,尼非卡兰,瑞巴派特,苯达莫司汀,利伐沙班,法舒地尔,普拉格雷,维格列汀,索非布韦,文拉法辛等。

▲盐酸吡格列酮定义以干燥品计,盐酸吡格列酮含C19H20N2O3S²HCl不少于98.0%不大于102.0%。
鉴别²A.红外吸收《197》²B.常规鉴别氯化物《191》:称取25mg盐酸吡格列酮溶解于0.5ml硝酸,加入2ml稀硝酸。
结果符合氯化物检验的要求。
²C.照含量测定项下记录色谱图,供试品溶液的主峰保留时间与标准品溶液的主峰保留时间一致。
含量测定²操作流动相:乙腈-0.1M醋酸铵-冰醋酸(25:25:1)标准品溶液:制备一份USP盐酸吡格列酮标准品溶液,先用甲醇稀释浓度为0.5mg/mL,再用流动相稀释制成含盐酸吡格列酮50ug/mL的溶液。
系统适用性储备液:用甲醇配制含USP盐酸吡格列酮标准品0.5mg/mL和含二苯甲酮0.13mg/mL的溶液。
系统适用性溶液:用流动相将系统适用性储备液稀释成含盐酸吡格列酮50ug/mL和含二苯甲酮13ug/mL的溶液。
样品溶液:用甲醇配制一份含盐酸吡格列酮0.5mg/mL的溶液,再用流动相稀释成含盐酸吡格列酮50ug/mL的溶液。
色谱系统(见色谱《621》,系统适用性。
)方法:液相色谱法检测器:UV 269nm色谱柱:4.6mm³15cm;5um 填料 L1柱温:25±2.5°流速:0.7mL/min。
[注:调整流速使吡格列酮峰的保留时间在7min左右。
]进样量:20uL系统适用性样品:系统适用性溶液和标准品溶液[注:吡格列酮和二苯甲酮的相对保留时间分别约为1.0和2.6。
]适用性要求拖尾因子:系统适用性溶液中,吡格列酮和二苯甲酮的拖尾因子不大于1.5分离度:系统适用性溶液中,吡格列酮和二苯甲酮之间的分离度不小于15相对标准偏差:标准品溶液六次重复进样的相对标准偏差不大于2.0%分析样品:标准品溶液和样品溶液通过下列公式计算盐酸吡格列酮中含C19H20N2O3S²HCl的百分比:结果=(r U/ r S)³(c U/c S)³100r U=样品溶液的峰响应值r S =标准品溶液的峰响应值c S=标准品溶液中USP盐酸吡格列酮标准品的浓度(ug/mL)c U=样品溶液中盐酸吡格列酮的浓度(ug/mL)可接受标准:干燥品含量为98.0%—102.0%。

第三章 药物的杂质检查杂质(forin 、impurities )是指:1. 有毒副作用的物质2. 本身无毒副作用,但影响药物的稳定性和疗效的物质3. 本身无毒副作用,也不影响药物的稳定性和疗效,但影响药物的科学管理的物质药物中杂质的来源1. 生产过程中引入(1)原料、反应中间体及副产物(2)试剂、溶剂、催化剂类(3)生产中所用金属器皿、装置以及其他不耐酸、碱的金属工具所带来的杂质2. 贮藏过程中产生水解、氧化、分解、异构化、晶形转变、聚合、潮解和发霉等易发生水解反应的结构:酯、内酯、酰胺、卤代烃、苷类等药物中的杂质按来源分为1. 一般杂质(general impurities )如氯化物、硫酸盐、铁盐、重金属、砷盐、酸、碱、水分、易炭化物、炽灼残渣等。
一般杂质的检查方法收载在中国药典的附录中。
2. 特殊杂质(special impurities ):指某一个或某一类药物的生产或贮藏过程中引入的杂质,如阿司匹林中的游离水杨酸、异烟肼中的游离肼、甾体激素中的有关物质。
特殊杂质检查方法收载在中国药典正文各药品的质量标准中。
杂质限量:指药物中允许杂质存在的最大量,通常用百分之几或百万分之几来表示药物的杂质检查法1. 对照法限量检查法 (Limit Test )特点:不需知道杂质的准确含量2. 灵敏度法系指在供试品溶液中加入试剂,在一定反应条件下,不得有正反应出现。
特点:不需对照物质3. 比较法含量测定法:测定杂质的绝对含量,如测定吸光度、pH 值等。
特点:准确测定杂质的量,不需对照品杂质限量的计算供试品量允许杂质存在的最大量杂质限量一般杂质检查规则《药品检验操作标准》规定:1. 遵循平行操作原则(1)仪器的配对性:如纳氏比色管应配对,刻度线高低相差不超过 2mm ,砷盐检查时导气管长度及孔的大小要一致(2)对照品与供试品同步操作2. 正确的比色、比浊方法3. 检查结果不符合规定或在限度边缘时应对供试管和对照管各复查二份氯化物检查法(一)原理 对照法检查方法 药典附录除另有规定外,取各药品项下规定量的供试品,加水溶解使成25ml (溶液如显碱性,可滴加硝酸使成中性),再加稀硝酸10m1;溶液如不澄清,应滤过;置50ml 纳氏比色管中,加水使成约40m1,摇匀,即得供试溶液。

降糖药吡格列酮合成方法的比较与评价本文对降糖药吡格列酮的合成方法进行了归纳整理,对其操作步骤和特点作了概括总结,并分析了每种合成方法的特点,提出了汇聚式的合成路线是适合工业化的绿色环保工艺,可根据具体生产的实际情况选择适当方法。
[Abstract] A systematically review of the synthesis methods of Pioglitazone are summarized in this paper. The basic manipulation procedures are illustrated for each of the ten synthetic routes. Evaluation and comparison are also discussed for the further development of the industrial process.[Key words] Pioglitazone; Synthetic routes;Evaluation吡格列酮(Pioglitazone,1),化学名为5-[4-[2-(5-乙基-2-吡啶)乙氧基]苯甲基]-2,4-噻唑烷二酮[5-[4-[2-(ethyl-2-pyridyl)ethoxy] benzyl]-2,4-thiazolidinedione],商品名:瑞彤、安可拓,别名:ADD-3878,CA收录号:111025-46-8,临床用其盐酸盐。
该药是日本武田公司开发的噻唑烷二酮类降糖药,1999年首次在美国上市。
其主要作用机制为高选择性地激活过氧化物酶体增生物激活受体(PPAR)-γ,增强外围组织对胰岛素的敏感性,调节胰岛素应答基因的转录,降低胰岛素抵抗,控制血糖的生成、转运和利用,从而降低血糖,临床主治2型糖尿病[1-2]。
分析吡格列酮化学结构(图1),综合其相关文献[3],结合逆向合成推理,根据其骨架构建方式将其合成方法分为两大类,即“(A+B)+C”和“A+(B+C)”,本文将依此对1的合成方法进行归纳总结和评价比较。

专业承接美国、日本、法国、德国、瑞士、意大利、英国等国家参比制剂一次性进口和代购业务,提供进口(EP、USP、LGC、BP、TLC、TRC、QCC、MC)和国产对照品,有需要的欢迎联系我咨询哈.市振强生物技术劳先生QQ3004867396各种杂质名称及英文名:依鲁替尼(Ibrutinib)杂质6个,palbociclib杂质6个,泰地唑胺杂质tedizolid phosphate 12个达格列净杂质Dapagliflozin 7个,索非布韦杂质sofosbuvir 20个,替卡格雷杂质Ticagrelor 14个,米拉贝隆杂质Mirabegron 10个,TAK 438杂质10个,沃替西汀杂质Vortioxetine 15个,LCZ696杂质6个非布司他杂质Febuxostat 14个泊沙康唑异构体Posaconazole 14个阿普斯特杂质Apremilast 6个阿奇霉素杂质Azithromycin 14个阿考替胺杂质Acotiamide 14个依托考昔杂质Etoricoxib 14个尼达尼布杂质Nintedanib 8个罗库溴铵杂质Rocuronium Bromide 8个恩杂鲁胺杂质Enzalutamide 4个卢帕他定杂质Rupatadine 6个瑞格非尼杂质Regorafenib 20个色瑞替尼杂质Ceritinib 11个依美斯汀杂质Emedastine8个依匹唑派杂质Brexpiprazole6个依帕司他杂质epalrestat 6个乌苯美司杂质Ubenimex 19个福多司坦杂质Fudosteine 6个马来酸匹杉琼杂质Maleic acid Chinese fir, Joan 6个扎鲁司特杂质Zafirlukast 6个贝利司他杂质belinostat 6个奥扎格雷的杂质ozagrel 6个酒石酸伐尼克兰片杂质Varenicline T artrate T ablets 6个莫扎伐普坦杂质Mozavaptan 5个沙芬酰胺杂质Safinamide 4个沃雷生杂质suvorexant 5个依替巴肽杂质Eptifibatide 5个乐伐替尼杂质lenvatinib 8个1.埃索美拉唑杂质esomeprazole impurity2.奥拉西坦杂质oxiracetam3.罗氟司特杂质roflumilast4.阿戈美拉汀杂质Agomelatine5.鲁拉西酮杂质Lurasidone6.莫西沙星杂质moxifloxacin7.阿齐沙坦杂质Azilsartan8.达比加群酯杂质Pradaxa9.利拉利汀杂质Linagliptin10.托法替尼杂质T ofacitinib11.依托考昔杂质12.阿西替尼杂质Axitinib13.维格列汀杂质Vildagliptin14.帕瑞昔布杂质parecoxib15.伊马替尼杂质imatinib16.阿哌沙班杂质Apixaban17.替诺福韦酯杂质T enofovir Disoproxil Fumarate18.普拉格雷杂质Prasugrel19.伊拉地平杂质isradipine20.利托那韦杂质ritonavir21.培美曲塞二钠杂质pemetrexed disodium22.依达拉奉杂质Edaravone23.吉非替尼杂质gefitinib24.替吉奥杂质BCB25.苯达莫司汀杂质Cephalon26.替加环素杂质Tigecycline27.布南色林杂质Blonanserin28.文拉法辛杂质venlafaxine29.替卡格雷杂质30.利伐沙班杂质Rivaroxaban31.伊曲茶碱杂质Istradefylline32.依度沙班杂质Edoxaban33.三氟胸苷杂质Trifluorothymidine34.盐酸阿考替胺杂质acotiamide hydrochloride35.度洛西汀杂质Duloxetine36.泊沙康唑杂质37.泰地唑胺杂质38.沃替西汀杂质39.乐伐替尼杂志40.卡博替尼杂质Cabozantinib41.依鲁替尼杂质42.恩格列净杂质EMpagliflozin43.辛伐他汀杂质simvastatin44.恩杂鲁胺杂质45. 阿苯达唑Albendazole46. 阿达帕林adapalene47. 阿夫唑嗪alfuzosin48. 阿卡地新acadesine49. 阿立哌唑aripiprazole50. 阿莫曲普坦almotriptan51. 阿莫西林amoxicillin52. 阿瑞吡坦Aprepitant53. 阿昔洛韦acyclovir54. 埃罗替尼erlotinib55. 安非他酮bupropion56. 氨苄青霉素ampicillin57. 氨基葡萄糖Glucosamine58. 氨甲环酸tranexamic59. 氨溴索Ambroxol60. 胺碘酮Amiodarone61. 奥氮平olanzapine62. 奥沙利铂Oxaliplatin63. 奥司他韦oseltamivir64. 保胆键素dihydroxydibutylether65. 保特佐米Bortezomib66. 苯达莫司汀Bendamustin67. 比卡鲁胺bicalutamide68. 吡罗昔康piroxicam69. 吡嗪酰胺Pyrazinamide70. 别嘌醇allopurinol71. 波生坦bosentan72. 布洛芬Ibuprofen73. 布美他尼Bumetanide74. 雌甾四烯estratetraenol75. 醋氯芬酸aceclofenac76. 达非那新Darifenacin77. 大黄酸Diacerein78. 地尔硫卓diltiazem79. 地拉罗司deferasirox80. 氨氯地平Amlodipine81. 硝苯地平nifedipine82. 甲氨蝶呤Methotrexate83. 氨基蝶呤Aminopterin84. 丁螺环酮buspirone85. 多奈哌齐Donepezi86. 多立酮Domperidone87. 恩丹西酮ondansetron88. 恩他卡朋entacapone89. 伐昔洛韦valacyclovir90. 泛昔洛韦famciclovir91. 非布索坦Febuxostat92. 非那雄胺inasteride-ep93. 非诺贝特fenofibrate94. 弗斯特罗定fesoterodine95. 伏立康唑Voriconazole96. 氟替卡松丙酸酯fluticasone-propionate97. 氟维司群Fulvestrant98. 格列吡嗪glipizide99. 桂利嗪cinnarizine100. 环苯扎林cyclobenzaprine101. 加巴喷丁gabapentin102. 甲状旁腺激素西那卡塞Cinacalcet 103. 甲状腺素Levothyroxine104. 卡巴拉汀利凡斯的明Rivastigmine RC's 105. 喹硫平Quetiapine106. 奥美拉唑Omeprazole107. 兰索拉唑Lansoprazol108. 雷贝拉唑Rabeprazole109. 泮托拉唑pantoprazol110. 来氟米特leflunomide111. 雷洛昔芬raloxifene112. 雷莫拉宁Ramoplanin113. 雷奈佐利Linezolid114. 利伐沙班Rivaroxaban115. 利培酮Risperidal116. 罗匹尼罗ropinirole117. 阿替洛尔Atenolol118. 比索洛尔Bisoprolol119. 醋丁洛尔Acebutolol120. 美托洛尔metoprolol121. 奈必洛尔nebivolol122. 氯吡格雷Clopidogrel123. 氯雷他定Loratadine124. 霉酚酸mycophenolate125. 美洛昔康meloxicam126. 孟鲁司特montelukast127. 米氮平mirtazapine128. 尼美舒利nimesulide129. 帕罗西汀Paroxetine130. 帕立酮Paliperidone131. 生丁Dipyridamole Dipyridamole 132. 培美曲塞二钠Pemetrexed-disodium 133. 普拉克索Pramipexole134. 喹那普利Quinapril135. 卡托普利captopril136. 赖诺普利Lisinopril137. 雷米普利Ramipril138. 培哚普利Perindopril Imp139. 群多普利Trandolapril140. 伊拉普利Enalapril141. 普瑞巴林pregabalin142. 瑞格列奈Repaglinide143. 塞来西布Celecoxib144. 噻托溴铵Tiotropium bromide 145. 沙丁胺醇salbutamol146. 沙美特罗salmeterol147. 奥美沙坦Olmesartan148. 坎地沙坦Candesartan 149. 罗沙坦Losartan150. 替米沙坦T elmisartan 151. 缬沙坦Valsartan152. 加替沙星gatifloxacin 153. 氟哌酸norfloxacin154. 菲宁达、氧氟沙星Ofloxacin 155. 恩诺沙星enrofloxacin 156. 环丙沙星Ciprofloxacin 157. 莫西沙星moxifloxacin 158. 左氧氟沙星Levofloxacin 159. 舍曲林Sertraline160. 舒马曲坦sumatriptan 161. 双醋瑞因diacerein 162. 双氯芬酸Diclofenac 163. 他达那非T adalafil 164. 阿托伐他汀atorvastatin 165. 洛伐他汀Lovastatin 166. 匹伐他汀pitavastatin 167. 普伐他汀pravastatin 168. 瑞舒伐他汀Rosuvastatin 169. 辛伐他汀Simvastatin170. 坦索罗辛T amsulosin 171. 格列美脲glimepiride172. 吡格列酮pioglitazone 173. 尼扎替丁nizatidine 174. 替卡西林Ticarcillin 175. 酮咯酸氨丁三醇Ketorolac 176. 酮基布洛芬Ketoprofen 177. 头孢氨苄cefalexin178. 头孢克洛cefaclor179. 头孢磺啶cefsulodin 180. 托特罗定tolterodine 181. 拓扑替康topotecan 182. 万古霉素vancomycin 183. 文拉伐辛Venlafaxine 184. 那非Sildenafil185. 西他列汀Sitagliptin 186. 西酞普兰Citalopram 187. 西替利嗪cetirizine 188. 伊立替康Irinotecan 189. 伊马替尼imatinib190. 伊曲康唑Itraconazole 191. 依泽替米贝ezetimibe192. 左乙拉西坦Levetiracetam193. 佐米曲普坦zolmitriptan194. 唑吡坦zolpidem195. 唑尼沙胺Zonisamide依鲁替尼(Ibrutinib)杂质6个,palbociclib杂质6个,泰地唑胺杂质tedizolid phosphate 12个达格列净杂质Dapagliflozin 7个,索非布韦杂质sofosbuvir 20个,替卡格雷杂质Ticagrelor 14个,米拉贝隆杂质Mirabegron 10个,TAK 438杂质10个,沃替西汀杂质Vortioxetine 15个,LCZ696杂质6个非布司他杂质Febuxostat 14个泊沙康唑异构体Posaconazole 14个阿普斯特杂质Apremilast 6个阿奇霉素杂质Azithromycin 14个阿考替胺杂质Acotiamide 14个依托考昔杂质Etoricoxib 14个尼达尼布杂质Nintedanib 8个罗库溴铵杂质Rocuronium Bromide 8个恩杂鲁胺杂质Enzalutamide 4个卢帕他定杂质Rupatadine 6个瑞格非尼杂质Regorafenib 20个色瑞替尼杂质Ceritinib 11个依美斯汀杂质Emedastine8个依匹唑派杂质Brexpiprazole6个依帕司他杂质epalrestat 6个乌苯美司杂质Ubenimex 19个福多司坦杂质Fudosteine 6个马来酸匹杉琼杂质Maleic acid Chinese fir, Joan 6个扎鲁司特杂质Zafirlukast 6个贝利司他杂质belinostat 6个奥扎格雷的杂质ozagrel 6个酒石酸伐尼克兰片杂质Varenicline T artrate T ablets 6个莫扎伐普坦杂质Mozavaptan 5个沙芬酰胺杂质Safinamide 4个沃雷生杂质suvorexant 5个依替巴肽杂质Eptifibatide 5个乐伐替尼杂质lenvatinib 8个。
HPLC法测定吡格列酮二甲双胍片中盐酸吡格列酮的有关物质雍春赵琛杭州华东医药集团生物工程研究所有限公司杭州 310011[摘要] 目的:建立吡格列酮二甲双胍片中盐酸吡格列酮有关物质的高效液相色谱方法。
方法:采用为依利特C18色谱柱(250×4.6mm, 5μm);以水-乙腈-乙酸=550:450:1.2(用氨试液调节pH值至5.8)作为流动相;检测波长为225nm。
结果:三批样品(BE1101、BE1102、BE1103)盐酸吡格列酮单个杂质(%)分别为0.15、0.14、0.14;有关物质(%)分别为0.22、0.21、0.21。
结论:采用HPLC法测定盐酸吡格列酮有关物质方法简便,结果准确可靠,二甲双胍无干扰。
关键词:吡格列酮二甲双胍片;盐酸吡格列酮;有关物质;高效液相色谱方法HPLC method for determinnation of the related substances of Pioglitazone hydrochloride of Pioglitazone Metformin TabletsChun Yong(Hangzhou Huadong Medicine Group, Institute of Biological Engineering Co., Ltd. hangzhou 310011)Abstract Purpose: To establish an RP- HPLC method for determinnation of the related substances of Pioglitazone hydrochloride of Pioglitazone Metformin Tablets . Methods: The separation was performed on an Elite C18column (250 × 4.6mm, 5μm); and the mobile phase consisted of water - acetonitrile - acetic acid = 550:450:1.2 (ammonia solution adjusted to pH5.8).The detection was set at 225nm. Results: The three batches of samples(BE1101,BE1102,BE1103) hydrochloride pioglitazone single impurity (%) were 0.15,0.14,0.14; related substances (%) were 0.22,0.21,0.21. Conclusion: the method for determination of pioglitazone hydrochloride related substances method is simple, accurate and reliable, metformin no interference.Keywords:Pioglitazone Metformin Tablets; pioglitazone hydrochloride; related substances; HPLC盐酸吡格列酮(pioglitazone HC1)/盐酸二甲双胍(meformin HC1)片是日本武田制药株式会社研制开发的一种新型用于治疗Ⅱ型糖尿病的复方口服制剂。
吡格列酮结构
引言概述:
吡格列酮(Pioglitazone)是一种口服抗糖尿病药物,属于胰岛素增敏剂,用于治疗2型糖尿病。
吡格列酮结构具有独特的化学特性和作用机制,对于了解其药理学和药效学具有重要意义。
本文将从吡格列酮的结构特点、作用机制、药效学、药代动力学以及副作用等五个大点进行阐述。
正文内容:
1. 吡格列酮的结构特点
1.1 吡格列酮的分子式和分子量
1.2 吡格列酮的化学结构
1.3 吡格列酮的物理性质
2. 吡格列酮的作用机制
2.1 吡格列酮与PPAR-γ的相互作用
2.2 吡格列酮对胰岛素抵抗的调节作用
2.3 吡格列酮对脂肪组织的影响
3. 吡格列酮的药效学
3.1 吡格列酮的降糖效果
3.2 吡格列酮的胰岛素增敏作用
3.3 吡格列酮对血脂的调节作用
4. 吡格列酮的药代动力学
4.1 吡格列酮的吸收与分布
4.2 吡格列酮的代谢与消除
4.3 吡格列酮的药物相互作用
5. 吡格列酮的副作用
5.1 吡格列酮的常见副作用
5.2 吡格列酮的严重副作用
5.3 吡格列酮的禁忌症和注意事项
总结:
综上所述,吡格列酮作为一种胰岛素增敏剂,具有独特的化学结构和作用机制。
其通过与PPAR-γ的相互作用、调节胰岛素抵抗以及对脂肪组织的影响,发挥降糖、胰岛素增敏和调节血脂的作用。
在药代动力学方面,吡格列酮的吸收、分布、代谢和消除过程对其药效学产生重要影响。
然而,吡格列酮也存在一些副作用和禁忌症,需要患者在使用时注意。
因此,对于吡格列酮结构的深入了解,有助于我们更好地理解其药理学和药效学,从而更合理地应用于临床实践中。
[3]Menger MD,Richter S,Yamauchi J,et al.Role of m icrocir-culation in hepatic ischem ia/reperfusioninjury[J].Hepatogast ro-entero logy,1999,46(6):1452.[4]原金红,马茂,马振华.乌司他丁对大鼠肝脏缺血再灌注损伤治疗作用的研究[J].陕西医学杂志,2007,36(9):1134.[5]Vollmar B,Glasz J,Leiderer R,et al.Hepatic microcircula-tory perfusion failure is a determinant of liver dysfunction in warm ischemia-reperfusion[J].Am J Physiol,1994,145(6):1421.[6]Knowles RG,Moncada S.Nitric oxide synthase in mammals [J].Biochem J,1994,298(2):249.[7]Guix FX,Uribesalgo I,Coma M,et al.The physiology and pathophysiology of nitric oxide in the brain[J].2005,76(2):126.[8]Clemens MG.Nitric oxide in liver injury[J].Hepatoloty,1999,30(1):1.[9]Wullaert A,Van Loo G,Heyninck K,et al.Hepatic TNF signaling and NFkB:effects on liver homeostasis and beyond[J].Endocr Rev,2007,28(4):365.[10]Orrenius S,Zhivotovsky B,Nicotera P.Regulation of cell death:the calcium–apoptosis link[J].Nat Rev Cell Biol,2003,4(7):552.[11]Rizzuto R,Brini M,Murgia M,et al Microdomains with high Ca2+close to IP3-sensitive channels that are sensed by neighboring mitochondira[J].Science,1993,262(5134):744.[12]Goll DE,Thompson VF,Li H,et al.The Calpain system [J].Physiol Rev,2003,83(3):731.[13]Nakagawa T,Yuan J.Cross-talk between two cystenine protease families.Activation of caspase-12by calpain in apopto-sis[J].J Cell Biol,2000,150(4):887.[14]Wood DE,Newcomb EW.Caspase-dependent activation of calpain during drug-induced apoptosis[J].J Biol Chem,1999,274(12):8309.[15]Mandic A,Viktorsson K,Strandberg L,et al.Calpain-me-diated Bid cleavage and calpain–independent Bak modulation:two separate pathways in cisplatin-induced apoptosis[J].Mol Cell Biol,2002,22(9):3303.[收稿日期:2012-10-26编校:徐强]吡格列酮作用研究进展王立华(天津市宁河县医院,天津301500)[关键词]吡格列酮;内皮细胞;动脉硬化;降低尿酸胰岛素增敏剂噻唑烷二酮类药物吡格列酮(PIO)自1999年8月在美国上市以来逐渐受到医疗工作者的重视。
吡格列酮临床应用进展刘平;梁运珊;胡建华【期刊名称】《海南医学院学报》【年(卷),期】2006(12)6【摘要】噻唑烷二酮类药物(thiazolidinediones.TZDs)是一类新型的胰岛素增敏剂,主要包括:噻格列酮(ciglitazone)、曲格列酮(troglitazone)、罗格列酮(rosigtiaxone)、吡格列酮(piogltazone)、嗯格列酮(englitazone)等。
1997年曲格列酮被欧美及日本最早应用于临床。
发现曲格列酮可引起严重的肝脏毒性,甚至肝坏死,现已禁止使用。
1999年吡格列酮作为该类药中的第2种新药被美国食品和药品管理局(FDA)批准上市.我国自己研发的吡格列酮于2001年经中华人民共和国食品和药品监督管理局(CFDS)批准上市,该药降糖作用比曲格列酮强10倍,且无明显毒副作用。
【总页数】3页(P559-561)【作者】刘平;梁运珊;胡建华【作者单位】海南省海口市人民医院监管科,海南,海口,570208;海南省海口市人民医院监管科,海南,海口,570208;山东淄博第五中学医疗室,山东,淄博,255000【正文语种】中文【中图分类】R977.1+5【相关文献】1.复方盐酸吡格列酮二甲双胍缓释片中盐酸吡格列酮溶出度的测定 [J], 徐芳媛;李娟2.HPLC法测定吡格列酮二甲双胍片中盐酸吡格列酮的有关物质 [J], 雍春;赵琛3.吡格列酮临床应用进展 [J], 任跃忠;宋作珪;单江4.吡格列酮药典杂质5-羟基吡格列酮的一锅法合成 [J], 吴国芳;邓建梅;廖永志5.达格列净与吡格列酮联合二甲双胍治疗2型糖尿病的疗效及对胰岛素敏感性和胰岛α和β细胞功能的影响 [J], 黎俏洁因版权原因,仅展示原文概要,查看原文内容请购买。