纳氏试剂光度法测定水质氨氮不确定度的评估
- 格式:pdf
- 大小:189.99 KB
- 文档页数:4

浅谈纳氏试剂分光光度法对水中氨氮的测定摘要:水中氨氮含量会对其中的微生物产生一定的毒害影响,与此同时,生活污水中的氮氨含量超标,也会对人们身体带来一定伤害。
分光光度法是测定水中氮氨含量的常用方法,利用这一方法对水中氮氨浓度进行合理监测十分必要。
基于此,文章就纳氏试剂分光光度法对水中氨氮的测定展开了详细分析。
关键词:纳氏试剂分光光度法氨氮前言:氮氨是评价水环境质量的一项重要指标,研究其实际测定方法,由简单的比色法一直到常用的分光光度法,可以有效监测水环境整体质量,当前在分光光度法测定氮氨中,纳氏试剂十分常见。
基于此文章就纳氏试剂分光光度法测定水中氮氨展开了探究。
1 氨氮内容阐述水中氨氮的产生主要是因为生活污水在经过一定的微生物分解所产生的物质,当然在工业废水及农田排水中也包含这些物质。
城市食物残渣中通过微生物分解也会产生氨氮,另外农作物生长期间使用的氨氮肥料在分解后也会产生氮氨,然后随着生活污水排放到污水中。
另外,无氧环境里面,水中的亚硝酸在微生物的分解下会被还原成氨。
有氧条件下,水中的氨还会再次转变成硝酸盐。
对比水中的氨氮含量进行测定有助于了解水体的干净情况。
2 纳氏试剂分光光度法测定水中氨氮氨氮以离子的形式在水当中游离,二者的实际组成要结合水的酸碱性及水温情况判断。
若水中的酸度较高,那么游离的氨的成分就会升高,相反,水中的铵盐则会增高,而在不同水温情况下,这种情况却是相反的。
碘化汞及碘化钾碱性溶液和氨发生反应会形成淡红棕色胶态化合物,这种颜色能在宽波长中进行吸收,一般来讲用长度为的波长测定其吸光度,以此对水中的氨氮情况进行计算。
这种方法测定的氨氮浓度范围为0.025~2mg/L。
利用目视比色法,可以测出的最低浓度是0.02mg/L。
通过对水样进行简单的预处理,使用纳氏试剂分光光度法可以对工业废水、地表水及生活污水中的氨氮含量进行测定。
水样保存:将采集的水样放到玻璃瓶当中,及时对其展开实验分析,如有必要可以在其中添加适当的硫酸调节水中的酸碱度在2以内,然后控制存放温度在2~5℃,样品保存期间应防止玷污。

纳氏试剂分光光度法测定水中氨氮的测量不确定度评定1 检测方法1.1方法依据依据GB/T7479-1987《水质铵的测定纳氏试剂比色法》,对水中氨氮的测量不确定度进行评定。
1.2方法原理本方法使碘化汞和碘化钾的碱性溶液与氨反应生成淡红棕色胶态化合物,此颜色在较宽的波长内具强烈吸收,通常测定波长在410-425nm范围。
1.3仪器设备721分光光度计,玻璃量器:500ml,移液管(A)级,5.00Ml,移液管(A)级,50mL比色管。
1.4操作步骤1.4.1校准曲线的绘制1.4.1.1标准使用液的配置标准溶液由环境保护部标准样品研究所提供,编号为102206,质量浓度为500mg/L,扩展不确定度为5mg/L(k=2)。
用5.00mL无刻度吸管(A级)准确移取标准溶液5.00mL至500mL容量瓶(A级),用去离子水稀释至标线,配的质量浓度为5ug/mL的铵使用液,将标样稀释100倍。
1.4.1.2标准曲线绘制(1)分别吸取0,1.00,3.00,5.00,700和10.00mL,铵标准使用液于50mL比色管中,加水至标线。
(2)加1.0mL酒石酸钾钠溶液,混匀。
加1.5mL纳氏试剂,混匀。
放置10min后,在波长420mL处,用光程20mm比色皿,以水为参比测量吸光度。
(3)测得的吸光度,减去零溶液空白的吸光度,得到校正吸光度,绘制以氨氮含量(ug)对校正吸光度的校正曲线。
1.4.2 样品测定(1)分取适量经絮凝沉淀预处理后的污水水样(使氨氮含量不超过0.1mg),加入50mL比色管中,稀释至标线,以下同校准曲线绘制步骤(2),(3)。
(2)分取适量经蒸馏预处理后的馏出液,加入50mL比色管中,加一定量1mol/L,氢氧化钠以中和硼酸,稀释至标线。
以下同校准曲线绘制步骤(2),(3)。
1.4.3 空白实验以无氨水代替水样做全程序空白测定。
2数学模型校准曲线拟合的回归方程:y=a+bx式中:y----溶液的吸光度x-----从曲线查的的氨氮量,ug;a-----回归方程的截距b-----回归方程的斜率水中氨氮浓度的计算公式为:C=MV式中:c------水样中氨氮浓度m-------由校准曲线计算的氨氮量,同式(A11.1)中的x,ug;V------水样体积,ml。

科技创新□刘嘉玮摘要从氨氮的测定原理、使用试剂、实验室环境等方面分析其影响因素,并提出减小误差的方法。
关键词纳氏试剂;氨氮;影响因素;减小误差收稿日期:2018-03-15作者简介:刘嘉玮,女,满族,承德水文水资源勘测局,工程师。
氨氮是指水中以游离氨(NH3)和铵离子(NH4+)形式存在的氮,氨氮是水体中的营养素,可导致水富营养化现象产生。
也是水体中的主要耗氧污染物,会引起水生生物的死亡。
水中的氨氮可以在一定条件下转化成亚硝酸盐,如果长期饮用,水中的亚硝酸盐将和蛋白质结合形成亚硝胺,这是一种强致癌物质,对人体健康危害较大,所以氨氮的含量是评判水质的主要项目之一。
1.方法原理纳氏试剂分光光度法(HJ535-2009)是环境水体最广泛的氨氮测试方法,其测定原理是以游离态的氨或铵离子等形式存在的氨氮与纳氏试剂反应生成淡红棕色络合物,该络合物的吸光度与氨氮含量成正比,在420nm 处测定吸光度计算水体氨氮含量。
当水样体积为50mL ,使用20mm 比色皿时,本方法的检出限为0.025mg/L ,测定下限为0.10mg/L ,测定上限为2.0mg/L (均以N 计),如果水体氨氮值较高则取适量水样稀释后测定。
水体经适当预处理后,适用于地表水、地下水、污水及工业废水。
2.影响因素及解决方法2.1显色时间对测定的影响标准规定,放置10min 后,以水作参比,测量吸光度。
实际测定发现,小于10min 水样反应不完全,吸光度偏小;10~30min ,反应较完全,吸光度较稳定;第40min ,吸光度有所加深;50min 后吸光度减少。
由此可见样品的测定要在10~30min 内完成,这就要求实验人员测定样品时要及时、准确。
2.2实验室环境的影响大多实验室分析的项目较多,影响氨氮的项目较多,如总硬度和硝酸盐氮,他们在测定的过程中要用到氨水,氨水又极易挥发,使其污染实验器皿、试验用水和试剂,导致测定氨氮的数值偏高,所以要在独立、通风、无尘、无氨的实验室中对氨氮进行测定。

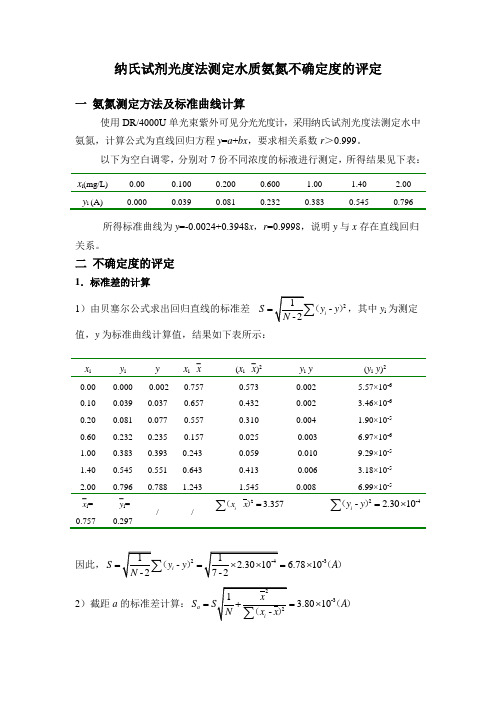
纳氏试剂光度法测定水质氨氮不确定度的评定一 氨氮测定方法及标准曲线计算使用DR/4000U 单光束紫外可见分光光度计,采用纳氏试剂光度法测定水中氨氮,计算公式为直线回归方程y =a +bx ,要求相关系数r >0.999。
以下为空白调零,分别对7份不同浓度的标液进行测定,所得结果见下表: x i (mg/L) 0.00 0.100 0.200 0.600 1.00 1.40 2.00 y i (A)0.0000.0390.0810.2320.3830.5450.796所得标准曲线为y =-0.0024+0.3948x ,r =0.9998,说明y 与x 存在直线回归关系。
二 不确定度的评定1.标准差的计算1)由贝塞尔公式求出回归直线的标准差2-i S y y =(),其中y i 为测定值,y 为标准曲线计算值,结果如下表所示: x iy iyx i -⎺x(x i -⎺x )2 y i -y(y i -y )2 0.00 0.000 -0.002 -0.757 0.573 0.002 5.57×10-6 0.10 0.039 0.037 -0.657 0.432 0.002 3.46×10-6 0.20 0.081 0.077 -0.557 0.310 0.004 1.90×10-5 0.60 0.232 0.235 -0.157 0.025 -0.003 6.97×10-6 1.00 0.383 0.393 0.243 0.059 -0.010 9.29×10-5 1.40 0.545 0.551 0.643 0.413 -0.006 3.18×10-5 2.00 0.796 0.788 1.243 1.5450.008 6.99×10-5⎺x i = 0.757⎺y i = 0.297//2- 3.357ix x =∑()2-4- 2.3010iy y =⨯∑()因此,2-3- 6.7810iS y y A ===⨯()() 2)截距a的标准差计算:-33.8010a S A ==⨯()3)斜率b的标准差计算:-313.7010(/())b S A mg L -==⨯⋅ 2.标准不确定度分量及自由度的计算1)截距a 的不确定度()33.8010a a u S A -==⨯(),按正态分布属A 类,自由度v a =7-1=6,传播系数()1--2.53a c b==2) 斜率b 的不确定度()31 3.7010(/())b b u S A mg L --==⨯⋅,按正态分布属A 类,自由度v b =7-1=6,传播系数()21.92b y ac b-== 3) u (y)计算:u (y)= u 1+u 2+u 3+u 4ⅰ) u 1为y 残差的标准偏差S ,按正态分布属A 类31 6.7810u S A -==⨯(),v 1=7-1=6,传播系数()1 2.53y c b==ⅱ) u 2为仪器读数的标准不确定度,按均匀分布属B 类,仪器读数最小变化为0.001A,因此42 5.7710()u A -==⨯,v 2=∞,传播系数()12.53y c b ==ⅲ) u 3为标准样品的不确定度。

纳氏试剂分光光度法测定水中氨氮实验报告一、前言随着社会的发展,人们对水资源的需求越来越大,水质问题也越来越受到关注。
而氨氮是衡量水体中氮含量的重要指标之一,对于水体的生态环境和人类健康具有重要意义。
因此,研究和掌握纳氏试剂分光光度法测定水中氨氮的方法具有重要的理论和实际意义。
本文将对纳氏试剂分光光度法测定水中氨氮的原理、方法、影响因素以及实验结果进行详细分析和讨论。
二、纳氏试剂分光光度法测定水中氨氮的原理纳氏试剂分光光度法测定水中氨氮的原理是基于纳氏试剂与氨氮在碱性条件下生成红色络合物的特性。
当纳氏试剂与氨氮反应生成红色络合物时,络合物吸收特定波长的光线,通过测量吸收光强度的变化来计算氨氮的浓度。
三、纳氏试剂分光光度法测定水中氨氮的方法1. 样品制备:将待测水样过滤,去除水中的悬浮物和杂质。
然后,将过滤后的水样与适量的纳氏试剂混合,使纳氏试剂充分溶解。
在此过程中,需要控制好纳氏试剂的用量,以保证反应的准确性和稳定性。
2. 比色测定:将反应好的水样转移到比色皿中,加入适量的氧化剂(如高锰酸钾),使红色络合物转化为无色的络合物。
此时,根据比色皿中溶液的颜色深浅,可以计算出水样中氨氮的浓度。
3. 数据处理:为了准确评价测定结果,需要对测定数据进行一定的处理。
要对不同时间点的测定值进行线性拟合,得到一条拟合曲线。
然后,根据已知的水样浓度范围,通过比较拟合曲线与标准曲线的交点位置,可以确定待测水样的氨氮浓度。
四、影响纳氏试剂分光光度法测定水中氨氮的因素1. 纳氏试剂用量:纳氏试剂用量的选择对测定结果具有重要影响。
过少的纳氏试剂会导致反应不充分,影响测定精度;过多的纳氏试剂则会使络合物过于稳定,难以分离,同样会影响测定结果。
因此,在实验过程中需要严格控制纳氏试剂的用量。
2. 氧化剂用量:氧化剂(如高锰酸钾)的用量也会影响测定结果。
过少的氧化剂会导致红色络合物无法完全转化为无色的络合物,影响测定精度;过多的氧化剂则会使溶液颜色过深,干扰比色过程。
水质氨氮的测定方法纳氏试剂分光光度法1.含义本测定方法适用于地表水、地下水、生活污水和工业废水中氨氮的测定。
当水样体积为 50 ml,使用 20 mm 比色皿时,本方法的检出限为 0.025 mg/L,测定下限为 0.10 mg/L,测定上限为 2.0 mg/L(均以 N 计)。
2.方法原理以游离态的氨或铵离子等形式存在的氨氮与纳氏试剂反应生成淡红棕色络合物,该络合物的吸光度与氨氮含量成正比,于波长 420 nm 处测量吸光度。
3.检测依据水质氨氮的测定纳氏试剂分光光度法HJ 535-20094.检测程序4.1 试剂和材料除非另有说明,分析时所用试剂均使用符合国家标准的分析纯化学试剂,实验用水为按4:1 制备的水。
4.1.1无氨水,在无氨环境中用下述方法之一制备。
(1)离子交换法蒸馏水通过强酸性阳离子交换树脂(氢型)柱,将流出液收集在带有磨口玻璃塞的玻璃瓶内。
每升流出液加 10 g 同样的树脂,以利于保存。
(2)蒸馏法在1 000 ml 的蒸馏水中,加 0.1 ml 硫酸(ρ=1.84 g/ml),在全玻璃蒸馏器中重蒸馏,弃去前 50 ml 馏出液,然后将约 800 ml 馏出液收集在带有磨口玻璃塞的玻璃瓶内。
每升馏出液加 10 g 强酸性阳离子交换树脂(氢型)。
(3)纯水器法用市售纯水器临用前制备。
4.1.2轻质氧化镁(MgO)不含碳酸盐,在 500℃下加热氧化镁,以除去碳酸盐。
4.1.3盐酸,ρ(HCl)=1.18 g/ml。
4.1.4纳氏试剂,可选择下列方法的一种配制。
(1)二氯化汞-碘化钾-氢氧化钾(HgCl2-KI-KOH)溶液称取 15.0 g 氢氧化钾(KOH),溶于 50 ml 水中,冷却至室温。
称取 5.0 g 碘化钾(KI),溶于 10 ml 水中,在搅拌下,将 2.50 g 二氯化汞(HgCl2)粉末分多次加入碘化钾溶液中,直到溶液呈深黄色或出现淡红色沉淀溶解缓慢时,充分搅拌混合,并改为滴加二氯化汞饱和溶液,当出现少量朱红色沉淀不再溶解时,停止滴加。
纳氏试剂分光光度法测定水中氨氮实验报告一、前言在当今社会,水资源的保护和利用已经成为了一个重要的议题。
随着工业化的发展,水体污染问题日益严重,其中氨氮作为水体中的重要污染物之一,对水生生物和人类健康造成了极大的威胁。
因此,研究和掌握氨氮的测定方法具有重要的现实意义。
本文将详细介绍纳氏试剂分光光度法测定水中氨氮的原理、实验步骤及结果分析,以期为氨氮的测定提供一种有效的方法。
二、纳氏试剂分光光度法测定水中氨氮的原理1.1 纳氏试剂的作用纳氏试剂是一种含有铜离子、铁离子和碘离子的络合剂,它可以与氨氮形成稳定的络合物。
这种络合物在紫外可见光谱区域有明显的吸收峰,通过测量该吸收峰的吸光度,可以间接地测定水中氨氮的浓度。
1.2 分光光度法的基本原理分光光度法是一种基于物质对特定波长光线吸收或发射的定量分析方法。
在这种方法中,首先需要将待测溶液与已知浓度的标准溶液进行比较,得到一个相对吸光度值。
然后,通过比较待测溶液与标准溶液的相对吸光度值,可以计算出待测溶液中氨氮的浓度。
三、实验步骤3.1 实验准备(1) 称取适量的纳氏试剂。
(2) 准备一定量的水样。
(3) 准备一定量的已知浓度的标准氨氮溶液。
(4) 准备分光光度计及相关仪器。
3.2 实验操作(1) 将纳氏试剂溶解于适量的水中,制成纳氏试剂溶液。
(2) 分别取一定量的水样和标准氨氮溶液,加入适量的纳氏试剂溶液。
(3) 记录下加入纳氏试剂后的颜色变化。
(4) 利用分光光度计测量吸收光谱的吸光度值。
(5) 根据标准曲线计算出待测水样中氨氮的浓度。
四、实验结果分析4.1 实验数据处理根据实验步骤记录的数据,绘制出吸光度-浓度曲线。
通过比较标准曲线和待测水样的吸光度-浓度曲线,可以计算出待测水样中氨氮的浓度。
还可以对实验数据进行统计分析,如计算平均值、标准差等,以评估实验结果的准确性和可靠性。
4.2 结果讨论通过实验结果分析,我们发现纳氏试剂分光光度法测定水中氨氮具有较高的准确度和灵敏度,适用于各种水质条件下的氨氮测定。