化工原理-精馏
- 格式:ppt
- 大小:4.08 MB
- 文档页数:96


化工原理精馏知识点总结嘿,朋友!咱们今天来聊聊化工原理里的精馏这个有趣的话题。
你知道吗,精馏就像是一场精细的舞蹈,每个步骤都得踩在准确的节拍上。
它可是化工生产中非常重要的分离技术。
先来说说什么是精馏。
想象一下,有一堆混合物,就像一个混乱的大杂烩,各种成分搅和在一起。
而精馏呢,就是要把它们一个一个地挑出来,让它们各归各位。
这就好比把一堆五颜六色的珠子按照颜色分类,可不容易呢!精馏的原理,简单说就是利用混合物中各组分的沸点不同。
沸点低的先汽化,沸点高的后汽化。
这就像跑步比赛,速度快的先冲线,速度慢的落在后面。
通过多次的汽化和冷凝,就能把混合物逐步分离成较纯的组分。
再讲讲精馏塔。
这可是精馏的核心装备,就像一个大城堡,里面有着各种机关和通道。
塔板或者填料就是它的战场,混合物在这里展开激烈的争斗,决出胜负,实现分离。
说到塔板,那可是有讲究的。
塔板的类型多种多样,有筛板、浮阀板等等。
它们就像是不同的武器,各有各的特点和优势。
还有回流比,这可是个关键的参数。
回流比大,分离效果好,但能耗也高;回流比小,能耗低,但分离效果可能就打折扣了。
这是不是有点像花钱买东西,花得多可能买得好,花得少可能品质就一般啦?再说说操作压力。
压力高,沸点高,对设备要求高;压力低,沸点低,可能容易出现一些安全问题。
这就像开车,速度快风险大,速度慢又着急。
掌握好精馏的知识点,就像是掌握了一把神奇的钥匙,可以打开化工生产中高效分离的大门。
能精准地分离出我们需要的物质,提高产品的质量和纯度,这难道不是很厉害吗?总之,化工原理中的精馏,看似复杂,其实只要用心去理解,就会发现其中的奥秘和乐趣。
它就像一个神秘的魔法,等待着我们去探索和掌握。
朋友,你准备好去揭开它的神秘面纱了吗?。

化工原理精馏知识点总结一、精馏原理概述精馏是一种通过升华和凝华的方法来分离液体混合物组分的技术,通过升华和凝华的过程可以使组分分离,最终获得纯净的组分产品。
精馏是一种重要的分离技术,在化工生产中得到广泛应用。
精馏的基本原理是依靠物质的汽化、冷凝和重新汽化等过程来实现组分的分离。
混合物在加热后,其中的易挥发成分首先汽化,形成蒸汽,然后在冷凝器中冷凝成液体,从而获得纯净的组分。
通过将蒸汽重新加热、汽化和冷凝,可以进行多次分离,提高分离效果。
二、精馏塔结构和工作原理1. 精馏塔结构精馏塔是进行精馏操作的设备,其结构一般由一种或多种填料、提升子、冷凝器和再沸器等组成。
填料是用来增大塔内表面积和混合物与液体之间的接触面积,提升子是用来提高温度场,从而使混合物更容易汽化。
冷凝器则是用来将蒸汽冷凝成液体,再沸器是用来将再次汽化的液体加热成蒸汽。
2. 精馏塔工作原理精馏塔是通过在填料层内和填料层与液体流动层之间的传质作用实现气液两相的接触混合。
填料层利用填料表面积大、气液接触面积大和液膜传质效果高的特点,以实现气液两相的有效滞留和有效接触,从而提高气相和液相之间的传递速率。
从而实现混合物组分的分离。
三、精馏操作过程及控制方法1. 精馏操作过程(1)进料进料是指将需要分离的混合物输入到精馏塔中。
进料的温度、压力和流量等参数对分馏操作的影响很大,需要注意调节。
(2)加热加热是将混合物中易挥发成分加热至其汽化温度的过程。
通常使用蒸汽加热或电加热等方式来进行加热。
(3)蒸馏蒸馏是指将加热后的混合物通过精馏塔,在填料层内和填料层与液体流动层之间进行传质过程,以实现组分的蒸发和再凝结的过程。
(4)冷凝冷凝是指将产生的蒸汽通过冷凝器使之冷却成液体,从而得到纯净的组分。
冷凝器通常采用水冷或风冷等方式来进行冷却。
2. 精馏操作控制方法(1)温度控制保持适当的加热温度是进行精馏操作的关键,通过合理控制加热温度,可以使易挥发组分蒸发,而留下不易挥发组分。


化工原理精馏实验化工原理精馏实验是化工工程中的一项重要实验内容,它主要用于分离和提纯混合物中的组分。
本文将介绍化工原理精馏实验的基本原理、实验步骤以及实验中需要注意的事项。
1. 实验目的化工原理精馏实验的主要目的是通过温度差异,利用液体蒸汽和凝结的原理,将混合物中的组分分离并得到纯净的产品。
通过这个实验,我们可以了解精馏作为一种分离技术的原理和应用。
2. 实验原理化工原理精馏实验的基本原理是利用混合物中各组分的不同沸点,通过升温使其中具有较低沸点的组分先蒸发,然后通过冷凝使其变为液体,从而实现分离。
在实验过程中,我们需要使用精馏塔,该塔内部设置有填料,用于增加混合物和蒸汽之间的交流面积,并实现更充分的分离。
3. 实验步骤(1) 准备实验所需设备和药品,包括精馏装置、混合物、填料等。
(2) 将混合物加入精馏瓶中,并将瓶塞密封。
(3) 将冷凝管和进料管连接到精馏瓶上,确保连接牢固。
(4) 将精馏瓶放入加热设备中,逐渐升温。
(5) 观察精馏瓶内的液体是否开始蒸发,当温度上升到某一点时,开始收集冷凝液。
(6) 根据实验需要,调整加热温度和收集冷凝液的时间,以实现所需组分的分离和提纯。
4. 实验注意事项(1) 在进行化工原理精馏实验前,需先对所需设备进行检查和清洁,确保实验过程的安全性。
(2) 在实验操作中,热量的传递速度会影响分馏过程的效果,因此需要掌握合适的加热速率。
(3) 为了避免精馏烧坏填料或其他设备,需要控制温度,确保温度在安全范围内。
(4) 实验结束后,应将设备进行清洗和消毒,防止残留物对下次实验的影响。
5. 实验结果分析通过化工原理精馏实验,可以得到分离出的纯净组分,并进行定量分析。
根据实验结果,可以进一步探讨精馏的分离效果、提纯效率等指标,并对所得纯净组分进行性质分析。
总结:化工原理精馏实验是一项重要的实验内容,通过实验可以了解精馏作为一种分离技术的原理和应用。
在实验过程中,需要注意设备的清洁和安全操作,合理控制加热温度和加热速率,以达到较好的分馏效果。

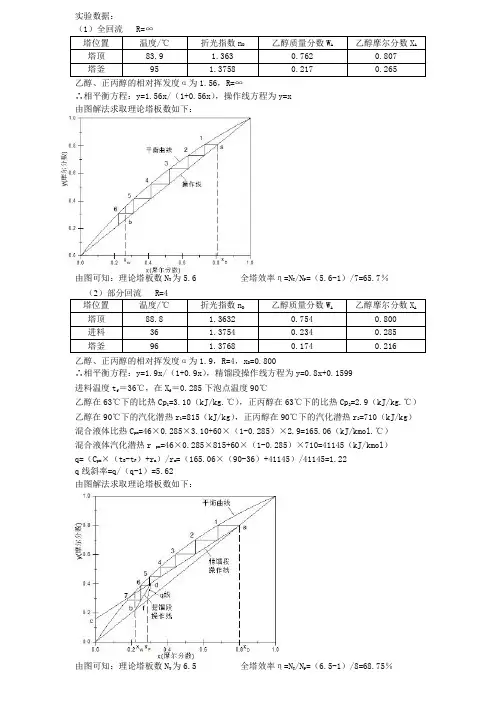
实验数据:
(1)全回流 R=∞
乙醇、正丙醇的相对挥发度α为1.56,R=∞
∴相平衡方程:y=1.56x/(1+0.56x),操作线方程为y=x
由图解法求取理论塔板数如下:
由图可知:理论塔板数N T为5.6 全塔效率η=N T/N P=(5.6-1)/7=65.7%
乙醇、正丙醇的相对挥发度α为1.9,R=4,x D=0.800
∴相平衡方程:y=1.9x/(1+0.9x),精馏段操作线方程为y=0.8x+0.1599
进料温度t f=36℃,在X f=0.285下泡点温度90℃
乙醇在63℃下的比热Cp1=3.10(kJ/kg.℃),正丙醇在63℃下的比热Cp2=2.9(kJ/kg.℃)乙醇在90℃下的汽化潜热r1=815(kJ/kg),正丙醇在90℃下的汽化潜热r2=710(kJ/kg)混合液体比热C pm=46×0.285×3.10+60×(1-0.285)×2.9=165.06(kJ/kmol.℃)
混合液体汽化潜热r pm=46×0.285×815+60×(1-0.285)×710=41145(kJ/kmol)
q=(C pm×(t B-t F)+r m)/r m=(165.06×(90-36)+41145)/41145=1.22
q线斜率=q/(q-1)=5.62
由图解法求取理论塔板数如下:
由图可知:理论塔板数N T为6.5 全塔效率η=N T/N P=(6.5-1)/8=68.75%。

化工原理精馏实验数据处理1. 引言化工原理精馏实验是化工专业中非常重要的实验之一。
在精馏实验中,通过分离液体混合物中的组分,得到纯净的产品。
实验过程中需要收集大量的实验数据,并对这些数据进行处理和分析。
本文将详细探讨化工原理精馏实验数据处理的方法和技巧。
2. 实验目的化工原理精馏实验的目的是通过精馏过程将液体混合物中的组分分离出来。
实验数据处理的目的是对实验数据进行整理、分析和解释,以得到有关精馏过程的关键信息和结果。
3. 实验数据处理方法在化工原理精馏实验中,我们需要收集的实验数据包括温度、压力、流量等参数的变化情况。
为了对这些数据进行处理,我们可以采用以下方法:3.1 数据的整理和筛选首先,我们需要对收集到的实验数据进行整理和筛选。
将不符合要求或有误差的数据排除,确保数据的准确性和可靠性。
3.2 数据的统计和分析接下来,我们可以对整理后的数据进行统计和分析。
可以计算平均值、标准差、方差等统计指标,以了解数据的分布情况和稳定性。
3.3 数据的可视化为了更直观地展示数据的变化趋势和关系,我们可以将数据进行可视化处理。
可以使用图表、曲线图、散点图等方式来展示数据,以便更好地理解和解释实验结果。
4. 实验数据处理的意义和应用实验数据处理在化工原理精馏实验中具有重要的意义和应用。
通过对实验数据的处理,我们可以得到以下信息和结果:4.1 组件的分离效果通过对实验数据的分析,我们可以判断精馏过程中组分的分离效果。
可以通过计算馏分的组分含量、回收率等指标来评估分离效果的好坏。
4.2 工艺参数的优化实验数据处理还可以帮助我们优化精馏过程中的工艺参数。
通过分析数据,我们可以找到影响分离效果的关键因素,并对工艺参数进行调整和优化,以提高产品的纯度和产量。
4.3 实验结果的验证实验数据处理还可以用于验证实验结果的准确性和可靠性。
通过对实验数据的处理和分析,我们可以判断实验结果是否符合预期,从而对实验方法和操作进行改进和优化。



化工原理精馏的应用一、精馏的基本原理精馏是一种常见的分馏技术,广泛应用于化工工业中。
它基于物质的不同挥发性,在恒定的温度和压力条件下,将混合物中的组分分离出来。
精馏的基本原理是利用不同物质的沸点差异,通过加热混合物使之煮沸,然后利用冷凝装置将蒸汽转化为液体,从而实现分离。
二、精馏的应用领域精馏广泛应用于化工工业中的物质分离和纯化过程中。
以下列举了一些常见的应用领域:1. 石油炼制工业在石油炼制过程中,原油经过初步处理后,通常会进行精馏过程,以将其分离成不同沸点范围内的馏分。
通过多级精馏塔,可以得到石油气、汽油、柴油、煤油等不同的产品。
2. 酒精生产工业酒精生产工业中的精馏过程主要用于酒精的纯化。
发酵产生的液体经过精馏,可以去除其中的杂质,提高酒精的纯度。
这在制造白酒、伏特加等高纯度酒精产品时尤为重要。
3. 化学品生产工业在化学品生产过程中,精馏常被用于分离混合物中的各种组分。
例如,用于制造酸、碱、有机溶剂和涂料等化学品的原材料通常需要进行精馏来获得高纯度的产品。
4. 精细化工工业在精细化工工业领域,精馏技术被广泛应用于制药、医药等行业中。
通过精馏过程,可以提取药物中的有效成分,纯化药物和去除其中的杂质,以满足药品的安全和纯度要求。
5. 生物燃料工业精馏技术在生物燃料工业中可以用于提取生物质燃料中的乙醇或生物柴油等有机物。
这不仅可以提高生物燃料的能量效率,还可以减少环境污染。
三、精馏过程的关键因素精馏过程的效果受到许多因素的影响,下面列举了其中几个关键因素:1.温度:温度的控制是精馏过程中非常重要的因素。
合适的温度可以促使混合物中的组分充分汽化,并实现高效的分离。
2.压力:压力对精馏过程的影响也非常显著。
较低的压力有助于降低沸点,提高挥发性较高的组分的分离效率。
3.塔板数量和间距:在多级精馏塔中,塔板的数量和间距对分离效果起着重要作用。
适当的塔板数量和间距可以增加混合物的接触面积和停留时间,提高分离效果。
化工原理精馏
精馏是化工过程中常用的分离方法,用于将混合物中的组分按照其挥发性分离为不同纯度的产品。
精馏过程中,混合物首先加热至沸腾点,然后将生成的蒸气输送到冷凝器中进行冷凝。
冷凝后,液体收集器中会得到不同纯度的产品。
精馏过程基于混合物中不同组分的挥发性差异。
挥发性大的组分在加热后较早转化为蒸气,而挥发性小的组分则在较高温度下才蒸发。
经过冷凝后,收集器中会得到高挥发性组分的纯产品。
余下的低挥发性组分则在塔底收集。
精馏过程中,塔是一个重要的设备。
塔内通常包括填料或板片,用于增大接触面积,促进挥发和冷凝。
高挥发性组分在塔上部可迅速逸出,而低挥发性组分则被慢慢分离。
精馏还可用于提纯液体产品。
通过多级精馏,可以获得更高纯度的产品。
多级精馏是基于挥发性差异的温度差异实现的,每一级都以前一级的塔顶产品作为进料。
总之,精馏是一种重要的化工分离方法,通过控制温度和塔内工艺参数,可以将混合物分离为不同纯度的产品。
精馏实验一、实验目的1、了解筛板式精馏塔及其附属设备的基本结构,掌握精馏操作的基本方法;2、掌握精馏过程全回流和部分回流的操作方法;3、掌握测定板式塔全塔效率。
二、实验原理1、全塔效率E T全塔效率又称总板效率,是指达到指定分离效果所需理论板数与实际板数的比值,即-1=T T P N E N (1)式中:T N -完成一定分离任务所需的理论塔板数,包括塔釜;P N -完成一定分离任务所需的实际塔板数。
全塔效率简单地反映了整个塔内塔板的平均效率,表明塔板结构、物性系数、操作状况等因素对塔板分离效果的影响。
对于双组分体系,塔内所需理论塔板数N T ,可通过实验测得塔顶组成x D 、塔釜组成x W 、进料组成x F 及进料热状况q 、回流比R等有关参数,利用相平衡关系和操作线用图解法或逐板计算法求得。
图1塔板气液流向示意图2、单板效率ME 单板效率又称莫弗里板效率,如图1所示,是指气相或液相经过一层实际塔板前后的组成变化值与经过一层理论塔板前后的组成变化值之比。
按气相组成变化表示的单板效率为1*1y =n n MV n n y E y y ++--(2)按液相组成变化表示的单板效率为1*1n n ML n n x x E x x ---=-(3)式中:y n 、1n y +-分别为离开第n 、n+1块塔板的气相组成,摩尔分数;1n x -、n x -分别为离开第n-1、n 块塔板的液相组成,摩尔分数;*ny -与x n 成平衡的气相组成,摩尔分数;*nx -与y n 成平衡的液相组成,摩尔分数。
3、图解法求理论塔板数N T图解法又称麦卡勃-蒂列(McCabe-Thiele)法,简称M-T 法,其原理与逐板计算法完全相同,只是将逐板计算过程在y-x 图上直观地表示出来。
对于恒摩尔流体系,精馏段的操作线方程为:111D n n x R y x R R +=+++(4)式中:1n y +-精馏段第n+1块塔板上升的蒸汽组成,摩尔分数;n x -精馏段第n 块塔板下流的液体组成,摩尔分数;D x -塔顶溜出液的液体组成,摩尔分数;R -回流比。
化工原理实验—精馏化工原理实验—精馏精馏是一种重要的分离技术,主要用于分离、纯化液体混合物中的各种成分。
在实际生产和科研实验中,精馏已经成为不可或缺的重要技术。
本文将就化工原理实验中的精馏实验进行详细介绍。
一、实验原理精馏的基本原理是根据不同成分在液态和气态之间的平衡关系,在加热条件下将混合物中单一成分蒸发和冷凝来实现分离、提纯目标成分。
实验中要分离的混合物首先被加热到沸腾点以上,因为各种成分的沸点不同,有些成分的沸点比另一些成分高得多,因此在离开混合物比较早的时候,一些液体成分便会压缩成气体形式,通过冷凝的方式回到液体形式,从而分离。
二、实验步骤1.实验前准备:确定实验目的,熟悉仪器使用方法和名词术语,检查实验物品是否准备充分。
2.实验流程:(1)调整设备:将水箱放在上部,并根据实验需要将装有混合物的烧瓶安装在下部。
(2)加热混合物:先在小火下加热,让混合物慢慢升温,确定加热速度以防止挥发速度过快。
随着温度的升高,由混合物挥发出来的单一成分便会通过塞子进入冷凝器,冷凝器中的水为其退回到液体形态,收集并量取所需要的物质。
3.实验结束:(1)关闭所有开关:实验完成后,将电源关闭,并将实验设备切断电源和气源。
(2)清洗设备与仪器:清洗所有已使用的材料和设备,以确保下次的实验能保证卫生和安全。
三、实验注意事项1.将水箱放置在塞子上方,仔细检查所有漏洞的位置和具有修复能力的地方,以避免机械故障与事故到来。
2.在进行实验时,必须小心谨慎地装填液体混合物,尤其是对于易燃物质,必须保持警惕,并根据实验条件和混合物来选择实验设备和材料。
3.在加热过程中,如果需要调整加热器的温度,必须慢慢调整,直到较稳定的加热水平达到。
总之,精馏实验是一项非常重要的化工原理实验,同学们在进行实验时一定要小心谨慎,严格遵守实验规范,才能保证实验的顺利进行。
化工原理实验报告精馏实验
化工原理实验报告:精馏实验
实验目的:
本次实验旨在通过精馏实验,掌握精馏过程的基本原理,了解精馏技术在化工
生产中的应用,并掌握精馏实验的操作技能。
实验原理:
精馏是一种利用液体混合物中不同成分的沸点差异进行分离的物理方法。
在精
馏过程中,液体混合物首先被加热至沸点,然后蒸气被冷凝成液体,最终得到
不同成分的纯净产物。
实验步骤:
1. 准备实验装置:将精馏瓶、冷凝管、加热设备等装置搭建好,并连接好管道。
2. 将待分离的液体混合物倒入精馏瓶中。
3. 加热液体混合物,使其达到沸点,产生蒸气。
4. 蒸气通过冷凝管冷却成液体,分别收集不同成分的产物。
实验结果:
经过精馏实验,我们成功地将液体混合物分离成了不同成分的产物。
通过实验,我们观察到不同成分的沸点差异导致了它们在精馏过程中的分离。
这表明精馏
技术在化工生产中具有重要的应用价值。
实验结论:
通过本次精馏实验,我们深入了解了精馏技术的原理和操作方法,掌握了精馏
实验的操作技能。
精馏技术在化工生产中具有广泛的应用,能够有效地分离液
体混合物中的不同成分,提高产品的纯度和质量,具有重要的经济意义和社会
价值。
总结:
精馏实验是化工原理课程中的重要实验之一,通过本次实验,我们对精馏技术有了更深入的了解,为今后的学习和工作打下了坚实的基础。
希望通过不断的实践和学习,我们能够更加熟练地掌握精馏技术,为将来的化工生产做出更大的贡献。
精馏实验一、实验任务和目的:1、充分利用计算机采集和控制系统具有的快速、大容量和实时处理的特点,进行精馏过程多实验方案的设计,并进行实验验证,得出实验结论。
以掌握实验研究的方法。
2、学会识别精馏塔内出现的几种操作状态,并分析这些操作状态对塔性能的影响。
3、学习精馏塔性能参数的测量方法,并掌握其影响因素。
4、测定精馏过程的动态特性,提高学生对精馏过程的认识。
二、实验原理:在板式精馏塔中,由塔釜产生的蒸汽沿塔板逐板上升与来自塔板下降的回流液,在塔板上实现多次接触,进行传热与传质,使混合液达到一定程度的分离。
回流是精馏操作得以实现的基础。
塔顶的回流量与采出量之比,称为回流比。
回流比是精馏操作的重要参数之一,其大小影响着精馏操作的分离效果和能耗。
回流比存在两种极限情况:最小回流比和全回流。
若塔在最小回流比下操作,要完成分离任务,则需要有无穷多块塔板的精馏塔。
当然,这不符合工业实际,所以最小回流比只是一个操作限度。
若操作处于全回流时,既无任何产品采出,也无原料加入,塔顶的冷凝液全部返回塔内中,这在生产中无实际意义。
但是,由于此时所需理论塔板数最少,又易于达到稳定,故常在工业装置的开停车、排除故障及科学研究时使用。
3、实验流程(简图);4、操作步骤;4.1、设置参数设置精馏段塔板数为5,设置提馏段塔板数为3,配置浓度比为0.66的乙醇/正丙醇混合液,设置进料罐的一次性进料量为2L。
4.2、精馏塔进料(1)连续点击"进料"按钮,进料罐开始进料,直到罐内液位达到70%以上。
(2)启动进料泵。
(3)设定进料泵功率,将进料流量控制器的 OP 值设为50%。
(4)设定预热器功率,将进料温度控制器的 OP 值设为60%,开始加热。
(5)打开塔釜液位控制器,控制液位在70%-80%之间。
4.3、启动再沸器(1)将塔顶冷凝器内通入冷却水。
(2)设定塔釜加热功率,将塔釜温度控制器的 OP 值设为 50%。