手性季鏻盐相转移催化剂在不对称反应中的应用_喻理德
- 格式:pdf
- 大小:483.13 KB
- 文档页数:8


手性金属配合物催化剂对不对称反应所起作用不对称反应是有机合成中的重要反应类型,可用于合成具有特定立体结构的化合物。
在过去的几十年里,手性金属配合物催化剂已经被广泛应用于不对称合成领域,并取得了重要的进展。
本文将探讨手性金属配合物催化剂在不对称反应中的作用机制和应用。
手性金属配合物催化剂具有手性中心,可以有效地诱导不对称反应的进行。
它们在催化剂的选择区域、立体诱导和亲核活性等方面起到关键作用。
手性金属配合物催化剂通常由金属离子和手性配体组成。
金属离子的选择取决于反应的具体需求,常见的金属包括钯、铱、铑和铜等。
手性配体可以提供立体效应,通过与底物的相互作用,影响催化剂与底物的立体和电子性质。
手性金属配合物催化剂在不对称反应中的作用机制可以解释为手性诱导和控制。
催化剂通过与底物形成手性配位体位点,使得反应途径更具立体选择性。
这种立体选择性可以通过Handedness Transfer Model进行解释。
在此模型中,底物与手性金属配合物催化剂之间发生相互作用,通过“交换”手性中心,手性信息被传递给底物并引导其手性生成。
手性金属配合物催化剂在不对称反应中的应用非常广泛。
它们已成功地应用于不对称加氢、氧化、羰基还原、Michael加成等反应中。
其中,不对称氢化反应被认为是最具代表性的不对称反应之一。
手性金属配合物催化剂可以通过与底物形成配位键,有效地实现对不对称氢化反应的立体选择性控制。
这种反应广泛应用于药物和农药的合成,产物的手性纯度高,对实验室和产业具有重要意义。
另外,手性金属配合物催化剂还可以应用于不对称C-C键和C-X键形成反应中。
通过催化剂的选择和优化,可以实现底物的不对称催化转化。
这些反应对于合成特定立体结构的天然产物或药物分子非常重要。
尽管手性金属配合物催化剂在不对称反应中具有很多优势,但也存在一些挑战。
其中,催化剂的活性和选择性是关键问题。
虽然很多手性配体被设计和合成,但很少有一种配体可以广泛适用于不同反应类型。

第15卷 第1期 武汉科技学院学报 V ol.15 No.1 手性磷试剂/Ti(OPr-i )4催化醛的不对称烷基化 反应及其机理杨卓鸿 (武汉科技学院 纺织研究所,湖北 武汉 430073)摘要:以合成的手性磷化合物作为催化剂,将它们用于醛的不对称烷基化反应,所得芳香仲醇大都具有较好的化学产率和较低至中等的ee.值,并对反应机理进行了研究。
关键词:手性磷化合物;不对称烷基化反应; 对映选择性;反应机理 中图分类号:O627.51 文献标识码:A 文章编号:1009—5160(2002)01—0025—03醛与二烷基锌的加成反应是延长碳链的一类很重要的反应。
这类反应的不对称催化方法引起了广泛的关注,它不但可以在有机金属配合物催化下进行,也可以在非有机金属试剂即所谓配体催化下进行。
已报道过的手性配体催化剂主要有氨基醇[1]、氨基硫醇[2]、二醇[3]、磺酰胺[4]、磷酰胺[5-7]等。
我们曾报道了几种新型的具有醇羟基或酚羟基的磷酸酯或磷酰胺以及环状磷酰胺酯的合成及其催化活性[8-9],本文选择手性磷化合物1、2作为研究对象,在有机金属配合物作用下,即与Ti(OPr-i )4络合,将它们用于醛的不对称烷基化反应,并对其催化机理进行了研究。
1 实验部分 1.1 仪器与试剂 比旋光值在Perkin Elmer 241MC 旋光仪上测定,所有溶剂按文献方法经干燥重蒸处理。
Et 2Zn 及Ti(OPr-i )4为Fluka 试剂。
1.2 手性磷试剂的合成 合成方法及有关数据参照文献[8]。
1.3 二乙基锌与醛的烷基化反应(典型实例,entry 1)25 mL 反应瓶中导入氮气流,加入85 mg (0.2 mmol )手性磷化合物1的6 mL 甲苯溶液,566 mg (2 mmol )Ti(OPr-i )4,室温反应1 h ,将反应液冷却至-20℃ ,加入212 mg (2 mmol )苯甲醛和3.61 mL (4 mmol )1.1 mol/L Et 2Zn 的甲苯溶液,反应混合物于-20℃∼-50℃搅拌反应12 h ,然后加入20 mL 盐酸溶液(2 mol/L )终止反应,分出有机层,水层用乙醚提取,合并有机层,无水Na 2SO 4干燥,过滤,滤液蒸出溶剂,粗产物过硅胶柱层析提纯(200∼300目硅胶,石油醚/乙酸乙酯梯度淋洗),得1-苯基丙醇260 mg 。

有机合成中的不对称催化不对称催化是一种在有机合成中广泛应用的重要方法。
它通过引入手性配体,使得对称的反应转化为具有手性产物的反应。
在这篇文章中,将介绍不对称催化的原理、应用以及发展趋势。
一、不对称催化的原理不对称催化的原理基于手性配体和手性催化剂的应用。
手性配体是具有手性结构的有机化合物,可以与金属离子配位形成手性配位化合物。
这些手性配体能够通过选择性吸附、空间位阻等方式影响反应的立体选择性,从而实现对称反应的不对称性转化。
而手性催化剂则是由手性金属配合物和手性有机分子组成的复合物,能够通过催化作用使反应产生手性产物。
二、不对称催化的应用1. 不对称还原反应不对称还原反应是不对称催化中的一种重要应用。
通过引入手性配体和催化剂,可以实现对不对称有机物的还原,得到具有手性的醇、胺等化合物。
这种方法在医药、农药、香料等领域中有广泛的应用。
2. 不对称氧化反应不对称氧化反应是不对称催化的另一种重要应用。
通过引入手性配体和催化剂,可以使对称的氧化反应转化为不对称的氧化反应,得到手性醛、酮等化合物。
这种方法在合成有机中间体和天然产物的过程中起着重要的作用。
3. 不对称烯烃化反应不对称烯烃化反应是一种在不对称催化中较具挑战性的应用。
通过引入手性配体和催化剂,可以实现对不对称烯烃化反应的控制,得到具有手性的烯醇、烯醛等化合物。
这种方法在生物活性分子的合成中具有广阔的应用前景。
三、不对称催化的发展趋势随着合成化学的发展,不对称催化在有机合成中的应用越来越重要。
未来,不对称催化的发展趋势主要体现在以下几个方面:1. 发展更多的手性配体和催化剂为了提高不对称催化的效率和选择性,需要开发更多的手性配体和催化剂。
这些新型配体和催化剂能够应对更广泛的反应类型,提高催化剂的稳定性和反应活性。
2. 开发新的反应类型目前,大多数不对称催化反应都是针对特定的反应类型。
未来,需要发展更多新的反应类型,探索更广泛的不对称催化反应。
这将有助于拓宽不对称催化的应用范围,并提供更多的合成路线。


不对称反应及应用—手性合成前沿研究不对称合成是有机化学领域中一种重要的合成方法,通过该方法可以制备手性分子,即具有手性空间结构的有机分子。
手性分子在药物、农药、材料等领域具有广泛的应用价值,因此手性合成一直是有机化学研究的热点之一、不对称反应是实现手性合成的核心技术之一,其优势在于可以选择性地控制产物的手性结构,提高产品的立体选择性和产率。
本文将重点介绍不对称反应及其在手性合成前沿研究中的应用。
不对称反应是指在反应中产生手性产物,同时控制产物手性结构的过程。
不对称反应主要包括催化剂不对称反应和合成不对称反应两大类。
催化剂不对称反应是通过手性催化剂促进反应进行,如不对称氢化、不对称氨基化、不对称烯基化等。
合成不对称反应是通过手性试剂实现反应不对称性,如不对称亲核取代、不对称环化等。
不对称反应在有机合成中起着重要的作用,可以用于制备手性有机分子、手性药物等。
手性合成是有机化学研究的重要方向之一,目前在手性合成领域中,不对称反应的研究是一个热点。
一些新型不对称反应的开发和应用正在成为手性合成领域的前沿研究。
例如,最近几年来,金属催化的不对称反应得到了广泛关注。
金属催化的不对称反应具有底物范围广、反应条件温和等优点,因此在手性合成中具有广阔的应用前景。
目前,已经有许多金属催化的不对称反应已经成功开发,例如不对称氢化、不对称羟基化、不对称氨基化等。
此外,还有一些其他新型的不对称反应也在手性合成领域中得到了应用。
例如,不对称有机催化反应、不对称电化学反应等。
不对称有机催化是利用手性有机分子作为催化剂促进反应的进行,该方法具有催化条件温和、底物范围广等优点,因此在手性合成中具有很大的应用潜力。
不对称电化学反应是通过电化学手性诱导实现反应的手性选择性,该方法具有可控性强等优点,可以用于制备手性分子。
总的来说,不对称反应及其在手性合成领域的应用是有机化学研究的热点之一,不同类型的不对称反应各有特点,可以根据具体的需求选择合适的方法。

不对称有机催化剂的设计与应用催化剂在有机合成中起着至关重要的作用,通过它们的作用可以促进反应的进行并提高反应的立体选择性。
而不对称有机催化剂作为一类特殊的催化剂,能够选择性地催化手性有机物的合成,具有广泛的应用前景。
本文将重点探讨不对称有机催化剂的设计原理以及在有机合成中的应用。
一、不对称有机催化剂的设计原理不对称有机催化剂的设计原理基于手性诱导效应(chirality induction effect)。
手性诱导效应是指催化剂分子的手性结构能够传递到反应物分子中,从而在反应过程中产生手性产物。
为了实现这一效应,催化剂的分子结构需要满足一定的条件:首先,催化剂本身需要具备手性结构,可以是手性配体(chiral ligand)或手性基团(chiral auxiliary)。
其次,催化剂分子必须能够与反应物进行紧密的相互作用,通过各种相互作用力(如氢键、范德华力等)实现手性诱导效应。
二、不对称有机催化剂的应用领域1. 不对称催化合成手性有机物不对称有机催化剂在手性有机物的合成中具有广泛的应用。
其中,不对称氢化反应是最常见的应用之一。
通过选择合适的不对称有机催化剂,可以将不对称酮或不对称醛还原为手性醇。
此外,不对称有机催化剂还可以催化其他多种反应,如不对称亲核取代、不对称氧化等,从而合成具有高立体选择性的手性有机物。
2. 不对称催化制备药物不对称有机催化剂在制备药物中扮演着重要角色。
药物通常需要具备一定的手性结构,因为具有手性的药物分子往往在体内具有更好的活性和选择性。
通过不对称有机催化剂的催化作用,可以实现药物的高立体选择性合成,从而提高药物的活性和药效。
3. 不对称催化合成功能性小分子不对称有机催化剂在合成功能性小分子方面也有着重要的应用。
功能性小分子广泛存在于化学领域的各个分支中,具有着广泛的应用前景。
通过不对称有机催化剂的催化作用,可以高效合成具有特定功能的小分子化合物,如荧光探针、生物传感器等,为进一步研究和应用提供了重要工具。
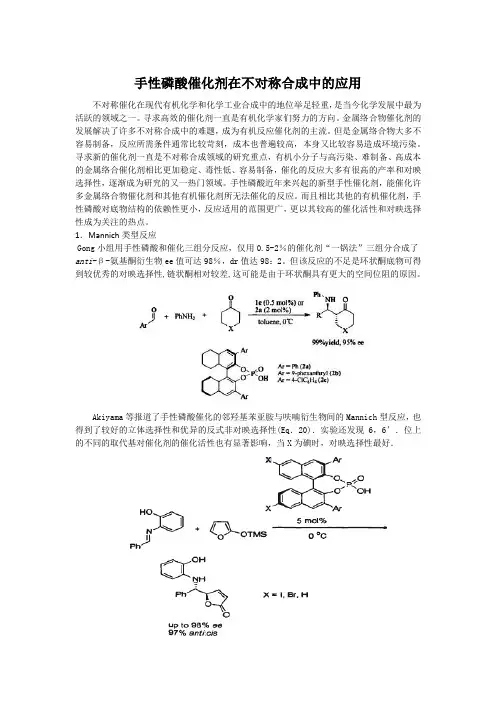
手性磷酸催化剂在不对称合成中的应用不对称催化在现代有机化学和化学工业合成中的地位举足轻重,是当今化学发展中最为活跃的领域之一。
寻求高效的催化剂一直是有机化学家们努力的方向。
金属络合物催化剂的发展解决了许多不对称合成中的难题,成为有机反应催化剂的主流。
但是金属络合物大多不容易制备,反应所需条件通常比较苛刻,成本也普遍较高,本身又比较容易造成环境污染。
寻求新的催化剂一直是不对称合成领域的研究重点,有机小分子与高污染、难制备、高成本的金属络合催化剂相比更加稳定、毒性低、容易制备,催化的反应大多有很高的产率和对映选择性,逐渐成为研究的又一热门领域。
手性磷酸近年来兴起的新型手性催化剂,能催化许多金属络合物催化剂和其他有机催化剂所无法催化的反应。
而且相比其他的有机催化剂,手性磷酸对底物结构的依赖性更小,反应适用的范围更广,更以其较高的催化活性和对映选择性成为关注的热点。
1.Mannich类型反应Gong小组用手性磷酸和催化三组分反应,仅用0.5-2%的催化剂“一锅法”三组分合成了anti-β-氨基酮衍生物ee值可达98%,dr值达98:2。
但该反应的不足是环状酮底物可得到较优秀的对映选择性,链状酮相对较差,这可能是由于环状酮具有更大的空间位阻的原因。
Akiyama等报道了手性磷酸催化的邻羟基苯亚胺与呋喃衍生物间的Mannich型反应,也得到了较好的立体选择性和优异的反式非对映选择性(Eq.20).实验还发现6,6’.位上的不同的取代基对催化剂的催化活性也有显著影响,当X为碘时,对映选择性最好.Yamanaka M等人通过化学计算研究了手性磷酸催化的Mannich反应可能的机理【1】Guo Q.X,Uu H,Gong L Z,Z.Chiral BronsteA Acid-Catalyzed Direct Asymmetric Mannich Reaction.J.Am.Chem.Soc.,2007,129:3790一3791【2】Aldyama T,Honma Y,Itoh J,Fuehibe K,Adv.Symth.Catal.2008,350,399.【3】Yamanaka M,Itoh J,Akiyama T,eta1.J.Am.Chem.Soc.,2007,129:6756—67。

不对称合成中的手性膦(磷)酸酯(酰胺)催化剂张占金;万伯顺;陈惠麟【摘要】讨论了手性膦(磷)酰胺及膦(磷)酸酯催化剂在不对称烷基化、不对称缩合、不对称氢化、不对称氰硅化等反应中应用的最新研究进展.参考文献48篇.【期刊名称】《合成化学》【年(卷),期】2004(012)003【总页数】9页(P237-244,272)【关键词】手性膦(磷)酸酯;手性膦(磷)酰胺;不对称合成;综述【作者】张占金;万伯顺;陈惠麟【作者单位】渤海大学化学与食品科学学院,辽宁,锦州,121000;中国科学院大连化学物理研究所精细化工研究室,辽宁,大连,116023;中国科学院大连化学物理研究所精细化工研究室,辽宁,大连,116023;中国科学院大连化学物理研究所精细化工研究室,辽宁,大连,116023【正文语种】中文【中图分类】O621.3近十几年来,不含金属的手性有机小分子催化的不对称合成反应取得了可喜的进展[1]。
在大多数情况下,这些有机小分子催化的不对称反应给出了相当高的对映选择性。
总体来看,它们具有如下优点:首先是反应不受空气及水分的影响,因此不需要保护并可以在湿的溶剂中进行;其次是催化剂的价格比较便宜,而且它们比某些金属配合物、酶及生物有机催化剂稳定;另外这些手性有机小分子能够负载在有机高分子上进行组合筛选,并且比较方便地经过化学处理后重复使用,因此该类催化剂对传统催化剂起到了很好的补充作用。
一般所使用的手性有机小分子包括天然的和人工合成的两部分。
天然的有机小分子由于性质及价格等方面的原因使用得很少,因此已报道的手性有机小分子催化剂大部分是人工合成的。
除了本文将要讨论的膦(磷)酸酯(酰胺)外,已见报道的还有手性噁唑硼催化剂[2]、手性二茂铁杂环类催化剂[3,4]、手性氨基酸催化剂[5,6]、手性氨基酸盐催化剂[7~9]等等。
最近美国的MacMillan研究小组连续报道了一类新型的咪唑啉酮催化剂[10~15],该类催化剂用于1, 3-偶极环加成等反应中,取得了比较理想的结果。

手性相转移催化剂及其不对称催化反应
宓爱巧;楼荣良;蒋耀忠
【期刊名称】《合成化学》
【年(卷),期】1996(4)1
【摘要】综述了手性季铵盐和手性冠醚两类手性相转移催化剂及其在不对称催化反应(包括加成,取代,氧化及还原等反应)中的应用,参考文献97篇。
【总页数】10页(P13-22)
【作者】宓爱巧;楼荣良;蒋耀忠
【作者单位】不详;不详
【正文语种】中文
【中图分类】O643.32
【相关文献】
1.手性相转移催化剂及其在不对称催化反应中的应用 [J], 曾莎莎;唐瑞仁;Artem Melman;黄可龙
2.L-色氨酸衍生的手性相转移催化剂的合成及其不对称诱导效应 [J], 薛爱英;刘文陆;李培刚;矫桂丽;常学顺;邹志琛
3.手性相转移催化剂合成及其不对称诱导效应--Ⅲ.手性双季铵盐的合成与研究 [J], 李培刚;薛爱英;邹志琛
4.手性相转移催化剂的合成和不对称诱导效应Ⅳ——手性双季铵盐 [J], 邹志琛;矫桂丽;刘文陆;焦晓云;华玉夏
5.手性相转移催化剂的合成和不对称诱导效应——以L-酪氨酸为原料合成的手性单季铵盐和双季铵盐 [J], 任慧平;矫桂丽;杨丽斌;马海兵;邹志琛
因版权原因,仅展示原文概要,查看原文内容请购买。

⼿性磷酸催化剂在不对称合成中的应⽤⼿性磷酸催化剂在不对称合成中的应⽤卫格⾮3130000884摘要⼿性磷酸是⼀类具有新型结构的⾼效,⾼对映选择性强酸性 Brφnsted酸催化剂,21 世纪以来的研究进展迅速,已经成为有机⼩分⼦催化剂的⼀个重要部分。
⼿性磷酸催化剂分⼦内同时含有Lewis 碱性位点和 Brφnsted 酸性位点,可同时活化亲电与亲核底物。
作为⼀种新型双功能有机催化剂,⼿性磷酸具有较⾼的催化活性和对映选择性,⼴泛应⽤于各式各样的有机不对称合成反应中。
关键词⼿性磷酸;不对称有机催化,对映选择性⼿性合成⼀直是有机合成⽅⾯研究的重点之⼀,通过反应获得单⼀⼿性化合物的⽅法主要有三种:⼿性源直接合成;⼿性诱导;不对称催化合成。
⽽不对称催化分为酶催化与化学催化。
由于⼿性酶催化剂价格⾼昂,难以通过⼈⼯合成,故化学催化的意义⼗分重⼤。
⽽化学催化⼜可以根据所⽤到的催化剂种类不同,细分为⾦属催化和有机⼩分⼦催化。
因为⾦属催化⼤多需要⽤到重⾦属,不仅成本较⾼,⽽且易造成重⾦属污染,所以有机⼩分⼦催化剂的研究作为⼀个新兴的催化领域在全世界范围内受到了极⼤的关注。
有机催化剂⼤致可划分为 Lewis 酸、Lewis 碱、Brφnsted 酸、 Brφnsted 碱四类,其中⼿性 Brφnsted 酸有机催化剂是⼀个正在飞速发展的研究领域。
⼿性 Brφnsted 酸催化剂通过与底物形成氢键或向底物转移质⼦,从⽽活化底物,类似于酶通过氢键与底物形成活化过渡态的过程,是⼀种催化不对称反应极为有效的途径。
磷酸衍⽣物与其它 Brφnsted 酸有机催化剂不同,是⼀种具有较强酸性的催化剂。
⼿性磷酸分⼦中,磷原⼦处于⼀个环状的结构中,⽆法通过单键⾃由旋转,因此催化剂具有刚性⽴体构型,从⽽具有⼀定的⽴体构型 , 通过调节其周围的取代基便可改变分⼦在催化过程中的对映选择性;磷原⼦上所连的羟基可作为 Brφnsted 酸的酸性位点提供质⼦或与底物形成氢键,⽽磷原⼦上的双键氧⼜可以作为 Lewis 碱性位点提供孤对电⼦,因此⼿性磷酸类化合物本⾝具有双性催化剂的特点,同时活化亲电试剂与亲核试剂,这不仅可进⼀步提⾼其催化活性,⽽且还可以在反应中更有效地控制⽴体选择性,从⽽实现⾼对映选择性合成。
不对称催化反应在手性物质合成中的应用班级:应用化学08—2班学号:2008302052 姓名:殷金昌摘要:概述了应用不对称催化技术在各类手性有机物合成反应中表现的立体化学特性及优势,因具有催化效率高、选择性高、催化剂用量少、对环境污染小、成本低等优点,不对称催化将发展成合成手性物质最经济有效的一种方法。
另外介绍了不对称催化技术在几种手性物质合成反应中的应用举例,包括:脯胺酸及其衍生物催化的不对称Michael加成反应、由甲基酮不对称催化合成非环状脂肪族光学活性胺的合成反应、由樟脑不对称催化合成莰胺这三个有机合成反应,展现出不对称催化合成技术在合成复杂有机化合物中表现的明显优势。
最后,对不对称催化合成的应用前景作出展望,这种高催化性、高选择性的手性合成技术将会为全世界带来巨大的经济效益和社会效益。
关键词:不对称催化、手性物质、有机合成、应用1.概述不对称催化反应[1-3]的发现与发展是上个世纪化学界乃至整个自然科学领域取得的重要成就之一。
2001年,Knowles、Noyori和Sharpless三位化学家基于他们在不对称氢化反应和不对称氧化反应中的杰出贡献而获得了诺贝尔化学奖,显示该研究领域取得了重大的进展,但是不对催化研究还面临诸多挑战,依然是目前化学学科,乃至药物和材料领域的前沿和研究热点。
我们国家对不对称催化的研究虽然起步较晚,但近十年来,随着国家对手性科学与技术的日益重视,目前我国科学家不仅在基础理论研究方面,诸如具有完全知识产权手性配体及催化剂的制备;新的不对称反应的建立;新概念与新方法的创立;以及手性识别、放大与传递、催化机理等研究方面取得了长足的进展,已在某些方面占据了国际领先的水平,而且在手性技术的开发和手性药物的制备等方面也显示了很好的发展前景。
不对称催化反应是使用非外消旋手性催化剂进行反应的,仅用少量手性催化剂,可将大量前手性底物对映选择性地的转化为手性产物,具有催化效率高、选择性高、催化剂用量少、对环境污染小、成本低等优点。
不对称催化反应的原理
不对称催化反应是指催化剂能够使反应物以两种不对称的方式发生反应,产生对映异构体。
其原理可以归结为手性诱导和对映选择性两个主要因素。
1. 手性诱导:手性催化剂在反应中能够有效地诱导反应物中的手性中心发生不对称转化。
这是因为手性催化剂分子本身具有手性结构,与反应物形成具有一定立体排列的中间体,从而使得反应物在催化剂作用下选择性地发生不对称反应。
2. 对映选择性:手性催化剂在反应中对不对称产物的对映异构体进行选择性催化,使得特定的对映异构体优先生成。
这是因为手性催化剂与反应物之间的相互作用会导致反应中间体具有不同的构象,从而使得不同的对映异构体在反应中的能量差异不同,从而选择性地生成某种对映异构体。
总而言之,不对称催化反应的原理可以归结为手性诱导和对映选择性两个主要因素,通过催化剂的手性结构作用,使反应物以特定的立体排列发生不对称转化,并选择性地生成特定的对映异构体。
不对称催化制备手性药物的研究及应用手性药物是治疗疾病的重要药物之一,它们具有具有对称性的立体异构体,其中至少存在一个手性中心。
手性药物的药效、代谢以及副作用往往会因为它们的对映异构体而产生差异。
因此,对手性药物的合成制备研究具有重要意义。
在手性药物制备中,不对称催化成为目前最为有效的制备手性药物的手段之一。
一、不对称催化的概念与分类不对称催化是指在反应体系中加入具有手性催化剂促进对映异构体产率不同的催化反应。
不对称催化可以被分为金属催化和非金属催化两类。
金属催化是通过一系列匹配的金属离子和手性配体组成复杂体系,使得金属催化剂得到对映异构体产率不同的结果。
非金属催化则主要依靠有机小分子催化剂,通过空间位阻等效应催化反应进行不对称反应,实现对手性药物的制备。
二、不对称催化在手性药物制备中的应用1. 脯氨酸和异亮氨酸的不对称合成脯氨酸和异亮氨酸是人体必需氨基酸,被广泛使用在医药和日用化工等行业。
对于脯氨酸和异亮氨酸的不对称合成,钯催化在手性Cbz谷氨酰胺上(DmsL)与戊烯的羰基重排反应中,将不对称催化转化为了一种非对称环合成方法,成功合成了手性脯氨酸和异亮氨酸类似物。
2. 不对称羟醛合成不对称羟醛的制备是合成手性化合物的一种重要方式。
其一般是通过催化剂诱导的不对称重排反应或不对称醛缩合反应性(如错合反应)形成。
在不对称羟醛合成中,黄教授组提出的新的手性罗丹明催化剂分子是根据原子转移催化(ATC)理论设计的,在非常优异的对映选择性和接受性下,优化反应条件使得合成产率提高到80%以上。
三、不对称催化面临的挑战尽管不对称催化可以推动手性药物制备的进步,但这项技术还是面临着一些挑战。
1. 反应缺陷不对称催化由于催化剂选择性差,容易受到其他反应物影响,导致反应失效。
2. 催化剂的研究尽管已经有许多有效的催化剂,但因催化剂选择性有限或副反应严重,仍需要更有效、更选择性的催化剂。
3. 抗酸碱性钯催化剂在反应中很容易受到酸碱催化剂的影响,进而导致催化剂失去活性,因此需要选择稳定的催化剂或优化反应条件,来提高催化剂的抗酸碱性。