第八章 地球化学系统中的氧化还原反应
- 格式:doc
- 大小:421.50 KB
- 文档页数:11




《氧化还原反应》讲义一、什么是氧化还原反应在化学世界中,氧化还原反应是一类极其重要的化学反应。
简单来说,氧化还原反应是指在反应过程中,元素的氧化态(化合价)发生了变化的反应。
氧化态的变化是氧化还原反应的核心特征。
当一种物质中的元素氧化态升高,我们就说这个元素被氧化了;反之,当元素的氧化态降低,我们就说这个元素被还原了。
例如,氢气(H₂)和氧气(O₂)反应生成水(H₂O)的过程就是一个典型的氧化还原反应。
在这个反应中,氢元素的化合价从 0 价升高到+1 价,氢被氧化;氧元素的化合价从 0 价降低到-2 价,氧被还原。
二、氧化还原反应的特征氧化还原反应有几个显著的特征。
首先,氧化还原反应一定伴随着电子的转移。
电子从被氧化的物质转移到被还原的物质。
其次,氧化还原反应中,氧化剂和还原剂同时存在。
氧化剂在反应中得到电子,化合价降低;还原剂在反应中失去电子,化合价升高。
再者,氧化还原反应前后,元素的种类和原子的个数不变,遵循质量守恒定律。
三、氧化剂和还原剂氧化剂是在氧化还原反应中能够得到电子,使其他物质氧化,自身被还原的物质。
常见的氧化剂有氧气、氯气、高锰酸钾等。
以高锰酸钾(KMnO₄)受热分解制取氧气的反应为例,高锰酸钾中的锰元素化合价从+7 价降低到+4 价和+6 价,高锰酸钾是氧化剂。
还原剂则是在氧化还原反应中能够失去电子,使其他物质还原,自身被氧化的物质。
常见的还原剂有氢气、一氧化碳、金属单质等。
比如在氢气还原氧化铜(H₂+ CuO = Cu + H₂O)的反应中,氢气中的氢元素化合价从 0 价升高到+1 价,氢气是还原剂。
四、氧化还原反应的表示方法为了清晰地表示氧化还原反应中电子的转移情况,我们通常采用双线桥法和单线桥法。
双线桥法是从反应物中化合价发生变化的元素指向生成物中相应元素,在线桥上标明电子的得失和化合价的升降。
例如,对于铜与硝酸的反应:3Cu + 8HNO₃(稀) = 3Cu(NO₃)₂+2NO↑ + 4H₂O双线桥表示为:从 Cu 指向 Cu(NO₃)₂,线上标明“失去 6e⁻,化合价升高”;从 HNO₃指向 NO,线上标明“得到 6e⁻,化合价降低”。
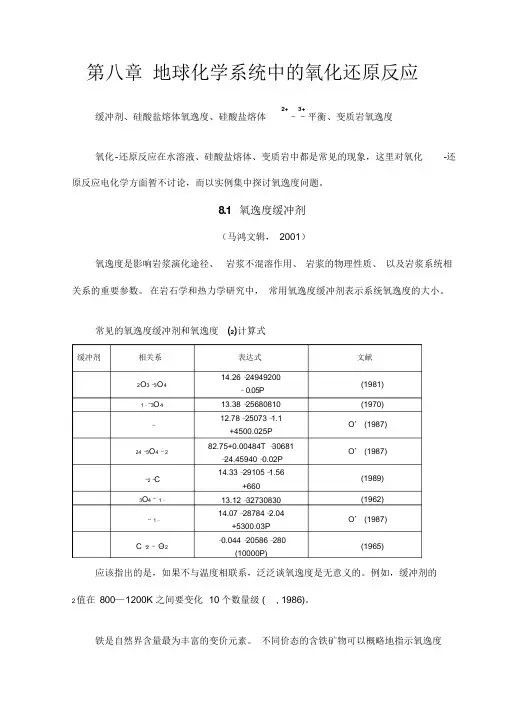
缓冲剂 相关系表达式 文献 2O 3–3O 414.26 –24949200–0.05P 13.38 –25680810 12.78–25073–1.1 +4500.025P 82.75+0.00484T –30681–24.45940 –0.02P 14.33–29105–1.56+660 13.12 –32730830 14.07–28784–2.04+5300.03P –0.044 –20586–280(10000P)(1981) 1––3O 4(1970) –O ’ (1987) 24–3O 4–2O ’ (1987)–2–C (1989) 3O 4–1–(1962) –1– O ’ (1987)C –2 ––O 2(1965)第八章 地球化学系统中的氧化还原反应缓冲剂、硅酸盐熔体氧逸度、硅酸盐熔体2+3+––平衡、变质岩氧逸度氧化-还原反应在水溶液、硅酸盐熔体、变质岩中都是常见的现象,这里对氧化 -还原反应电化学方面暂不讨论,而以实例集中探讨氧逸度问题。
8.1 氧逸度缓冲剂(马鸿文辑, 2001)氧逸度是影响岩浆演化途径、 岩浆不混溶作用、 岩浆的物理性质、 以及岩浆系统相关系的重要参数。
在岩石学和热力学研究中, 常用氧逸度缓冲剂表示系统氧逸度的大小。
常见的氧逸度缓冲剂和氧逸度 (2)计算式应该指出的是,如果不与温度相联系,泛泛谈氧逸度是无意义的。
例如,缓冲剂的2 值在 800—1200K 之间要变化 10 个数量级 ( , 1986)。
铁是自然界含量最为丰富的变价元素。
不同价态的含铁矿物可以概略地指示氧逸度222 222 2的相对大小。
由自然铁 ()→方铁矿( 2+)→磁铁矿( 23+)→赤铁矿( 3+),反映了其结晶时的氧逸度依次增高。
在火山岩中,铁镁矿物和氧逸度之间的平衡主要决定于熔体和斑晶相矿物的总成分。
在相似的温度下, 随氧逸度由低到高, 铁镁矿物一般将依次出现橄榄石、 斜方辉石、角闪石和黑云母。






第八章地球化学系统中的氧化还原反应缓冲剂、硅酸盐熔体氧逸度、硅酸盐熔体Fe2+––Fe3+平衡、变质岩氧逸度氧化-还原反应在水溶液、硅酸盐熔体、变质岩中都是常见的现象,这里对氧化-还原反应电化学方面暂不讨论,而以实例集中探讨氧逸度问题。
8.1 氧逸度缓冲剂(马鸿文辑,2001)氧逸度是影响岩浆演化途径、岩浆不混溶作用、岩浆的物理性质、以及岩浆系统相关系的重要参数。
在岩石学和热力学研究中,常用氧逸度缓冲剂表示系统氧逸度的大小。
常见的氧逸度缓冲剂和氧逸度(lgfO2)计算式应该指出的是,如果不与温度相联系,泛泛谈氧逸度是无意义的。
例如,HM缓冲剂的lgfO2值在800—1200K之间要变化10个数量级(Nordstrom and Munoz, 1986)。
铁是自然界含量最为丰富的变价元素。
不同价态的含铁矿物可以概略地指示氧逸度的相对大小。
由自然铁(Fe)→方铁矿(Fe 2+)→磁铁矿(Fe 2++Fe 3+)→赤铁矿(Fe 3+),反映了其结晶时的氧逸度依次增高。
在火山岩中,铁镁矿物和氧逸度之间的平衡主要决定于熔体和斑晶相矿物的总成分。
在相似的温度下,随氧逸度由低到高,铁镁矿物一般将依次出现橄榄石、斜方辉石、角闪石和黑云母。
为讨论问题的方便,人们常用相对于FMQ 缓冲剂的氧逸度(FMQ)lgf Δ2O 来表示岩浆系统氧逸度的大小,定义为(FMQ)f lg lgf (FMQ)lgf Δ222O O O -=。
某些火成岩(FMQ)lgf Δ2O 值如为:接近液相线的各种基性熔岩和大多数亏损型地幔尖晶石二辉橄榄石(mg# = 0.90)的(FMQ)lgf Δ2O = ±2.0,含铁橄榄石斑晶的流纹岩的(FMQ)lgf Δ2O = 0.5—2.0,含斜方辉石和角闪石斑晶的流纹岩和英安岩的(FMQ)lgf Δ2O = 1.0—2.0,含黑云母和/或角闪石斑晶的流纹岩的(FMQ)lgf Δ2O = 2.0—3.0。
第八章 地球化学系统中的氧化还原反应缓冲剂、硅酸盐熔体氧逸度、硅酸盐熔体Fe 2+––Fe 3+平衡、变质岩氧逸度氧化-还原反应在水溶液、硅酸盐熔体、变质岩中都是常见的现象,这里对氧化-还原反应电化学方面暂不讨论,而以实例集中探讨氧逸度问题。
8.1 氧逸度缓冲剂(马鸿文辑,2001)氧逸度是影响岩浆演化途径、岩浆不混溶作用、岩浆的物理性质、以及岩浆系统相关系的重要参数。
在岩石学和热力学研究中,常用氧逸度缓冲剂表示系统氧逸度的大小。
缓冲剂的lgfO 2值在800—1200K 之间要变化10个数量级(Nordstrom and Munoz, 1986)。
铁是自然界含量最为丰富的变价元素。
不同价态的含铁矿物可以概略地指示氧逸度的相对大小。
由自然铁(Fe)→方铁矿(Fe 2+)→磁铁矿(Fe 2++Fe 3+)→赤铁矿(Fe 3+),反映了其结晶时的氧逸度依次增高。
在火山岩中,铁镁矿物和氧逸度之间的平衡主要决定于熔体和斑晶相矿物的总成分。
在相似的温度下,随氧逸度由低到高,铁镁矿物一般将依次出现橄榄石、斜方辉石、角闪石和黑云母。
为讨论问题的方便,人们常用相对于FMQ 缓冲剂的氧逸度(FMQ)lgf Δ2O 来表示岩浆系统氧逸度的大小,定义为(FMQ)f lg lgf (FMQ)lgf Δ222O O O -=。
某些火成岩(FMQ)lgf Δ2O 值如为:接近液相线的各种基性熔岩和大多数亏损型地幔尖晶石二辉橄榄石(mg# = 0.90)的(FMQ)lgf Δ2O = ±2.0,含铁橄榄石斑晶的流纹岩的(FMQ)lgf Δ2O = 0.5—2.0,含斜方辉石和角闪石斑晶的流纹岩和英安岩的(FMQ)lgf Δ2O = 1.0—2.0,含黑云母和/或角闪石斑晶的流纹岩的(FMQ)lgf Δ2O = 2.0—3.0。
大多数洋底玄武岩的相对氧逸度在NNO 之下3个lg 单位。
富碱贫硅的基性熔岩较之拉斑玄武岩的氧逸度要高许多,并可出现早期结晶的硫酸盐矿物。
洋底玄武岩具有相对稳定的氧逸度的原因是其含有足够量的硫,足以作为500ppm O 2的缓冲池。
对于任何富铁玄武岩的分异趋势,为使O 2缓冲所需的硫为500ppm 。
对于较小富铁的液相下降线,所需硫的浓度更小。
实际上,洋底玄武岩硫的丰度为1000—1800ppm 。
这就使整个岩浆通过硫化物氧化为硫酸盐的反应、从而作为一个封闭的化学系统而分异,维持一个相对恒定的氧逸度范围。
在粗安岩-流纹岩质熔体中,硬石膏在(NNO)lgf Δ2O >1.0—1.5的范围稳定存在。
在(NNO)lgf Δ2O <2.5—3.0的区域内,磁黄铁矿(或富FeS 的液态硫化物相)稳定存在。
在(NNO)lgf Δ2O =1.0—1.5至2.5—3.0区间,硬石膏与磁黄铁矿稳定共存。
8.2 岩浆岩的氧逸度(马鸿文辑,2001)铁是硅酸盐浆中呈两种价态存在的主要元素,Fe 2+––Fe 3+平衡不仅显著地影响岩浆作用的演化趋势,而且由于Fe 2+和Fe 3+在熔体相中具有不同的结构,从而影响熔体的性质,例如密度和黏度等。
氧是岩浆中具有相当化学活动性的组分。
岩浆演化过程中氧逸度的变化明显地影响岩浆的结构、流变学性质、化学成分和岩浆系统的相关系。
对熔体相Fe 2+––Fe 3+平衡的研究,可以获得氧逸度变化的信息,因而具有重要的岩石学意义。
8.2.1 橄榄石+斜方辉石+尖晶石组合与火成岩的氧逸度氧逸度是地幔作用过程中一个基本的、但又是了解得较少的一个强度变量。
对上地幔氧逸度的研究具有以下重要意义:(1)研究上地幔的氧逸度是否适合于富铁金属相的分凝作用而形成地核。
这对于研究地球的早期演化历史至关重要;(2)上地幔的氧逸度控制着与元素碳(石墨或金刚石)处于平衡状态下C-H-O 系统流体相的赋存状态。
C-H-O 流体在相对高氧逸度(约FMQ)的氧化条件下,主要呈CO 2+H 2O 。
在中等还原条件下(FMQ 缓冲剂以下2—3个lg 单位),呈H 2O+CH 4。
在低氧逸度(IW 缓冲剂)的强还原条件下,则主要呈CH 4+H 2(Wood and Virgo, 1989)。
因此,氧逸度通过影响流体相的赋存状态间接地影响含挥发份条件下的上地幔部分熔融作用和地幔交代作用。
氧逸度也直接控制着在地球深部是否存在着永远耗不尽的天然气(O’Neill and Wall, 1987)?确定上地幔氧逸度的方法主要有三种:(1)采用电化学方法直接测定地幔橄榄岩包体的内在氧逸度;(2)通过分析原生玄武岩的Fe 2O 3、FeO 含量来间接了解上地幔源区的氧逸度;(3)采用矿物温压计方法,根据相平衡实验或有关的热力学资料,计算地幔岩的矿物组合平衡的氧逸度。
对于上地幔I 型(或A 型,铬透辉石组合)和II 型(或B 型,铝普通辉石组合)尖晶石二辉橄榄岩和方辉橄榄岩,其矿物组合平衡的氧逸度可以由以下的平衡反应来计算(Mattioli and Wood, 1988):6Fe 2SiO 4 + O 2 = 3Fe 2Si 2O 6 + 2Fe 3O 4olivine fluid orthopyroxene spinel这一反应可称为FFM(fayalite-ferrosilite-magnetite)缓冲剂。
但是,实际上,由FFM 组合计算氧逸度时受到尖晶石相中Fe 3O 4组分活度-成分关系(模型)的不确定度的严格限制。
因为在地幔尖晶石中,Fe 3O 4端元组分的含量很低(X Fe3O4=0.02—0.10,Mattioli and Wood, 1988)。
对天然矿物的电子探针分析的一般误差将导致氧逸度计算结果相当大的误差。
鉴于此,Ballaus et al. (1991)对人工合成的尖晶石二辉橄榄岩、方辉橄榄岩进行了相平衡实验,对ol+opx+spn 氧逸度计予以标定。
实验条件为T=1040—1300ºC 、P=0.3—2.7 GPa 。
氧逸度由Fe-FeO(IW)、WC-WO 2-C(WCO)、Ni-NiO(NNO)、Fe 3O 4-Fe 2O 3(HM)缓冲剂所控制。
选择石墨、橄榄石、PdAg 合金作为试样容器。
实验在活塞压力罐中和流体过剩的条件下进行。
结果表明,在实验的温度、压力、成分范围内,尖晶石相的Fe 3+/tot Fe 比值是氧逸度的线性函数(f O2=IW, Fe 3+/tot Fe=0.02, WCO, 0.10, NNO, 0.25, HM, 0.75)。
在一定的(FMQ)lgf ΔO2下,尖晶石相的Fe 3+/tot Fe 比值与温度无关,而随尖晶石的Cr 含量的增大略有减小,随压力的增大而降低。
在一定的温度、熔融程度、总成分下,尖晶石的Cr/(Cr+Al)比值随氧逸度的升高而增大。
Ballhaus et al. (1991)的实验中,尖晶石覆盖了很宽的成分范围:Cr/(Cr+Al) = 0.20—0.85, Fe 3+/tot Fe = 0.020—0.80。
因此,有可能对FFM 缓冲剂进行标定。
对于橄榄石+斜方辉石+尖晶石(FFM)组合,氧逸度由下式给出:Spn Mgt Opx Fs OlFa 000O22lga 3lga 6lga 2.303RTV P ΔH ΔS T Δlgf ++---= 相对于FMQ 缓冲剂的氧逸度为: Spn MgtOpx Fs OlFa 0FMQ 0FFM 0FMQ 0FFM 0FMQ 0FFM O22lga 3lga 6lga 2.303RT )V Δ P(V ) H H (Δ)S ΔS T (Δ(FMQ)lgf Δ++------=Ballhaus et al. (1991)采用最小二乘法拟合实验资料,得到如下氧逸度计算公式:/T )2630(X 4lgX 2lgX /T)X 3200(16lga 400P/T 2505/T 0.27(FMQ)lgf Δ2SpnAl SpnFe3SpnFe22Ol Fe Ol Fa O2+++----+=++式中P 的单位为GPa ,+++=33Spn Fe3R /ΣFe X ,+=3Spn Al R Al/ΣX ,)Fe /(FeFe X 322Fe2+++++=。
为了简化计算,上式中消去的相当于OlFa a 理想部分的斜方辉石一项。
以上公式仅适用于地幔岩,不应该外推到Ol Fe X >0.15的富铁岩石。
对于更富铁的岩石,消去斜方辉石的简化是不正确的。
该方法也不适用于石榴石二辉橄榄岩和金刚石稳定区的条件。
因为在高Spn Cr X 和低氧逸度下,会出现镁方铁矿不符合化学计量性质或尖晶石相Cr 2+的替代作用。
实际应用表明,将上式应用于低至约800ºC 的温度下,仍可获得合理的结果。
应该强调指出,虽然在上式中未出现斜方辉石,但是,只有在橄榄石和斜方辉石同时存在而使系统的SiO2a 得以缓冲的条件下,所计算的氧逸度才是正确的。
Ionov and Wood (1992)应用Ballhaus et al. (1991)的方法,发现与实验平衡的Ol+Opx+Spn 组合的氧逸度并不一致,其误差达0.5—1.0个lg 单位,与尖晶石的Cr/Al比值具有依赖关系。
Ionov and Wood (1992)指出,采用尖晶石相中Fe 3O 4活度的Nell —Wood 模型,可以获得更精确的(0.3—0.5个lg 单位)与实验结果相吻合的氧逸度计算结果。
在800—1300ºC 下,对于Fe3O4X = 0.008—0.060的地幔尖晶石,其Fe 3O 4的活度为:Cr Mg Cr Al 2Cr AlMg 2Al 2Fe3Fe2Fe3O4N 346N N 199N 229N N 653N 1/T (406N /4)N lg(N lga +++++=++式中Ni 为以4个氧为准计算的尖晶石分子式中元素的数量。
反应43622242O 2Fe O Si 3Fe O SiO 6Fe +=+的氧逸度为:Spn Fe3O4Opx M2Fe M1Fe 2Ol Mg OlFeO2O22lga )X 3lg(X /T )2620(X - 12lgX -/T 3690P(GPa)-0.35220/T (K)(FMQ)lgf lgf ++++=由该式计算的氧逸度误差为±0.5个lg 单位。
氧逸度的岩石学应用将Ballhaus et al. (1991)的方法应用于典型的地幔岩和地幔衍生的原生熔体,揭示了如下的氧逸度变化趋势:未亏损的、富集型地幔源区及其衍生的熔体呈中等还原状态((FMQ)lgf Δ2O ≌FMQ —2);亏损型MORB 和深海橄榄岩呈(FMQ)lgf Δ2O ≌FMQ —1的氧化状态,可能代表了最上部大洋岩石圈的典型的氧逸度条件;富集型MORB 和交代的尖晶石方辉橄榄岩更为氧化((FMQ)lgf Δ2O =FMQ —FMQ+1);而岛弧玄武岩(IAB)和阿拉斯加型侵入体是最为氧化的火成岩(((FMQ)lgf Δ2O ≌FMQ+2)。