有关晶胞的计算
- 格式:ppt
- 大小:1.78 MB
- 文档页数:60




晶胞的有关计算:体积、微粒数、晶体密度一、如何利用晶胞参数计算晶胞体积?平行六面体的几何特征可用边长关系和夹角关系确定。
布拉维晶胞的边长与夹角叫做晶胞参数。
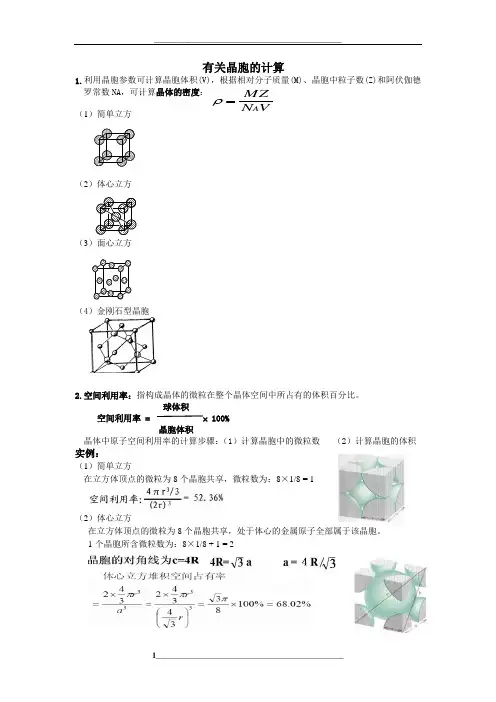
共有7种不同几何特征的三维晶胞,称为布拉维系,它们的名称、英文名称、符号及几何特征如下:立方cubic(c)a=b=c,α=β=γ=90°,(只有一个晶胞参数a)四方tetragonal(t)a=b≠c,α=β=γ=90°,(有2个晶胞参数a 和c)六方hexagonal(h)a=b≠c,α=β=90°,γ=120°,(有2个晶胞参数a 和c)正交orthorhombic(o)a≠b≠c,α=γ=90°,(有3个晶胞参数a,b 和c)单斜monoclinic(m)a≠b≠c,α=γ=90°,β≠90°,(有4个晶胞参数a,b,c 和β) 三斜anorthic(a)a≠b≠c,α≠β≠γ,(有6个晶胞参数a,b,c,α,β和γ)菱方rhombohedral(R)a=b=c,α=β=γ≠90°,(有2个晶胞参数a 和α)六方a^2Xcsin120正交V=abc单斜V=abcsin β三斜V=abc(1-cos2α-cos2β-cos2γ+2cos αcos βcos γ)菱方V=a^3(1-3cos2α+2(cos α)^3)二、均摊法---计算晶胞中的粒子数位于晶胞顶点的微粒,实际提供给晶胞的只有1/8;位于晶胞棱边的微粒,实际提供给晶胞的只有1/4;位于晶胞面心的微粒,实际提供给晶胞的只有1/2;位于晶胞中心的微粒,实际提供给晶胞的只有1.三、晶胞的密度计算1) 利用晶胞参数可计算晶胞体积(V),根据相对分子质量(M)、晶胞中粒子数(Z)和阿伏伽德罗NA ,可计算晶体的密度ρ:V N MZ A =ρ。

晶胞的计算一、晶胞在高考中的地位分析:2008、2009年新课标,未对晶胞的计算进行考查;2010年新课标:37(4),一空,化学式的计算;2011年新课标:37(5),三空,晶胞中原子个数及密度的计算;2012年新课标:37(6),两空,晶胞密度、离子距离的计算。
二、常见的晶胞计算题:第一类:金属堆积方式的简单计算(空间利用率和密度)[选三P76] 晶胞密度 =m(晶胞)/V(晶胞)空间利用率=[V(球总体积)/V(晶胞体积)]×100%【注】1m=10dm=102 cm=103 mm=106 um=109 nm=1012 pm①简单立方堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:②体心立方堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:③面心立方最密堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:再假设该金属的摩尔质量为Mg/mol,N A为阿伏伽德罗常数的数值,试计算该晶胞的密度:【总结】必须掌握的常见晶胞及晶体结构分子晶体:干冰、冰晶胞图形、晶胞组成特点;原子晶体:金刚石(晶体硅)、二氧化硅晶胞组成特点、边长(体积、密度、原子最近距离)的计算方式;金属晶体:四种堆积方式的名称、图形、代表金属、边长(体积、密度、原子最近距离)的计算方式;离子晶体:NaCl、CsCl、CaF2晶胞图形、晶胞组成、边长(体积、密度、原子最近距离)的计算方式。
【练习】中学化学教材中展示了NaCl晶体结构,它向三维空间延伸得到完美晶体。
NiO(氧化镍)晶体的结构与NaCl 相同,Ni2+与最临近O2-的核间距离为 a cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7 g/mol)。
(2)天然和绝大部分人工制备的晶体都存在各种缺陷,例如在某氧化镍晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。
其结果为晶体仍呈电中性,但化合物中Ni 和O的比值却发生了变化。

晶胞参数计算公式晶胞参数是材料表征的重要参数,因而晶胞参数的计算十分重要。
本文针对晶胞参数的计算,详细介绍了晶胞参数计算公式中的一些重要概念及计算方法。
首先,晶胞参数是描述物质电学性质的概念,包括晶胞体积、晶胞定律、晶格常数和晶体结构等。
其中晶胞体积指:物质经过特定初始条件下晶胞构型变化后占用的总空间,是两个基本晶胞参数。
晶胞定律指:晶胞的长、宽、高之间的关系,是一种结构参数的表示。
晶格常数指:两个原子之间的距离,是一种晶胞结构参数的表示。
晶体结构是指:物质中原子构成的定向三维晶体结构。
晶胞参数计算公式包括晶胞参数计算公式和晶格常数计算公式。
晶胞参数计算公式用于计算晶胞体积,晶胞定律及晶体结构,主要有两种计算方法:一种是基于原子坐标的公式,如Bravais(1848)公式、Voronoi(1908)公式和Ginzburg-Landau(1950)公式;另一种是基于晶胞参数的公式,如Hilbert(1912)公式、Madelung(1925)公式和Ladd(1977)公式。
晶格常数计算公式用于计算晶格参数,主要有两种计算方法:一种是基本元素计算法,如Weaire(1892)公式和Morse(1931)公式;另一种是分子力学计算法,如Lennard-Jones(1938)公式和Stillinger-Weber(1985)公式。
现代晶体学通过实验测量元素晶体中原子间距离,利用晶胞参数和晶格常数计算公式,可以准确地确定晶体结构,进而研究物质的物理性质,为应用物理学的发展作出贡献。
在电子结构的计算中,也使用晶胞参数和晶格常数计算公式,分析不同晶体结构的能带结构和电子电荷密度等。
因此,晶胞参数计算公式和晶格常数计算公式是材料表征的重要工具,它们是物理化学所不可缺少的技术手段,极大地提高了研究物质性质的精度。
无论是在材料物理研究中,还是在电子结构计算中,晶胞参数计算公式和晶格常数计算公式都是物理学家必备的技术工具,必将对物理研究和应用物理学的发展产生重要作用。

晶胞的计算一、晶胞在高考中的地位分析:2008、2009年新课标,未对晶胞的计算进行考查;2010年新课标:37(4),一空,化学式的计算;2011年新课标:37(5),三空,晶胞中原子个数及密度的计算;2012年新课标:37(6),两空,晶胞密度、离子距离的计算。
二、常见的晶胞计算题:第一类:金属堆积方式的简单计算(空间利用率和密度)[选三P76]晶胞密度 =m(晶胞)/V(晶胞)空间利用率=[V(球总体积)/V(晶胞体积)]×100%【注】1m=10dm=102 cm=103 mm=106 um=109 nm=1012 pm①简单立方堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:②体心立方堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:③面心立方最密堆积:假设球的半径为r cm,则该堆积方式的空间利用率为:再假设该金属的摩尔质量为Mg/mol,N A为阿伏伽德罗常数的数值,试计算该晶胞的密度:【总结】必须掌握的常见晶胞及晶体结构分子晶体:干冰、冰晶胞图形、晶胞组成特点;原子晶体:金刚石(晶体硅)、二氧化硅晶胞组成特点、边长(体积、密度、原子最近距离)的计算方式;金属晶体:四种堆积方式的名称、图形、代表金属、边长(体积、密度、原子最近距离)的计算方式;离子晶体:NaCl、CsCl、CaF2晶胞图形、晶胞组成、边长(体积、密度、原子最近距离)的计算方式。
【练习】中学化学教材中展示了NaCl晶体结构,它向三维空间延伸得到完美晶体。
NiO(氧化镍)晶体的结构与NaCl 相同,Ni2+与最临近O2-的核间距离为a cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7 g/mol)。
(2)天然和绝大部分人工制备的晶体都存在各种缺陷,例如在某氧化镍晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。
其结果为晶体仍呈电中性,但化合物中Ni 和O的比值却发生了变化。



布拉格方程算晶胞参数
布拉格方程是描述衍射现象的基本公式,它可以用于计算晶体的晶胞参数。
晶胞参数是描述晶体结构的重要参数,包括晶胞长度、晶胞角度等。
通过布拉格方程,我们可以通过测量晶体衍射图案的角度和波长信息,推导出晶胞参数的数值。
布拉格方程的数学表达式为:
nλ=2dsinθ
其中,n为衍射的阶次,λ为入射光的波长,d为晶胞的晶格常数,θ为衍射角度。
通过这个方程,我们可以通过已知的入射光波长和衍射角度,来计算晶胞的晶格常数。
具体计算晶胞参数的步骤如下:
首先,进行实验测量,获取入射光波长和衍射角度的数值。
然后,根据布拉格方程,代入已知数值进行计算。
根据所得到的结果,可以进一步推导出晶格常数。
最后,根据晶格常数的数值,可以计算出晶胞的长度和角度等参数。
需要注意的是,在进行实验测量时,要确保测量的准确性和可靠性。
同时,需要注意晶体的特性以及衍射条件的选择,以保证计算结果的准确性。
通过布拉格方程计算晶胞参数,可以帮助我们深入了解晶体的结构特性。
这对于材料科学、固体物理等领域的研究具有重要意义。
同时,对于材料的合成和性能优化等方面也有一定的指导作用。
总之,布拉格方程是计算晶胞参数的重要工具,通过合理的实验设计和准确的测量数据,可以得到精确的结果,为晶体结构研究提供有力支持。
晶胞的计算二、常见的晶胞计算题:晶胞密度ρ =m(晶胞)/V(晶胞)空间利用率=[V(球总体积)/V(晶胞体积)]×100% 【注】1m =10dm =102cm =103mm =106um =109nm =1012pm① 简单立方堆积:假设球的半径为r cm ,则该堆积方式的空间利用率为:② 体心立方堆积:假设球的半径为r cm ,则该堆积方式的空间利用率为:③ 面堆积:,则该堆积方式的空间利用率为:Mg/mol ,N A 为阿伏伽德罗常数的数值,试计算该晶胞的密度:总结】必须掌握的常见晶胞及晶体结构分子晶体:干冰、冰晶胞图形、晶胞组成特点;原子晶体:金刚石(晶体硅)、二氧化硅晶胞组成特点、边长(体积、密度、原子最近距离)的计算方式;金属晶体:四种堆积方式的名称、图形、代表金属、边长(体积、密度、原子最近距离)的计算方式;离子晶体:NaCl 、CsCl 、CaF 2晶胞图形、晶胞组成、边长(体积、密度、原子最近距离)的计算方式。
【练习】中学化学教材中展示了NaCl 晶体结构,它向三维空间延伸得到完美晶体。
NiO(氧化镍)晶体的结构与NaCl 相同,Ni 2+与最临近O 2-的核间距离为a cm ,计算NiO晶体的密度(已知NiO 的摩尔质量为74.7 g/mol)。
(2)天然和绝大部分人工制备的晶体都存在各种缺陷,例如在某氧化镍晶体中就存在如图所示的缺陷:一个Ni 2+空缺,另有两个Ni 2+被两个Ni 3+所取代。
其结果为晶体仍呈电中性,但化合物中Ni 和O 的比值却发生了变化。
某氧化镍样品组成为Ni 0.97O ,试计算该晶体中Ni 3+ 与Ni 2+的离子个数之比。
第二类:晶胞灵活变形及计算【例1:2012年新课标·37】【化学——选修3物质结构与性质】(15分)VIA 族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA 族元素的化合物在研究和生产中有许多重要用途。
晶胞的计算
化学晶胞计算公式:M=Na×N。
构成晶体的最基本的几何单元称为晶胞(Unit Cell),其形状、大小与空间格子的平行六面体单位相同,保留了整个晶格的所有特征。
晶胞是能完整反映晶体内部原子或离子在三维空间分布之化学-结构特征的平行六面体最小单元。
分子是由组成的原子按照一定的键合顺序和空间排列而结合在一起的整体,这种键合顺序和空间排列关系称为分子结构。
由于分子内原子间的相互作用,分子的物理和化学性质不仅取决于组成原子的种类和数目,更取决于分子的结构。
六方晶系晶胞体积计算公式晶胞是晶体中最基本的结构单位,晶胞的体积大小对于研究晶体性质和结构具有重要意义。
在六方晶系中,晶胞的形状是一个长方体,其中两条边相等,与其他四条边垂直。
晶胞体积的计算公式可以通过晶胞的边长和夹角来求解。
六方晶系晶胞的体积计算公式如下:V = a^2 * c * sin(β)其中,V表示晶胞的体积,a表示晶胞的边长,c表示晶胞的高度(也称为c轴长度),β表示两条边夹角(也称为α角)。
为了更好地理解这个公式,我们可以通过一个具体的例子来说明。
假设有一个六方晶系晶胞,其中边长a为5 Å,c轴长度c为8 Å,两条边夹角β为120°。
我们可以利用上述公式来计算该晶胞的体积。
根据给定的数值,我们将其代入公式中:V = (5 Å)^2 * 8 Å * sin(120°)接下来,我们需要计算sin(120°)的值。
根据三角函数表,sin(120°)等于√3/2。
将这个值代入公式中,我们可以得到:V = (5 Å)^2 * 8 Å * √3/2简化计算后,我们得到:V = 100 Å^3 * 8 Å * √3/2进一步简化,我们得到:V = 400 Å^3 * √3我们可以使用计算器或数学软件来计算√3的值,得到:V ≈ 692.82 Å^3因此,该六方晶系晶胞的体积约为692.82 Å^3。
通过这个例子,我们可以看到,六方晶系晶胞体积的计算公式是非常简单和直观的。
只需知道晶胞的边长、高度和两条边的夹角,就可以轻松地计算出晶胞的体积。
需要注意的是,在使用该公式计算晶胞体积时,边长和高度的单位需要保持一致,常见的单位有Å(埃)和nm(纳米)。
此外,夹角β的单位通常为度数。
六方晶系晶胞体积计算公式的应用非常广泛。
在材料科学、固体物理、化学等领域,研究人员经常需要计算晶体的体积,以了解晶体的结构和性质。