神经内分泌肿瘤 病例分享 胃神经内分泌肿瘤
- 格式:ppt
- 大小:5.73 MB
- 文档页数:48
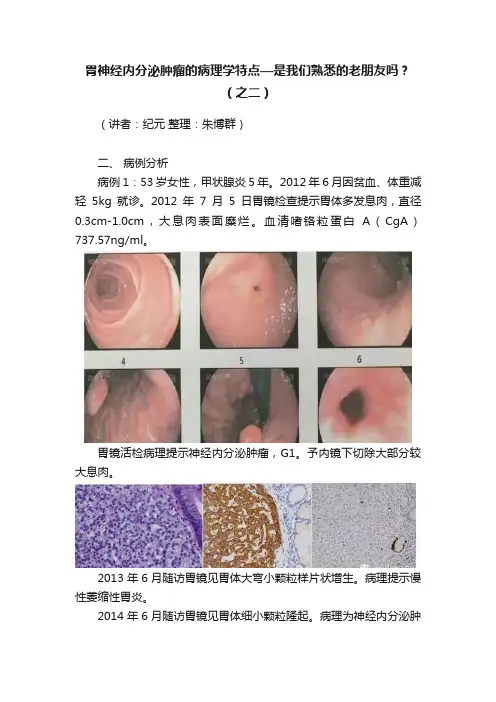
胃神经内分泌肿瘤的病理学特点—是我们熟悉的老朋友吗?(之二)(讲者:纪元整理:朱博群)二、病例分析病例1:53岁女性,甲状腺炎5年。
2012年6月因贫血、体重减轻5kg就诊。
2012年7月5日胃镜检查提示胃体多发息肉,直径0.3cm-1.0cm,大息肉表面糜烂。
血清嗜铬粒蛋白A(CgA)737.57ng/ml。
胃镜活检病理提示神经内分泌肿瘤,G1。
予内镜下切除大部分较大息肉。
2013年6月随访胃镜见胃体大弯小颗粒样片状增生。
病理提示慢性萎缩性胃炎。
2014年6月随访胃镜见胃体细小颗粒隆起。
病理为神经内分泌肿瘤G1。
2015年4月来我院复查并行ESD切除。
低倍镜下可见胃黏膜萎缩变薄周围胃黏膜可见腺瘤样增生、异性增生/原位类癌:直径<0.5mm。
腺瘤样增生异性增生/原位类癌:直径<0.5该患者的最终病理诊断:胃I型神经内分泌肿瘤。
(胃底多发息肉ESD切除)分化好神经内分泌瘤,G1 (ki-67 +1%, 核分裂<1>1>2), 以粘膜内为主,个别肿瘤浸润至粘膜下层; 肿瘤周围固有腺体萎缩伴幽门腺化生及肠化,并可见神经内分泌细胞呈线性增生、微小结节状增生、腺瘤样增生及异性增生等多种增生改变。
(胃体活检)固有腺体萎缩伴肠化、粘膜肌增生, 神经内分泌细胞呈线性增生及微小结节状增生。
(胃窦活检)胃泌素阳性G细胞呈线性增生。
I型gNENs的发病机制如下图所示,因此组织病理学表现多为分化良好的NET G1,伴有胃底/体神经内分泌细胞增生,胃窦G细胞增生,胃底/体腺体减少等。
临床特点是:常见于女性,多为非功能性,70-80%患者在50岁和70岁时被诊断,容易复发,少有转移。
临床表现多不典型,表现为嗳气、上腹部胞胀或头晕乏力(大细胞或缺铁性贫血贫血:胃酸排除进行性减少导致VitB12吸收障碍)。
胃镜特点是胃底/体多发息肉样隆起,病灶小,直径多为0.2cm-1.5cm,周围胃粘膜呈萎缩性胃炎表现。
根据Simona Grozinsky-Glasberg2013年在WJG发表的一篇关于神经内分泌瘤的文章指出1型gNETs转移的相关危险因素包括:肿瘤直径≥1cm,Ki-67指数较高(平均为6.8%),胃泌素水平较高(平均为2138U/L)。
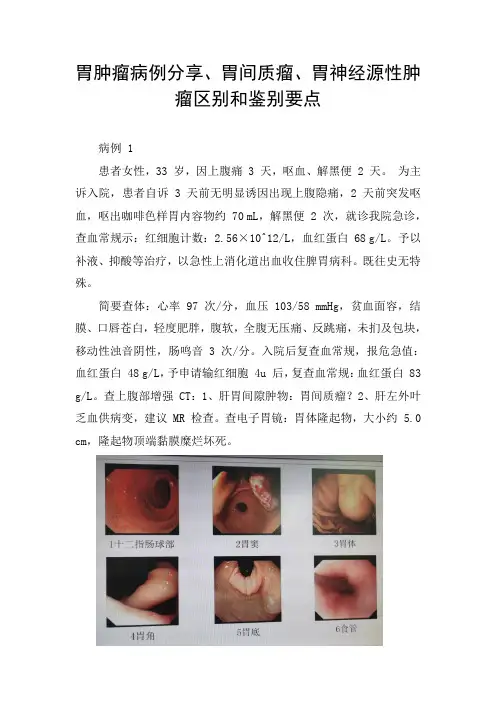
胃肿瘤病例分享、胃间质瘤、胃神经源性肿瘤区别和鉴别要点病例 1患者女性,33 岁,因上腹痛 3 天,呕血、解黑便 2 天。
为主诉入院,患者自诉 3 天前无明显诱因出现上腹隐痛,2 天前突发呕血,呕出咖啡色样胃内容物约 70 mL,解黑便 2 次,就诊我院急诊,查血常规示:红细胞计数:2.56×10^12/L,血红蛋白 68 g/L。
予以补液、抑酸等治疗,以急性上消化道出血收住脾胃病科。
既往史无特殊。
简要查体:心率 97 次/分,血压 103/58 mmHg,贫血面容,结膜、口唇苍白,轻度肥胖,腹软,全腹无压痛、反跳痛,未扪及包块,移动性浊音阴性,肠鸣音 3 次/分。
入院后复查血常规,报危急值:血红蛋白 48 g/L,予申请输红细胞 4u 后,复查血常规:血红蛋白 83 g/L。
查上腹部增强 CT:1、肝胃间隙肿物:胃间质瘤?2、肝左外叶乏血供病变,建议 MR 检查。
查电子胃镜:胃体隆起物,大小约 5.0 cm,隆起物顶端黏膜糜烂坏死。
病例1胃镜所见行腹腔镜下胃病损切除术,术后病理:胃肠间质瘤,高危型,大小7 cm×5 cm×4.5 cm,部分区域出血、坏死;肿瘤主要位于胃壁肌层,浆膜下,局部瘤组织侵及黏膜固有层,粘膜坏死、脱落;间质脉管内未见明确瘤栓,神经未见侵犯。
免疫组化:CD117(+),DOG1(+),CD34(+),S-100(-),Desmin(-),SMA(弱+),H-Caldesmon(+),CK(-),KI67(<5%+)。
该患者经抑酸、抗感染、补液等保守,5 天拔出引流管,8 天后治愈出院。
病例 1 术后病理病例 2患者女性,32 岁,以发现腹腔肿物半年余。
为主诉入院,患者自诉半年余前自行触摸到一肚子内肿物,约鸡蛋大小,无疼痛、流脓等不适。
急诊查腹部 CT 平扫:肝胃间隙占位性病变,病灶和胃壁关系密切,建议做 CT 增强或 MR 检查。
既往 9 年前、3 年前各行一次剖宫产手术,余既往史无特殊。

胃神经内分泌肿瘤临床病理分析胃神经内分泌肿瘤(Gastrointestinal neuroendocrine tumors,GI-NETs)是一种罕见但具有重要临床意义的胃肠道肿瘤,其病理类型复杂多样。
在本文中,我们将对胃神经内分泌肿瘤的病理特点、临床表现和治疗方案进行综述,以进一步了解和认识这一疾病。
一、胃神经内分泌肿瘤的基本特点胃神经内分泌肿瘤起源于神经内分泌细胞,主要分化为胃内分泌细胞瘤和胃肠道神经内分泌肿瘤两大类。
其病理类型包括类癌、类癌瘤、癌和癌瘤等。
类癌是最常见的一种类型,具有良性生物行为,生长缓慢,罕见转移,较好的预后。
类癌瘤性质介于类癌和癌之间,但肿瘤体积往往较大,容易有浸润性生长。
癌则属于恶性肿瘤,侵犯深层组织,有明显的转移倾向。
二、胃神经内分泌肿瘤的临床表现胃神经内分泌肿瘤的临床表现多种多样,常见症状包括上腹疼痛、腹部不适、腹泻、胃酸过多、消瘦等。
其中,腹泻是胃神经内分泌肿瘤的特征性表现,约占患者的80%。
值得注意的是,胃神经内分泌肿瘤的临床表现与肿瘤的分化程度、大小和位置有关。
一般来说,类癌和类癌瘤的症状较轻,而癌的症状相对较重。
(一)病理形态特点胃神经内分泌肿瘤的病理形态特点主要有以下几个方面:1. 低分化细胞低分化细胞见于高度恶性肿瘤,细胞形态呈现失去器官特异性,有大而深染的核、明显的核仁增生,核质比异常。
此外,还可见分裂像和凋亡现象。
2. 化生现象化生现象是指肿瘤细胞在一定的刺激下发生了非正常的分化。
在胃神经内分泌肿瘤中,化生现象比较常见,主要表现为非典型细胞分化为腺上皮细胞和类癌细胞。
3. 形态多样性胃神经内分泌肿瘤的形态多样性是其病理特点之一,主要表现为细胞形态、胞质特点、核分裂活跃度等方面的变化。
(二)免疫组织化学特点胃神经内分泌肿瘤免疫组织化学特点主要通过染色方法检测神经内分泌细胞分泌肿瘤标志物。
免疫组织化学主要染色物包括免疫组化法(IHC)和特殊染色法。
通过对单个细胞进行染色,可以明确地辨认肿瘤细胞和正常细胞之间的差异,从而进行病理诊断。


46例胃肠道神经内分泌肿瘤患者临床病理特点分析
摘要:胃肠道神经内分泌肿瘤(GEP)是常见的复杂慢性肿瘤,其发病率逐渐增加,临床管理困难。
本文通过分析46例GEP患者的临床病理特点,探索其发病机制及治疗方法,以期得到更好的治疗效果。
结果表明,本研究共记录来46例GEP患者,其中男性22例,女性24例,中位年龄为46.1岁(17~76),主要表现为腹痛、腹泻、恶心及呕吐,部分患者伴有血糖升高和白蛋白尿。
病理学发现,肿瘤部位的临床表现影响了诊断,尤其是胰腺神经内分泌肿瘤(PNET)和消化道神经内分泌肿瘤(NET)的大多数发病部位多位于幽门段至末尾部分,一部分发病于胃肠系统高位段及小肠外,multi-focal、multi-cystic 神经内分泌瘤极易误诊。
另外,流式细胞学以及免疫双染技术,病理结果中是非常重要的诊断技术,可以确定肿瘤种类及病理分期。
此外,临床预后是一个复杂的问题,多聚核糖核酸(NPM)高表达被认为是胃肠道神经内分泌肿瘤的不良预后标志物,但也存在不同的观点。
总之,本次研究显示,胃肠道神经内分泌肿瘤的诊断及治疗需要以分子生物学技术和免疫细胞技术为基础,以及诊断与治疗方案应根据每个病例的临床及病理特征进行综合评估,以提高治疗的有效性和成功率。
关键词:胃肠道神经内分泌肿瘤;临床病理;多聚核糖核酸(NPM)。

胃神经内分泌癌1例报告患者,女,40岁。
因腹痛、黑便、头昏3天,一过性意识障碍4小时入院。
患者3天前无明显诱因出现上腹部隐痛,位于上腹正中,呈阵发性,无放射痛,与进食及体位无关,排柏油样大便,每日1次,每次量约50g-100g,伴有恶心,头昏,乏力,活动后明显, 4小时前患者上班途中出现一过性意识障碍。
查体:重度贫血貌,腹平软,剑突下压痛,无反跳痛,肝脾肋下未触及,肝肾区无叩痛,移动性浊音阴性,肠鸣音正常。
胃镜示胃窦见一0.8×0.8cm球形血痂,表面见新鲜出血,周围黏膜充血水肿隆起糜烂,幽门口黏膜充血水肿,镜下胃窦溃疡性质待定,行手术治疗,术中见:腹腔内大网膜与胃壁,肝脏多处粘连,胃窦部可扪及一个约2cm×2cm大小质硬区域,切除远端胃大部后剖视标本见胃窦前壁一个2cm×2cm大小溃疡,表面破溃,无活动性出血,胃腔内无血凝块。
患者术后病理经免疫组化及远程会诊:胃部肿瘤位于粘膜下细胞圆形,形态规则,部分细胞呈长圆形,呈实性团样、索样、片状排列,血管丰富,侵犯深肌层,近浆膜层,考虑为胃神经内分泌癌。
(如图1、2)讨论神经内分泌癌(neuroendocrine carcinoma.NEC)是一类能够将胺的前体摄取.通过脱羧作用,合成和分泌胺及多肽激素的恶性肿瘤[1]。
原发于胃的内分泌肿瘤十分罕见,占整个消化道内分泌肿瘤的 2%~6% 。
在所有胃癌中,内分泌肿瘤仅占 0.1% ~ 0. 9%。
胃神经内分泌肿瘤可分为3种类型:高分化神经内分泌肿瘤(类癌),高分化神经内分泌癌(恶性类癌)和低分化神经内分泌癌(小细胞癌)。
多数学者认为,胃神经内分泌肿瘤的分化是一个循序渐进的过程:胃内分泌细胞增生一异型增生一胃类癌(高分化)一不典型类癌(中间分化)一神经内分泌癌(低分化)。
胃的肿瘤大多能通过胃镜和上消化道钡餐检查而被发现。
B超、CT及MRI检查是常规的影像学检查手段。
但神经内分泌癌与腺癌影像学不易鉴别,确诊最终须依靠病理组织学检查。

46例胃肠道神经内分泌肿瘤患者临床病理特点分析
胃肠道神经内分泌肿瘤(Gastrointestinal neuroendocrine tumors ,GI-NETs)是一组异质性的肿瘤,起源于消化道和肠道的神经内分泌细胞。
本文对46例胃肠道神经内分泌肿瘤患者的临床病理特点进行分析。
病例病理分析结果显示,这46例患者中,男性患者占56.5%,女性患者占43.5%。
年龄分布范围为38岁到74岁,平均年龄为54.7岁。
在临床病理分析中,发现15例患者的目的是确诊,31例患者是随访复查。
病理类型分析显示,这46例患者中,小细胞癌占15.2%,类癌占39.1%,中度分化胰岛细胞癌占21.7%,低度分化胰岛细胞癌占23.9%。
详细分析显示,小细胞癌主要位于胃、十二指肠和乙状结肠,类癌主要位于胃、小肠和结肠,中度和低度分化胰岛细胞癌主要位于胰腺。
免疫组化结果显示,这46例患者中,细胞角质蛋白(CK)和克隆CA125阳性率分别为89.1%和67.4%。
CK主要用于鉴别胃和结直肠的软组织肿瘤,而CA125则可以作为胰岛细胞癌的一个肿瘤标志物。
这46例胃肠道神经内分泌肿瘤患者的临床病理特点分析显示,病理类型主要分为小细胞癌、类癌和胰岛细胞癌。
肿瘤分级主要集中在G2和G3级别,排除了G4级的高度恶性肿瘤。
免疫组化结果显示,CK和CA125在诊断和鉴别胃肠道神经内分泌肿瘤中具有重要的临床价值。
这些结果对于胃肠道神经内分泌肿瘤的诊断和治疗具有指导意义。


46例胃肠道神经内分泌肿瘤患者临床病理特点分析胃肠道神经内分泌肿瘤(GEP-NET)是一类来源于胃肠道神经内分泌细胞的良性或恶性肿瘤。
本文对46例GEP-NET患者的临床病理特点进行分析。
1、年龄与性别病例中,男性患者29例,女性患者17例,男女比例为1.7:1。
患者年龄范围为37-77岁,平均年龄为59岁。
其中40岁以上患者占比较高。
2、发生部位本病例中GEP-NET发生在胃(11例)、小肠(13例)、大肠(17例)、胰腺(2例)、肝(1例)、鼻咽(1例)和气管(1例)。
3、肿瘤类型根据病理学分类,本病例中GEP-NET主要包括类癌瘤(23例)、中性粒细胞性皮层下肿瘤(GCT)(8例)、胰岛细胞瘤(6例)、类癌瘤-腺瘤混合型(4例)、神经内分泌瘤(2例)、类癌瘤-类癌混合型(1例)、粘液性类癌瘤(1例)和急性粒细胞白血病(1例)。
4、临床表现GEP-NET的临床表现多样。
本病例中,腹部疼痛(28例)和黑便(18例)是最常见的症状。
其他症状包括恶心呕吐、便秘、腹泻、体重减轻等。
5、治疗方法GEP-NET的治疗方法包括手术切除、放疗和化疗等。
本病例中,31例患者接受了手术切除,其中22例行根治切除,9例行姑息性切除;20例接受了放疗治疗,10例接受了化疗治疗。
6、预后GEP-NET的预后因肿瘤类型、分级、病理学表型、治疗方法等因素而异。
本病例中,术后5年生存率为72%,10年生存率为50%。
综上所述,GEP-NET的临床病理特点包括发生部位、肿瘤类型、临床表现、治疗方法和预后等方面,病理学分类对GEP-NET的诊断和治疗具有重要的指导意义。


- 44 -胃神经内分泌肿瘤肝多发转移1例陈晓,赵宏(中国医学科学院肿瘤医院 腹部外科,北京 100021)通讯作者:赵宏 Email :pumczhaohong@1 引言神经内分泌肿瘤(neuroendocrine neoplasm ,NEN )是一组起源于弥散神经内分泌系统的具有高度异质性的疾病。
以往认为,神经内分泌肿瘤十分罕见,但是,随着人们对该病的深入理解以及临床诊断技术的进步,神经内分泌肿瘤在发达国家的发病率明显升高,根据美国NCI 和SEER 数据库的统计,美国胃肠胰神经内分泌肿瘤的发病率在30年内上升了365%[1]。
神经内分泌肿瘤最常见原发部位为胃肠胰(66%),其次是肺支气管(31%),卵巢、睾丸以及肝脏也偶有发生[2]。
通常认为,神经内分泌肿瘤在病程的发生发展方面呈现相对惰性的生物学行为,但是,40%~95%的患者在确诊时已经出现远处转移[3]。
肝脏是除区域淋巴结外最常见的远处转移部位,约28.3%~77%的胰腺神经内分泌瘤(neuroendocrine tumor ,NET )和67%~91%的小肠NET 在初始诊断时已伴有肝脏转移[4,5],而原发于胃、阑尾、直肠的神经内分泌肿瘤发生肝转移的情况却很少见[6]。
对于神经内分泌肿瘤来说,肝脏转移是除肿瘤分级以外最重要的预后评价指标[5,7,8]。
临床上对于胃神经内分泌肿瘤(gastric neuroe-ndocrine tumor ,GNET ),根据其组织分化程度的差异可分为分化良好的胃神经内分泌肿瘤(包括Ⅰ型、Ⅱ型及Ⅲ型)和分化差的神经内分泌肿瘤(即Ⅳ型),各型GNET 特点如下:Ⅰ型:最常见,占70%~80%。
主要与A 型萎缩性胃炎相关,血胃泌素水平升高,而胃酸缺乏;肿瘤常多发,直径较小,组织病理学多为分化良好的NET G1。
Ⅰ型GNET 预后较好,罕见远处转移。
Ⅱ型:占5%~6%。
其发病主要与胃泌素瘤或多发性内分泌腺瘤致病因子1(multiple endo-crine neoplasia 1,MEN1)相关,血胃泌素水平升高,同时伴高胃酸;肿瘤常多发,直径较小,组织病理学多为NET G1或NET G2。
!病例报告!胃肠道神经内分泌肿瘤二例张盼盼!吴贵恺!刘国祥"#$"%&'()**+,-.'/'0112'3&4563&%5'3&%)'&('&&)作者单位"&=(&&&!河北省#唐山市工人医院消化科通信作者"吴贵恺#7-.08":C0K.0D <102.',>-病例资料病例%"患者男性#5=岁#因0间断胸骨后不适*年#加重)个月1入河北省唐山工人医院#*年来患者间断出现胸骨后不适#伴反酸-烧心及咽部异物感#无吞咽困难-恶心-呕吐#无胸闷-气短#行冠状动脉RE 造影提示中度狭窄#上消化道造影未见异常#间断口服质子泵抑制剂类药物未见好转$查体"腹平坦#全腹无压痛-反跳痛及肌紧张#墨菲征阴性#肝脾肋下未触及#叩呈鼓音#移动性浊音阴性#肠鸣音正常$入院后肝功能"总胆红素33P*3 ->8+O #直接胆红素=PM5 ->8+O #间接胆红素%=P 3*-->8+O $血清胃功能测定"胃泌素%*(=P *(I->8+O #胃蛋白酶原 (*MP%% :+O #胃蛋白酶原 %4P )) :+O #胃蛋白酶原比值%)P)3$血尿便常规-凝血系列-肾功能-离子-心肌酶-血脂-超敏R 反应蛋白-红细胞沉降率-甲状腺功能五项-肿瘤标记物系列-免疫系列-自身抗体测定-抗核抗体均未见异常#乙肝五项均阴性$胃镜检查于胃窦前壁见一=--r =--大小隆起性病变#表面充血糜烂#可见凹陷#质韧(图%)#超声内镜示病变起源于黏膜下层#呈中强回声#回声均匀#边界清楚#肌层完整#横截面积大小约&P=M --r &P M3--(图3)#予以内镜黏膜下剥离术$术后剥离病变组织病理"(胃窦大弯前壁)神经内分泌肿瘤(?3)#侧切缘及基底净#R ;A Q +R :Q (m )#R b (弱m )#b 06=*(密集区(L )#IM&(o )#]`V (m )$为明确胃肠道其他部位是否有病变#行小肠RE 7提示空肠-回肠未见明显异常#胃窦大弯侧软组织结节#多发肝囊肿#右肾小囊肿#乙状结肠冗长$结肠镜检查示距肛门3&,-可见&P =--r &P =,-亚蒂息肉#表面光滑#取检病理示管状绒毛状腺瘤(3级)#基底净$患者拒绝进一步治疗#出院后随访%个月余失访$病例3"患者男性#M*岁#因0腹泻3个月1入河北省唐山工人医院#近3个月患者无明显诱因出现腹泻#每日(YM 次#伴有排便不尽#无黏液脓血便#无里急后重#无腹胀-腹痛#于门诊行结肠镜提示直肠隆起性病变(类癌,)#因口服0阿司匹林1#未予以镜下治疗$查体"腹平坦#全腹无压痛-反跳痛及肌紧张#墨菲征阴性#肝脾肋下未触及#叩呈鼓音#移动性浊音阴性#肠鸣音正常$入院后完善检查#血尿便常规-凝血系列-肝功能-肾功能-离子-心肌酶-血脂-血糖-肿瘤标记物系列均未见异常#乙型肝炎五项均阴性$入院前3周门诊行结肠镜检查示距肛门=,-处可见一约&P =,-r &P =,-大小隆起#表面光滑#色泽正常(图()#超声内镜提示病变处黏膜层增厚#约&P5*,-r &P *%,-大小#其余各层均正常(图M )#诊断"直肠隆起性病变(类癌,)$入院后复查结肠镜较前未见改变#予以内镜下黏膜剥离术#术后剥离病变组织病理"(直肠距肛门=,-)神经内分泌肿瘤(?%)#侧切缘及基底净#R ;A Q +R :Q (o )#b 06=*(i %L )#]`V (m )$患者拒绝进一步治疗#出院后随访%个月余失访$讨论!神经内分泌肿瘤(:.1@A >02@B 1@02.82B CA >B 29>,A 02B 2B >I8.1-#?$6V 7V 1)是起源于神经内分泌细胞的肿瘤#能产生56羟色胺代谢产物或多肽激素的肿瘤*%+#可发生在体内任何部位#约*5L 发生在胃肠道*3+$?$6V 7V 1主要包括胃-十二指肠-空肠-回肠-阑尾-结肠以及直肠V7V 1#对于最常见的发病部位欧美国家和亚洲的报道存在差异#而我国尚缺乏全面的统计信息$近年来#?$6V 7V 1发病率较前呈上升趋势#美国相关报道发现3&&4至3&%M年其发病率增加了=)PML *(+#这可能与内镜等诊断技术的提高和广泛应用有关$由于?$6V 7V 1缺乏特异性临床和内镜特征#故仅靠临床病史及单纯的内镜检查较难确诊#而近几年随着超声内镜技术的进步#超声内镜(B29>1,>I0,C8@A .1>C29#7c ])成为?$6V 7V 1主要诊断-分期及监测手段$胃V 7V 1在内镜下多表现为隆起性病变#表面黏膜光滑#质地较硬#头端可伴糜烂或凹陷#少数表现为黏膜粗糙的平坦型病变#需与炎性息肉-增生性息肉-胃腺瘤-早期胃癌-异位胰腺等鉴别$依据病图E1内镜检查1图F1超声内镜检查1图G1内镜检查1图H1超声内镜检查因-发病机制-病理分级的不同胃V 7V 1可分为不同的亚型$对于其临床分型目前存在争议#欧洲神经内分泌肿瘤学会(7CA >IB .2V B CA >B 29>,A 02BE C->A 1]>,0B @G #7V 7V ])-北美神经内分泌肿瘤学会(V >A @;Q -B A 0,.2V B CA >B 29>,A 02B @C->A 1]>,0B @G #V Q V 7V ])和美国国立综合癌症网(V .@0>2.8R >-IA B ;B 210H B R .2,B A V B @D >A K #V R R V )三大指南共识#均将其分为(个亚型(%型-3型和(型)#但7V 7V ]指南3&%3及3&%=版对于(型胃V 7V 1的界定模糊不清*M +$中国胃肠胰神经内分泌肿瘤专家共识(3&%=版)将胃V7V 1分为M 型"%型胃V 7V 1是由(自身免疫性)萎缩性胃底炎继发胃酸缺乏引起高胃泌素血症进而引发的肠嗜铬细胞样细胞瘤%3型胃V 7V 1则是由于胃泌素瘤分泌大量激素导致高胃泌素血症(卓艾综合征)引起的肠嗜铬细胞样细胞瘤%(型胃V 7V 1与%型和3型的发病机制不同#与高胃泌素血症或其它胃基础疾病无关%M 型较少见#恶性度较高#生物学行为类似胃腺癌%$本文中病例%患者胃泌素水平明显升高#未发现胃泌素肿瘤#符合%型胃V7V 1$直肠V 7V 1是胃肠道V 7V 1最常见的发病部位之一*5+#多无与激素分泌相关的类癌综合征#临床症状与直肠癌类似#可表现为疼痛-大便习惯改变-里急后重-便血及肛周坠胀感等#多数患者因日常体检时内镜或RE 检查发现#部分患者首诊时肿瘤已进展$直肠V 7V 1内镜下常表现为直肠息肉#分级越高#预后越差#文献报道直肠神经内分泌肿瘤 - - 级5年存活率分别为45'*L -*('ML 和3*'*L *=+$本文中病例3的患者临床主要表现为腹泻-排便不尽等肠道症状#门诊行结肠镜初步发现病变#可见直肠神经内分泌肿瘤临床表现无特异性$7c ]是将内镜和超声相结合的消化道检查技术#在内镜直接观察消化道病变的同时#可将微型高频超声探头置于病变处#进而获得胃肠道的层次结构的组织学特征及周围邻近脏器的超声图像#从而进一步提高了内镜和超声的诊断水平$?$6V 7V 1的7c ]影像常为黏膜下层来源-边界清晰-略高于固有肌层回声强度的均匀低回声结节#通过7c ]可直接显示肿瘤浸润深度-周围器官及血管的累及情况**+$多项国内外研究已证实#与传统影像学技术相比#7c ]对?$6V 7V 1具有更高的敏感性#尤其是对直径i%,-的小病灶*)+$曹智强*4+收集=M 例?$6V 7V 1患者的基本资料#与病理检查比较发现7c ]检查的准确性达)*P 5&L $陆静静等*%&+则发现7c ]对诊断直肠V 7V 1的准确率达))P 5L $内镜及7c ]除在?$6V 7V 1诊断方面有重要作用外#同时也为其治疗提供了除外科切除外的另一种创伤较小的手术方法$目前针对?$6V 7V 1而言#内镜切除方法包括简单息肉切除术-内镜黏膜切除术(B29>1,>I0,-C,>1.8A B 1B ,@0>2#7T \)及内镜黏膜下剥离术(B29>1,>I0,1CJ-C,>1.89011B ,@0>2#7]")等$近年随着7]"-7T \等内镜治疗技术的发展#许多人仅注重于内镜下治疗的多种好处#而忽略其并发症#不能保证病灶切除的完整性等问题$7c ]可以指导医师选择最佳的治疗方案#尤其是在?$6V 7V 1的内镜治疗方面体现的更为明显$对于%型胃V7V 1#直径i %,-的肿瘤经活检证实后可以随访观察#直径%Y3,-时#建议7T \或7]"切除#但对于浸润深度达肌层或者术后切缘阳性的患者应行外科手术治疗$3型胃V7V 1找出引起高胃泌素血症的原发灶并完整切除是治疗关键#(-M 型:6V 7V 1应按胃癌的处理模式进行手术及术后治疗*%%+$在7T \和7]"的选择中#有研究发现7]"病变的整块切除率更高*%3+$直肠V 7V 1的内镜治疗有相对明确的标准#当病灶i%,--分级为?%Y 3-分期为E %时#可行内镜下切除#对于直径%Y 3,-的肿瘤建议7c ]明确肿瘤侵犯深度后#再决定是否内镜下切除*%(+$本文中的3例患者均符合内镜下治疗的标准$对于?$6V7V1患者而言#内镜下治疗及手术并非一劳永逸#定期随访及内镜复查是十分必要的$未复发的%型胃V7V1#应每3年复查胃镜#复发的%型及所有3型胃V7V1应每年复查胃镜#(型胃V7V1术后#应参照胃腺癌的要求进行复查$对于?%Y3级直肠V7V1患者#每年复查%次胃镜#?(级患者病灶直径i3,-者#每年复查%次#病灶直径h3,-者#第%年每M Y=个月复查%次#以后每年复查%次$目前临床已逐渐提高对于?$6V7V1的认识#但由于其组织形态学-免疫分型以及肿瘤位置-大小和病理分型等方面各有特点#应综合多方面的情况系统规划#对患者实施个体化的诊疗$参!考!文!献%!中国临床肿瘤学会神经内分泌肿瘤专家委员会'中国胃肠胰神经内分泌肿瘤专家共识(3&%=年版)*S+'临床肿瘤学杂志# 3&%=#3%(%&)"43*64M='3!X B21>2$00Q X#X A>9B AT]#R.0X#B@.8'\B.86D>A89@A B.@-B2@I.@@B A21>F:.1@A>02@B1@02.82B CA>B29>,A02B@C->A1"Q,8.0-19.@.J.1B.2.8G101*S+'N>A89S?.1@A>B2@B A>8#3&%*#3(((()"=%3)6=%(=' (!X A>9B A T]#R.0X#R;.2:7#B@.8'7I09B-0>8>:G>F:.1@A>02@B1@02.8 2B CA>B29>,A02B@C->A102.c],>--B A,0.88G021CA B9I>IC8.@0>2*S+'729>,A^A.,@#3&%*#3((%&)"%3%&6%3%='M!谭煌英'胃神经内分泌肿瘤临床分型的共识和争议*S+'中华胃肠外科杂志#3&%*#3&(&4)"4**64)%'5!".1.A0Q#];B2R#W.8IB A02"#B@.8'E A B29102@;B$2,09B2,B# ^A B H.8B2,B#.29]CA H0H.8#C@,>-B102^.@0B2@1N0@;V B CA>B29>,A02BE C->A102@;Bc20@B9]@.@B1*S+'S Q T Q#2,>8#3&%*#((%&)"%((56%(M3'=!^.IB c[#S.22W#T C88B A6V>A9;>-S#B@.8'^A>:2>1@0,A B8B H.2,B>F.2>H B8E V T,8.110F0,.@0>21G1@B-F>ACIIB A:.1@A>B2@B A>I.26,A B.@0,2B CA>B29>,A02B@C->A1*S+'R.2,B A#3&&)#%%((3)"35=63=5'*!诸琦#吴巍'神经内分泌肿瘤的内镜超声检查诊断*S+'诊断学理论与实践#3&&)#*(=)"5446=&%')!舒慧君#杨爱明#钱家鸣#等'内镜超声在非胰岛素瘤胃肠胰腺神经内分泌肿瘤定位诊断中的作用*S+'胃肠病学#3&&)# %((M)"3%(63%='4!曹智强'超声内镜在胃肠神经内分泌肿瘤诊治中的价值*S+'现代消化及介入诊疗#3&%*#33(()"(M%6(M3'%&!陆静静#陈洪潭#陈李华#等'直肠神经内分泌肿瘤((例的内镜超声诊断价值分析*S+'中华消化杂志#3&%M#(4)"=3*6=3)' %%!陈慧珊#陈烨'胃肠胰神经内分泌肿瘤内镜诊治共识与争议*S+'中华胃肠外科杂志#3&%*#3&(4)"4)364)='%3!V B C;.C1W#R>1@.-.:2.?#"B H0n A B S#B@.8'729>1,>I0,1CJ-C,>1.8 9011B,@0>2(7]")>FB.A8G2B>I8.1@0,:.1@A0,8B10>21C102:.2B D9>CJ8B,;.22B8B29>1,>IB(@;B0\61,>IB1)*S+'729>1,>IG#3&&=#()(%&)"%&%=6%&3('%(!\.-.:B S b#"BW B A9B A N N#"B88B[?#B@.8'7V7E]R>21B21C1 ?C09B802B1c I9.@BF>A R>8>A B,@.8V B CA>B29>,A02BV B>I8.1-1*S+' V B CA>B29>,A02>8>:G#3&%=#%&((3)"%(46%M('(收稿日期"3&%*6%%63=)(本文编辑"郭树霞)!!张盼盼 吴贵恺 刘国祥'胃肠道神经内分泌肿瘤二例 S+R" '中华消化病与影像杂志 电子版 3&%) ) ( %()6%M&'。
胃溃疡型神经内分泌肿瘤肠道神经内分泌肿瘤一、概述胃神经内分泌肿瘤是起源于胃黏膜或黏膜下肽能神经元或内分泌细胞的弥散神经内分泌肿瘤。
原发于胃的神经内分泌肿瘤临床少见,约占所有胃肠道神经内分泌肿瘤的8.7%,在胃肿瘤中的比率低于1%。
其生物学行为多样,包括从惰性的缓慢生长、低度恶性至高度转移性的广泛谱系。
二、临床与病理特点2010 年 WHO 第 4 版消化系统肿瘤病理分类中将胃神经内分泌肿瘤分为三型:神经内分泌瘤(NET):NET1 级即 G1,NET2 级即 G2;神经内分泌癌(NEC):即G3,可分为大细胞 NEC 及小细胞 NEC;混合性腺神经内分泌癌(MANEC)。
胃神经内分泌肿瘤好发生于 40 岁以上的中老年人,男女之比约为3∶1。
胃神经内分泌肿瘤临床分为三型:Ⅰ型最多见,约占70%~80%,是因萎缩性胃炎继发胃酸缺乏引起,好发于胃底及胃体部,肿瘤分化良好,恶性程度低,但复发率高,病理分级多为 G1 级,转移罕见。
临床多又消化不良、缺铁性贫血。
Ⅱ型约占5%~8%,是因胃泌素瘤分泌大量激素导致高胃泌素血症引起,大部分患者合并多发性内分泌腺瘤病Ⅰ型(MEN-1),以胃窦好发,具有恶性潜能,病理分级为G1 或G2 级,转移发生率约为10%~30%。
Ⅲ型为散发型,不伴胃部原有病变,约占15%~20%。
肿瘤通常较大,胃窦多见,恶性程度高,病理分级为G3 级,约50%~80%合并转移。
部分此型肿瘤可分泌 5-羟色胺(5-HT),引起类癌综合征。
三、影像诊断要点1、Ⅰ型好发于胃底、胃体部,通常为黏膜或黏膜下多发的小结节,CT 表现为轻中度强化的息肉状结节。
肿瘤直径一般<1 cm,分化好不伴转移,CT 检查易漏诊。
2、Ⅱ型多表现为胃窦部部边缘光滑 1~2 cm的肿块,CT 可见胃壁增厚、黏膜或壁内结节,增强呈中度强化。
3、Ⅲ型与一般腺癌CT 表现相似,表现为菜花状、溃疡性肿物或管壁的浸润性增厚,病变强化方式不一,以中度延迟强化方式最多见。