化学常见常见沉淀及溶解性口诀
- 格式:doc
- 大小:858.00 KB
- 文档页数:9

常见沉淀白色:BaSO4/BaCO3/CaCO3/AgCl/Ag2CO3/Mg(OH)2/Fe(OH)2/Al(OH)3/CuCO3/ZnCO3/MnCO3/Zn(OH)2 Fe(OH)2蓝色:Cu(OH)2浅黄色:AgBr红褐色:Fe(OH)3沉淀鉴别Cu(OH)2蓝色沉淀Fe(OH)3红褐色沉淀AgBr淡黄色沉淀AgI ,Ag3PO4黄色沉淀CuO 黑色沉淀Cu2O 红色沉淀Fe2O3 红棕色沉淀FeO 黑色沉淀FeS2 黄色沉淀PbS 黑色沉淀FeCO3 灰色沉淀Ag2CO3 黄色沉淀AgBr 浅黄色沉淀AgCl 白色沉淀Cu2(OH)2CO3 暗绿色沉淀BaCO3白色沉淀(且有CO2生成)CaCO3白色沉淀(且有CO2生成)BaSO4白色沉淀不溶的碳酸盐白色沉淀(且有CO2生成)不溶的碱、金属氧化物白色沉淀(且有CO2生成)Fe(OH)2为白色絮状沉淀(在空气中很快变成灰绿色,再变成Fe(OH)3红褐色沉淀)相关口诀钾钠铵盐硝酸盐均可溶盐酸盐银不溶硫酸盐钡不溶白色沉淀: CaCO3. BaCO3 . BaSO4. AgCL. Mg(OH)2蓝色沉淀: Cu(OH)2红褐色沉淀: Fe(OH)3不建议死记硬背,只需记住每个阴离子里哪个不溶即可,钾钠铵硝都溶溶解性口诀一钾钠铵盐溶水快,①硫酸盐除去钡银铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③氢氧根多溶一个钡④口诀中未有皆下沉。
⑤注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀);③硝酸盐都溶于水;④碱性物质中除了钾离子钠离子铵离子锂离子还有钡离子也可溶⑤口诀中没有涉及的盐类都不溶于水;溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
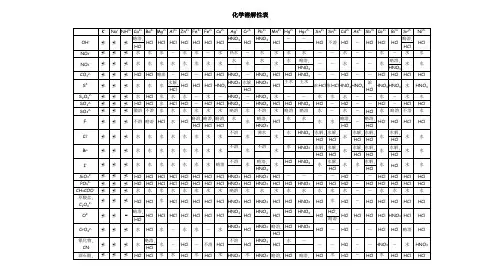
化学溶解性表盐类溶解性表的规律可编成如下口诀记忆:钾、钠铵盐都可溶,硝盐遇水影无踪;硫(酸)盐不溶铅和钡,氯(化)物不溶银、亚汞。
氢气还原氧化铜实验,操作顺序可编成如下口诀记忆:氢气应早去晚归,酒精灯迟到早退,试管口下倾水滴。
氧化一还原反应的定义、性质、特征可编成如下口诀记忆:升失氧,降得还;若说剂,两相反。
盐类水解规律可编成如下口诀记忆:无“弱”不水解,谁“弱”谁水解;愈“弱”愈水解,又“弱”剧水解;谁“强”显谁性,双“弱”由K定。
盐类水解离子方程式的书写可编成如下口诀:左边水写分子式,中间符号写可逆,右边不写“↑”和“↓”。
溶解性口诀一钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
④注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅、硫酸钙不溶;③硝酸盐都溶于水;④口诀中没有涉及的盐类都不溶于水;溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五钾钠铵盐硝酸盐完全溶解不困难氯化亚汞氯化银硫酸钡和硫酸铅生成沉淀记心间氢硫酸盐和碱类碳酸磷酸硝酸盐可溶只有钾钠铵钾钠铵盐溶水快,①硫酸盐除去钡铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③口诀中未有皆下沉。
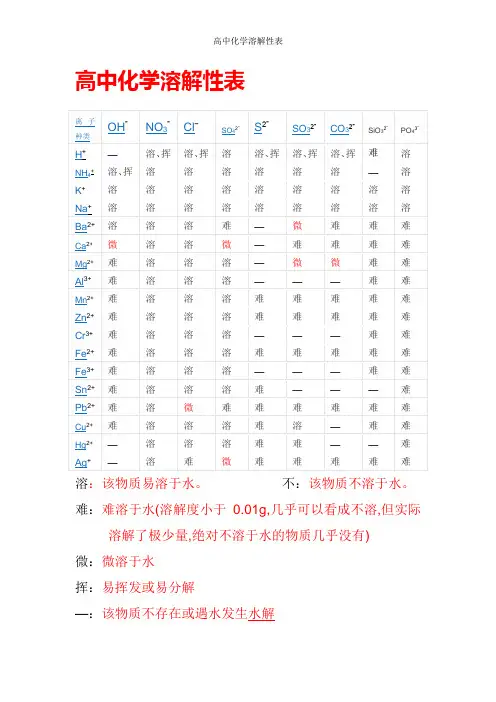
高中化学溶解性表
溶:该物质易溶于水。
不:该物质不溶于水。
难:难溶于水(溶解度小于0.01g,几乎可以看成不溶,但实际溶解了极少量,绝对不溶于水的物质几乎没有)
微:微溶于水
挥:易挥发或易分解
—:该物质不存在或遇水发生水解
红褐色:Fe(OH)3
沉淀鉴别
沉淀;Cu2O 红色沉淀;Fe2O3红棕色沉淀;FeO 黑色沉淀FeS2黄色沉淀;PbS 黑色沉淀;FeCO3灰色沉淀;
Ag2CO3白色沉淀(制作过程中Ag2CO3易分解成褐色Ag2O,混合物常常为黄色);Cu2(OH)2CO3暗绿色沉淀;BaCO3白色沉淀(且有CO2生成);CaCO3白色沉淀(且有CO2生成);
BaSO4白色沉淀;不溶的碳酸盐白色沉淀(且有CO2生成);
不溶的碱、金属氧化物白色沉淀(且有CO2生成);Fe(OH)2为白色絮状沉淀(在空气中很快变成灰绿色,再变成Fe(OH)3红褐色沉淀)
溶解性口诀:
钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)
盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)
硫酸盐除钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)
其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物);只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)
碱类中,钾、钠、铵、钡溶。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)
另有几种微溶物,可单独记住(见上表)。
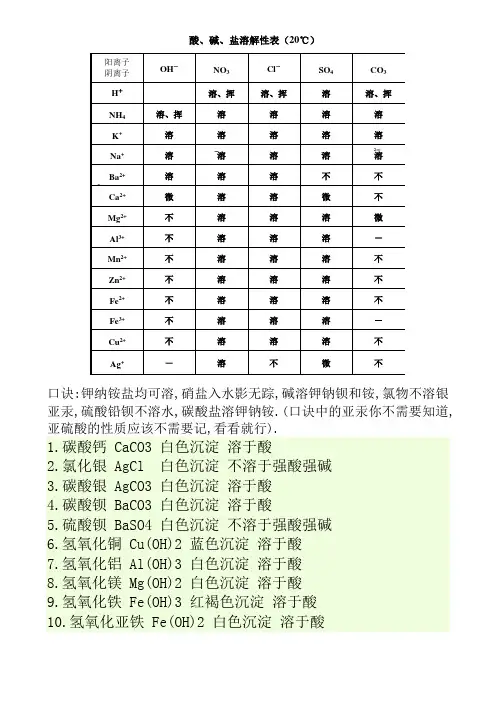
口诀:钾纳铵盐均可溶,硝盐入水影无踪,碱溶钾钠钡和铵,氯物不溶银亚汞,硫酸铅钡不溶水,碳酸盐溶钾钠铵.(口诀中的亚汞你不需要知道,亚硫酸的性质应该不需要记,看看就行).
1.碳酸钙 CaCO3 白色沉淀 溶于酸
2.氯化银 AgCl 白色沉淀 不溶于强酸强碱
3.碳酸银 AgCO3 白色沉淀 溶于酸
4.碳酸钡 BaCO3 白色沉淀 溶于酸
5.硫酸钡 BaSO4 白色沉淀 不溶于强酸强碱
6.氢氧化铜 Cu(OH)2 蓝色沉淀 溶于酸
7.氢氧化铝 Al(OH)3 白色沉淀 溶于酸
8.氢氧化镁 Mg(OH)2 白色沉淀 溶于酸
9.氢氧化铁 Fe(OH)3 红褐色沉淀 溶于酸 10.氢氧化亚铁 Fe(OH)2 白色沉淀 溶于酸
阳离子 阴离子
OH - NO 3 Cl - SO 4 CO 3 H + 溶、挥 溶、挥 溶 溶、挥 NH 4 溶、挥 溶 溶 溶 溶 K + 溶 溶
溶 溶
溶
Na +
溶 溶 溶 溶 溶 Ba 2+ 溶 溶 溶 不 不 Ca 2+ 微 溶 溶 微 不 Mg 2+ 不 溶 溶 溶 微 Al 3+ 不 溶 溶 溶 - Mn 2+ 不 溶 溶 溶 不 Zn 2+ 不 溶 溶 溶 不 Fe 2+ 不 溶 溶 溶 不 Fe 3+ 不 溶 溶 溶 - Cu 2+ 不 溶 溶 溶 不 Ag +
-
溶
不
微
不
+
酸、碱、盐溶解性表(20℃)
-
2-
2-。

化学常见常见沉淀及溶解性口诀work Information Technology Company.2020YEAR沉淀鉴别Cu(OH)2蓝色沉淀Fe(OH)3红褐色沉淀AgBr淡黄色沉淀AgI ,Ag3PO4黄色沉淀CuO 黑色沉淀Cu2O 红色沉淀Fe2O3红棕色沉淀FeO 黑色沉淀FeS2黄色沉淀PbS 黑色沉淀FeCO3 灰色沉淀Ag2CO3黄色沉淀AgBr 浅黄色沉淀AgCl 白色沉淀Cu2(OH)2CO3暗绿色沉淀BaCO3白色沉淀(且有CO2生成)CaCO3白色沉淀(且有CO2生成)BaSO4白色沉淀不溶的碳酸盐白色沉淀(且有CO2生成)不溶的碱、金属氧化物白色沉淀(且有CO2生成)Fe(OH)2为白色絮状沉淀(在空气中很快变成灰绿色,再变成Fe(OH)3红褐色沉淀)相关口诀钾钠铵盐溶水快,①硫酸盐除去钡银铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③氢氧根多溶一个钡④口诀中未有皆下沉。
⑤注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀);③硝酸盐都溶于水;④碱性物质中除了钾离子钠离子铵离子锂离子还有钡离子也可溶⑤口诀中没有涉及的盐类都不溶于水;几种重要阳离子的检验(l)H+能使紫色石蕊试液或橙色的甲基橙试液变为红色。
(2)Na+、K+用焰色反应来检验时,它们的火焰分别呈黄色、浅紫色(通过钴玻片)。
(3)Ba2+能使稀硫酸或可溶性硫酸盐溶液产生白色BaSO4沉淀,且沉淀不溶于稀硝酸。
(4)Mg2+能与NaOH溶液反应生成白色Mg(OH)2沉淀,该沉淀能溶于NH4Cl溶液。
(5)Al3+能与适量的NaOH溶液反应生成白色Al(OH)3絮状沉淀,该沉淀能溶于盐酸或过量的NaOH溶液。
(6)Ag+ 能与稀盐酸或可溶性盐酸盐反应,生成白色AgCl沉淀,不溶于稀HNO3。
(7)NH4+铵盐(或浓溶液)与NaOH浓溶液反应,并加热,放出使湿润的红色石蕊试纸变蓝的有刺激性气味NH3气体。

化学常见常见沉淀及溶解性口诀化学中,溶液中的溶质和溶剂能够发生反应,产生一些沉淀物。
这些沉淀物中有些是可以溶解的,有些则不可溶解。
下面是一些常见的沉淀及其溶解性,可以用以下的口诀来记忆:硫酸盐化学挂,钨酸盐和硼酸;养金银铜,发氨铵;石头能溶解,氢氧化铝挂着;碳酸盐碳酸,氢氧化铵不能碰。
这首口诀可以依次解释如下:硫酸盐化学挂:硫酸盐很容易与其他离子结合成不溶性盐类,因此称为“化学挂”。
例如,氯化铵和硫酸铵反应时,会生成硫酸铵和氯化钾。
硫酸铵是可溶于水的,而氯化钾是不溶于水的沉淀。
钨酸盐和硼酸:钨酸盐和硼酸都是不溶于水的沉淀。
例如,钠钨酸和钠硼酸在溶液中反应时,会生成钨酸钠和硼酸钠。
这两种化合物在水中都是不溶的,因此会形成沉淀。
养金银铜,发氨铵:金、银、铜是一些贵重金属,它们的氨合物都是可溶的。
例如,硝酸铜和氨水反应后可以得到深蓝色的四氨合铜离子,是可溶于水的盐类。
而氨合金离子在空气中会发生氧化,生成一些混浊的沉淀。
石头能溶解,氢氧化铝挂着:一些石头中含有的金属离子,在强碱性条件下会形成相应的氢氧化物,例如羟基石英和羟基铝石榴石等。
其中,氢氧化铝是不溶于水的,会形成白色的沉淀。
碳酸盐碳酸,氢氧化铵不能碰:碳酸盐是一类含有碳酸根离子的化合物,它们和酸或金属离子结合时会形成沉淀。
例如,碳酸钙和盐酸反应会生成氯化钙和二氧化碳气体。
此外,一些金属离子和碳酸根离子结合也会形成不溶的沉淀。
而氢氧化铵在高温下才能分解,因此在常温条件下不能与碳酸盐结合,否则会形成不可溶的白色沉淀。
总的来说,上述口诀可以帮助我们记忆一些常见的沉淀及其溶解性,但在实验中最好还是要进行实验室测试,以确定每种沉淀的具体性质和溶解度。

初中化学溶解度表及口诀
初中化学溶解度表及口诀如下:
口诀:
钾钠铵盐硝酸盐,完全溶解不困难,氯化亚汞氯化银,硫酸钡和硫酸铅,生成沉淀记心间,氢硫酸盐和碱类,碳酸磷酸硝酸盐,可溶只有钾钠铵。
钾钠铵硝皆可溶,盐酸不溶银亚汞;硫酸不溶钡和铅,碳磷酸盐多不溶;多数酸溶碱少溶,只有钾钠铵钡钙。
钾钠铵盐硝酸盐,溶入水中都不见;硫酸盐类不溶钡,氯化物中不溶银;碳酸盐类多不溶,只有钾钠铵盐溶。
溶解度表:
钾盐、钠盐、铵盐、硝酸盐都溶于水。
硫酸盐除了硫酸钡、硫酸铅不溶,硫酸钙、硫酸银微溶外,其他都溶。
盐酸盐除了氯化银不溶外,其他都溶。
碳酸盐除了碳酸钾、碳酸钠、碳酸铵溶外,其他都不溶。
需要注意的是,口诀和表格只是帮助记忆的工具,具体物质的溶解度还需要参考实验数据和资料。
此外,溶解度不仅受物质本身性质的影响,还与温度、压强等条件有关。
因此,在理解和应用溶解度概念时,需要综合考虑各种因素。

酸碱盐溶解性表钾钠铵盐硝酸银,永远溶解不沉淀!碳酸盐不溶钡、钙、银!硫酸钡氯化银!四大强碱记心间!(特别说明:上述沉淀全部为白色沉淀!)重要化学知识三大强酸:盐酸;HCL硫酸:H2SO4硝酸:HNO3四大强碱:氢氧化钾:KOH氢氧化钠:NaOH氢氧化钙:Ca(OH)2氢氧化钡:Ba(OH)2常见微溶物:(微溶物指该物质溶解度很低,不能大量存在,当生成的量过多时会有白色沉淀析出)硫酸钙CaSO4、硫酸银Ag2SO4碳酸镁MgCO3氢氧化钙Ca(OH)2中学重要的带有颜色的沉淀:氢氧化亚铁(白色沉淀)Fe(OH)2氢氧化铁(红褐色沉淀)Fe(OH)3氢氧化铜(蓝色沉淀)Cu(OH)2溴化银(浅黄色沉淀)AgBr碘化银(黄色沉淀)AgI常见的有色离子是Cu2+(蓝色)、Fe2+(浅绿色)、Fe3+(黄棕色)、MnO4-锰酸根离子(紫色)不能大量共存的离子1、生成难溶物或微溶物:SO42-与Ba2+、Ag+;OH-与Cu2+、Fe3+、Mg2+、Al3+;Ag+与Cl-、CO32-、SO32-(亚硫酸根离子)、S2-(硫离子);Mg2+、Ba2+、Ca2+与CO32-、SO32-(亚硫酸根离子)、PO43-(磷酸根离子)等不能大量共存.2、生成气体或挥发性物质:如NH4+与OH-,H+与CO32-、HCO3-(碳酸氢根离子)等不能大量共存。
3、生成水:OH-与H+不能大量共存。
碱性溶液中肯定不存在与OH-起反应的离子;酸性溶液中肯定不存在与H+起反应的离子。
酸性溶液、pH=1的溶液、能使pH试纸变红的溶液、使石蕊试液变红等,在分析各选项组的离子时,还需考虑H+的存在;碱性溶液、pH=14的溶液、能使pH试纸变蓝的溶液,使石蕊试液变蓝或使酚酞试液变红的溶液等;在分析各选项组的离子时,还需考虑OH-的存在;练习:1、下列各组离子在溶液中一定能大量共存的是()A.H+、Cl-、OH- B. H+、SO42-、HCO3-C. Ba2+、H+、SO42-D.Cu2+、Cl-、NO3-2、下列各组物质能在同一溶液中大量共存的是()A.NaCl、HCl、MgSO4、Cu(NO3)2B.AgNO3、NaCl、Mg(NO3)2、NaOHC.Ca(OH)2、NaNO3、Na2CO3、NH4ClD.HCl 、K2SO4、NaOH、NaNO33、分别将下列各组物质同时加到足量的水中,能得到无色透明溶液的是()A. NaNO3、Ba(OH)2、HNO3B. H2SO4、NaNO3、Na2SO4C. H2SO4、NaNO3、FeSO4D.CaCl2、Na2SO4、BaCl24、化学兴趣小组的同学在分析某种含有三种溶质的无色透明溶液时,得出了以下结论,其中的三种溶质可能正确的是()A. CuCl2、Ba(OH)2、NaClB. Na2SO4、HCl、Ba(NO3)2C. KCl、HCl、Al2(SO4)3D. HCl、NaCO3、Na2SO45、下列各组物质能在PH为1的溶液中大量共存,且溶液为无色透明的是()A. CaCl2、NaNO3、KOH、MgCl2 B. CuSO4、NaCl、H2SO4、KNO3C. Na2CO3、NaCl 、KNO3、NH4ClD. ZnSO4、MgCl2、NaNO3、KCl。

常见沉淀白色:BaSO4/BaCO3/CaCO3/AgCl/Ag2CO3/Mg(OH)2/Fe(OH)2/Al(OH)3/CuCO3/ZnCO3/MnCO3/ Zn(OH)2Fe(OH)2蓝色:Cu(OH)2浅黄色:AgBr红褐色:Fe(OH)3沉淀鉴别Cu(OH)2蓝色沉淀Fe(OH)3红褐色沉淀AgBr淡黄色沉淀AgI ,Ag3PO4黄色沉淀CuO 黑色沉淀Cu2O 红色沉淀Fe2O3 红棕色沉淀FeO 黑色沉淀FeS2 黄色沉淀PbS 黑色沉淀FeCO3 灰色沉淀Ag2CO3 黄色沉淀AgBr 浅黄色沉淀AgCl 白色沉淀Cu2(OH)2CO3 暗绿色沉淀BaCO3白色沉淀(且有CO2生成)CaCO3白色沉淀(且有CO2生成)BaSO4白色沉淀不溶的碳酸盐白色沉淀(且有CO2生成)不溶的碱、金属氧化物白色沉淀(且有CO2生成)Fe(OH)2为白色絮状沉淀(在空气中很快变成灰绿色,再变成Fe(OH)3红褐色沉淀)相关口诀钾钠铵盐硝酸盐均可溶盐酸盐银不溶硫酸盐钡不溶白色沉淀: CaCO3. BaCO3 . BaSO4. AgCL. Mg(OH)2蓝色沉淀: Cu(OH)2红褐色沉淀: Fe(OH)3不建议死记硬背,只需记住每个阴离子里哪个不溶即可,钾钠铵硝都溶溶解性口诀一钾钠铵盐溶水快,①硫酸盐除去钡银铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③氢氧根多溶一个钡④口诀中未有皆下沉。
⑤注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀);③硝酸盐都溶于水;④碱性物质中除了钾离子钠离子铵离子锂离子还有钡离子也可溶⑤口诀中没有涉及的盐类都不溶于水;溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。

高二化学溶解性表记忆口诀溶解性表是大家学习化学必备的解题技巧,大家记住了这个,后面的学习就相对简单了。
下面由店铺给你带来关于高二化学溶解性表记忆口诀,希望对你有帮助!高二化学溶解性表记忆口溶解性口诀一钾钠铵盐溶水快,① 硫酸沉钡银铅钙。
②氯盐不溶氯化银,硝盐溶液都透明。
③碱溶锂钾钠钡氨,④ 口诀未提皆下沉。
⑤注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀);③硝酸盐都溶于水;④碱性物质中除了钾离子钠离子铵离子锂离子还有钡离子也可溶⑤口诀中没有涉及的盐类都不溶于水;溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅; 碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶,氯盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五(适合初中化学课本后面的附录)钾钠铵盐硝酸盐① 氢氧根多钡离子② 硫酸盐除钡钙银③碳酸溶氢钾钠铵④ 生成沉淀氯化银⑤溶解性口诀六(初学记忆)钾、钠、铵、硝都可溶氯化物里银不溶硫酸盐里钡不溶磷酸碳酸多不溶解释①钾盐、钠盐、铵盐、硝酸盐都溶于水②除了以上四种,氢氧根和钡离子结合时也溶于水③硫酸根除了和钡离子、钙离子、银离子结合时不溶于水,其他都溶④碳酸根除了和氢离子、钾离子、钠离子和铵离子结合时溶于水,其他都不溶⑤氯离子只有和银离子结合时不溶于水⑥磷酸盐除钾钠铵都不溶溶解性口诀七铵钾钠钡氢氧溶① 碳酸只溶铵钾钠② 所有硝酸都能溶③盐酸只有银不溶④ 硫酸只有钡不溶⑤解释①氢氧化铵,氢氧化钾,氢氧化钠,氢氧化钡都溶于水,其余带氢氧根的都不溶于水。

化学常见常见沉淀及溶解性口诀电子教案化学常见沉淀及溶解性口诀
一、常见沉淀反应:
1.氯化银,溴化银,碘化银,沉淀颜色白。
2.氯化铋,碘化铋,黄色沉淀难溶解。
3.氯化铅,溴化铅,碘化铅,沉淀色深棕。
4.氧化铁,沉淀是红色的。
5.氢氧化铜,氢氧化镁,颜色是蓝色。
6.硫化钡,硫化锶,沉淀是白色。
7.硫化铈,沉淀是黄色。
8.矾石溶解,呈酸性。
9.硝酸镁,溶解性大,无沉淀不分家。
二、常见溶解性规律及口诀:
1.碱金银铵,氯化氢能溶。
2.碱苏打,海盐碘化钾,硫化氢溶。
3.除镍钴铜蓝,含铁的都溶。
4.氢氧化物溶液加热,铝锌铬不溶解。
5.硝酸银,氯化银,硝酸汞,氯化汞,氯化铋,碘化铋,季铵盐,溶解大。
6.钙盐阳离子,沉淀多。
7.硫酸根阳离子,溶解好。
8.铬酸盐阳离子,沉淀红。
9.碳酸根阴离子,沉淀白。
10.溴离子存在时,碘化物不能生成。
11.季铵盐,意外形成。
自离解。
三、常见离子的溶解性:
1.卤根离子:氟离子溶解无。
氯溴碘硫氟,加入溴水将共沉。
2.硫酸根离子,除硫酸盐铅以外,其他都溶解。
3.碳酸根离子,碱属离子沉淀多。
4.氢氧根离子,钙镁还有铝。
5.铬酸盐阳离子,铅铜曾见。
不相逢。
6.铁盐盐阳离子,淡红沉淀呈现。
7.银铅氯根离子,差别很大,重铅轻银好。
这些口诀通过简单的押韵和重复巩固知识点,帮助学生更好地记忆常见的沉淀反应和溶解性规律。
溶解性表背诵口诀
溶解性表是化学中常见的一个知识点,它描述了不同物质在不同溶剂中的溶解情况,是化学学习的重要内容。
为了更好地掌握溶解性表,我们可以采用背诵口诀的方式来记忆它。
下面是一份适合初学者背诵的溶解性表口诀,希望大家能够掌握好这门学科。
1. 亲水、亲油不相宜,酸碱性能异乎寻常。
2. 碳酸根、铵盐结尾多,氯化物、硫酸盐零散。
3. 溴化物、碘化物宜水,氧化物、磷酸盐寻油。
4. 氢氧化物多易溶,硫化物常见悬浮。
5. 钾盐常看电解质,硝酸盐运动成家。
6. 草酸盐浓度要注意,铜盐红色最难忘。
7. 下面四个记牢了,别忘了这半老徐娘:
硝酸银加氢氧化,水热反应难遗忘。
氢氧化钠沉淀多,氯化钡鉴定亮闪闪。
8. 最后一个装饰词,未尝不如试一试:
若不试,如何知,再好好学,成大器。
通过这个口诀,我们可以把溶解性表记忆下来,并且不容易遗忘。
不过需要注意的是,这只是一个辅助记忆的方式,要想真正掌握溶解性,还需要多做题,多联系。
常见沉淀白色:BaSO4/BaCO3/CaCO3/AgCl/Ag2CO3/Mg(OH)2/Fe(OH)2/Al(OH)3/CuCO3/ZnCO3/MnCO3/Zn(OH)2 Fe(OH)2蓝色:Cu(OH)2浅黄色:AgBr红褐色:Fe(OH)3沉淀鉴别Cu(OH)2蓝色沉淀Fe(OH)3 红褐色沉淀AgBr淡黄色沉淀AgI ,Ag3PO4 黄色沉淀CuO 黑色沉淀Cu2O 红色沉淀Fe2O3 红棕色沉淀FeO 黑色沉淀FeS2 黄色沉淀PbS 黑色沉淀FeCO3 灰色沉淀Ag2CO3 黄色沉淀AgBr 浅黄色沉淀AgCl 白色沉淀Cu2(OH)2CO3 暗绿色沉淀BaCO3白色沉淀 (且有CO2生成) CaCO3白色沉淀 (且有CO2 生成) BaSO4白色沉淀不溶的碳酸盐白色沉淀 (且有CO2生成) 不溶的碱、金属氧化物白色沉淀(且有CO2生成) Fe(OH)2 为白色絮状沉淀(在空气中很快变成灰绿色,再变成Fe(OH)3 红褐色沉淀 )相关口诀钾钠铵盐硝酸盐均可溶盐酸盐银不溶硫酸盐钡不溶白色沉淀: CaCO3. BaCO3 . BaSO4. AgCL. Mg(OH)2蓝色沉淀: Cu(OH)2红褐色沉淀: Fe (OH)3不建议死记硬背,只需记住每个阴离子里哪个不溶即可,钾钠铵硝都溶溶解性口诀一钾钠铵盐溶水快,①硫酸盐除去钡银铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③氢氧根多溶一个钡④ 口诀中未有皆下沉。
⑤ 注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀);③硝酸盐都溶于水;④ 碱性物质中除了钾离子钠离子铵离子锂离子还有钡离子也可溶⑤口诀中没有涉及的盐类都不溶于水;溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8 类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
溶解性表是大家学习化学必备的解题技巧,这张表的知识点所占的分值是比较大的,比如大家不太擅长的化学推导题就会依照这张表的性质去推断,所以大家一定要掌握这部分知识,那么今天就为大家带来了十一个口诀,无论如何都要记住这部分知识哦!溶解性口诀一钾钠铵盐溶水快,硫酸沉钡银铅钙。
氯盐不溶氯化银,硝盐溶液都透明。
碱溶锂钾钠钡氨,口诀未提皆下沉。
注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀);③硝酸盐都溶于水;④碱性物质中除了钾离子钠离子铵离子锂离子还有钡离子也可溶⑤口诀中没有涉及的盐类都不溶于水。
溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明:以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶,氯盐不溶银亚汞;硫酸盐不溶钡和铅,碳磷酸盐多不溶。
多数酸溶碱少溶,只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不溶有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五(适合初中化学课本后面的附录)钾钠铵盐硝酸盐①氢氧根多钡离子②硫酸盐除钡钙银③碳酸溶氢钾钠铵④生成沉淀氯化银⑤溶解性口诀六(初学记忆)钾、钠、铵、硝都可溶,氯化物里银不溶;硫酸盐里钡不溶,磷酸碳酸多不溶。
解释:①钾盐、钠盐、铵盐、硝酸盐都溶于水②除了以上四种,氢氧根和钡离子结合时也溶于水③硫酸根除了和钡离子、钙离子、银离子结合时不溶于水,其他都溶④碳酸根除了和氢离子、钾离子、钠离子和铵离子结合时溶于水,其他都不溶⑤氯离子只有和银离子结合时不溶于水⑥磷酸盐除钾钠铵都不溶溶解性口诀七铵钾钠钡氢氧溶①碳酸只溶铵钾钠②所有硝酸都能溶③盐酸只有银不溶④硫酸只有钡不溶⑤解释①氢氧化铵,氢氧化钾,氢氧化钠,氢氧化钡都溶于水,其余带氢氧根的都不溶于水。
常见沉淀白色:BaSO4/BaCO3/CaCO3/AgCl/Ag2CO3/Mg(OH)2/Fe(OH)2/Al(OH)3/CuCO3/ZnCO3/MnCO3/ Zn(OH)2Fe(OH)2蓝色:Cu(OH)2浅黄色:AgBr红褐色:Fe(OH)3沉淀鉴别Cu(OH)2蓝色沉淀Fe(OH)3红褐色沉淀AgBr淡黄色沉淀AgI ,Ag3PO4黄色沉淀CuO 黑色沉淀Cu2O 红色沉淀Fe2O3 红棕色沉淀FeO 黑色沉淀FeS2 黄色沉淀PbS 黑色沉淀FeCO3 灰色沉淀Ag2CO3 黄色沉淀AgBr 浅黄色沉淀AgCl 白色沉淀Cu2(OH)2CO3 暗绿色沉淀BaCO3白色沉淀(且有CO2生成)CaCO3白色沉淀(且有CO2生成)BaSO4白色沉淀不溶的碳酸盐白色沉淀(且有CO2生成)不溶的碱、金属氧化物白色沉淀(且有CO2生成)Fe(OH)2为白色絮状沉淀(在空气中很快变成灰绿色,再变成Fe(OH)3红褐色沉淀)相关口诀钾钠铵盐硝酸盐均可溶盐酸盐银不溶硫酸盐钡不溶白色沉淀: CaCO3. BaCO3 . BaSO4. AgCL. Mg(OH)2蓝色沉淀: Cu(OH)2红褐色沉淀: Fe(OH)3不建议死记硬背,只需记住每个阴离子里哪个不溶即可,钾钠铵硝都溶溶解性口诀一钾钠铵盐溶水快,①硫酸盐除去钡银铅钙。
②氯化物不溶氯化银,硝酸盐溶液都透明。
③氢氧根多溶一个钡④口诀中未有皆下沉。
⑤注:①钾钠铵盐都溶于水;②硫酸盐中只有硫酸钡、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀);③硝酸盐都溶于水;④碱性物质中除了钾离子钠离子铵离子锂离子还有钡离子也可溶⑤口诀中没有涉及的盐类都不溶于水;溶解性口诀二钾、钠、铵盐、硝酸盐;氯化物除银、亚汞;硫酸盐除钡和铅;碳酸、磷酸盐,只溶钾、钠、铵。
说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。
溶解性口诀三钾钠铵硝皆可溶、盐酸盐不溶银亚汞;硫酸盐不溶钡和铅、碳磷酸盐多不溶。
多数酸溶碱少溶、只有钾钠铵钡溶溶解性口诀四钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。
)盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。
)再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。
)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物)只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶)最后说碱类,钾、钠、铵和钡。
(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
溶解性口诀五(适合初中化学课本后面的附录)钾钠铵盐硝酸盐①氢氧根多钡离子②硫酸盐除钡钙银③碳酸溶氢钾钠铵④生成沉淀氯化银⑤溶解性口诀六(初学记忆)不是沉淀物……我们初中的口诀是钾【化合物】、钠【化合物】、铵【铵根】、硝【硝酸盐】都可溶氯化物里银不溶硫酸盐里钡不溶解释①钾盐、钠盐、铵盐、硝酸盐都溶于水②除了以上四种,氢氧根和钡离子结合时也溶于水③硫酸根除了和钡离子、钙离子、银离子结合时不溶于水,其他都溶④碳酸根除了和氢离子、钾离子、钠离子和铵离子结合时溶于水,其他都不溶⑤氯离子只有和银离子结合时不溶于水初中常用溶解性口诀(溶解性口诀七)铵钾钠钡氢氧溶①碳酸只溶铵钾钠②所有硝酸都能溶③盐酸只有银不溶④硫酸只有钡不溶⑤解释①氢氧化铵,氢氧化钾,氢氧化钠,氢氧化钡都溶于水,其余带氢氧根的都不溶于水。
②碳酸铵,碳酸钾,碳酸钠都溶于水,其余带碳酸根的都不溶于水。
③所有带硝酸根的都能溶于水。
④带氯离子的只有氯化银不溶于水,其余都溶于水。
(因为盐酸中有氯离子,所以在这里所有带氯离子的都称为盐酸的同一类物质,注意:此说法只用于理解此溶解性口诀,实际中没有此说法)⑤带硫酸根的只有硫酸钡不溶于水,其余都溶于水。
适合高中使用的口诀:碳酸只溶钾钠铵;(碳酸盐里钾钠铵盐易溶)氢氧多溶了钡的碱。
(氢氧根比碳酸根多溶解一个钡离子)硫酸不溶钡和铅;(硫酸盐里钡和铅不溶)三价碳酸天地间。
(三价的阳离子和碳酸根离子都生成气体和沉淀,即上天和入地)还是氢氧人水性好,水底忍渴好几年。
(氢氧根和银离子会生成氧化银沉淀是为水底,忍渴指还生成了水)氯化不溶唯有银;(氯化物中只有银盐不溶)硝酸大度溶万金。
(硝酸盐都易溶)溶解性口诀八钾钠铵盐均可溶;硝盐入水无影踪。
难溶硫酸铅和钡;还有氯化银亚汞。
至于磷酸碳酸盐;绝大多数均难溶。
溶解性口诀九钾钠铵盐均可溶;硝盐遇水影无踪。
硫盐不溶铅与钡;氯物不溶银亚汞。
碳酸与磷酸,钾钠铵才溶。
常见的酸根离子有:碳酸根CO3 -2价碳酸氢根HCO3 -1价硫离子常显-2价硫酸根SO4 -2价亚硫酸根SO3 -2价磷酸根PO4 -3价磷酸氢根HPO4 -2价磷酸二氢根H2PO4 -1价高锰酸根MnO4 -1价锰酸根MnO4 -2价氯离子常显-1价氯酸根ClO3 -1价亚氯酸根ClO2 -1价次氯酸根ClO -1价高氯酸根ClO4 -1价硝酸根NO3 -1价亚硝酸根NO2 -1价碘酸根IO3 -1价硼酸根BO3 -3价钨酸根WO4 -2价硅酸根SiO3 -2价硒酸根SeO4 -2价铬酸根CrO4 -2价二铬酸根Cr2O7 -2价铁酸根FeO2 -1价高铁酸根FeO4 -2价铝酸根AlO3 -3价偏铝酸根AlO2 -1价氢氰根CN -1价草酸根C2O4 -2价初中课本常见:碳酸根CO3 -2价,硫酸根SO4 -2价,亚硫酸根SO3-2价,次氯酸根ClO -1价,硝酸根NO3 -1价。
几种重要阳离子的检验(l)H+ 能使紫色石蕊试液或橙色的甲基橙试液变为红色。
(2)Na+、K+ 用焰色反应来检验时,它们的火焰分别呈黄色、浅紫色(通过钴玻片)。
(3)Ba2+ 能使稀硫酸或可溶性硫酸盐溶液产生白色BaSO4沉淀,且沉淀不溶于稀硝酸。
(4)Mg2+ 能与NaOH溶液反应生成白色Mg(OH)2沉淀,该沉淀能溶于NH4Cl溶液。
(5)Al3+ 能与适量的NaOH溶液反应生成白色Al(OH)3絮状沉淀,该沉淀能溶于盐酸或过量的NaOH溶液。
(6)Ag+ 能与稀盐酸或可溶性盐酸盐反应,生成白色AgCl沉淀,不溶于稀HNO3,但溶于氨水,生成〔Ag(NH3)2〕+。
(7)NH4+ 铵盐(或浓溶液)与NaOH浓溶液反应,并加热,放出使湿润的红色石蕊试纸变蓝的有刺激性气味NH3气体。
(8)Fe2+ 能与少量NaOH溶液反应,先生成白色Fe(OH)2沉淀,迅速变成灰绿色,最后变成红褐色Fe(OH)3沉淀。
或向亚铁盐的溶液里加入KSCN溶液,不显红色,加入少量新制的氯水后,立即显红色。
2Fe2++Cl2=2Fe3++2Cl-(9)Fe3+ 能与KSCN溶液反应,变成血红色Fe(SCN)3溶液,能与NaOH溶液反应,生成红褐色Fe(OH)3沉淀。
(10)Cu2+ 蓝色水溶液(浓的CuCl2溶液显绿色),能与NaOH溶液反应,生成蓝色的Cu(OH)2沉淀,加热后可转变为黑色的CuO沉淀。
含Cu2+溶液能与Fe、Zn片等反应,在金属片上有红色的铜生成。
几种重要的阴离子的检验(1)OH-能使无色酚酞、紫色石蕊、橙色的甲基橙等指示剂分别变为红色、蓝色、黄色。
(2)Cl-能与硝酸银反应,生成白色的AgCl沉淀,沉淀不溶于稀硝酸,能溶于氨水,生成[Ag(NH3)2]+。
(3)Br-能与硝酸银反应,生成淡黄色AgBr沉淀,不溶于稀硝酸。
(4)I-能与硝酸银反应,生成黄色AgI沉淀,不溶于稀硝酸;也能与氯水反应,生成I2,使淀粉溶液变蓝。
(5)SO42-能与含Ba2+溶液反应,生成白色BaSO4沉淀,不溶于硝酸。
(6)SO32-浓溶液能与强酸反应,产生无色有刺激性气味的SO2气体,该气体能使品红溶液褪色。
能与BaCl2溶液反应,生成白色BaSO3沉淀,该沉淀溶于盐酸,生成无色有刺激性气味的SO2气体。
(7)S2-能与Pb(NO3)2溶液反应,生成黑色的PbS沉淀。
(8)CO32-能与BaCl2溶液反应,生成白色的BaCO3沉淀,该沉淀溶于硝酸(或盐酸),生成无色无味、能使澄清石灰水变浑浊的CO2气体。
(9)HCO3-取含HCO3-盐溶液煮沸,放出无色无味CO2气体,气体能使澄清石灰水变浑浊。
或向HCO3-盐酸溶液里加入稀MgSO4溶液,无现象,加热煮沸,有白色沉淀MgCO3生成,同时放出CO2气体。
(10)PO43-含磷酸根的中性溶液,能与AgNO3反应,生成黄色Ag3PO4沉淀,该沉淀溶于硝酸。
(11)NO3-浓溶液或晶体中加入铜片、浓硫酸加热,放出红棕色气体。
几种重要有机物的检验(1)苯能与纯溴、铁屑反应,产生HBr白雾。
能与浓硫酸、浓硝酸的混合物反应,生成黄色的苦杏仁气味的油状(密度大于1)难溶于水的硝基苯。
(2)乙醇能够与灼热的螺旋状铜丝反应,使其表面上黑色CuO变为光亮的铜,并产生有刺激性气味的乙醛。
乙醇与乙酸、浓硫酸混合物加热反应,将生成的气体通入饱和Na2CO3溶液,有透明油状、水果香味的乙酸乙酯液体浮在水面上。
(3)苯酚能与浓溴水反应生成白色的三溴苯酚沉淀。
能与FeCl3溶液反应,生成紫色溶液。
(4)乙醛能发生银镜反应,或能与新制的蓝色Cu(OH)2加热反应,生成红色的Cu2O 沉淀。
用一种试剂或不用试剂鉴别物质用一种试剂来鉴别多种物质时,所选用的试剂必须能和被鉴别的物质大多数能发生反应,而且能产生不同的实验现象。
常用的鉴别试剂有FeCl3溶液、NaOH溶液、Na2CO3溶液、稀H2SO4、Cu(OH)2悬浊液等。
不用其他试剂来鉴别一组物质,一般情况从两个方面考虑:①利用某些物质的特殊性质(如颜色、气味、溶解性等),首先鉴别出来,然后再用该试剂去鉴别其他物质。
②采用一种试剂与其他物质相互反应的现象不同,进行综合分析鉴别。