金属的防护和回收
- 格式:doc
- 大小:27.05 KB
- 文档页数:2

金属的回收以及金属资源的保护
展开全文
金属资源可以说是人类生产生活中非常宝贵的资源,金属的回收已经成为了一种金属再利用的方式之一,今天我们就来学习金属资源的回收以及保护措施。
【金属保护定义】
金属回收是指从废旧金属中分离出来的有用物质经过物理或机械加工成为再生利用的制品。
是从回收、拆解、到再生利用的一条产业链。
【金属资源的保护措施】
1.减缓或防止金属的腐蚀;常用的方法有:
(1)用完铁制品后及时擦洗干净,置于干燥的环境,保持其表面的洁净、干燥.
(2)在铁制品表面涂上一层保护膜.例如,机械零件等表面涂油,家用电器、自行车车架、钢窗等表面刷漆,等等.
(3)在铁制品表面进行烤蓝、煮黑等处理(使其表面形成一层致密的四氧化三铁薄膜).例如,锯条、链条等.
(4)在铁制品表面镀上一层其它金属.例如,自行车车把、钢圈以及门把手和水龙头等表面上,经常镀锌、锡或铬等.
(5)改变铁制品的内部结构,将其制成不锈钢等合金.
2.回收利用废旧金属,这样不仅可以节约金属资源,而且还可以减少对环境的污染.
3.有计划、合理地开采矿物,严禁不顾国家利益的乱采矿.
4.寻找金属的代用品,例如,现在经常用塑料来代替钢和其它合金制造管道、齿轮和汽车外壳等.
【金属回收优点】
金属资源面临枯竭,保护金属资源的有效途径之一就是回收再利用,其中回收废旧金属的好处有节约金属资源、减少环境污染、节约能源
【金属回收意义】
资源再利用,减少金属对污染环境。
通过这篇文章我们可以知道金属资源保护的必要性和可行性,我们在平常生活中就可以做到这些金属保护,同时,我们在生活中可以将金属保护这部分的知识加以学习和掌握。


金属防护和废金属回收1.铁在潮湿的空气环境中最易生锈,铁生锈实际上是铁与氧气和水发生一系列发杂的反应。
铁锈是混合物,其主要成分为红棕色Fe2O3,它的结构比较疏松多孔。
环境中的稀硫酸、醋酸溶液和氯化钠等物质能够加快铁的锈蚀,而铝在空气中表面会生产一层致密的氧化铝薄膜,保护内部的铝不被氧化。
铜在氧气、水、CO2共存的条件下表面会出现铜绿。
2.保护铁制品少生锈的最常用方法为:(1)保持铁制品表面的洁净与干燥;(2)通常采用在铁制品表面覆盖保护层;如轴承涂防锈油,电冰箱表面刷油漆。
刺刀、锯条表面涂防锈油、烤蓝,铁制脸盆烧涂搪瓷等或者在铁制品表面镀锡、镀锌和镀铬,如自行车龙头镀铬。
(3)改变铁制品的内部结构,如制不锈钢等合金。
3.铁的常见氧化物为FeO、Fe2O3、Fe3O4。
(写化学式)铜的常见氧化物为CuO、Cu2O。
(写化学式)铝的自我保护的化学方程式为:4Al+3O2=2Al2O34.废金属不但会造成资源浪费,还会产生镉、汞、铅等有毒金属对环境的污染。
回收废金属的好处为:节约资源和减少污染。
5.某化学兴趣小组为了测定鸡蛋壳中碳酸钙的含量,进行如下实验:将25.0g洗净、粉碎后的鸡蛋壳样品放于烧杯中,往烧杯中滴加稀盐酸(整个过程不考虑盐酸的挥发和气体的溶解),实验测得烧杯中剩余物质的质量与加入盐酸的质量之间的关系如图所示。
求:(1)产生CO2的总质量为9.9g(2)鸡蛋壳中碳酸钙的质量分数。
解:(1)m(CO 2)=25.0g+150g-165.1g=9.9g(2)设碳酸钙的质量为x↑++=+22232CO O H CaCl HCl CaCO 100 44 x 9.9g gx 9.944100= g x 5.22=W(CaCO 3)=%90%100255.22=⨯gg 答:鸡蛋壳中碳酸钙的质量分数为90%.。

课题:第五章第3节金属防护和废旧金属回收【教学目标】(一)知识与技能1.理解防止金属锈蚀的简单方法;2.知道废弃金属对环境的污染,理解回收金属的重要性。
通过铁锈蚀条件的探究活动,进一步提升科学探究的欲望和分析、归纳水平。
(三)情感态度与价值观1.理解处理废金属,回收金属的价值,提升资源意识和环保意识。
2.让学生知道学习化学的重要性,树立学生的爱国热情。
【教学重点及难点】重点:铁生锈的原因及防止铁生锈的办法。
难点:钢铁锈蚀条件的探究【教学思路】教师创设情景,学生讨论日常生活中观察到的金属锈蚀现象,总结出金属锈蚀的危害,让学生通过探究金属的锈蚀实验,归纳出金属的锈蚀条件,通过观察生活、生产中金属防锈措施,讨论、交流、总结出金属的防锈方法,通过理解、阅读资料,理解废金属对环境的影响和回收的重要性,具体教学思路如下所示:教学内容(二)防止金属锈蚀的方法教师活动学生活动【演示实验、激发兴趣】在切过咸菜的铁质菜刀同一面上选相近三处实行以下实验:一处(a处)用湿棉球润湿另一处(b处)用干布擦干。
第三处(c处)用干布擦干后,涂上一层食用油。
放置一昼夜,猜猜菜刀三处表面有何变化?然后展示菜刀【提出问题】根据以上实验,并结合日常生活中观察,你能总结出防止铁生锈的办法吗?【小结并板书】钢铁的防锈方法。
【创新应用】1、自行车是人们常用的交通工具,请按以下要求,回答以下问题。
(1)自行车的主要零件是由 (填“生铁”或“钢”)制造的。
(2)请写出自行车上各部分零件都采用了什么防锈方法?(3)被雨水淋湿的自行车能否直接用带油的布擦?为什么?2、如下图,取一团光亮无锈的铁丝绒,放入一支洁净试管底部,将试管倒放在盛水的烧杯里。
数天后,能观察到的现象是。
【交流、思考、讨论】学生通过观察实验现象,思考、讨论,分析原因。
【交流、讨论】分组交流、讨论,然后小组汇报同学们讨论的结果。
钢铁的防锈方法:(1)“洁身自好”:保持铁制品表面的干燥和洁净。

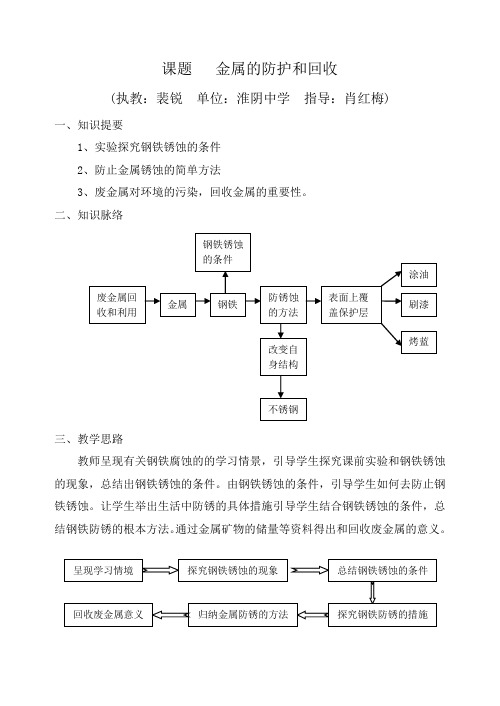
课题金属的防护和回收(执教:裴锐单位:淮阴中学指导:肖红梅)一、知识提要1、实验探究钢铁锈蚀的条件2、防止金属锈蚀的简单方法3、废金属对环境的污染,回收金属的重要性。
二、知识脉络三、教学思路教师呈现有关钢铁腐蚀的的学习情景,引导学生探究课前实验和钢铁锈蚀的现象,总结出钢铁锈蚀的条件。
由钢铁锈蚀的条件,引导学生如何去防止钢铁锈蚀。
让学生举出生活中防锈的具体措施引导学生结合钢铁锈蚀的条件,总结钢铁防锈的根本方法。
通过金属矿物的储量等资料得出和回收废金属的意义。
四、组块设计通过创设情境导入金属的锈蚀比较自然,易于激发学生的学习兴趣,增强了学生的责任感和使命感。
从学生熟悉的身边现象入手探究铁钉的锈蚀,引导他们发现问题,分析问题,获得知识和方法。
通过学生已有的生活经验入手,引导他们发现问题,分析和解决问题,拉近化学与学生的距离,使学生感受到身边处处有化学,感悟到化学学科的价值和化学学习的意义和方法。
组块3废金属的回收和利用资料二:随着社会进步,人们的生活水平的提高,在日常生活中出现了大量金属废弃物,如废弃的汽车以及电脑、电视机,金属的易拉罐等。
评注:现代高素质的社会公民的标志之一,是具有较强的资源观和环保的理念。
通过本部分知识的学习,力求促进学生树立科学的资源观和环保理念。
五、参考资料金属的防腐根据腐蚀机理和不同环境,金属主要有以下几种防腐方法:(1)改变金属的成分,提高材料本身的抗腐能力。
如在冶炼金属时加入一些合金元素(如镍、铬、硅、锰、钛、钨、钼、钒、稀土等),铁与这些元素结合,可增强抗蚀性能,不锈钢就是如此。
此外,利用热处理或渗铬、渗铝、渗氮等来改变金属的内部结构,或使金属产生一层抗蚀性能很强的表面。
(2)用耐腐蚀材料覆盖金属表面。
可以用辗压、浸镀、喷镀、电镀和化学镀等方法在金属器件的表面覆盖耐腐蚀的金属层。
这种金属覆盖层分为两类:一类是阳极保护层,它用的金属材料电位比主体金属要低,如在铁上镀锌、镉等。
第三节金属的防护和废金属的回收新桥中学张艳教学目标(一)知识与技能1、了解金属锈蚀的条件以及防止其锈蚀的简单方法;2、知道废旧金属对环境的污染.认识回收废旧金属的重要性。
(二)过程和方法1、通过观察、实验、阅读材料、联系实际等方法获取信息;2、运用比较、分析、联想、分类等方法对所获取的信息进行加工、提取;(三)情感态度与价值观1、增强对生活和自然界中化学现象的好奇心和探究欲;2、关注与化学有关的社会问题;3、逐步树立珍惜资源、爱护环境、合理使用化学物质的观念。
教学重点及难点重点:1.铁锈蚀的条件及其防护方法;2.合理利用金属资源的意识。
难点:对铁锈蚀条件及其防护措施的初步探究。
1、在下列情况下,埋在地下的铸铁管道腐蚀最快的是 ( ) A 在干燥、致密、不透气的土壤中 B 在潮湿、疏松、透气的土壤中 C 在潮湿、致密、不透气的土壤中 D 在潮湿、疏松、透气的酸性土壤中2、下列防锈措施不当的是 ( ) A 在铁制品表面镀上一层锌 B 在车船表面喷涂油漆C 将使用后的菜刀用布擦干D 用洗涤剂把铁制品表面的油膜洗去3、如图所示电线杆的铁丝拉杆上M 、N 、P 三点,最易生锈的是 ( ) A 、M 点 B 、N 点 C 、P 点 D 、无法确定4、如图所示,大试管中是螺旋状的光亮的铁丝,把试管倒插入水中,放置一段时间(约一周)后,观察到铁丝表面有生成试管内水面将,产生以上现象的原因是。
板书设计:§5-3金属的回收和防护一、钢铁的锈蚀及其防护1、金属的防护和回收(1)铁制品锈蚀条件的探究▪在水、氧气同时存在的环境中铁能锈蚀▪铁锈的主要成分是Fe2O3 (红棕色)▪铁锈是疏松多孔的物质,易吸水,所以钢铁制品一旦生锈应及时除去否则会加快锈蚀的速度(2)防锈的方法总结2:涂油刷油漆镀上一层其他金属涂保护膜烧制一层搪瓷烤蓝做成不锈钢——改变金属的内部结构保持表面清洁干燥二、废金属的回收和利用:1、废弃金属的危害(1)极大的浪费土地资源(2)严重地环境污染2、回收金属的重要意义节约矿产资源、节约能源等,有着巨大的社会效益和经济效益;减少环境污染。
第三节金属的防护和回收1.知道金属生锈的危害和所造成的浪费,每年因被腐蚀而损耗的钢铁材料,约占全年钢铁总产量的十分之一。
2.通过探究实验知道钢铁生锈的条件:铁在空气中锈蚀,实际上是铁跟氧气、水等物质相互作用,发生一系列复杂的化学反应,使铁转化为铁的化合物的过程。
3.知道铁锈的成分,铁锈成分复杂,主要是氧化铁。
4.知道铁锈的特点:疏松多孔,能让水分和空气中的氧气通过,不断向里渗透,继续跟铁反应,直至铁被完全锈蚀。
因此铁制品一旦生锈,要及时把锈除掉。
5.钢铁除能被空气腐蚀外,还能被其他物质腐蚀或锈蚀。
如盐酸和硫酸等也能把钢铁腐蚀。
6.知道钢铁制品保护的原理:常采用在钢铁表面覆盖保护层的方法来防止钢铁的生锈。
7.知道钢铁制品防锈的常见用的方法:在钢铁制品表面喷油漆,在机械表面涂防锈油,在面盆、杯子等表面烧涂搪瓷等。
另外,还可以在钢铁表面镀上一层能起保护作用的其他金属。
8.知道铝等金属的自我保护:在空气中生成了一层致密的氧化物的保护膜。
从而保护了里面的金属进一步被腐蚀。
同时也提醒同学们注意,如铝制品表面生了“一层灰暗色的物质”,不要把它擦掉。
9.知道什么是废金属:指冶金工业、金属加工业和日常生活中丢弃的金属碎屑、碎块,锈蚀和报废的金属物品等。
10.能说出废金属造成的危害:废金属不仅造成资源浪费,还会造成镉、汞等有毒金属对环境的污染。
11.能说出回收利用废金属的意义:既可以节约大量的煤和铁矿石,又能减少污染空气的悬浮颗粒物。
12.知道回收利用废金属的巨大社会效益和经济效益:目前全球钢产量的45%是通过对废钢的冶炼来完成的,全球铜产量的40%是通过对废铜的冶炼来完成的。
目前我国金属产品三分之一以上的原料来自再生资源。
1.重点:钢铁的锈蚀及其防护。
2.难点:探究钢铁的锈蚀的条件,以及设计对照实验。
3.疑点:是否只有空气才能使钢铁锈蚀?怎样保存钢铁制品才能既很好地防止钢铁制品的生锈又不影响钢铁制品的使用?是否不同的钢铁制品的防锈方法都相同?一、防止汽车金属机件锈蚀汽车长期停驶,由于自然条件影响,会使技术状况不断变坏,金属机件锈蚀。
第3节金属防护和废金属回收【自主学案】一、金属的锈蚀与防护1.铁在空气中锈蚀,实际上是铁跟_______、_______等物质相互作用,发生一系列复杂的化学反应,使铁转化为铁的化合物的过程。
铁锈的主要成分是_______,它是一种疏松多孔的物质,具有吸水性。
2.防止钢铁生锈的方法有:(1)______________;(2)______________;(3)改变钢铁的组成和结构,制成不易生锈的合金。
3.铝的“自我保护”是指铝在空气中与氧气反应,生成的氧化铝可以形成一层致密而结实的膜覆盖在铝的表面,阻止铝进一步与_______反应。
所谓“电化铝”,是用特殊的方法使铝表面形成加厚的_______保护层的铝制品。
二、废金属的回收和利用废金属主要是指冶金工业、金属加工业和日常生活中丢弃的金属碎屑、碎块,_______的金属物品等。
废金属不但造成_______,还会造成_______等有毒金属对环境的污染。
目前,全球钢产量的_______和铜产量的_______是通过对废金属的冶炼完成的。
【教材解读】一、钢铁锈蚀的条件1.探究锈蚀条件的实验:实验室里探究钢铁锈蚀的条件运用的是控制变量法。
即让铁处在水的环境中、空气的环境中、水和空气同时存在的环境中、酸与空气的环境中、盐溶液与空气的环境中来看铁锈蚀的情况。
在进行实验时,最重要的是形成不同的环境和仔细观察铁在不同环境中的变化情况,其次是注意将每个实验进行分析、比较、综合推理,得出正确的结论。
【教材答疑】P127“活动与探究”【点拨】使铁生锈的因素有酸、盐、水与空气同时存在的环境。
2.条件:钢铁在有水和空气同时存在的条件下易生锈,当与酸溶液或盐溶液接触后会加快锈蚀。
其实质是钢铁与水和空气发生复杂的化学反应生成铁锈。
3.铁锈:铁锈的成分很复杂,主要成分是氧化铁(Fe2O3)。
铁锈是一种疏松多孔的物质,不能阻止里层的铁与氧气、水分等反应,且能够涵养水分,加快铁的锈蚀。