材料科学基础-固体的结构
- 格式:ppt
- 大小:18.33 MB
- 文档页数:149

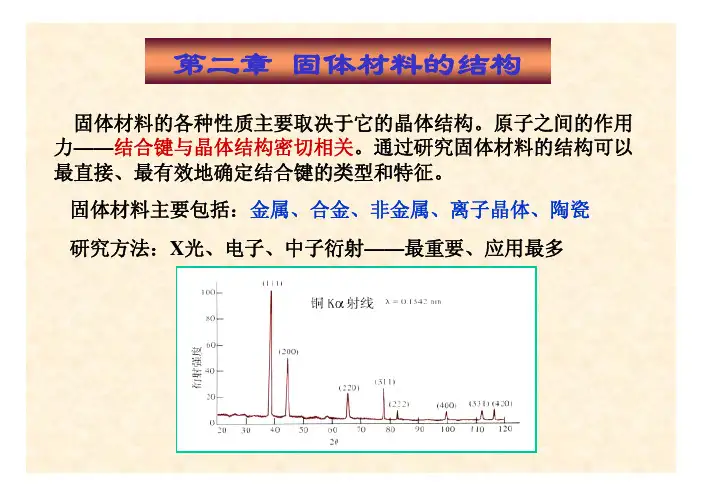
第二章固体材料的结构固体材料的各种性质主要取决于它的晶体结构。
原子之间的作用结合键与晶体结构密切相关。
通过研究固体材料的结构可以最直接、最有效地确定结合键的类型和特征。
固体材料主要包括:金属、合金、非金属、离子晶体、陶瓷研究方法:X光、电子、中子衍射——最重要、应用最多§2-1 结合键结合键——原子结合成分子或固体的结合键决定了物质的物理、化学、力学性质。
一切原子之间的结合力都起源于原子核与电子间的静电交互作用(库仑力)。
不同的结合键代表了实现结构)的不同方式。
一、离子键典型的金属与典型的非金属元素就是通过离子键而化合的。
从而形成离子化合物或离子晶体由共价键方向性特点决定了的SiO2四面体晶体结构极性共价键非极性共价键五、氢键含有氢的分子都是通过极性共价键结合,极性分子之间结合成晶体时,通过氢键结合。
例如:H 2O ,HF ,NH 3等固态冰液态水§2-2 金属原子间的结合能一、原子作用模型固态金属相邻二个原子之间存在两种相互作用:a) 相互吸引——自由电子吸引金属正离子,长程力;b) 相互排斥——金属正离子之间的相互排斥,短程力。
平衡时这二个力相互抵消,原子受力为0,原子处于能量最低状态。
此时原子间的距离为r0。
§2-3 合金相结构基本概念♦合金——由两种或两种以上的金属或金属非金属元素通过化学键结合而组成的具有金属特性的材料。
♦组元、元——组成合金的元素。
♦相——具有相同的成分或连续变化、结构和性能的区域。
♦组织——合金发生转变(反应)的结果,可以包含若干个不同的相,一般只有一到二个相。
♦合金成分表示法:(1) 重量(质量)百分数A-B二元合金为例m B——元素B的重量(质量m A——元素A的重量(质量合金中的相分为:固溶体,化合物两大类。
固溶体金属晶体(溶剂)中溶入了其它元素(溶质)后,就称为固溶体。
一、固溶体的分类:♦按溶质原子在溶剂中的位置分为:置换固溶体,间隙固溶体♦按溶解度分为:有限固溶体,无限固溶体♦按溶质原子在溶剂中的分布规律分为:有序固溶体,无序固溶体置换固溶体:溶质原子置换了溶剂点阵中部分溶剂原子。

第1章固体结构1.何谓晶体?晶体与非晶体有何区别?2.已知MgO晶体中Mg2+和O2-在三维空间有规律地相间排列,其晶体结构相当于两套面心立方点阵互相套叠在一起,晶胞常数a=b=c=4.20 ,α=β=γ=90℃,请回答:①画出MgO晶体二维和三维空间的晶体结构图.②从①的图形中抽象出MgO晶体的空间点阵图形.③从②中划分出单位空间格子,计算其结点数.④画出晶胞结构图,指出晶胞中的分子数.3.何谓元素电负性,有何意义?在元素周期表中分布规律如何?4.何谓晶格能,用途?试计算MgO晶格能。
已知:MgO属NaCl型结构,立方面心点阵N0=6.023×1023,e=4.8×10-10静电单位,r =1.32 , r =0.78 ,A=1.74765.画出MgO晶体(立方面心点阵)在(1 0 0)、(1 1 0)、(1 1 1)晶面上的结点和离子排布图.6.立方晶系中①画出下列晶面:(0 0 1)、(1 0)、(1 1 1)②在①所画晶面上分别标出下列晶向:[2 1 0]、[1 1 1]、[1 0 ].7.在立方晶系中给出(1 1 1)面和(1 1 )面交棱的晶棱符号.8.找出正交晶系(斜方)(P点阵)宏观对称型.9.何谓布拉维点阵?举例论证为什么仅有14种?14种布拉维点阵分属的七个晶系名称?点阵常数特点?14种布拉维点阵分为几个类型?结点数计算?10.表示晶体的宏观对称性,其特点?如何表示晶体的微观对称性,其特点?11.划分单位平行六面体应遵循那些原则?何谓晶格常数?12.何谓晶胞、原胞、单位空间格子?13.试举例说明:晶体结构与空间点阵?晶胞与单位空间格子的关系?14.什么叫离子半径?有何实用意义?什么叫离子极化?极化对晶体结构有什么影响?15.解释原子,离子配位数. 根据半径比关系,说明下列离子与O2-配位时的配位数及配位多面体的类型.r =1.32 , r =0.39 ,r =0.57 ,r =0.78 ,r =1.10 .16.胞林规则有几条?其要点是什么?应用胞林规则有何局限性?17.试用胞林规则分析MgO晶体结构.(r =0.78 ,r =1.32 )18.运用胞林规则来解释在氧离子立方密堆体中,对于获得稳定结构各需要何种电价的离子,其中:①所有八面体间隙位置均填满.②所有四面体间隙位置均填满.③填满一半八面体间隙位置.④填满一半四面体间隙位置.19.已知:r =0.78 ,Mg的原子量为24.30,r =1.32计算:①MgO的点阵常数;②MgO的密度.20.画出闪锌矿、萤石晶胞结构在(0 0 1)面上的投影图.21.金红石的晶胞为什么不属于四方体心格子而是四方原始格子呢?而萤石的结构为什么不是立方原始格子而是立方面心格子?22.比较ThO2、TiO2、MgO结构中间隙的大小.23.简单说明下列名词的含义:反萤石结构,反尖晶石结构.24.指出下列化合物的结构类型,并改写成化学式:γ-Ca2[SiO4]、Ca2Al[AlSiO7]、CaMg[Si2O6]、Mg3[Si4O10](OH)2、K[AlSi3O8].25.高岭石、叶腊石和云母具有相似的结构,画出它们的结构草图,说明它们结构的区别及由此而引起的性质上的差异.26.下列物质的结构式,化学组成式写成相应的化学组成式和结构式:a) Al2O3·2SiO2·2H2O; ②2CaO·5MgO·8SiO2·H2O;③CaMg[Si206]; ④Na[AlSi3O8]27.说明高岭石、叶腊石和白云母结构区别及由此引起的性质上差异.28.在层状硅酸盐结构中,八面体层中的Al3+可以取代四面体层中的Si4+、而四面体层中的Si4+从来不会置换八面体层中的Al3+为什么?已知:r =1.40 , r =0.40 ,r =0.53 .29.青石2MgO·2Al2O3·5SiO2具有与绿柱石Be3Al2[Si6O8]类型结构,写出它的结构式,并指出它是由绿柱石进行怎样的离子置换而得来的?30.α—方石英属立方晶系,面心立方点阵,a=7.05 ,请a) 画出晶胞在(0 0 1)面上的投影图,注明各离子相对标高。



第2章 固体材料的结构一、选择题1.空间电子的意义为()。
[浙江大学2006研]A.晶体中杂质原子的分布规律B.晶体中原子或分子的空间规则排列C.晶体中与原子或分子的电荷空间分布规律【答案】B2.间隙相和间隙固溶体的区别在于()。
[东南大学2005研]A.间隙相的结构比间隙固溶体简单B.间隙相中原子结合符合化合价规律,间隙固溶体不符合化合价规律C.间隙固溶体中间隙原子在溶剂晶格的间隙中,间隙相中原子在正常原子位上D.间隙相中有点阵畸变,间隙固溶体中没有点阵畸变【答案】C3.离子晶体通常借助表面离子的极化变形和重排来降低其表面能,对于下列离子晶体的表面能,最小的是()。
[南京工业大学2008研]A.CaF2B.PbF2C.Pbl2D.BaSO4E.SrSO4【答案】C二、填空题1.材料的结合键决定其弹性模量的高低。
氧化物陶瓷材料以______键为主,结合键______故其弹性模量______;金属材料以______键为主,结合键______故其弹性模量______;高分子材料的分子链上是______键,分子链之间是______键,故其弹性模量______。
【答案】离子;较强;较高;金属;较弱;较低;共价;分子;最低2.固溶体中,当溶质原子和溶剂原子分别占据固定位置,且每个晶胞中溶质原子和溶剂原子数之比一定时,这种有序结构被称为______。
[北京工业大学2009研]【答案】超点阵3.形成有序固溶体的必要条件是:______、______、______。
[中南大学2003研]【答案】异类原子之间相互吸引力大于同类原子之间吸引力;一定的化学成分;较慢的冷却速度4.无序固溶体转变为有序固溶体时,合金性能变化的一般规律是:强度和硬度______,塑性______,导电性______。
[中南大学2003研]【答案】升高;降低;降低三、判断题1.固溶体是一种溶解了杂质组分的非晶态固体。
[中南大学2004研]【答案】×2.形成连续固溶体的最主要条件是溶质和溶剂的晶体结构要一致,例如,银和铝都具有面心立方结构。


《材料科学基础》上半学期内容重点第一章固体材料的结构基础知识键合类型(离子健、共价健、金属健、分子健力、混合健)及其特点;键合的本质及其与材料性能的关系,重点说明离子晶体的结合能的概念;晶体的特性(5个);晶体的结构特征(空间格子构造)、晶体的分类;晶体的晶向和晶面指数(米勒指数)的确定和表示、十四种布拉维格子;第二章晶体结构与缺陷晶体化学基本原理:离子半径、球体最紧密堆积原理、配位数及配位多面体;典型金属晶体结构;离子晶体结构,鲍林规则(第一、第二);书上表2-3下的一段话;共价健晶体结构的特点;三个键的异同点(举例);晶体结构缺陷的定义及其分类,晶体结构缺陷与材料性能之间的关系(举例);第三章材料的相结构及相图相的定义相结构合金的概念:固溶体置换固溶体(1)晶体结构无限互溶的必要条件—晶体结构相同比较铁(体心立方,面心立方)与其它合金元素互溶情况(表3-1的说明)(2)原子尺寸:原子半径差及晶格畸变;(3)电负性定义:电负性与溶解度关系、元素的电负性及其规律;(4)原子价:电子浓度与溶解度关系、电子浓度与原子价关系;间隙固溶体(一)间隙固溶体定义(二)形成间隙固溶体的原子尺寸因素(三)间隙固溶体的点阵畸变性中间相中间相的定义中间相的基本类型:正常价化合物:正常价化合物、正常价化合物表示方法电子化合物:电子化合物、电子化合物种类原子尺寸因素有关的化合物:间隙相、间隙化合物二元系相图:杠杆规则的作用和应用;匀晶型二元系、共晶(析)型二元系的共晶(析)反应、包晶(析)型二元系的包晶(析)反应、有晶型转变的二元系相图的特征、异同点;三元相图:三元相图成分表示方法;了解三元相图中的直线法则、杠杆定律、重心定律的定义;第四章材料的相变相变的基本概念:相变定义、相变的分类(按结构和热力学以及相变方式分类);按结构分类:重构型相变和位移型相变的异同点;马氏体型相变:马氏体相变定义和类型、马氏体相变的晶体学特点,金属、陶瓷中常见的马氏体相变(举例)(可以用许教授提的一个非常好的问题――金属、陶瓷马氏体相变性能的不同――作为题目)有序-无序相变的定义玻璃态转变:玻璃态转变、玻璃态转变温度、玻璃态转变点及其黏度按热力学分类:一级相变定义、特点,属于一级相变的相变;二级相变定义、特点,属于二级相变的相变;按相变方式分类:形核长大型相变、连续型相变(spinodal相变)按原子迁动特征分类:扩散型相变、无扩散型相变第5章 金属材料的显微结构特征一、纯金属的凝固及结晶1、结晶的热力学条件结晶后系统自由能下降。

材料科学基础名词解释第一章固体结构1、晶体:原子按一定方式在三维空间内周期性地规则重复排列,有固定熔点、各向异性。
非晶体:原子没有长程的周期排列,无固定的熔点,各向同性等。
2、中间相:两组元A 和B 组成合金时,除了形成以A 为基或以B 为基的固溶体外,还可能形成晶体结构与A,B 两组元均不相同的新相。
由于它们在二元相图上的位置总是位于中间,故通常把这些相称为中间相。
3、晶体点阵:由实际原子、离子、分子或各种原子集团,按一定几何规律的具体排列方式称为晶体结构或晶体点阵。
4、配位数:晶体结构中任一原子周围最近邻且等距离的原子数。
5、晶格:描述晶体中原子排列规律的空间格架称之为晶格。
6、晶胞:在点阵中取出一个具有代表性的基本单元(最小平行六面体)作为点阵的组成单元,称为晶胞。
7、空间点阵:由周围环境相同的阵点在空间排列的三维列阵成为空间点阵。
8、晶向:在晶格中,穿过两个以节点的任一直线,都代表晶体中一个原子列在空间的位向,称为晶向。
9、晶面:由节点组成的任一平面都代表晶体的原子平面,称为晶面。
10、晶向指数(晶面指数):为了确定晶面、晶向在晶体中的相对取向、就需要一种符号,这种符号称为晶面指数和晶向指数。
国际上通用的是密勒指数。
一个晶向指数并不是代表一个晶向,二十代表一组互相平行、位向相同的晶向。
11、晶向族:原子排列相同但空间位向不同的所有晶向称为晶向族,以<uvw>表示。
12、晶面间距:相邻两个平行晶面之间的垂直距离。
低指数晶面的面间距较大,而高指数晶面的面间距较小。
晶面间距越大,则该晶面上原子排列越紧密,该原子密度越大。
13、配位数:每个原子周围最近邻且等距离的原子数目,称为配位数。
14、多晶型性:有些金属固态在不同温度或不同压力范围内具有不同的晶体结构,这种性质称为晶体的多晶型性。
15、多晶型性转变:具有多晶型性的金属在温度或压力变化时,由一种结构转变为另一种结构的过程称为多晶型性转变,也称为同素异构转变。

考研必备之《材料科学基础》学霸笔记材料科学基础笔记第⼀章原⼦结构与键合概述:决定材料性能的最根本的因素是组成材料的各元素的原⼦结构,原⼦间的相互作⽤、相互结合,原⼦或分⼦在空间的排列分布和运动规律以及原⼦集合体的形貌特征等。
为此,我们需要了解材料的微观构造,即其内部结构和组织状态,以便从其内部的⽭盾性找出改善和发展材料的途径。
第⼀节原⼦结构1 物质的组成物质是由⽆数微粒按⼀定⽅式聚集⽽成的,这些微粒可能是原⼦、分⼦或离⼦;分⼦是能单独存在且保持物质化学特性的⼀种微粒;原⼦是化学变化中的最⼩微粒。
2 原⼦的结构(原⼦结构直接影响原⼦间的结合⽅式)3 原⼦的电⼦结构3.1电⼦既有粒⼦性⼜具有波动性,具有波粒⼆象性。
3.2电⼦的状态和在某处出现的机率可⽤薛定谔⽅程的解/波函数来描述,即原⼦中每个电⼦的空间位置和能量可⽤四个量⼦数来确定:a主量⼦数(n):决定原⼦中电⼦的能量及与核的平均距离(⼀般能量低的趋向近轨道,r较⼩,反之则反),即表⽰电⼦所处的量⼦壳层。
如K、L、M…,n=1,2,3;b 轨道⾓动量量⼦数(l):表⽰电⼦在同⼀壳层内所处的能级,与电⼦运动的⾓动量有关。
如s、p、d、f…(0,1,2,…n-1);c 磁量⼦数(m):给出每个轨道⾓动量量⼦数的能级数或轨道数,为2l+1,决定电⼦云的空间取向;d ⾃旋⾓动量量⼦数(s):反映电⼦不同的⾃旋⽅向,其值可取*只有n,l决定能量和能级3.3能级和能级图把电⼦不同状态对应着相同能量的现象称为简并。
将所有元素的各种电⼦态(n,l)按能量⽔平排列成能级图。
3.4核外电⼦的排布规则a 能量最低原理:电⼦的排布总是尽可能使体系的能量最低;b Pauling不相容原理:在⼀个原⼦中,不可能有上述运动状态完全相同的两个电⼦,即不能有上述四个量⼦数都相同的两个电⼦;c 洪德Hund规则:在同⼀个亚层中的各个能级中,电⼦的排布尽可能分占不同的能级,⽽且⾃旋⽅向相同(尽可能保持⾃旋不成对);3.5 元素周期表元素是具有相同核电荷数的同⼀类原⼦的总称;元素的外层电⼦结构随着原⼦序数的递增⽽呈周期性的变化规律称为元素周期律;元素周期表是元素周期律的表现形式;元素的性质、原⼦结构和该元素在周期表中的位置三者之间有着密切的关系。
材料科学基础-固体结构(总分:430.00,做题时间:90分钟)一、论述题(总题数:43,分数:430.00)1.试证明四方晶系中只有简单四方点阵和体心四方点阵两种类型。
(分数:10.00)__________________________________________________________________________________________ 正确答案:(可作图加以证明。
四方晶系表面上也可含简单四方、底心四方、面心四方和体心四方结构,然而根据选取晶胞的原则,晶胞应具有最小的体积,尽管可以从4个体心四方晶胞中勾出面心四方晶胞(图2(a)),从4个简单四方晶胞中勾出1个底心四方晶胞(图2(b)),但它们均不具有最小的体积。
因此,四方晶系实际上只有简单四方和体心四方两种独立的点阵。
[*])解析:2.为什么密排六方结构不能称为一种空间点阵?(分数:10.00)__________________________________________________________________________________________ 正确答案:(空间点阵中每个阵点应具有完全相同的周围环境,而密排六方晶胞内的原子与晶胞角上的原子具有不同的周围环境。
在A和B原子连线的延长线上取BC=AB,然而C点却无原子。
若将密排六方晶胞角上的一个原子与相应的晶胞内的一个原子共同组成一个阵点(0,0,0阵点可视作由0,0,0和[*]这一对原子所组成),如图3所示,这样得出的密排六方结构应属简单六方点阵。
[*])解析:3.标出面心立方晶胞中(111)面上各点的坐标,并判断是否位于(111)的线密度。
(分数:10.00)__________________________________________________________________________________________ 正确答案:(为了确定[*]是否位于(111)面上,可运用品带定律:hu+kv+lw=0加以判断,这里1×(-1)+l×1+1×0=0因此[*]位于(111)面上。
固体结构(一) 原子结构与键合原子结构(元素的核外电子分布)原子间的键合☆金属键:掌握金属的电子结构特征,金属键的特征,懂得用上述内容解释金属的特有的性能⊙金属键(Metallic bonding)(一次键)典型金属原子结构:最外层电子数很少,即价电子(valence electron)极易挣脱原子核之束缚而成为自由电子(Free electron),形成电子云(electron cloud)金属中自由电子与金属正离子之间构成键合称为金属键特点:电子共有化,既无饱和性又无方向性,形成低能量密堆结构性质:良好导电、导热性能,延展性好☆离子键:键合特点和离子晶体的特点⊙离子键(Ionic bonding)(一次键)特点:以离子而不是以原子为结合单元,要求正负离子相间排列,且无方向性,无饱和性性质:熔点和硬度均较高,良好电绝缘体(熔融状态可导电)☆共价键:键合特点和共价晶体的特点⊙共价键(covalent bonding)(一次键)亚金属(C、Si、Sn、Ge),聚合物和无机非金属材料实质:由二个或多个电负性差不大的原子间通过共用电子对而成特点:饱和性配位数较小,方向性(s电子除外)性质:熔点高、质硬脆、导电能力差(二) 固体结构☆晶体结构的基本特征:原子(或分子)在三维空间呈周期性重复排列,即存在长程有序懂得下列名词的含义:☆空间点阵:这些阵点在空间呈周期性规则排列并具有完全相同的周围环境,这种由它们在三维空间规则排列的阵列称为空间点阵,简称点阵。
☆阵点:为了便于分析研究晶体中质点的排列规律性,可先将实际晶体结构看成完整无缺的理想晶体并简化,将其中每个质点抽象为规则排列于空间的几何点,称之为阵点。
☆晶胞:具有代表性的基本单元(最小平行六面体)作为点阵的组成单元,称为晶胞。
将晶胞作三维的重复堆砌就构成了空间点阵。
☆简单晶胞:晶胞中的阵点数为一。
☆复合晶胞:晶胞中的阵点数大于一。
晶体结构与空间点阵的关系:1.同一空间点阵可因选取晶胞的方式不同而得出不同的晶胞;2.○1空间点阵是晶体中质点排列的几何学抽象,用以描述和分析晶体结构的周期性和对称性,由于各阵点的周围环境相同,它只能有14中类型;○2晶体结构则是晶体中实际质点(原子、离子或分子)的具体排列情况,它们能组成各种类型的排列,因此,实际存在的晶体结构是无限的。