最新九年级化学溶解度曲线专题
- 格式:doc
- 大小:501.50 KB
- 文档页数:4
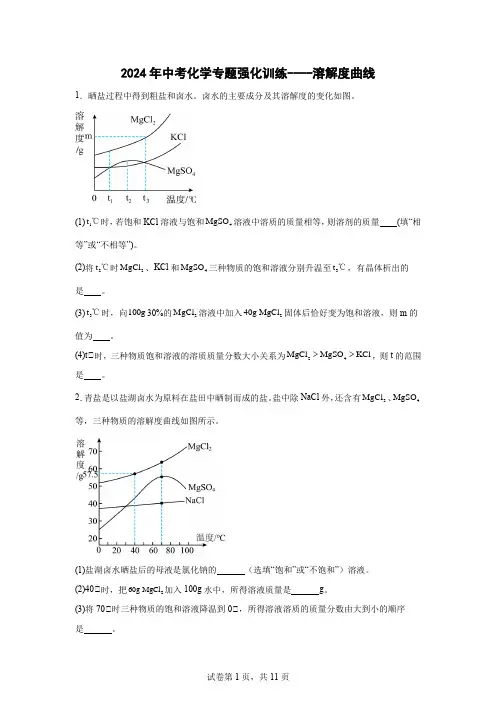
2024年中考化学专题强化训练----溶解度曲线1.晒盐过程中得到粗盐和卤水。
卤水的主要成分及其溶解度的变化如图。
(1)1t ℃时,若饱和KCl 溶液与饱和4MgSO 溶液中溶质的质量相等,则溶剂的质量 (填“相等”或“不相等”)。
(2)将2t ℃时2MgCl 、KCl 和4MgSO 三种物质的饱和溶液分别升温至3t ℃,有晶体析出的是 。
(3)3t ℃时,向100g 30%的2MgCl 溶液中加入240g MgCl 固体后恰好变为饱和溶液,则m 的值为 。
(4)t℃时,三种物质饱和溶液的溶质质量分数大小关系为24MgCl MgSO KCl >>,则t 的范围是 。
2.青盐是以盐湖卤水为原料在盐田中晒制而成的盐。
盐中除NaCl 外,还含有2MgCl 、4MgSO 等,三种物质的溶解度曲线如图所示。
(1)盐湖卤水晒盐后的母液是氯化钠的 (选填“饱和”或“不饱和”)溶液。
(2)40℃时,把260g MgCl 加入100g 水中,所得溶液质量是 g 。
(3)将70℃时三种物质的饱和溶液降温到0℃,所得溶液溶质的质量分数由大到小的顺序是 。
(4)氯化钠中含有少量硫酸镁,若要提纯氯化钠,可采用的方法是。
3.某同学进行了如图1所示实验,结合硝酸钾和氯化钠的溶解度曲线回答下列问题。
(1)20℃时,氯化钠的溶解度是g;(2)若氯化钠中混有少量硝酸钾,可采用的方法提纯氯化钠;(3)图1中烧杯℃为硝酸钾的(填“饱和”或“不饱和”)溶液;若通过升高温度使℃中固体继续溶解,则其溶液中溶质的质量分数(填“增大”“减小”或“不变”)。
4.如图是A、B、C三种固体物质的溶解度曲线,据图作答:(1)P点的意义是。
(2)A、B、C三种物质中,溶解度随着温度上升而减小的物质是。
(3)t2℃时,将30g A物质加入50g水中可形成g溶液。
5.如图是某苏打气泡水的标签。
(1)该气泡水中溶剂的化学式是。
C H O。
从赤藓糖醇的化学式中能获得与其有关的(2)赤藓糖醇是一种甜味剂,其化学式为4104信息是(任写一条)。

初三化学中考专题(5)溶解度曲线练习及答案1.a、b两种物质的溶解度曲线如图所示。
下列说法不正确的是A.将t1℃时b的饱和溶液加水可变为不饱和溶液B.将t2℃时a的饱和溶液降温至t1℃,溶液质量不变C.t2℃时,两种物质的饱和溶液中溶质质量分数a>bD.将t2℃时a、b的饱和溶液分别降温至t1℃,两溶液的溶质质量分数相等2.下图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是A.t2℃时,甲、乙两种物质的溶解度相等B.甲的溶解度随温度的升高而增大C.分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙D.t1℃时,丙的饱和溶液中溶质的质量分数为40%3.下图是甲、乙、丙三种固体物质的溶解度曲线,将甲、乙、丙三种物质t2℃时的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系正确的是A.甲>乙>丙B.甲=乙=丙C.甲=乙>丙D.丙>甲=乙4.(多选)甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是A.t1℃时,甲物质的溶解度为20gB.t1℃时,30g甲加入到50g水中最多可得70g溶液C.t2℃时,乙物质的饱和溶液升温变成不饱和溶液D.t2℃时,甲乙两物质的饱和溶液分别降温到t1℃时,所得溶液溶质质量分数的大小关系是:甲<乙5.(多选)甲、乙两种固体物质的溶解度曲线如图所示。
20℃时,进行了如下图所示的实验,下列叙述正确的是A.甲的溶解度大于乙的溶解度B.实验过程中,属于不饱和溶液的是A溶液和C溶液C.实验过程中,只有B溶液和D溶液属于饱和溶液D.实验过程中,B溶液与E溶液中溶质的质量分数相同6.(多选)甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是A.t2℃时将50g甲物质放入50g水中,充分搅拌后得到100g甲溶液B.t2℃时配制等质量的三种物质的饱和溶液,甲所需要的水最少C.分别将t2℃时三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数的大小关系是乙>甲>丙D.分别将t2℃时三种物质的饱和溶液降温到t1℃,甲溶液中析出的晶体最多丙溶液中无晶体析出7.甲、乙、丙三种物质的溶解度曲线如下图所示。


溶解度曲线专题训练1.如图是甲乙两种物质的溶解度曲线。
下列说法正确的是A.甲的溶解度比乙的溶解度大B.a2℃时,将30g甲放入50g水中充分搅拌可得80g溶液C.a1℃时甲、乙两种物质的饱和溶液溶质的质量分数相同D.将a1℃时甲、乙两种物质的饱和溶液升温至a2℃,溶质的质量分数都增大2.如图是a、b、c三种固体物质的溶解度曲线图,请判断下列说法,其中正确的是()A.使a、c的饱和溶液析出晶体的方法都可以是降温结晶B.t1℃时,a、c两种物质的溶液的溶质质量分数一定相等C.在t2℃时,将a物质30g加入50g水中,充分溶解,所得溶液质量为80gD.t2℃时,a、b、c三种物质的饱和溶液的溶质质量分数由大到小的关系是:a>b>c3.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是A.甲物质的溶解度随温度的升高而增大B.t2℃时,甲、乙两种物质的溶解度相等C.t1℃时,丙的饱和溶液中溶质的质量分数为40%D.当甲中混有少量丙时,可采用降温结晶的方法提纯4.如图是a、b、c三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是()A.a的溶解度大于b的溶解度B.P点表示t1℃时a、c两物质溶解度相等C.将t1℃饱和的c溶液升温到t2℃,得到的是不饱和溶液D.将t2℃,a、b、c三种物质的饱和溶液降温到t1℃时,所得溶液中溶质质最分数由大到小的顺序为:b>a=c5.甲、乙两种固体的溶解度曲线如右图所示,下列说法正确的是A.甲的溶解度大于乙的溶解度B. t1°C时,甲乙饱和溶液中溶质的质量分数相等C. t2°C时,60g 甲的饱和溶液稀释到20%需加水10gD.将t1°C时相等质量的甲、乙的饱和溶液升温到t2°C,溶液中溶质的质量甲大于乙6.A、B、C三种固体物质的溶解度曲线如图所示,下列说法正确的是()A.阴影区域中,A、C均处于不饱和状态B.除去B固体中含有的少量A杂质,可采用配成热饱和溶液,降温结晶、过滤、洗涤、干燥的方法提纯BC.将A和B的饱和溶液从t2℃降到t1℃时,析出晶体的质量关系为A>BD.t1℃时,将50g固体A加入到200g水中,所得溶液溶质的质量分数约为16.7%7.甲、乙两种物质溶解度曲线如图所示。



九年级化学溶解度曲线专题
化学溶解度曲线专题主要涉及以下内容:
1. 溶解度的定义:溶解度是指在一定温度下,单位溶剂中能
溶解的最大溶质量。
溶解度的大小与溶质和溶剂的性质、温度、压力等因素有关。
2. 饱和溶解度曲线:饱和溶解度是指在某一温度下,溶液中
溶质的浓度达到最大值时的溶质质量。
饱和溶解度曲线是指在不同温度下测定饱和溶解度后绘制的曲线,可以用来研究溶解度与温度的关系。
3. 温度对溶解度的影响:一般情况下,溶解度随温度的升高
而增加,即温度越高,溶解度越大。
但也存在一些特殊情况,如饱和溶解度随温度的升高而减小的物质,称为逆温度溶解度曲线。
4. 溶解度曲线的应用:溶解度曲线可以用来预测溶解度值、
判断溶液的饱和度、计算溶解度相关的热力学参数等。
在实际应用中,可以通过溶解度曲线来优化晶体生长、提高药物溶解度、控制溶解速率等。
5. 溶解度曲线的实验方法:常用的测定溶解度的方法包括连
续加热法、连续冷却法、恒温法等。
实验中需要准确测量溶质质量和溶液的浓度,控制温度和压力等条件,以获得可靠的数据。
总之,九年级化学溶解度曲线专题主要包括溶解度的定义、饱和溶解度曲线、温度对溶解度的影响、溶解度曲线的应用以及实验方法等内容。


微专题5 溶解度曲线及溶解度表分析考向一溶解度曲线分析1、解答此类题目的关键(1)明确溶解度曲线上点的含义(某点是在某温度时某物质的溶解度是多少g。
交点是在某温度时,两物质的溶解度相等。
线上方的点表示是饱和溶液,下方的点表示不饱和溶液);(2)明确物质的溶解度随温度变化的趋势(线越陡,表示该物质溶解度受温度影响较大);(3)明确饱和溶液中溶质的质量大小的判断方法;(4)明确判断溶质的质量分数大小关系的方法。
2、溶解度曲线:线的含义:三线:①“陡升型” :大多数固体物的溶解度随温度升高而升高。
如KNO3;②“缓升型”:少数固体物质的溶解度受温度的影响很小。
如NaCl;③“下降型”:极少数物质溶解度随温度升高而降低。
如Ca(OH)2。
3、点的含义:四点:①曲线上的点:所示某温度下某物质的溶解度是多少(该温度下饱和状态)。
②两曲线的交点:表示在该点所示的温度下,两种物质的溶解度相等。
③线上方的点表示:在该温度下,该溶液是饱和且有部分晶体;③线下方的点表示:该温度下,该溶液是不饱和溶液。
1. 【2023四川内江真题】甲、乙两种物质的溶解度曲线如图所示,下列有关说法错误的是()A. 两种物质的溶解度都随温度升高而增大B. t1°C时,甲、乙两物质的溶液中溶质质量分数一定相等C. 通常采用蒸发结晶的方法从乙的溶液中获得晶体D. t2°C时,在100g水中加入25g甲,可形成甲的不饱和溶液【答案】B【解析】A. 由溶解度曲线可知,两种物质的溶解度都随温度升高而增大,此选项正确;B. t1°C时,甲、乙两物质的溶解度相等,则t1°C时,甲、乙两物质的饱和溶液中溶质质量分数一定相等,此选项错误;C. 乙的溶解度受温度影响不大,对于溶解度受温度影响不大的物质,一般采用蒸发结晶法从溶液中获取晶体,此选项正确;D. 由溶解度曲线可知,t2°C时,甲的溶解度大于25g,则在100g水中加入25g甲,可形成甲的不饱和溶液,此选项正确。


微专题09溶解度及溶解度曲线1.(2022·贵州黔西·中考真题)如图为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线。
(1)t 3℃时,甲、乙、丙三物质溶解度由小到大的顺序是_____。
(2)t 2℃时,甲和丙两饱和溶液的溶质质量分数关系是_____。
(3)P 点对应混合物,甲、乙、丙中处于不饱和状态的是_____。
【答案】(1)丙<甲<乙(2)甲=丙(3)乙【解析】(1)如图所示,t 3℃时,甲、乙、丙三物质溶解度点在上的是乙表示乙的溶解度最大,其次是甲,最下面的是丙,表示丙的溶解度最小,因此三者溶解度小到大的顺序是:丙<甲<乙;(2)如图所示,t 2℃时,甲和丙的溶解度曲线交于一点,说明此温度下甲和丙的溶解度相等,则根据t 2℃时,甲和丙两饱和溶液的溶质质量分数可以用公式100%100g⨯+溶解度溶解度:计算,因此t 2℃时,甲和丙两饱和溶液的溶质质量分数关系是:甲=丙;(3)如图所示,P 点对应的甲和丙溶解度点都在P 点以下,说明此时甲和丙都处于饱和状态,而P 点在所对应的乙的溶解度点以下,说明此温度下乙是不饱和状态,故填:乙。
2.(2022·湖北襄阳·统考中考真题)如图为甲、乙、丙三种固体物质的溶解度曲线,据图回答问题。
突破一、溶解度曲线(1)t 1℃时,甲、丙两种物质的溶解度大小关系是甲______丙(填“>”“<”或“=”)。
(2)溶解度随温度的升高而减小的物质是______。
(3)t 2℃时,将甲、乙两种物质的饱和溶液降温至t 1℃,对所得溶液的叙述正确的是(填序号)。
A.甲溶液仍是饱和溶液,乙溶液变为不饱和溶液B.溶液中溶剂的质量甲<乙C.溶液中溶质的质量分数甲<乙【答案】(1)=(2)丙(3)C【解析】(1)由溶解度曲线可知,1t ℃时甲、丙两条曲线相交于一点,即1t ℃时,甲、丙两种物质的溶解度大小关系是甲=丙。
人教新版九年级化学溶解度曲线专题
一.有关溶解度曲线的常见试题(见右下图) 1.t 3℃时A 的溶解度为 。
2.P 点的的含义是: 。
3.t 1℃时A 、B 、C 、溶解度由大到小的顺序 。
4.除去A 中的泥沙用 法;分离A 与少量B 的混合物,用 法。
5.从A 溶液中获取A 晶体可用 降温结晶 的方法获取晶体。
6.从B 的溶液中获取晶体,适宜采用 蒸发结晶 的方法获取晶体。
7.N 点为t 3℃时A 的 溶液,可通过 加入A 物质,降温,蒸发溶剂 的方法使
它变为饱和溶液。
8.t 2℃ 时A 、B 、C 的饱和溶液各W 克,降温到t 1℃会析出大量晶体的是 ,无晶体析出的是 ,所得溶液中溶质的质量分数由小到大依次为 。
9. 曲线以上的点代表示对应温度的饱和溶液,曲线以下的点代表对应温度的不饱和溶液。
加溶质相当于把点向正上方移动,加溶剂相当于向下竖直移动,降温相当于向左水平移动,升温相当于向右水平移动。
二.填空题
1、(2010年·武汉市·元调)右图为氯化铵和硫酸钠的溶解度曲线。
请回答:
(1)40℃时硫酸钠的溶解度比氯化铵的溶解度 (填“大”或“小”)。
(2)要把60℃氯化铵饱和溶液转化为不饱和溶液,可以采取的办
法 (只写一种即可)。
(3)25℃时,将硫酸钠和氯化铵各35 g 分别放入100 g 水中,形成的溶液其溶
质质量分数较大的物质是 。
(4)除去硫酸钠中少量氯化铵时,比较高效的物理方法是 。
2、(2010年·武汉市·四调)(3分)A 、B 两种固体物质的溶解度曲线如右图所
示。
据图回答下列问题:
⑴ 图中A 、B 两物质的溶解度相等时,对应的温度是____ _℃。
⑵ t 3℃时,将50 g A 物质溶于50 g 水中,得到的溶液是 _________(填“饱
和”或“不饱和”)溶液。
⑶ 将t 2℃时A 物质的饱和溶液降低温度至t 1℃时,其溶质质量分数会
(填“变大”、“变小”或“不变”)。
3. (2010年·武汉市·四调)(3分)下图是A 、B 两种物质的溶解度曲线。
根据图示回答下列问题。
(1) t 1℃时,向两只盛有100 g 水的烧杯中,分别加入A.、B 两种物质至不
能溶解为止,所得溶液的溶质质量分数较大的是___________溶液(填“A ”或
“B ”)。
(2) 若不考虑水分的蒸发,将t 2℃的A 物质的饱和溶液升温至t 3℃,溶液中
溶质的质量分数将___ __。
(填“变大”、“变小” 或“不变”)
· ·
0 t
t t 3 N s /g P A
B C
(3) 将t2℃的A.、B两种物质的饱和溶液各200g,升温至t3℃。
若不改变溶剂质量,欲使它们仍为饱和溶液,所需加入固体溶质的质量关系是A_______B。
(填“>”、“<”或“=”)
4、(2011年·武汉市·四调)(4分)40℃时,取等质量的a、b、c三种物质的饱和溶液于三个烧杯中,再分别蒸发等质量的水,将温度降到30℃,固体溶解情况如图1所示。
图2为a、b、c三种物质的溶解度曲线。
状态1
蒸发等质量的水,降温至30℃
状态2
仔细读图1和图2,回答下列问题。
(1)三种物质溶解度的关系:若b>a>c时的温度为t,则t的取值范围是:。
(2)烧杯甲里是物质的溶液(选填a、b、c,下同),烧杯乙里是物质的溶液。
(3)40℃时,烧杯_______里溶液中水的质量最少(选填甲、乙、丙)。
5、(2012年·武汉市·五调)(4分)某化学兴趣小组的同学在20℃时进行了如下图3l—l所示实验。
已知,图3l一2是KNO3的溶解度曲线。
(1)50℃时,l00 g水最多可溶解硝酸钾的质量为 g。
(2)充分搅拌后,可观察到:A中无剩余固体,B中。
(3)A—E的溶液中,属于不饱和溶液的是 (填字母,下同)。
A—E的溶液中,溶质质量分数相等的是。
6、(2012年·武汉市·五调)(5分) 70 ℃时,将100 g溶质的质量分数为
20%的R溶液不断降温,析出固体R的质量与温度的变化关系如右图所示。
根据图像回答下列问题:
(1) R 的溶解度随温度的升高而______________(填“增大”、“不变”或“减小”);
(2)从70 ℃降到50 ℃的过程中,该溶液中溶质的质量 分数_________(填“变大”、“变小”或“不变”); (3)要配制50℃时50 g R 的饱和溶液,需要R 的质量是 ________ g , 需要的玻璃仪器有____ _____ 。
7. (2013年·武汉市·四调)(4分)右图是甲、乙两种固体物质的溶解度曲
线。
(1)t 1℃时甲、乙两种物质的溶解度大小关系为:甲 乙(填“>”、
“<”或“=”。
下同)
(2)将t 3℃等质量的甲、乙两种物质的饱和溶液降温到t 2℃时,所得溶液
质量的大小关系为:甲 乙。
(3)欲从甲溶液中得到甲的固体,可采取的办法是 。
(4)用t 3℃时甲的饱和溶液配制5%的甲溶液,需要用到的仪器
是 。
【走进中考】
1、(2010年·武汉市·中考)(3分)有些金属的氢氧化物有相似的化学性质,但物理性质却有所不同,如 Ca(OH)
2、 Ba(OH)2的溶解度就存在一定的差异,如下表所示:
温度/℃
0 40 80 溶解度/g Ca(OH)2
0.187
0.141 0.094 Ba(OH)2
1.67 8.22 101.4 根据以上信息回答下列问题:
(1)右图中,表示Ca(OH)2溶解度曲线的是 (填“A ”或“B ”)。
(2)如果要将 Ca(OH)2的不饱和溶液转变为饱和溶液,可采取的
方法是 (只举一种)。
(3)现有常温..
时,含有Ca(OH)2、 Ba(OH)2两种溶质的某饱和
溶液,若要得到较纯净的Ba(OH)2溶液,所采取的简单方法
为 。
2、(2011年·武汉市·中考)(4分)烧杯中盛有一定质量、温度为80 ℃、溶质为M 的溶液,将其置于室温环境中,测定不同温度时析出固体M 的质量。
测定结果记录如下表。
溶液的温度/℃
75 65 50 35 20 析出固体M 的质量/g 0 0 2.0 4.5 8.4
若不考虑水蒸发对实验的影响,请回答下列问题。
(1)65℃时,该溶液是否为饱和溶液?______(填“是”、“否”或“无法判断”);
A
溶解度/g 温度/℃
0 B
(2)将40℃时接近饱和的M溶液变成饱和溶液,下列方法中一定能达到目的的有_ (填序号)。
①升温②降温③加溶质M ④加水
⑤加另一种固体N ⑥恒温蒸发水⑦与40℃时M的饱和溶液混合
(3)20℃时,用固体粉末M和水配制100g溶质质量分数为5%的M溶液,必须用到的仪器有:托盘天平(带砝码盒)、烧杯、__ ____。
3、(2012年·武汉市·中考)(4分)右图是甲、乙两种固体物质的溶解度曲线。
⑴℃时,甲、乙两种物质的溶解度相等。
⑵t2℃时,将等质量的甲、乙两种物质加水溶解配制成饱
和溶液,所得溶液质量的大小关系为:甲乙(填“>”、
“<”或“=”)。
⑶把甲物质的不饱和溶液变为饱和溶液,下列有关说法正
确的是(填序号,下同)。
A.溶剂的质量一定变小
B.溶质的质量可能不变
C.溶质的质量分数一定变大
D.溶液的质量一定变大
E.该饱和溶液还可以溶解其它物质
⑷通常情况下,在实验室配制一定溶质质量分数的甲溶液,需用到的仪器有:托盘天平(带砝码盒)、烧杯和。
A.酒精灯
B. 药匙
C.玻璃棒
D.漏斗
E.铁架台
F.量筒
G.胶头滴管。