钙离子测定
- 格式:docx
- 大小:13.13 KB
- 文档页数:2

钙离子测定的参考方法
嘿,朋友们!今天咱来聊聊钙离子测定的参考方法。
你说这钙离子啊,就像我们生活中的小助手,虽然看不见摸不着,但却在很多地方起着至关重要的作用呢!想象一下,如果身体里的钙离子不平衡了,那可就像一台机器的零件出了问题,运转起来可不顺畅啦!
那怎么才能准确测定钙离子呢?这可就有讲究啦!就好像要抓住一只调皮的小猴子,得用对方法才行。
比如说原子吸收分光光度法,这就像是一个精准的瞄准镜,能一下子锁定钙离子的位置,然后准确地告诉我们它的含量。
这方法可靠得很呢!
还有络合滴定法,这就像是一场和钙离子的巧妙游戏。
通过加入合适的试剂,和钙离子来一场你追我赶的“互动”,最终确定它的量。
离子选择电极法呢,就像是一个敏感的小侦探,能敏锐地察觉到钙离子的存在并报告出来。
每种方法都有它的特点和优势呀!就像我们每个人都有自己的长处一样。
咱可不能小瞧了这些方法,它们可是为了我们的健康保驾护航呢!
那在实际操作中,可得仔细着点儿。
就跟做饭一样,调料放多了放少了都不行。
要严格按照步骤来,不能马虎。
不然测出来的结果不准确,那可就麻烦啦!
你说,要是没有这些准确的测定方法,我们怎么能知道身体里的钙离子情况呢?那不是两眼一抹黑嘛!所以啊,这些方法就像是我们的指明灯,让我们能清楚地了解身体的状况。
总之啊,钙离子测定的参考方法可重要啦!大家一定要重视起来呀!可别不当回事儿哦!。

钙离子测定标准全文共四篇示例,供读者参考第一篇示例:钙离子测定是生物化学实验中常见的一种实验方法,用于检测样品中的钙离子浓度。
钙离子在生物体内起着至关重要的作用,如参与神经传递、细胞信号传导、肌肉收缩等生理过程。
测定钙离子浓度对于研究生物体内相关生理过程具有重要意义。
在实验室中,通常采用螯合剂法、光度法、电化学法和原子吸收光谱法等方法进行钙离子测定。
最常用的方法之一是EDTA螯合剂法。
这种方法基于EDTA(乙二胺四乙酸)和钙离子之间的络合反应,通过滴定的方式确定钙离子的浓度。
钙离子测定实验通常需要一系列标准品来建立标准曲线。
标准品是已知浓度的钙离子溶液,通常包括不同浓度的钙标准溶液。
通过对标准品进行一系列测定,得到钙离子的吸光度与浓度之间的关系,建立标准曲线。
在测定未知样品时,根据其吸光度值在标准曲线上确定对应的钙离子浓度。
建立标准曲线的过程需要严格控制实验条件,包括使用相同的仪器参数、操作步骤和试剂质量等。
在测定过程中还需要注意避免干扰物质的干扰,例如金属离子、有机物等可能影响测定结果的物质。
除了实验室方法,钙离子浓度还可以通过生物传感器技术进行在线监测。
生物传感器是一种将生物分子与传感器技术相结合的设备,可以实时监测生物体内的代谢产物、离子浓度等重要参数。
钙离子生物传感器通常采用螯合剂或荧光探针来实现钙离子的快速检测。
在实际应用中,钙离子测定可以用于食品检测、环境监测、生物医学研究等领域。
钙含量是衡量食品营养价值的重要指标之一,通过测定食品中的钙离子浓度可以评估其营养成分。
在环境监测中,钙离子的浓度可以反映水体中的硬度,对于评估水质、石灰沉淀处理等具有重要意义。
钙离子测定是一种重要的生物化学分析方法,通过建立标准曲线,控制实验条件,应用适当的检测技术,可以准确快速地测定样品中的钙离子浓度。
在未来,随着生物传感技术的发展和应用,钙离子测定方法将得到进一步完善和推广,为生命科学研究和相关应用领域带来更多的便利和新的突破。

循环水钙离子的测定国标循环水中钙离子的测定是一项非常重要的分析工作,它对于水质评价及工业生产具有指导意义。
根据相关国标,我们可以通过以下方法来准确测定循环水中的钙离子浓度。
首先,我们可以采用滴定法来测定循环水中钙离子的浓度。
此方法基于硬度滴定分析原理,通过溶液中的指示剂变色来确定钙离子的浓度。
在进行滴定实验之前,我们需要准备好标准溶液、试剂以及滴定仪器等。
首先,我们将循环水样品与适量的指示剂溶液混合,并加入酸性试液进行反应。
然后,我们将标准溶液逐滴加入滴定瓶中,同时不断搅拌,直到指示剂变色为止。
通过记录所需的标准溶液体积,我们可以计算出循环水中钙离子的浓度。
除了滴定法,还可以采用化学分析法来测定循环水中钙离子的浓度。
在这种方法中,我们可以利用络合滴定的原理来分析样品中的钙离子含量。
简单来说,络合滴定是通过加入络合剂与钙离子发生络合反应,然后采用指示剂检测络合反应的终点。
与滴定法相比,络合滴定法可以提供更准确和可靠的结果。
此外,还有离子选择电极(ISE)法可以用于测定循环水中的钙离子浓度。
这种方法基于测量溶液中的电位变化来确定钙离子的含量。
通过校准ISE电极并将其浸入循环水样品中,可以直接读取钙离子浓度。
尽管离子选择电极法需要准确的仪器和操作技术,但它具有操作简单、结果直观等优点。
除了上述方法,近年来还有一些基于光学、分子生物学和电化学原理的新型测定方式出现。
这些方法有的在速度、灵敏度和准确性方面都有不错表现,但仍处于实验室验证阶段。
值得注意的是,无论选择哪种方法进行钙离子测定,我们都必须严格按照国标的要求进行操作,确保结果的准确性和可靠性。
同时,我们还应当定期校准仪器、验证方法的准确性,并进行质量控制。
只有这样,我们才能获得可靠的结果,并根据结果进行相应的控制措施。
综上所述,循环水中钙离子的测定是一项重要且复杂的工作。
通过滴定法、化学分析法和离子选择电极法等多种方法,我们能够准确测定循环水中钙离子的含量。
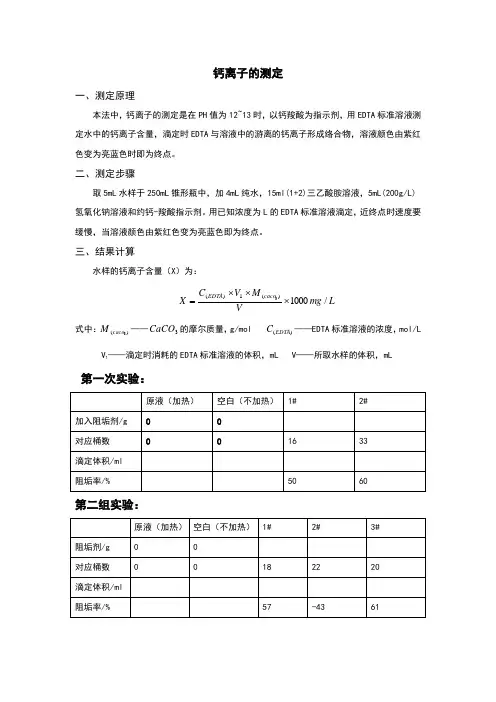
钙离子的测定
一、测定原理
本法中,钙离子的测定是在PH 值为12~13时,以钙羧酸为指示剂,用EDTA 标准溶液测定水中的钙离子含量,滴定时EDTA 与溶液中的游离的钙离子形成络合物,溶液颜色由紫红色变为亮蓝色时即为终点。
二、测定步骤
取5mL 水样于250mL 锥形瓶中,加4mL 纯水,15ml(1+2)三乙酸胺溶液,5mL(200g/L)氢氧化钠溶液和约钙-羧酸指示剂。
用已知浓度为L 的EDTA 标准溶液滴定,近终点时速度要缓慢,当溶液颜色由紫红色变为亮蓝色即为终点。
三、结果计算
水样的钙离子含量(X )为:
L mg V
M V C X caco EDTA /1000)
(1)(3⨯⨯⨯=
式中:)(3caco M ——3CaCO 的摩尔质量,g/mol )(EDTA C ——EDTA 标准溶液的浓度,mol/L
V 1——滴定时消耗的EDTA 标准溶液的体积,mL V ——所取水样的体积,mL
第一次实验:
第二组实验:。

钙离子测定的几种方法1. 火焰原子吸收光谱法(FAAS)原理:FAAS方法利用钙离子在火焰中产生特定的吸收峰,通过测量钙离子吸收光线的强度来确定其浓度。
优点:- 灵敏度高,能够测定低至微克级别的钙离子浓度。
- 分析速度快,适用于大批量样品分析。
- 使用简单,设备成本相对较低。
缺点:- 仪器对样品的干扰较为敏感,需要进行前处理或矫正。
- 不能同时测定多种金属离子,可能需要分离步骤。
2. 离子选择电极法(ISE)原理:ISE方法是通过使用特定的离子选择电极来测定钙离子浓度,电极的响应与钙离子浓度呈现一定的关系。
优点:- 高选择性,可测定特定离子的浓度。
- 测定范围广,可适用于不同浓度水平的样品。
- 快速测定结果,无需显著的前处理步骤。
缺点:- 仪器价格较高。
- 电极使用寿命有限,需要定期更换。
- 在某些样品中可能受到干扰,需要进行矫正。
3. 比色法原理:比色法测定钙离子浓度是通过与钙离子反应生成有色产物,进而通过测量产物的吸光度或颜色来确定钙离子浓度。
优点:- 使用方便,操作简单。
- 适用于多种样品,如水、食品等。
- 可以进行快速测定,结果准确。
缺点:- 比色法对于样品颜色的影响较大,颜色较深的样品可能需要进行稀释或前处理。
- 针对不同样品需要选择适当的试剂,有可能导致分析复杂化。
总结以上是钙离子测定的几种常用方法,每种方法都有其优缺点。
在选择合适的方法时,需要考虑样品特性、所需测定范围和分析准确性等因素。
根据具体需求,可选择适合的方法进行钙离子浓度的测定。
参考文献:1. Smith, J. et al. (2015). Determination of calcium ion concentration by flame atomic absorption spectrometry. Analytical Methods, 7(21), 9140-9146.2. Wang, L. et al. (2018). Electrochemical ion selective electrodes for calcium ion detection. Journal of Materials Chemistry C, 6(18), 4816-4826.3. Zhang, H. et al. (2012). Spectrophotometric determination of calcium ion concentration in water samples. Chinese Journal of Analytical Chemistry, 40(12), 1804-1807.4. Li, L. et al. (2019). Colorimetric determination of calcium ion concentration in food samples. Food Analytical Methods, 12(1), 184-191.。

钙离子的测定方法钙离子是一种重要的生物无机离子,对生物体的正常生长和生理功能起着至关重要的作用。
因此,准确测定钙离子浓度具有很高的研究和应用价值。
本文将详细介绍几种常用的钙离子测定方法。
一、EDTA滴定法EDTA(乙二胺四乙酸)滴定法是一种常用的钙离子测定方法。
该方法基于Ca2+与EDTA之间的络合反应。
当EDTA与钙离子形成络合物时,溶液的颜色会发生明显变化,从而可以根据颜色的变化确定钙离子的浓度。
实验中,首先取少量样品溶液,加入酸化物(通常为硝酸)去除样品中的其他干扰物质,然后加入指示剂,如酚酞指示剂。
酚酞指示剂会在有机溶剂中溶解,形成红色络合物。
然后用已知浓度的EDTA溶液作为滴定剂,滴定样品溶液。
当EDTA的配位量与钙离子的摩尔数相等时,酚酞指示剂的颜色会由红色转变为无色。
通过记录滴定剂的体积变化,就可以计算出样品中钙离子的浓度。
EDTA滴定法优点是准确度高、操作简单。
但是,该方法在测定钙离子时对样品的处理要求较高,且滴定过程较长,不适用于快速分析。
二、分光光度法分光光度法是测定钙离子浓度的一种常用方法。
该方法基于物质对特定波长的光的吸收特性。
实验中,首先制备一系列浓度不同的钙离子标准溶液。
然后,用紫外-可见分光光度计测定这些标准溶液在特定波长处的吸光度。
利用所测得的吸光度-浓度曲线,可以通过测定待测样品的吸光度得到其钙离子的浓度。
分光光度法的优点是快速、准确,适用于大批量分析。
但是,该方法对仪器的要求较高,且容易受到其他物质干扰。
三、电化学法电化学法是测定钙离子浓度的一种常用方法。
该方法基于钙离子与电极的反应,通过电极上的电流变化来确定钙离子的浓度。
常用的电化学方法包括离子选择电极和离子选择电极结合电位滴定法。
离子选择电极是一种特殊的电极,它对特定离子具有高度选择性。
在钙离子测定中,常用的是钙离子选择电极。
该电极能够快速而准确地测定钙离子浓度。
离子选择电极结合电位滴定法是一种将滴定法和电化学法结合起来的测定方法。

钙离子测定标准
钙离子测定的标准主要依赖于其在正常生理条件下的浓度范围。
对于成人,血清钙离子的正常范围通常为2.08~2.75mmol/L,也有观点认为是2.25~2.75mmol/L。
游离钙的正常值则为0.94~1.26mmol/L。
对于不同年龄段的人群,钙离子正常值也有所不同。
新生儿血钙的正常值为1.08-1.18mmol/L,成人的血钙值通常会比新生儿高一些,为1.12-1.23mmol/L。
而大于60岁的人群,钙离子值通常在1.13-1.30mmol/L之间。
请注意,这些数值只是参考范围,实际的钙离子浓度可能会因个体差异、疾病状态、饮食和其他因素而有所变化。
因此,在进行钙离子测定时,应根据具体的临床情况和实验室方法进行解读。
如果钙离子浓度超出正常范围,可能需要进一步的医学评估和治疗。

钙离子测定方法范文钙离子是生物体内重要的无机离子之一,对维持骨骼健康、神经传导、肌肉收缩等过程起着重要作用。
因此,准确测定钙离子的浓度对于医学、生化、食品科学等领域具有重要意义。
本文将介绍几种常用的钙离子测定方法。
一、钙离子的化学分析方法1.复合指示剂滴定法复合指示剂滴定法是一种常用的分析方法,通过指示剂与钙离子形成可见的指示色变来实现测定。
常用的指示剂有钙黄素(EBT)、钙蓝(BPC)和尔琼钙(CPB)等。
例如,钙黄素是一种特定颜色变化的指示剂,它在酸性溶液中是黄色的,与钙离子形成络合物后变为蓝紫色。
研究者可以将待测样品加入酸性溶液中,然后逐滴加入含有钙黄素的滴定剂,当出现颜色变化时,记录所加入的滴定剂体积,从而计算钙离子的浓度。
2.EDTA滴定法EDTA(乙二胺四乙酸)是一种具有强络合能力的螯合剂,可以与钙离子形成稳定的络合物。
这种方法适合于钙、镁等阳离子的测定。
EDTA滴定法的步骤如下:a.将样品溶液和指示剂(如甲基橙)混合,在pH较高的条件下调节至碱性;b.逐滴加入含有EDTA的滴定剂,反应至滴定终点出现颜色变化;c.计算钙离子的浓度。
3.钙离子选择性电极法钙离子选择性电极是一种常用的测定方法,根据溶液中钙离子浓度与电势之间的关系进行测定。
钙离子选择性电极由一个具有高选择性的离子敏感膜、参比电极和测量电位计组成。
操作步骤如下:a.在样品中加入一定量的标准钙溶液,使其浓度范围适合测定;b.将离子选择性电极置于样品中,与参比电极连接,并测量电位;c.根据标准曲线或测量电位与钙离子浓度的经验关系计算钙离子浓度。
二、钙离子的光谱分析方法1.原子吸收光谱法原子吸收光谱法是一种常用的分析方法,可用于钙离子的测定。
该方法基于样品中钙原子对特定波长的吸收将光能量转化为电能量。
操作步骤如下:a.将样品溶液吸入原子吸收光谱仪中的气体炉,使其转化为气态的原子态钙;b.通过样品吸收特定波长的紫外或可见光,测量样品吸收光强度;c.根据标准曲线或校准曲线计算样品中钙离子的浓度。

测钙的方法有哪些测钙的方法有很多种,适用于不同样品类型和测量目的。
以下是一些常用的测钙方法:1. 酸碱滴定法:这是一种常见的测定水溶液中钙离子含量的方法。
通过加入一种酸性或碱性指示剂,并逐渐滴加浓度已知的酸或碱溶液,从而确定溶液中钙离子的浓度。
这种方法简便易行,广泛用于水质监测、食品分析等领域。
2. EDTA滴定法:EDTA(乙二胺四乙酸)是一种螯合剂,可以与钙离子形成稳定的络合物。
通过向待测溶液中滴加已知浓度的EDTA溶液,然后加入金属指示剂(如Eriochrome Black T),通过颜色变化来判断钙离子的浓度。
此方法准确可靠,广泛应用于生物、环境和地质样品的钙离子测定。
3. 光度法:光度法是利用光的吸收、透射或散射来测量溶液中物质浓度的方法。
通过测量样品吸收或散射光的强度,可以计算出其中钙离子的浓度。
光度法具有高精度和灵敏度,广泛用于医药、食品、环境和地质等领域。
4. 原子吸收光谱法:原子吸收光谱法(AAS)基于样品在被加热到高温后,产生的原子吸收和发射光谱特征。
通过将样品中的钙离子转化为原子状态,然后测量其吸收光谱强度,可以确定钙离子的浓度。
这种方法具有高精度、高灵敏度和高特异性,并广泛应用于临床医学、药物研发和环境监测等领域。
5. X射线荧光光谱法:X射线荧光光谱法(XRF)是一种非破坏性的分析方法,利用样品在受到X射线激发后产生的特征X射线荧光来确定元素的含量。
通过使用钙的标准样品进行校准,可以测量未知样品中钙的含量。
这种方法适用于分析固体、液体和气体样品中的钙含量。
6. 原子发射光谱法:原子发射光谱法(AES)是一种利用样品原子在高温燃烧或电弧放电中产生的特定发光谱线来分析元素含量的方法。
通过测量钙原子放射的特征光谱线强度,可以确定钙的含量。
该方法具有较高的准确度和灵敏度,并广泛应用于冶金、地质和环境领域。
7. 荧光法:荧光法是一种基于物质在受激后发射特定光谱的方法。
通过加入荧光试剂(如华氏试剂),使钙与荧光试剂形成络合物,然后测量荧光试剂在特定激发波长下发射的荧光强度来测定钙的含量。

化验室EDTA滴定法测定水质钙镁离子操作规程一、引用标准GB/T15452-2009工业循环冷却水中钙、镁离子的测定EDTA滴定法二、方法提要钙离子测定是在pH为12~13时,以钙—羧酸为指示剂,用EDTA标准滴定溶液测定水样中的钙离子含量。
滴定时EDTA与溶液中游离的钙离子仅应形成络合物,溶液颜色变化由紫红色变为亮蓝色时即为终点。
镁离子测定是在pH为10时,以铬黑T为指示剂,用EDTA标准滴定溶液测定钙、镁离子含量,溶液颜色由紫红色变为纯蓝色即为终点,由钙镁含量减去钙离子含量即为镁离子含量。
三、试剂和材料1、硫酸溶液:1+1。
2、过硫酸钾溶液:40g/L,存储于棕色瓶中(有效期1个月)。
3、三乙醇胺溶液:1+2。
4、氢氧化钾溶液:200g/L。
5、氨-氯化铵缓冲溶液(甲):pH=10;54gNH4Cl与350mL浓氨水,加少量水溶解,待温度在室温时,定容至1L棕色容量瓶中,上下颠倒混合均匀。
6、乙二胺四乙酸二钠标准溶液:c(EDTA)约0.01moL/L。
7、钙—羟酸指示剂:0.2g钙–羧酸指示剂[2-羟基-1-(2-羟基-4-磺基-1-萘偶氮)-3-萘甲酸]与100g氯化钾混合研磨均匀,存储于磨口瓶中。
8、铬黑T指示剂液:溶解0.50g铬黑T﹝1-(1-羟基-2-萘偶氨-6-硝基-萘酚-4-磺酸钠)﹞于85mL三乙醇胺中,再加入15mL乙醇。
四、分析步骤1、钙离子的测定用移液管移取50mL过滤后的水样于250mL锥形瓶中,加入1mL硫酸溶液和5mL过硫酸钾溶液,加热煮沸至近干,取下冷却至室温向其中加入50mL 水、3mL三乙醇胺溶液、7mL氢氧化钾溶液和约0.2g钙—羧酸指示剂,用EDTA标准滴定液滴定,近终点时速度要缓慢,当溶液颜色由紫红色变为亮蓝色时即为终点。
2、镁离子的测定用移液管移取50mL过滤后的水样于250mL锥形瓶中,加入1mL硫酸溶液和5mL过硫酸钾溶液,加热煮沸至近干,取下冷却至室温加50mL水、3mL 三乙醇胺溶液。

钙离子测定1、目的:通过检测将水中钙离子状况真实反应出来。
2、范围:适用于水的钙离子的检测。
3、工作程序:3.1方法提要:在碱性溶液中(pH=12)钙离子与钙试剂生成红色的铬和物,其不稳定常数大于钙与已胺四已酸二钠络和物的不稳定常数,在此溶液中加入已二胺四已酸二钠溶液,就会将络和的钙试剂取代出来,滴定到终点时,呈现出游离指示剂的纯兰色。
水样碱度比较大时,须加入盐酸,经煮沸后再进行测定,否则因加入氢氧化钠溶液而生成碳酸钙的沉淀,使结果边偏低。
3.2试剂:3.2.1刚果红试纸3.2.2盐酸(1+1)3.2.3氢氧化钠溶液(2mol/l)3.2.4钙试剂:加入25g氯化钾,在研苯中充分研磨成细粉末后,储存密封的暗色瓶子里。
3.2.5已二胺四已酸二钠标准溶液:0.01mol/l3.3分析步骤:3.3.1取水样100ml,注入150ml三角瓶中。
放入刚果红试纸一小块,加入盐酸溶液酸化,直到试纸变为蓝紫色。
3.3.2将溶液煮沸2~3分钟,冷却后,加2ml氢氧化钠溶液。
3.3.3加入钙试剂20~40mg,以EDTA—2NA标准溶液滴定至红色变至顿兰色为止,同时做空白试验,计下用量。
(溶液保存以测定镁离子)3.4计算:ρ(Ca)=(V1—V2)*C*40.08*1000/Vρ(Ca):水样中钙的质量浓度,mg/1V1:滴定中消耗的EDTA-2NA溶液体积mlV2:空白消耗的EDTA-2NA溶液体积mlC:EDTA-2NA标准溶液浓度,(0.01mol/1)40.08:与1.00mlEDTA-2NA标准溶液相当的以克表示钙的质量V:所取水样的体积,ml。
钙离子的测定
一、 测定原理
本法中,钙离子的测定是在PH 值为12~13时,以钙羧酸为指示剂,用EDTA 标准溶液测定水中的钙离子含量,滴定时EDTA 与溶液中的游离的钙离子形成络合物,溶液颜色由紫红色变为亮蓝色时即为终点。
二、测定步骤
取5mL 水样于250mL 锥形瓶中,加4mL 纯水,15ml(1+2)三乙酸胺溶液,5mL(200g/L)氢氧化钠溶液和约钙-羧酸指示剂。
用已知浓度为L 的EDTA 标准溶液滴定,近终点时速度要缓慢,当溶液颜色由紫红色变为亮蓝色即为终点。
三、结果计算
水样的钙离子含量(X )为:
L
mg V
M V C X caco EDTA /1000)
(1)(3⨯⨯⨯=
式中:)
(3caco M
——3
CaCO 的摩尔质量,g/mol
)
(EDTA C ——EDTA 标准溶液的浓度,mol/L V 1——滴定时消耗的EDTA 标准溶
液的体积,mL V ——所取水样的体积,
mL
第一次实验:
第二组实验:。
注射用重组人凝血因子Ⅷ-Fc融合蛋白辅料含量钙离子检测SOP1、实验原理:钙与邻-甲酚酞络合铜混合,在pH11.0±1.0缓冲溶液中形成紫色络合物,在570nm波长出现最大峰,用8-羟基喹啉消除镁离子的干扰。
2、试剂与试液:邻-甲酚酞络合铜溶液、钙标准溶液、8-羟基喹啉溶液、乙醇胺-硼酸盐缓冲液。
3、仪器与材料:实验仪器:紫外可见分光光度计。
材料:(1)储备乙醇胺-硼酸盐缓冲液:向盛有50ml水的500ml烧杯中加入18科硼酸并搅拌,加入50ml乙醇胺,搅拌,待硼酸溶解后,将溶液移入容量瓶中,并用乙醇胺定容至500ml。
临用时用蒸馏水做1:20倍稀释。
(2)邻-甲酚酞络合铜溶液:向25ml水中加入80mg邻-甲酚酞络合铜和0.5ml 1M的氢氧化钾溶液,搅拌至溶解后加入75ml的水和0.5ml的冰醋酸。
(3)储备8-羟基喹啉溶液:在100ml 95%酒精中溶解5g 8-羟基喹啉,作储备用液。
(4)工作显色液:乙醇胺-硼酸盐缓冲液50μl+950μl纯化水(1:20倍稀释),然后抽取500μl,再加500μl邻-甲酚酞络合铜再加250μl8-羟基喹啉溶液,定容至25ml。
(5)钙标准使用液:用西亚Ca标准溶液(浓度为1000μg/ml),稀释成0.025mmol/L、0.05mmol/L、0.1mmol/L、0.2mmol/L、0.25mmol/L做标曲(分别加10μl、20μl、40μl、80μl、100μl标准品定容至10ml.)。
4、操作方法:4.1样品预处理:将供试品溶解后,50倍稀释(10μl供试品溶液+490μl纯化水)。
4.2工作曲线制备及样品测定:(1)工作曲线制备:分别取系列浓度(mmol/L)钙标准使用液200μl 于试管中,向各管内加1ml工作显色液,混合后用紫外分光光度计于570nm 处读取吸光度,绘制工作曲线。
相关系数应不低于0.99。
(2)样品测定:将4.1中处理后的待测样品代替标准液,按上述方法测定,并将测定后的吸光度代入工作曲线的直线回归方程,求得钙离子的浓度(mmol/ L) ,得出的钙离子浓度乘以稀释倍数50即为供试品中的钙离子含量。
钙离子的测定——EDTA络合滴定法本方法适用于各种工业用水、原水中钙离子的测定。
1方法提要钙离子测定是在pH12~13时,以钙-羧酸为指示剂,用EDTA标准滴定溶液测定水样中钙离子含量,滴定时EDTA与溶液中游离的钙离子反应形成络合物,溶液颜色由红色变为亮蓝色时即为终点;2试剂与材料硫酸:1+1溶液过硫酸钾溶液:40g/L贮存于棕色瓶中(有效期1个月)三乙醇胺:1+2水溶液氢氧化钾溶液:200mg/L钙-羧酸指示剂:0.2g钙-羧酸指示剂[2-羟基-1-(2-羟基-4-磺基-1-萘偶氮)-3-萘甲酸]与100g氯化钾混合研磨均匀,贮存于磨口瓶中。
乙二胺四乙酸二钠(EDTA)标准滴定溶液:0.01mol/L铵-氯化铵缓冲溶液:pH=10铬黑T指示液:溶液0.05g铬黑T即[1-(1-羟基-2-萘偶氮-5-硝基-萘酚-4-磺酸钠)]于85mL三乙醇胺,再加入15mL乙醇。
3分析步骤用移液管吸取50mL水样于250mL锥形瓶中,加1mL(1+1)硫酸溶液和5mL过硫酸钾溶液,加热煮沸至近干,取下冷却至室温,加50mL水和3mL三乙醇胺溶液、7mL氢氧化钾溶液和0.2g钙-羧酸指示剂,用EDTA标准溶液滴定,近终点时速度要缓慢,当溶液颜色变为亮蓝色时即为终点。
4分析结果表述以mg/L表示的水样中钙离子含量ρ=(c×v1×0.04008)/v×106式中v1——滴定钙离子时消耗EDTA标准滴定溶液的体积,mLC——EDTA标准滴定溶液的浓度,mol/LV——所取水样体积,mL0.04008——与1000mLEDTA标准滴定溶液[c(EDTA)=1.000mol/L]相当的以克表示的钙的质量。
钙离子计操作规程
《钙离子计操作规程》
一、实验目的
本实验旨在通过钙离子计测定样品中的钙离子浓度,以便分析样品中钙的含量。
二、实验仪器和试剂
1. 钙离子计仪器
2. 校准溶液:含知秋测定的标准钙离子浓度的溶液
3. 样品:待测定的含钙样品溶液
三、实验步骤
1. 准备工作:打开钙离子计仪器,接通电源,等待仪器稳定。
2. 校准:将校准溶液注入钙离子计仪器,根据仪器提示进行校准操作。
3. 测定:将待测样品注入钙离子计仪器,根据仪器指示进行测定操作。
4. 记录结果:记录样品中钙离子的浓度值。
四、实验注意事项
1. 操作过程中要小心谨慎,避免碰撞仪器和溶液泄漏。
2. 校准溶液和样品溶液的注入要遵照仪器操作规程,避免污染。
3. 测定结果应当及时记录并标注样品信息,以便后续分析使用。
五、实验结束
实验结束后,关闭仪器电源并做好仪器清洁和维护工作,保证
仪器正常使用。
六、实验报告
实验结束后应当及时完成实验报告,包括实验目的、步骤、结果和分析等内容,并保留相关记录资料。
通过本实验规程的操作,可以准确测定样品中钙离子的浓度,为后续分析提供可靠数据。
水质中钙离子的测定
(循环水预膜)
1 试剂
1.1 三乙醇胺溶液:1+2
1.2 氢氧化钾溶液:200g/L
1.3 EDTA 标准溶液c(EDTA)≈0.01mol/L
1.4 钙-羧酸指示剂
2钙离子的测定
2.1 过滤水样。
2.2 用移液管移取50mL 过滤后的水样于250mL 锥形瓶中。
2.3 加3mL 三乙醇胺溶液、7mL 氢氧化钾溶液和约0.2g 钙-羧酸指示剂。
2.4 用EDTA 标准滴定溶液滴定,近终点时速度要缓慢,当溶液颜色由紫红色变为亮蓝色时即为终点。
3 结果计算
钙含量(以碳酸钙计)以质量浓度ρ1计,数值以mg/L 表示,按下式计算:
3
111008.100⨯⨯=V cV ρ
式中:
c——EDTA标准滴定溶液的浓度的准确数值,单位为摩尔每升(mol/L);
V1——滴定钙离子时,消耗EDTA标准滴定溶液的体积的数值,单位为毫升(mL);
V——所取水样的体积的数值,单位为毫升(mL);。
一、
1.1主要仪器与试剂
UV —756MC 型紫外可见分光光度计乙二醛双缩(2 —羟基苯胺)(GBHA) 0 .05 % 钙标准液:50μg/ml 、储备液VaOH 溶液0 .6mol/L 无水乙醇、分析纯
1 .
2 试验方法
取一定量钙标准溶液(5 .0μg/ml)2 .00ml , 加GBHA 溶液0 .6ml , 无水乙醇5 .0ml , 用0 .6mol/ NaOH 溶液调PH =12 .0(约0 .40ml), 用水定容至10ml , 摇匀.放置10min 左右, 用1cm 比色皿, 以试剂溶液为空白, 于516nm 处测其吸光度.
二、钙色素分光光度法
钙色素三个H 一酸偶氮化后结合而成的试剂,当在10% 丙酮,0. 08 mol /L 氢氧化钠中,该试剂与钙形成红色络合物,颜色可稳定10 min 以上。
该方法简便,快速,准确性好。
试验中酸对实验结果影响较大,发现在pH 4. 60 ~6. 20 范围内吸光度基本保持稳定,故试验确
定使用pH 为5. 20 的乙酸-乙酸钠缓冲溶液效果较好,可用于原料进厂和产品出厂的快速检验,也适用于一般实验室常规分析。
三、双氧水法
H2 SO4 和H2 O2 都是强氧化剂,在高温下放出新生态氧[O],使食品中的有机物破坏分解释放出CO2 、SO2 、NH3 及各种元素,Ca、P 等各种无机离子均留在消化液中。
用EDTA 法对此消化液进行钙的测定。
四、EDTA 法
EDTA 与钙离子可以生成络合物,试验表明,当食品中钙含量在0. 1% ~0. 4% 时,该方法和国标法测定结果比较差异显著,当钙含量低于0. 1% 或高于0. 4% 时,本方法和国标法测定结果一致。
对于高钙样品,EDTA 法测定结果比国标法高约1% 左右。
钙含量高于5% 的食品,用EDTA 法测定结果的精密度优于国标法。
在用EDTA 法对样品进行回滴时要快,如果回滴速度太慢,所加的掩蔽剂无法掩蔽磷酸根离子会引起测定值偏大。
EDTA滴定法,对于成分复杂,通常含色素的样品,终点较难判断,重现性差。