常见的离子符号,化学式
- 格式:ppt
- 大小:362.50 KB
- 文档页数:10

常见的离子符号和化学式一、一些常见离子1、阳离子:铵根离子:NH4+ 钾离子:K+钠离子:Na+ 氢离子:H+ 银离子:Ag+ 钙离子:Ca2+镁离子:Mg2+ 钡离子:Ba2+ 锌离子:Zn2+亚铜离子:Cu+ 铜离子:Cu2+ 亚铁离子:Fe2+ 铁离子:Fe3+铝离子:Al3+ 2、阴离子:氢氧根离子:OH- 硝酸根离子:NO3-氟离子:F- 氯离子:Cl - 溴离子:Br- 碳酸根离子:CO32-硫酸根离子:SO42- 氧离子:O2- 硫离子:S2-二、一些常见物质的化学式1、单质氢气:H2氮气:N2氧气:O2氯气:Cl2臭氧:O3氦气:He 氖气:Ne 氩气:Ar碳:C 硫:S 磷:P 石墨:C 金刚石:C钠:Na 镁:Mg 铝:Al 钾:K 钙:Ca 铁:Fe 铜:Cu 锌:Zn 汞:Hg2、化合物1氧化物:水:H2O 过氧化氢:H2O2一氧化碳:CO 二氧化碳:CO2一氧化氮:NO 二氧化氮:NO2 五氧化二磷:P2O5二氧化硫:SO2 氧化钠:Na2O 氧化钾:K2O 氧化镁:MgO 氧化铝:Al2O3氧化钙/生石灰:CaO 二氧化锰:MnO2氧化亚铁:FeO 氧化铁:Fe2O3四氧化三铁:Fe3O4氧化亚铜:Cu2O 氧化铜:CuO 氧化汞:HgO 2酸盐酸:HCl 的水溶液硝酸:HNO3硫酸:H2SO4碳酸:H2CO3 3碱氢氧化钠:NaOH 氢氧化钾:KOH 氢氧化镁:MgOH2氢氧化钙:CaOH2氢氧化铝:AlOH3氢氧化亚铁:FeOH2氢氧化铁:FeOH3氢氧化铜:CuOH24盐部分氯化钠:NaCl 硝酸钠:NaNO 3 硫酸钠:Na2SO4 碳酸钠:Na2CO3 氯化钾:KCl 硝酸钾:KNO 3 硫酸钾:K2SO4 碳酸钾:K2CO3 氯化铝:AlCl3 硝酸铝:AlNO33 硫酸铝:Al2SO43氯化亚铁:Fe Cl2硝酸亚铁:FeNO32 硫酸亚铁:FeSO4氯化铁:FeCl3 硝酸铁:FeNO33 硫酸铁:Fe2SO43氯化镁:MgCl2 硝酸镁:MgNO32 硫酸镁:MgSO4 碳酸镁:MgCO3氯化钙:CaCl2 硝酸钙:CaNO32 硫酸钙:CaSO4 碳酸钙:CaCO3氯化锌:ZnCl2硝酸锌:ZnNO32硫酸锌:ZnSO4氯化铜:CuCl2 硝酸铜:CuNO32 硫酸铜:CuSO4氯化银:AgCl 硝酸银:AgNO3硫酸银:Ag2SO4氯化钡:BaCl2 硝酸钡:BaNO32 硫酸钡:BaSO4碳酸钡:BaCO3氯化铵:NH4Cl 硝酸铵:NH4NO3硫酸铵:NH42SO4 碳酸铵:NH42CO3高锰酸钾:KMnO4 锰酸钾:K2MnO4 氯酸钾:KClO3三、物质构成的规律:1、由分子构成的物质:1某些非金属氧化物:如H2O、CO、CO2、H2O2、P2O5、SO2 ……2非金属气体单质:如H2、O2、N2、Cl2、O3 ……3稀有气体特殊的单原子分子:如He、Ne、Ar ……4酸:如HCl、H2SO4、H2CO3、HNO3、H2S……2、由原子构成的物质:1金属单质:如Hg、Fe、Mg……2某些固体非金属单质:如Si 金刚石、石墨……3、由离子构成的物质:1盐:如NaCl、KCl、MgCl2、CuSO4……2碱:如NaOH KOH ……。

五大原子团离子符号
五大原子团离子是指在化学中比较常见的由多个原子团组成的离子,它们分别是氨基离子(NH₂⁻)、碳酸根离子(CO₃²⁻)、硫酸根离子(SO₄²⁻)、磷酸根离子(PO₄³⁻)和氢氧根离子(OH⁻)。
氨基离子的化学式为NH₂⁻,由一个氮原子和两个氢原子组成。
它带有一个负电荷,在水中会与阳离子配对形成盐类。
碳酸根离子的化学式为CO₃²⁻,由一个碳原子和三个氧原子组成。
它带有两个负电荷,常见于碳酸盐类中,如钙碳酸、镁碳酸等。
硫酸根离子的化学式为SO₄²⁻,由一个硫原子和四个氧原子组成。
它带有两个负电荷,是一种广泛存在于矿物和生物体中的物质。
磷酸根离子的化学式为PO₄³⁻,由一个磷原子和四个氧原子组成。
它带有三个负电荷,在生物体中广泛存在,如骨骼、DNA、RNA等中。
氢氧根离子的化学式为OH⁻,由一个氧原子和一个氢原子组成。
它带有一个负电荷,在水中广泛存在,是碱性的化合物。
以上五大原子团离子在化学中都有着重要的应用,对于理解相关的物
理和化学现象具有至关重要的作用。
同时,它们也广泛应用于人类社
会中,如生产、医疗、环保等领域。
熟练掌握这些离子的性质和应用,是现代化学工作者的必备技能。
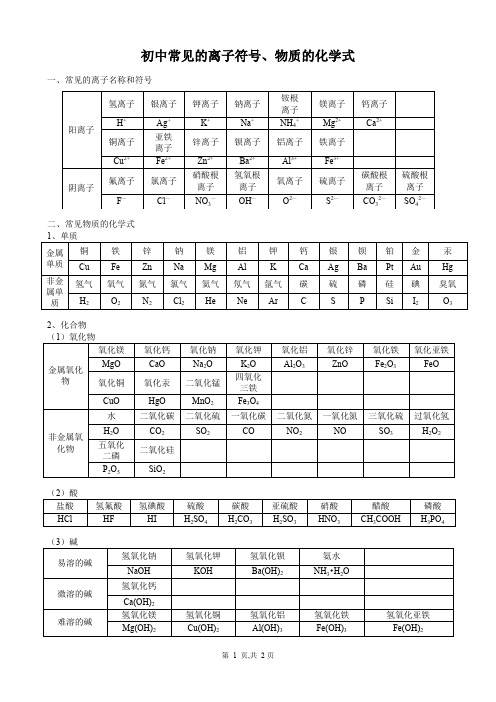

初中化学离子符号及化学用语的含义常见离子名称和符号:氢离子:H+;钠离子:Na+;钾离子:K+;银离子:Ag+;铵根离子:NH4+;镁离子:Mg2+;钙离子:Ca2+;铜离子:Cu2+;亚铁离子:Fe2+;钡离子:Ba2+;锌离子:Zn2+;铝离子:A13+;铁离子:Fe3+;氯离子:C1-;氟离子:F-;氢氧根离子:OH-;硝酸根离子:NO3-碳酸根离子:CO32-;硫酸根离子:SO42-;硫离子:S2-;氧离子:O2-化学用语的含义:一、元素符号、化学式、离子符号前面..的数字表示几个某原子或几个某分子或几个某离子:例:下列符号中“2”所表示的含义:2SO3:表示2个三氧化二硫分子2H:表示2个氢原子2.SO42-:表示2个硫酸根离子二、元素符号右下角...的数字表示一个某分子中含几个某原子:例:下列符号中“2”的含义:SO2:表示一个二氧化硫分子中含有2个氧原子H2:表示一个氢气分子中含有2个氢原子三、元素符号右上角...的数字表示某离子带几个单位正(负)电荷(数字先写,正负号后写,1可省略)如H-、NO3-:例:下列符号中“2”的含义:CO32-:表示碳酸根离子带2个单位负电荷Ca2+:表示钙离子带2个单位正电荷SO42-:表示硫酸根离子带2个单位负电荷四、元素符号正上方...的数字表示某物质中某元素的化合价(正负号先写,数字后写,1不能省略);+1 -2如: H2O; H2SO4;例:下列符号中“2”的含义:+2CuSO4:表示硫酸铜中铜元素的化合价为+2价-2CO:表示一氧化碳中氧元素的化合价为-2价+2BaCO3:表示碳酸钡中钡元素的化合价为+2价。

常见的离子符号和化学式一、一些常见离子1、阳离子:铵根离子:NH4+ 钾离子:K+钠离子:Na+ 氢离子:H+ 银离子:Ag+ 钙离子:Ca2+镁离子:Mg2+ 钡离子:Ba2+ 锌离子:Zn2+亚铜离子:Cu+ 铜离子:Cu2+ 亚铁离子:Fe2+ 铁离子:Fe3+铝离子:Al3+ 2、阴离子:氢氧根离子:OH- 硝酸根离子:NO3-氟离子:F- 氯离子:Cl - 溴离子:Br- 碳酸根离子:CO32-硫酸根离子:SO42- 氧离子:O2- 硫离子:S2-二、一些常见物质的化学式1、单质氢气:H2氮气:N2氧气:O2氯气:Cl2臭氧:O3氦气:He 氖气:Ne 氩气:Ar碳:C 硫:S 磷:P 石墨:C 金刚石:C钠:Na 镁:Mg 铝:Al 钾:K 钙:Ca 铁:Fe 铜:Cu 锌:Zn 汞:Hg2、化合物(1)氧化物:水:H2O 过氧化氢:H2O2一氧化碳:CO 二氧化碳:CO2一氧化氮:NO 二氧化氮:NO2 五氧化二磷:P2O5二氧化硫:SO2 氧化钠:Na2O 氧化钾:K2O 氧化镁:MgO 氧化铝:Al2O3氧化钙/生石灰:CaO 二氧化锰:MnO2氧化亚铁:FeO 氧化铁:Fe2O3四氧化三铁:Fe3O4氧化亚铜:Cu2O 氧化铜:CuO 氧化汞:HgO (2)酸盐酸:HCl 的水溶液硝酸:HNO3硫酸:H2SO4碳酸:H2CO3 (3)碱氢氧化钠:NaOH 氢氧化钾:KOH 氢氧化镁:Mg(OH)2氢氧化钙:Ca(OH)2氢氧化铝:Al(OH)3氢氧化亚铁:Fe(OH)2氢氧化铁:Fe(OH)3氢氧化铜:Cu(OH)2(4)盐(部分)氯化钠:NaCl 硝酸钠:NaNO 3 硫酸钠:Na2SO4 碳酸钠:Na2CO3 氯化钾:KCl 硝酸钾:KNO 3 硫酸钾:K2SO4 碳酸钾:K2CO3 氯化铝:AlCl3 硝酸铝:Al(NO3)3 硫酸铝:Al2(SO4)3氯化亚铁:Fe Cl2硝酸亚铁:Fe(NO3)2 硫酸亚铁:FeSO4氯化铁:FeCl3 硝酸铁:Fe(NO3)3 硫酸铁:Fe2(SO4)3氯化镁:MgCl2 硝酸镁:Mg(NO3)2 硫酸镁:MgSO4 碳酸镁:MgCO3 氯化钙:CaCl2 硝酸钙:Ca(NO3)2 硫酸钙:CaSO4 碳酸钙:CaCO3氯化锌:ZnCl2硝酸锌:Zn(NO3)2硫酸锌:ZnSO4氯化铜:CuCl2 硝酸铜:Cu(NO3)2 硫酸铜:CuSO4氯化银:AgCl 硝酸银:AgNO3硫酸银:Ag2SO4氯化钡:BaCl2 硝酸钡:Ba(NO3)2 硫酸钡:BaSO4碳酸钡:BaCO3氯化铵:NH4Cl 硝酸铵:NH4NO3硫酸铵:(NH4 )2SO4 碳酸铵:(NH4)2CO3 高锰酸钾:KMnO4 锰酸钾:K2MnO4 氯酸钾:KClO3三、物质构成的规律:1、由分子构成的物质:(1)某些非金属氧化物:如H2O、CO、CO2、H2O2、P2O5、SO2 ……(2)非金属气体单质:如H2、O2、N2、Cl2、O3 ……(3)稀有气体(特殊的单原子分子):如He、Ne、Ar ……(4)酸:如HCl、H2SO4、H2CO3、HNO3、H2S……2、由原子构成的物质:(1)金属单质:如Hg、Fe、Mg……(2)某些固体非金属单质:如Si 金刚石、石墨……3、由离子构成的物质:(1)盐:如NaCl、KCl、MgCl2、CuSO4……(2)碱:如NaOH KOH ……。
![常见的离子符号,化学式[优质PPT]](https://img.taocdn.com/s1/m/10046b52dd36a32d7275812a.png)
初中常见离子符号、化学式和化学方程式(初二部分)常见的离子符号常见的金属离子:1、带一个单位正电荷的锂离子:Li+钾离子:K+钠离子:Na+银离子:Ag+亚铜离子:Cu+2、带两个单位正电荷的钙离子:Ca2+镁离子:Mg2+钡离子:Ba2+锌离子:Zn2+亚铁离子:Fe2+铜离子:Cu2+3、带三个单位正电荷的铁离子:Fe3+ 铝离子:Al3+常见的非金属离子:1、带一个单位负电荷的氟离子:F—氯离子:Cl—溴离子:Br—碘离子:I—2、带两个单位负电荷的硫离子:S2—氧离子O2—3、带一个单位正电荷的氢离子:H+常见的原子团:(也叫酸根离子,NH4+除外)硝酸根离子:NO3—氢氧根离子:OH—氯酸根离子ClO3—磷酸根离子:PO43—碳酸氢根离子:HCO3—高锰酸根离子:MnO4—碳酸根离子:CO32—硫酸根离子:SO42—亚硫酸根离子:SO32—锰酸根离子:MnO42—铵根离子:NH4+说明:带正电荷的叫阳离子(如金属离子)带负电荷的叫阴离子(如常见的非金属离子和常见的原子团。
H+和NH4+除外。
)1、离子不可单独存在,有阴离子存在必然有阳离子,由阴阳离子构成的物质是离子化合物。
2、离子所带的电荷数与其在化合物中元素表现的化合价数值和正负均一致。
例如,硫离子S2—中S的化合价为—23、离子团所带的电荷数与其整体表现化合价数值和正负一致,其整体化合价是+的整体化合价是+1,这其组成元素所表现化合价的代数和。
例如,铵根离子NH4是由于其中N显—3价,H显+1价决定的。
常用化合价口诀:一价氢氯(-1)钾钠银,二价氧(-2)钙钡镁锌,三铝四硅五氮磷,二三铁二四碳,二(-2)四六硫都齐全,单质为零铜正二,金正非负和为零。
负一硝酸氢氧根,负二硫酸碳酸根,负三只有磷酸根,正一价的是铵根。
常见的化学式常见的化学方程式一、化合反应1、红磷在空气(或氧气)中燃烧:4P+5O2 2P2O52、氢气在空气中燃烧生成水:2H2+O22H2O3、硫磺在空气(或氧气)中燃烧:S+O2SO24、镁条在空气(或氧气)中燃烧:2Mg+O22MgO5、铁丝在氧气中燃烧:3Fe+2O2Fe3O46、木炭在空气(或氧气)中完全燃烧:C+O2 CO27、木炭不充分燃烧:2C+O22CO8、一氧化碳燃烧:2CO+O2 2CO29、二氧化碳和水反应生成碳酸:CO2+H2O ==H2CO310、二氧化碳通过灼热的炭层:CO2+C 2CO 二、分解反应11、高锰酸钾制氧气:2KMnO4K2MnO4+MnO2+O2↑12、氯酸钾制氧气:2KClO32KCl+3O2↑13、双氧水制氧气:2H2O22H2O + O2↑14、电解水:2H2O 2H2↑+ O2↑15、碳酸分解:H2CO3H2O+CO2↑16、高温煅烧石灰石:CaCO3 CaO +CO2↑三、其他反应类型17、石灰石与稀盐酸反应制取二氧化碳:CaCO3+2HCl =CaCl2+H2O+CO2点燃点燃点燃点燃点燃点燃点燃高温点燃△MnO2△MnO2通电高温18、硫酸铜溶液和氢氧化钠溶液反应:CuSO4+2NaOH = Na2SO4+Cu(OH)2↓19、二氧化碳通入澄清石灰水中:CO2+Ca(OH)2== CaCO3↓+H2O20、氢氧化钠吸收二氧化碳:CO2+2NaOH=Na2CO3+H2O21、氢氧化钠溶液吸收二氧化硫:SO2+ 2NaOH==Na2SO3+H2O22、酒精燃烧:C2H5OH + 3O22CO2+ 3H2O23、甲烷燃烧:CH4 + 2O2CO2+ 2H2O点燃点燃。
常见的离子符号和化学式一、一些常见离子1、阳离子:铵根离子:NH4+ 钾离子:K+钠离子:Na+ 氢离子:H+ 银离子:Ag+ 钙离子:Ca2+镁离子:Mg2+ 钡离子:Ba2+ 锌离子:Zn2+亚铜离子:Cu+ 铜离子:Cu2+ 亚铁离子:Fe2+ 铁离子:Fe3+铝离子:Al3+ 2、阴离子:氢氧根离子:OH- 硝酸根离子:NO3-氟离子:F- 氯离子:Cl - 溴离子:Br- 碳酸根离子:CO32-硫酸根离子:SO42- 氧离子:O2- 硫离子:S2-二、一些常见物质的化学式1、单质氢气:H2氮气:N2氧气:O2氯气:Cl2臭氧:O3氦气:He 氖气:Ne 氩气:Ar碳:C 硫:S 磷:P 石墨:C 金刚石:C钠:Na 镁:Mg 铝:Al 钾:K 钙:Ca 铁:Fe 铜:Cu 锌:Zn 汞:Hg2、化合物(1)氧化物:水:H2O 过氧化氢:H2O2一氧化碳:CO 二氧化碳:CO2一氧化氮:NO 二氧化氮:NO2 五氧化二磷:P2O5二氧化硫:SO2 氧化钠:Na2O 氧化钾:K2O 氧化镁:MgO 氧化铝:Al2O3氧化钙/生石灰:CaO 二氧化锰:MnO2氧化亚铁:FeO 氧化铁:Fe2O3四氧化三铁:Fe3O4氧化亚铜:Cu2O 氧化铜:CuO 氧化汞:HgO (2)酸盐酸:HCl 的水溶液硝酸:HNO3硫酸:H2SO4碳酸:H2CO3 (3)碱氢氧化钠:NaOH 氢氧化钾:KOH 氢氧化镁:Mg(OH)2氢氧化钙:Ca(OH)2氢氧化铝:Al(OH)3氢氧化亚铁:Fe(OH)2氢氧化铁:Fe(OH)3氢氧化铜:Cu(OH)2(4)盐(部分)氯化钠:NaCl 硝酸钠:NaNO 3 硫酸钠:Na2SO4 碳酸钠:Na2CO3 氯化钾:KCl 硝酸钾:KNO 3 硫酸钾:K2SO4 碳酸钾:K2CO3 氯化铝:AlCl3 硝酸铝:Al(NO3)3 硫酸铝:Al2(SO4)3氯化亚铁:Fe Cl2硝酸亚铁:Fe(NO3)2 硫酸亚铁:FeSO4氯化铁:FeCl3 硝酸铁:Fe(NO3)3 硫酸铁:Fe2(SO4)3氯化镁:MgCl2 硝酸镁:Mg(NO3)2 硫酸镁:MgSO4 碳酸镁:MgCO3 氯化钙:CaCl2 硝酸钙:Ca(NO3)2 硫酸钙:CaSO4 碳酸钙:CaCO3氯化锌:ZnCl2硝酸锌:Zn(NO3)2硫酸锌:ZnSO4氯化铜:CuCl2 硝酸铜:Cu(NO3)2 硫酸铜:CuSO4氯化银:AgCl 硝酸银:AgNO3硫酸银:Ag2SO4氯化钡:BaCl2 硝酸钡:Ba(NO3)2 硫酸钡:BaSO4碳酸钡:BaCO3氯化铵:NH4Cl 硝酸铵:NH4NO3硫酸铵:(NH4 )2SO4 碳酸铵:(NH4)2CO3 高锰酸钾:KMnO4 锰酸钾:K2MnO4 氯酸钾:KClO3三、物质构成的规律:1、由分子构成的物质:(1)某些非金属氧化物:如H2O、CO、CO2、H2O2、P2O5、SO2 ……(2)非金属气体单质:如H2、O2、N2、Cl2、O3 ……(3)稀有气体(特殊的单原子分子):如He、Ne、Ar ……(4)酸:如HCl、H2SO4、H2CO3、HNO3、H2S……2、由原子构成的物质:(1)金属单质:如Hg、Fe、Mg……(2)某些固体非金属单质:如Si 金刚石、石墨……3、由离子构成的物质:(1)盐:如NaCl、KCl、MgCl2、CuSO4……(2)碱:如NaOH KOH ……。
初中罕见离子符号、化学式和化学方程式(初二部分)之袁州冬雪创作罕见的离子符号罕见的金属离子:1、带一个单位正电荷的锂离子:Li+钾离子:K+钠离子:Na+银离子:Ag+亚铜离子:Cu+2、带两个单位正电荷的钙离子:Ca2+镁离子:Mg2+钡离子:Ba2+锌离子:Zn2+亚铁离子:Fe2+铜离子:Cu2+3、带三个单位正电荷的铁离子:Fe3+ 铝离子:Al3+罕见的非金属离子:1、带一个单位负电荷的氟离子:F—氯离子:Cl—溴离子:Br—碘离子:I—2、带两个单位负电荷的硫离子:S2—氧离子 O2—3、带一个单位正电荷的氢离子:H+罕见的原子团:(也叫酸根离子,NH4+除外)硝酸根离子:NO3—氢氧根离子:OH—氯酸根离子 ClO3—磷酸根离子:PO43—碳酸氢根离子:HCO3—高锰酸根离子:MnO4—碳酸根离子:CO32—硫酸根离子:SO42—亚硫酸根离子:SO32—锰酸根离子:MnO42—铵根离子:NH4+说明:带正电荷的叫阳离子(如金属离子)带负电荷的叫阴离子(如罕见的非金属离子和罕见的原子团.H+和NH4+除外.)1、离子不成单独存在,有阴离子存在必定有阳离子,由阴阳离子构成的物质是离子化合物.2、离子所带的电荷数与其在化合物中元素表示的化合价数值和正负均一致.例如,硫离子S2—中S的化合价为—23、离子团所带的电荷数与其整体表示化合价数值和正负一致,其整体化合价是其组成元素所表示化合价的代数和.例如,铵根离子NH4+的整体化合价是+1,这是由于其中N显—3价,H显+1价决议的.常常使用化合价口诀:一价氢氯(-1)钾钠银,二价氧(-2)钙钡镁锌,三铝四硅五氮磷,二三铁二四碳,二(-2)四六硫都齐全,单质为零铜正二,金正非负和为零.负一硝酸氢氧根,负二硫酸碳酸根,负三只有磷酸根,正一价的是铵根.罕见的化学式一、罕见单质(可以参考讲义后面的元素周期表)二、化合物1、氧化物2、其他化合物3、罕见有机化合物➢罕见的化学方程式一、化合反应1、红磷在空气(或氧气)中燃烧:4P+5O 2 2P 2O 52、氢气在空气中燃烧生成水:2H 2+O 2 2H 2O点燃点燃点燃3、硫磺在空气(或氧气)中燃烧:S+O 2SO 24、镁条在空气(或氧气)中燃烧:2Mg+O 2 2MgO5、铁丝在氧气中燃烧:3Fe+2O 2Fe 3O 46、柴炭在空气(或氧气)中完全燃烧:C+O 2 CO 27、柴炭不充分燃烧:2C+O 22CO8、一氧化碳燃烧:2CO+O 2 2CO 29、二氧化碳和水反应生成碳酸:CO 2+H 2O ==H 2CO 310、二氧化碳通过灼热的炭层:CO 2+C 2CO 二、分解反应11、高锰酸钾制氧气:2KMnO 4K 2MnO 4+MnO 2+O 2↑12、氯酸钾制氧气:2KClO 32KCl+3O 2↑13、双氧水制氧气:2H 2O 2 2H 2O + O 2↑14、电解水:2H 2O 2H 2↑+ O 2↑ 15、碳酸分解:H 2CO 3 H 2O+CO 2↑16、高温煅烧石灰石:CaCO 3 CaO +CO 2↑ 三、其他反应类型17、石灰石与稀盐酸反应制取二氧化碳:CaCO 3+2HCl =CaCl 2+H 2O+CO 218、硫酸铜溶液和氢氧化钠溶液反应:CuSO 4+2NaOH = Na 2SO 4+Cu(OH)2↓ 19、二氧化碳通入澄清石灰水中:CO 2+Ca(OH)2== CaCO 3↓+H 2O点燃点燃点燃点燃高温点燃△MnO 2△MnO 2通电高温20、氢氧化钠吸收二氧化碳:CO 2+2NaOH=Na 2CO 3+H 2O 21、氢氧化钠溶液吸收二氧化硫:SO 2+ 2NaOH==Na 2SO 3+H 2O22、酒精燃烧:C 2H 5OH + 3O 2 2CO 2 + 3H 2O23、甲烷燃烧:CH 4 + 2O 2 CO 2 + 2H 2O点燃点燃。
常见的离子符号和化学式一、一些常见离子1、阳离子:铵根离子:NH4+ 钾离子:K+钠离子:Na+ 氢离子:H+ 银离子:Ag+ 钙离子:Ca2+镁离子:Mg2+ 钡离子:Ba2+ 锌离子:Zn2+亚铜离子:Cu+ 铜离子:Cu2+ 亚铁离子:Fe2+ 铁离子:Fe3+铝离子:Al3+ 2、阴离子:氢氧根离子:OH- 硝酸根离子:NO3-氟离子:F- 氯离子:Cl - 溴离子:Br- 碳酸根离子:CO32-硫酸根离子:SO42- 氧离子:O2- 硫离子:S2-二、一些常见物质的化学式1、单质氢气:H2氮气:N2氧气:O2氯气:Cl2臭氧:O3氦气:He 氖气:Ne 氩气:Ar碳:C 硫:S 磷:P 石墨:C 金刚石:C钠:Na 镁:Mg 铝:Al 钾:K 钙:Ca 铁:Fe 铜:Cu 锌:Zn 汞:Hg2、化合物(1)氧化物:水:H2O 过氧化氢:H2O2一氧化碳:CO 二氧化碳:CO2一氧化氮:NO 二氧化氮:NO2 五氧化二磷:P2O5二氧化硫:SO2 氧化钠:Na2O 氧化钾:K2O 氧化镁:MgO 氧化铝:Al2O3氧化钙/生石灰:CaO 二氧化锰:MnO2氧化亚铁:FeO 氧化铁:Fe2O3四氧化三铁:Fe3O4氧化亚铜:Cu2O 氧化铜:CuO 氧化汞:HgO (2)酸盐酸:HCl 的水溶液硝酸:HNO3硫酸:H2SO4碳酸:H2CO3 (3)碱氢氧化钠:NaOH 氢氧化钾:KOH 氢氧化镁:Mg(OH)2氢氧化钙:Ca(OH)2氢氧化铝:Al(OH)3氢氧化亚铁:Fe(OH)2氢氧化铁:Fe(OH)3氢氧化铜:Cu(OH)2(4)盐(部分)氯化钠:NaCl 硝酸钠:NaNO 3 硫酸钠:Na2SO4 碳酸钠:Na2CO3 氯化钾:KCl 硝酸钾:KNO 3 硫酸钾:K2SO4 碳酸钾:K2CO3 氯化铝:AlCl3 硝酸铝:Al(NO3)3 硫酸铝:Al2(SO4)3氯化亚铁:Fe Cl2硝酸亚铁:Fe(NO3)2 硫酸亚铁:FeSO4氯化铁:FeCl3 硝酸铁:Fe(NO3)3 硫酸铁:Fe2(SO4)3氯化镁:MgCl2 硝酸镁:Mg(NO3)2 硫酸镁:MgSO4 碳酸镁:MgCO3 氯化钙:CaCl2 硝酸钙:Ca(NO3)2 硫酸钙:CaSO4 碳酸钙:CaCO3氯化锌:ZnCl2硝酸锌:Zn(NO3)2硫酸锌:ZnSO4氯化铜:CuCl2 硝酸铜:Cu(NO3)2 硫酸铜:CuSO4氯化银:AgCl 硝酸银:AgNO3硫酸银:Ag2SO4氯化钡:BaCl2 硝酸钡:Ba(NO3)2 硫酸钡:BaSO4碳酸钡:BaCO3氯化铵:NH4Cl 硝酸铵:NH4NO3硫酸铵:(NH4 )2SO4 碳酸铵:(NH4)2CO3 高锰酸钾:KMnO4 锰酸钾:K2MnO4 氯酸钾:KClO3三、物质构成的规律:1、由分子构成的物质:(1)某些非金属氧化物:如H2O、CO、CO2、H2O2、P2O5、SO2 ……(2)非金属气体单质:如H2、O2、N2、Cl2、O3 ……(3)稀有气体(特殊的单原子分子):如He、Ne、Ar ……(4)酸:如HCl、H2SO4、H2CO3、HNO3、H2S……2、由原子构成的物质:(1)金属单质:如Hg、Fe、Mg……(2)某些固体非金属单质:如Si 金刚石、石墨……3、由离子构成的物质:(1)盐:如NaCl、KCl、MgCl2、CuSO4……(2)碱:如NaOH KOH ……。