石灰性土壤无机磷分级的测定方法
- 格式:pdf
- 大小:181.93 KB
- 文档页数:9

土壤有机磷测定方法土壤全磷含量约10~1000 g/kg,与土层、质地、发育、利用方式与强度等有关。
土壤磷分为无机磷和有机磷两大部分,根据我国土壤普查资料,一般耕作土壤中,有机磷含量约占全磷量的25%~56%。
土壤有机磷测定,是指土壤有机磷是土壤全磷的重要组成部分,主要是植素、核酸等含磷有机物中的磷。
通常采用间接测定法,主要有烧灼法和浸提法。
烧灼法是用高温(550°C)或低温(250°C)烧灼,使有机磷矿化,然后用酸溶解,酸液中的磷来自有机磷和无机磷两部分;未经灼烧的土壤用同浓度酸浸提,酸液中的磷只来源于无机部分;两者相减即为土壤有机磷的含量。
浸提法先用硫酸再用氢氧化钠浸提出酸溶及碱溶有机和无机磷,减去其中无机磷从而得到有机磷含量。
两种方法均使用钼锑抗比色法测定溶液中的磷。
烧灼法的主要缺点是在烧灼过程中可能改变矿物态磷的溶解度,尤其是在高度风化的土壤中测定结果偏高;而且有机磷含量高时,高温可使部分磷挥发从而引入误差。
浸提法克服了烧灼法不适用于高度风化的热带土壤的缺点,其优点是将总有机磷进一步区分为酸溶性有机磷和碱溶性有机磷,二者的和即为土壤有机磷总量;缺点是浸提不易完全而且有机磷可能水解。
一、方法原理土壤经550℃灼烧,使有机磷化合物转化为无机态磷,然后与未经灼烧的同一土样,分别用0.2mol/L(1/2H2SO4)溶液浸提后测定磷量,所得结果的差值即为有机磷。
二、主要仪器高温电炉、烘箱、分光光度计。
三、试剂0.2mol/L(1/2H2SO4)溶液。
取浓H2SO46ml溶解于1000ml水中,标定。
四、操作步骤称取通过60目的风干土样品1.000g置于15ml瓷坩埚中,在550℃高温电炉内灼烧1h,取出冷却,用0.2mol/L(1/2H2SO4)溶液100ml将土样洗入200ml容量瓶中。
另外称取 1.000g同一土壤样品,放置在另一个200ml容量瓶中,加入0.2mol/L(1/2H2SO4)溶液100ml。


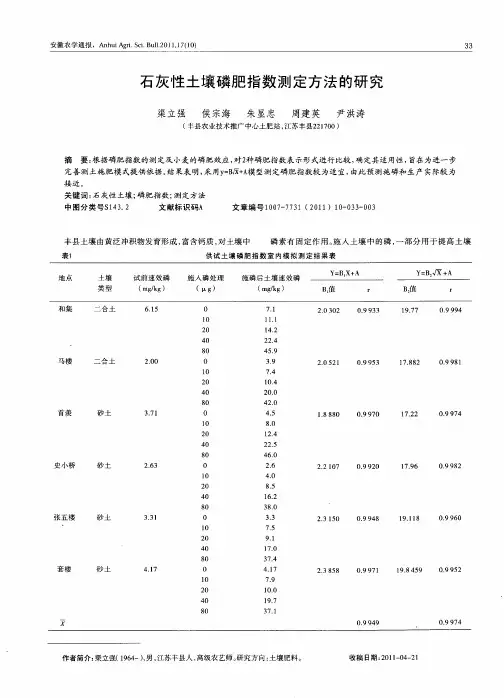
石灰性土壤有效磷测定方法的研究
磷是植物生长和发育的必需元素,是生物体体内最重要的低活性微量元素之一。
磷是
生物链中的一个重要的构成部分,其在植物生长和繁殖中发挥着重要的作用,因此,在大
多数土壤中磷含量的测定和管理非常重覀地唯一。
石灰性土壤广泛分布在中国的多个地区, 我们的实验的主要目的是研究石灰性土壤有效磷的测定方法。
石灰性土壤有效磷的测定方法主要有以下几种:离子交换法、酸解-物理溶出法、硝
酸解-有机溶出法以及施氮-浸渍法。
由于石灰性土壤中磷的含量很高, 在进行测定时需要硝酸解-有机溶出法。
这个方法
将新鲜混合土壤中的磷提取出来, 并用适当常量的硝酸来溶解提取物。
经过硝酸溶解, 土
壤若干不溶性的有机物质也被提取出来, 并使得原有的有效磷质被溶出。
整个提取过程可
以用100ml的硝酸来完成。
经过硝酸提取, 磷被溶解出来, 用碳酸钙沉淀以去除有机物, 然后用原子吸收光谱法
或紫外分光光度法检测溶液中磷的含量。
结果显示, 使用硝酸解-有机溶出法测定石灰性土壤中的有效磷含量, 与其他方法的
对比结果是吻合的。
所以, 为了测定石灰性土壤有效磷含量, 硝酸解-有机溶出法是一种
可行的方法。

关于土壤有效磷及其化学测试方法的分析作者:张钧来源:《中国化工贸易·中旬刊》2019年第03期摘要:土壤是一项重要自然资源,其对于支持植物生长有着重要作用。
土壤中含有大量的元素,磷是土壤中必不可少的一项元素,其含量在一定程度上决定了土壤的肥力。
如果土壤中磷元素的含量不足,势必会对土壤上的植物的生长造成不良影响。
但是,如果土壤中的磷元素含量过高,将会导致有效磷流出,这将会对环境造成一定污染。
由此可见,采取合理的方式对土壤中的有效磷的含量情况进行合理测定意义重大。
关键词:土壤;有效磷;化学测试;植物土壤中的磷元素都以不同的形式存在,主要包括无机磷化合物和有机磷化合物两种。
无机磷化合物存在不同类型的化合态,并且受外界因素影响,会发生不同程度改变,这也将会对土壤中磷的有效性造成一定影响。
有机磷在土壤中的占比较重,但是,其对于植物生长的作用并未得到全面开发,因此,有机磷转化为土壤有效磷是目前相关工作人员在具体研究过程中的关键方向。
通过对化学测试方法,完成对土壤的检测,能够准确、高效的完成对土壤中有效磷的测定。
1 土壤有效磷植物生长发育过程中需要大量的微量元素,磷是其中最为重要的一项微量元素,其在植物生长发育过程中,会参加植物的新陈代谢,并且会被循环利用。
植物在生长过程中利用的磷通常都来自土壤,其平均含量约在0.07%-0.3%。
近几年,我国不断对磷矿资源进行利用和开发,这也使磷资源快速减少。
土壤中存在的磷元素的具体含量,以及其具体化学性质对于植物生长来说有着重要意义。
土壤中中的有效磷主要以五价元素形态存在,而植物对于土壤中磷元素的吸收,初级磷酸要明显优于次级磷酸[1]。
植物种植过程中,虽然每年农户都会依据实际情况,适当的向土壤中施一定量的磷肥,但是从实际情况来看,这些磷肥无法被植物全部吸收,长期以往,土壤中有效磷肥的含量将会不断降低,这将会对植物的生长造成一定阻碍。
2 研究土壤中有效磷2.1 沉淀与溶解磷元素的沉淀与溶解都会对受到土壤类型有影响,同时,磷元素的具体转化也会受控制。

关于土壤有效磷及其化学测试方法分析摘要:我国自古就是一个以农耕为主的国家,农耕土地也是我国赖以生存的重要资源,其对于农业的发展以及作物的生长都有着至关重要的作用。
土壤中所含的元素的多少对于作物生长至关重要,其中有效磷是土壤中极为重要的元素之一,但是土壤中的磷的含量过高也会导致有效磷流出也会对环境造成污染,所以对于有效磷含量的合理检测在农业发展中至关重要。
关键字:土壤;有效磷;化学;测试方法植物的生长发育离不开磷这个微量元素,植物所需要的微量元素大多来源于土壤,磷元素就是存在在土壤中的微量元素之一,土壤中的磷元素主要有两种形式存在,一是无机磷化合物,二是有机磷化合物。
无机磷化合物是拥有多种化合态,容易受到外界诸多因素的影响而发生改变,这也会影响土壤中磷的有效性。
有机磷在土壤中是比例最多的存在,但是对作物的作用并没有得到全面的开发,所以把有机磷转化为有效磷的研究必然是土壤研究中的关键。
在有效磷及其化学测试方法中完成对土壤的检测,可以准确地,效率地完成对土壤中有效磷的测定。
1.土壤中有效磷与植物的关系植物在发育的过程中,需要吸收各种元素才能满足植物的生长需求。
磷元素是植物生长过程中必不可少的元素之一,但是并不是所有的磷元素都可以被吸收利用,有效磷也就是植物可以有效吸收到的磷元素称作有效磷,也就是说磷元素含量的多少并不代表植物都可以利用,只有有效磷才能被植物吸收利用到植物的生长发育中去,众所周知植物的生长离不开光合作用,磷元素在一定程度上也可以促进植物的光合作用,植物的脂肪代谢同样也离不开磷元素的帮助,它在作物的能量转换和代谢过程中起着重要的作用,并且能够提高作物的抗旱、抗寒、抗病的能力,缺失磷元素的植物容易发育不好,导致植物过于矮小,看上去营养不良。
但是如果磷元素过多也会使得植物早衰。
因此可见磷元素在植物的生长过程中有着重要的作用。
2.化学检测法过程研究在土壤有效磷的检测中,化学检测法是目前唯一且最准确方法,但是其中涉及的因素也比较多,无论什么因素对于结果都是有影响的,所以我们需要针对每一项因素进行预判,第一,不同的土壤所使用的提取剂不同,需要科学的去选取合适的提取剂,第二,提取时时间和温度的掌控也是至关重要的,一定要控制在科学合理的范围。

中性和石灰性土壤有效磷的测定方法0.5mol ・L-1NaHC0法1方法原理石灰性土壤由于大量游离碳酸钙存在,不能用酸溶液来提取有效磷。
一般用碳酸盐的碱溶液。
由于碳酸根的同离子效应,碳酸盐的碱溶液降低碳酸钙的溶解度,也就降低了溶液中钙的浓度,这样就有利于磷酸钙盐的提取。
同时由于碳酸盐的碱溶液,也降低了铝和铁离子的活性,有利于磷酸铝和磷酸铁的提取。
此外,碳酸氢钠碱溶液中存在着0H-, HC03- CO32- 于吸附态磷的置换,因此NaHCO不仅适用石灰性土壤,也适应于中性和酸性土壤中速效磷的提取。
待测液中的磷用钼锑抗试剂显色,进行比色测定。
2主要仪器3试剂(1)0.5mol •L - 1NaHCO3浸提液:溶解NaHCO3 42.0g T 800mL水中,以0.5mol •L-INaOH溶液调节浸提液的pH至8.5。
此溶液曝于空气中可因失去CO2 而使pH增高,可于液面加一层矿物油保存之。
此溶液贮存于塑料瓶中比在玻璃中容易保存,若贮存超过一个月,应检查pH值是否改变。
(2)无磷活性炭:活性炭常含有磷,应做空白试验,检验有无磷存在。
如含磷较多,须先用2mol •L-l HCl浸泡过夜,用蒸馏水冲洗多次后,再用0.5mol ・L-1NaHCO浸泡过夜,在平瓷漏斗上抽气过滤,每次用少量蒸馏水淋洗多次,并检查到无磷为止。
如含磷较少,则直接用NaHCO3其他钼锑抗试剂、磷标准溶液同522.3试剂中6,7。
5.334操作步骤20目筛子的风干土样2.5g(精确到0.001g)于150mL三角瓶(或大试管)中,加入0.5mol ・L-1NaHCO溶液50mL再加一勺无磷活性炭(注j),塞紧瓶塞,在振荡机上振荡30min(注2)立即用无磷滤纸过滤,滤液承接于100mL三角瓶中,吸取滤液10mL(含磷量高时吸取2.5〜5.0mL,同时应补加0.5mol ・L-1NaHCO溶液至10mL)于150mL三角瓶中(注3)加入蒸馏水35mL然后移液管加入钼锑抗试剂5mL注4),摇匀,放置30分钟后,用880nm或700nm波长进行比色。

5.1概述土壤全磷(P)量是指土壤中各种形态磷素的总和。
我国土壤全磷的含量(以P,g·kg-1表示)从第二次全国各地土壤普查资料来看[1],大致在0.44-0.85g·kg-1范围内,但最高可达1.8g·kg-1,低的只有0.17g·kg-1。
南方酸性土壤全磷含量一般低于0.56g·kg-1;北方石灰性土壤全磷含量则较高。
土壤全磷含量的高低,受土壤母质、成土作用和耕作施肥的影响很大。
一般而言,基性火成岩的风化母质含磷多于酸性火成岩的风化母质。
我国黄土母质全磷含量是比较高的,一般均在0.57—0.70g·kg-1之间。
另外,土壤中磷的含量与土壤质地和有机质含量也有关系,粘土含磷多于砂性土,有机质丰富的土壤含磷亦较多。
磷在土壤剖面中的分布,耕作层含磷量一般高于底土层。
大量资料的统计结果表明,我国不同地带的气候区的土壤其速效磷含量与全磷含量呈正相关的趋势。
在全磷含量很低的情况下(P 0.17—0.44g·kg-1以下),土壤中有效磷的供应也常感不足,但是全磷含量较高的土壤,却不一定说明它已有足够的有效磷供应当季作物生长的需要,因为土壤中磷大部分成难溶性化合物存在。
例如我国大面积发育于黄土性母质的石灰性土壤,全磷含量均在0.57—0.79g·kg-1之间,高的在0.87g·kg-1以上,但由于土壤中大量游离碳酸钙的存在,大部分磷成为难溶性的磷酸钙盐,能被作物吸收利用的有效磷含量很低,施用磷肥有明显的增产效果。
因此从作物营养和施肥的角度来看,除全磷分析外,特别要测定土壤中有效磷含量,这样才能比较全面地说明土壤磷素肥力的供应状况。
土壤中磷可以分为两大类,即无机磷和有机磷。
矿质土壤以无机磷为主,有机磷约占全磷的20—50%。
土壤有机磷是一个很复杂的问题,许多组成和结构还不清楚,大部分有机磷,以高分子形态存在,有效性不高,这个问题一直是土壤学中一个重要的研究课题。

石灰性土壤有效磷测定依据标准:L Y/T 1233-1999(0.5 mol/L碳酸氢钠浸提法)1方法要点以0.5 mol/L碳酸氢钠(pH8.5 )浸提石灰性土壤中的有效磷,可以抑制钙离子的活性,使其以碳酸钙的形式沉淀,使某些活性较大的磷酸钙(Ca2-P)得以溶解被浸提出来,同有部分比较活性的Fe-P,Al-P起水解作用而浸出。
本方法适用于石灰性土壤中有效磷的测定。
2试剂2.1浸提剂(0.5 mol/L碳酸氢钠,pH 8.5 ):42.0 g 碳酸氢钠(NaHCO3,分析纯),加水至近1L。
如pH不在8.5,则用4 mol/L氢氧化钠溶液调节pH到8.5,然后定容至1L。
每周检查一次溶液的pH.2.2 2,4一二硝基酚(或2,6一二硝基酚)指示剂(2g/L):溶解20 g 2,4-二硝基酚于100mL水中;2.3钼锑贮存液:153mL浓硫酸(分析纯,ρ=1.84g/mL),缓慢地倒入约400mL水中,搅拌,冷却。
另取10g钼酸铵[(NH4)6Mo7O24·4H2O,分析纯〕,溶解于约60℃的300mL水中,冷却。
然后将硫酸溶液缓缓倒入钼酸铵溶液中,再加人100mL 5g/L的酒石酸锑钾(KSbOC4H4O6,分析纯)溶液,最后用水稀释至1L,避光贮存。
此贮存液含10g/L钼酸铵,2.75mol/L硫酸。
2.4钼锑抗显色剂:1.50g抗坏血酸(C6H8O6,左旋,旋光度十21°—+22°,分析纯)溶于100mL 钼锑贮存液中。
此液须随配随用。
2.5磷(P,5μg/mL)标准溶液:0.4394g在50℃烘干的磷酸二氢钾(KH2PO4,分析纯),加100mL 水,加5mL浓硫酸(防腐),用水定容到1L,浓度为100 pg/mL磷(P),此溶液可以长期保存。
吸取上述溶液10 mL于200 mL容量瓶中,加水至标度,浓度为5 pg/mL磷(P)标准溶液,此溶液不宜久存。
2.6无磷活性碳(分析纯)。

中性和石灰性土壤速效磷的测定(0.5 mol/L NaHCO法) 3一、试验仪器往返振荡机、分光光度计或比色计、三角瓶、滴定管、移液管、pH试纸、无磷滤纸二、试验药剂NaHCO4、NaOH、2 mol/L HCI、酒石酸氧锑钾,K(SbO)C4H4O6,、钼酸铵、3 浓硫酸、左旋抗坏血酸1.5g、KHPO 24三、溶液配制1、NaHCO3 浸提液(0.5mol/L、pH=8.5)NaHCO3 42.0g溶解于800mL水中,以0.5 mol/L NaOH溶液调节浸提液的pH 至8.5 。
此溶液曝于空气中可应失去CO而使pH增高,可于液面加一层矿物油2 保存之。
此溶液贮存于塑料瓶中比在玻璃中容易保存,若贮存超过1个月,应检查pH值是否改变。
2、无磷活性炭活性炭常含有磷,应做空白试验,检查有无磷存在。
如含有磷较多,须先用2 mol/L HCI浸泡过夜,用蒸馏水冲洗多次后,再用0.5 mol/L NaHCO3浸泡过夜,在平瓷漏斗上抽气过滤,每次用少量蒸馏水淋洗多次,并检查到无磷为此。
如含少量磷,则直接用NaHCO3处理即可3、钼锑抗试剂A 、5g/L酒石酸氧锑钾溶液:取酒石酸氧锑钾,K(SbO)C4H4O6,0.5g,溶解于100mL水中。
B、钼酸铵一硫酸溶液:称取钼酸铵10g,溶于450mL水中,缓慢地加入153mL 浓硫酸,边加边搅。
再将A溶液加到B溶液中,最后加水至1L。
充分混匀,贮于棕色瓶中,此为钼锑混合液。
临用前,称取左旋抗坏血酸1.5g,溶于100mL钼锑混合液中,混匀,此为钼锑抗试剂。
(有效期为24h)4、磷标准溶液准确称取在105?烘箱中烘干的KH2PO4 0.2195g,溶解在400mL水中,加浓硫酸5mL,转入1L容量瓶中,加水至刻度。
此溶液为50ug/mLP标准溶液。
ug/mLP标准溶液。
吸取上述磷标准溶液25mL,稀释至250mL,即为5四、试验步骤:1、称取通过20目筛子的风干土样2.500g于150 mL 三角瓶(或大试管)中;2、加入0.5 mol/L NaHCO3 浸提液50 mL;3、加一勺无磷活性炭,塞紧瓶盖,在振荡机上振荡30分钟;4、震荡后立即用无磷滤纸过滤,滤液承接于100 mL 三角瓶中;5、吸取滤液10 mL (含磷量高时吸取2.5~5.0 mL ,同时应补加0.5溶液至10 mL)于150 mL三角瓶中;6、再用滴定管准确加入蒸馏水35 mL;7、然后移液管加入钼锑抗试剂5 mL,摇匀,放置30分钟后;8、用880nm或770nm波长进行比色,以空白液的吸收值为0,读出待测液的吸收值(A);9、分别准确吸收5ug/mL P硫酸标准液0,1.0,2.0,3.0,4.0,5.0 mL于150 mL三角瓶中;10、再加入0.5 mol/L NaHCO3 浸提液10 mL,准确加水使各瓶的总体积达到45 mL,摇匀;11、最后加入钼锑抗试剂5 mL,混匀显色;12、同待测液一样进行比色,绘成标准曲线(最后溶液中流的浓度分别为0 ,0.1 ,0.2 ,0.3 ,0.4 ,0.5ug/mL P)。
土壤中磷含量的测定(比色法)一、现阶段测定土壤中磷含量主要方法有如下几种:(一)中性和石灰性土壤速效磷的测定 (0.5mol/L NaHCO3法)石灰性土壤由于大量游离碳酸钙存在,不能用酸溶液来提取有效磷。
一般用碳酸盐的碱溶液。
由于碳酸根的同离子效应,碳酸盐的碱溶液降低碳酸钙的溶解度,也就降低了溶液中钙的浓度,这样就有利于磷酸钙盐的提取。
同时由于碳酸盐的碱溶液,也降低了铝和铁离子的活性,有利于磷酸铝和磷酸铁的提取。
此外,碳酸氢钠碱溶液中存在着OH-、HCO3-、 CO32-等阴离子,有利于吸附态磷的置换,因此NaHCO3不仅适用石灰性土壤,也适应于中性和酸性土壤中速效磷的提取。
待测液中的磷用钼锑抗试剂显色,进行比色测定。
(二)酸性土壤速效磷的测定方法A(0.03mol/L NH4F-0.025mol/L HCl法)NH4F--HCI法主要提取酸溶性磷和吸附磷,包括大部分磷酸钙和一部分磷酸铝和磷酸铁。
因为在酸性溶液中氟离子能与三价铝离子和铁离子形成络合物,促使磷酸铝和磷酸铁的溶解:3NH4F+3HF+AlPO4一H3PO4+(NH4)3AlF63NH4F+3HF+FePO4一H3PO4+(NH4)3FeF6溶液中磷与钼酸铵作用生成磷钼杂多酸,在一定酸度下被SnCl2还原成磷钼蓝,蓝色深浅与磷的浓度成正比。
(三)酸性土壤速效磷的测定方法B0.05mol/L HCl-0.025mol/L ( 1/2H2SO4 )法本法特别适用于固定磷较强的酸性土壤。
如土壤有机质含量较低,pH小于6.5,阳离子交换量小于100 cmol/kg的土壤。
本法不仅适用于酸性土壤速效磷的测定,也能用以测定其酸性土壤速效磷的测定方法B 0.05mol/L HCl-0.025mol/L ( 1/2H2SO4 )法他有效养分。
(四)土壤有机磷的分离测定方法原理:土壤经550℃灼烧,使有机磷化合物转化为无机态磷,然后与未经灼烧的同一土样,分别用0.2mol/L(1/2H2SO4)溶液浸提后测定磷量,所得结果的差值即为有机磷。
土壤含磷量测定土壤含磷量测定土壤全磷的测定土壤全磷量即磷的总贮量,包括有机磷和无机磷两大类。
土壤中的磷素大部分是以迟效性状态存在,因此土壤全磷含量并不能作为土壤磷素供应的指标,全磷含量高时并不意味着磷素供应充足,而全磷含量低于某一水平时,却可能意味着磷素供应不足。
因此了解土壤磷总贮量,对生产实践仅有一定的参考价值。
土壤全磷测定的待测液制备,一般分为碱熔法和酸溶法两类。
在碱熔法中以Na2CO3熔融分解最为完全,准确度较高,但熔融时需要铂坩埚,不适宜用于常规分析。
在酸溶法中以H2SO4———HCLO4法较好。
此法对钙质土壤分解率较高,但对酸性土壤分解不易十分完全,结果往往稍微偏低。
待测液中磷的测定,一般都采用钼蓝比色法,所用的显色剂有“钼锑抗”(钼酸铵—酒石酸锑钾—抗坏血酸试剂的简称),氯化亚锡,抗坏血酸和1,2,4—氨基萘酚磺酸等。
其中钼锑抗法有手续简便,颜色稳定,干扰离子允许量大等优点,目前国内应用较广。
1.酸溶—钼锑抗比色法:(1)方法要点:在高温条件下,土壤中含磷矿物和有机磷化合物与高沸点的H2SO4和强氧化剂HCLO4作用,使之完全分解,全部转化为正磷盐而进入溶液,然后用钼锑抗比色法测定。
(2)主要仪器:分光光度计,2KVA方电炉,3KVA调压变压器。
(3)试剂:A.浓H2SO4(二级)。
B.HCLO4(二级,70~72%)。
C.钼锑贮存液。
浓H2SO4(二级)153毫升缓慢倒入约400毫升水中,搅拌,冷却。
10克钼酸铵(二级)溶解于约60。
C的300毫升水中,冷却。
然后将H2SO4溶液缓缓倒入钼酸铵溶液中,再加入100毫升0.5%酒石酸锑钾溶液,最后用水移释至1升,避光贮存。
此贮存液含1%钼酸铵,5.5摩尔/升1/2 H2SO4。
D.钼锑抗显色剂。
1.50克抗坏血酸溶液于100毫升钼锑贮存液中。
此液须随配随用,有效期一天。
E.二硝基酚指示剂。
0.2克2,6-二硝基酚或2,4二硝基酚溶于1000毫升水中。
中性、石灰性土壤有效磷的测定方法和注意事项作者:栾桂云来源:《河南农业·综合版》 2013年第21期河南省土壤肥料站栾桂云对土壤中有效磷含量的准确测定有助于改善土壤肥力及农作物的配置,同时对环境监测、环境保护等也具有重大意义。
土壤有效磷含量也被作为评价土壤肥力的重要指标之一,也是测土配方施肥技术中的常规项目之一。
对于中性、石灰性土壤有效磷的测定,目前国内外普遍采用Olsen法,此法优点甚为显著,但此法尚存在一定的限制因素,如测定结果随浸提温度的升高而增高、分析过程较繁琐、对土液比例、振荡时间及频率的要求严格等问题,造成测土分析速度慢,费工费时。
为进一步提高工作效率,提高测定的准确性,减轻劳动量,现将工作中的经验做以小结,以期为测土配方施肥提供指导。
一、中性、石灰性土壤中有效磷的测定方法(一)方法原理石灰性土壤由于大量游离碳酸钙存在,不能用酸溶液来提取有效磷,一般用0.5mol/LNaHCO3浸提,由于该浸提液提高了CO32-离子的活性,使其与Ca2+形成CaCO3沉淀,从而降低了Ca2+的活性,使一定量活性较大的Ca-P被浸出,同时也可使活性较大的Fe-P 和AI-P通过水解作用而浸出,从而增加了碳酸氢钠提取中性和石灰性土壤有效磷的能力。
由于浸出液中Ca、Fe、Al浓度较低,不会产生磷的再沉淀,浸提液中的磷可用钼锑抗比色法测定。
(二)试剂及其配制1、氢氧化钠:10%(m/V)溶液。
2、碳酸氢钠浸提剂[c(NaHCO3)=0.50mol·L-1,pH=8.5]称取42.0gNaHCO3溶于950mL水中,用10%氢氧化钠溶液调节pH值至8.5(用酸度计测定),用水稀释至1L。
贮存于塑料瓶中备用。
如贮存期超过20d,使用时须重新校正pH值。
3、酒石酸锑钾[K(SbO)C4H4O6·1/2H2O]:0.30%(m/V)溶液。
4、钼锑贮备液:取10.0g钼酸铵溶于约60℃的300mL水中,冷却。
两种石灰性土壤有效磷测定方法比较李娟;张静月;王蓉;韩新盛;冯婷婷【摘要】本文用两种方法测定石灰性土壤有效磷含量.实验结果表明,两种方法的检测结果平均值均在误差范围之内,测定结果间没有显著性差异;方法二中不加活性炭条件下,在波长880 nm处能够有效地去除土壤有机质背景的干扰,测定结果与加活性炭法测定结果间无显著性差异,而且该方法准确、简单、快捷、成本低.因此,采用紫外可见分光光度计于波长880 nm处比色能够准确地测定土壤有效磷含量,有利于提高工作效率,降低检测成本.【期刊名称】《宁夏农林科技》【年(卷),期】2017(058)011【总页数】3页(P31-33)【关键词】石灰性土壤;有效磷;活性炭;紫外可见分光光度计【作者】李娟;张静月;王蓉;韩新盛;冯婷婷【作者单位】宁夏农业勘查设计院/农业部农产品质量安全监督检验测试中心(银川),宁夏银川 750002;宁夏农业勘查设计院/农业部农产品质量安全监督检验测试中心(银川),宁夏银川 750002;宁夏农业勘查设计院/农业部农产品质量安全监督检验测试中心(银川),宁夏银川 750002;银川西部供水有限公司,宁夏银川 750021;宁夏农业勘查设计院/农业部农产品质量安全监督检验测试中心(银川),宁夏银川750002【正文语种】中文【中图分类】S158;X833土壤有效磷是反映土壤肥力状况的一个重要指标,测定土壤有效磷含量可以了解土壤中磷素供应的能力[1],对合理施肥、改良土壤、提高产量和保护环境有重要的参考价值。
测定石灰性土壤有效磷含量最常用的方法是碳酸氢钠浸提-钼锑抗比色法(Olsen法)。
该方法在测定有效磷的过程中,由于土壤中有机质有很强的吸收背景,对有效磷的测定造成极大的干扰,必须去除其干扰,才可以准确地测定有效磷的含量[2]。
根据《土壤分析技术规范》[3]中有效磷的检测方法,可采用无磷活性炭吸附的办法去除有机质的干扰;也可以按照NY/T 1121.7—2014石灰性土壤有效磷测定方法[4],采用紫外可见分光光度计于波长880 nm处比色,此波长处对浸出的有机质已基本无吸收,这样就可以很好地去除有机质背景对有效磷测定结果的干扰,浸提时可不加活性炭[2]。
土壤无机磷分级的测定步骤:(l) Ca2--P的测定:称取过100目筛孔的风干土壤样品1.00g,置于100ml离心管中,加入碳酸氢钠溶液(0.25mol·L-1,pH7.5)50ml。
在20-25℃温度下振荡l小时,离心(3500r·min-1,约8min)。
上层清液倒入50ml三角瓶中,吸取上述清液10ml容量瓶中,加水稀释至约30ml,加二硝基酚指示剂2滴,用氢氧化钠溶液及稀硫酸溶液调节pH至深液呈微黄色。
然后加入钼锑抗显色剂5ml,摇匀,用水定容。
在25℃下显色30min后,在分光光度计上用波长700nm比色,以空白试验溶液为参比液调零点,读取吸收值,在工作曲线上查出显色液的Pmg·L-1。
工作曲线的绘制:分别吸取5mg/kg P标准溶液0,1,2,3,4,5,6ml于50ml容量瓶中,加水稀释至约30ml,加入钼锑抗显色液5ml,定容,摇匀。
即得0,0.1,0.2,0.3,0.4,0.5,0.6mg/kg P标准系列溶液,与待测液同时比色。
在半对数纸上以透光度为纵坐标,Pmg/kg为横坐标,绘制成工作曲线。
(2)Ca8-P的测定:浸提过Ca2-P的土样,用95%的乙醇洗两次(每次25ml)。
然后加乙酸铵溶液(0.5mol·L-1,pH4.2)50ml,将土块充分分散后放置4小时,待CO2逸出后在20-25℃温度下振荡1小时。
离心,将上清液倒入三角瓶中。
吸取浸出液20ml于50ml容量瓶中,调节酸碱度后,定容,比色测定。
(3) Ca10-P的测定:浸提过O-P的土样加入硫酸溶液(0.5mol·L-1)50ml,在20-25℃温度下振荡1小时,离心,倒出上层清液于三角瓶中。
吸取5ml浸出液于50ml容量瓶中,用钼锑抗比色法测定磷。
(4)结果计算:土壤中P,mg/kg=(显色液Pmg/kg*显色液体积*分取倍数)/W式中:显色液Pmg/kg-----从工作曲线上查得的Pmg/ kg数;显色液体积---50ml分取倍数----浸出液总体积/吸取浸出液体积w----土样重(g)。
石灰性土壤无机磷分级的测定河北省地矿中心实验室 有机有机分析分析分析室室 (参考参考蒋柏藩蒋柏藩蒋柏藩等的等的等的资料资料资料整理整理整理))1范围本方法适用于石灰性土壤中Ca2-P、Ca8-P、Al-P、Fe-P、O-P、Ca10-P 无机磷的6级分级测定。
2原理土壤中不同形态的磷被适当的提取剂震荡提取,采用钼锑抗比色法测定提取液,吸光度与磷的含量成正比,与标准系列比较定量。
3试剂3.1 NaHCO 3溶液(pH=7.5):称取21.0g NaHCO 3溶于990mL 水中,用1:1HCl 调节pH=7.5,用水稀释至1L ,塑料瓶中保存(不宜久放)。
3.2 HN 4AC 溶液(pH=4.2):量取29.5mL 冰醋酸于800mL 水中,用氨水调节pH=4.2,用水稀释至1L 保存。
3.4 HN 4F 溶液(pH=8.2): 称取18.5g HN 4F 溶于990mL 水中,用4mol/L HN 4OH 调节pH=8.2,用水稀释至1L ,塑料瓶中保存。
3.5 NaOH-Na 2CO 3溶液: 称取5.3g 无水Na 2CO 3和4.0gNaOH 溶于800mL 水中,用水稀释至1L ,塑料瓶中保存。
3.6 柠檬酸钠溶液:称取88.2g 柠檬酸三钠(Na 3C 6H 5O 7•2H 2O )溶于900mL 热水中,用水稀释至1L 。
3.7 NaOH 溶液: 称取20g NaOH 溶于800mL 水中,用水稀释至1L ,塑料瓶中保存。
3.8 H2SO4溶液: 15mL浓H2SO4、溶于约800mL水中,稀释至1升。
3.9饱和NaCl溶液:400gNaCl溶于1升水中,待溶液呈饱和后使用。
3.10 H3B03溶液:49g硼酸溶于900mL热水中,冷却后稀释至1升。
3.11三酸混合液:H2SO4:HCIO4:HNO3以1:2:7的体积比混合。
3.12连二亚硫酸钠(保险粉Na2S2O4) 密封避光、防潮保存。
3.13 钼锑贮存液:153mL浓H2SO4缓慢地倒入约400mL水中,搅拌,冷却。
10克钼酸铵溶于约60℃的300mL水中,冷却。
然后将H2SO4溶液缓缓倒入钼酸铵溶液中,再加入100mL0.5%酒石酸锑钾(KSbOC4H4O6·l/2H2O)溶液,最后用水稀释至1升,避光贮存。
此贮SO4。
存液含1%钼酸铵、5.5N H23.14钼锑抗显色剂:1.5g抗坏血酸(C6H8:O6,左旋,旋光度+21-22℃)溶于100mL钼锑贮存液中。
此液须随配随用,有效期一天。
3.15二硝基酚指示剂:0.2g2,6-二硝基酚或2,4-二硝基酚溶于100mL 水中。
3.16 磷标准溶液:称取0.4390gKH2PO4(二级,105℃烘2小时)溶于200mL水中,加入5mL浓H2SO4,转入1升容量瓶中,定容。
此为100μg/mLP标准溶液,可长期保存。
取此溶液准确稀择20倍,即为5μg/mLP标准溶液,此溶液不宜久存。
4仪器4.1分光光度计:T6 谱析通用4.2 振动器:HY-4 国华电器4.3 恒温水浴锅:六孔恒温水浴锅中兴电器5操作步骤5.1 NaHCO3溶性磷(Ca2-P型)的测定:称取土壤样品1.000g(通过100(3.1)溶液50mL,振荡目筛),置于100mL离心管中,加NaHCO31小时(20~25℃),离心(3500转/分,约8分钟)上层清液倾入50mL 三角瓶中,吸取上述清液5~20mL于50ml容量瓶中,用水稀释到25mL左右,加入2滴二硝基酚指示剂,用稀H2SO4或NH4OH溶液调至溶液呈微黄色,然后加入5mL钼锑抗显色剂,用水稀释至刻度,摇匀,在>15℃的环境中放置半小时后,于分光光度计上用波长700nm比色测定磷。
工作曲线的绘制分别吸取5μg/mLP标准溶液0,1,2,3,4,5,6mL 于50mL容量瓶中,加水稀释至约30mL,加入钼锑抗显色液5mL,定容,摇匀。
即得0,0.1,0.2,0.3,0.4,0.5,0.6μg/mLP标准系列溶液,与待测液同时比色。
以透光度为纵坐标,P浓度为横坐标,绘制工作曲线。
5.2 NH4Ac溶性磷(Ca8-P型)的测定: 将经NaHCO3溶液浸提过的土壤,用95%的酒精洗两次(每次25mL,离心后弃去清液)。
然后加NH4Ac(3.2)溶液50mL,将土块充分分散,放置4小时,待CO2逸出后在20~25℃振荡1小时,离心。
倾出上层清液于三角瓶中。
吸取浸提液2~5mL于50mL容量瓶中,用钼锑抗法比色测定磷(同NaHCO3溶性磷测定)。
5.3 NH4F溶性磷(Al-P型)的测定:将经NH4AC溶液浸提过的土壤用饱和NaCI溶液洗两次(每次25mL,离心后弃去清液)。
然后加入NH4F(3.3)溶液50mL,在20~25℃振荡1小时,离心,将上层清液倾入塑料瓶中。
吸取浸出液10~20mL容量瓶中,加入与吸取的浸BO3(3.9)溶液。
再加2滴二硝基酚指示剂,用提液体积相等的H3OH溶液将待测液调至微黄色,然后加入5mL钼锑抗稀HCI和NH4显色剂,定容,在40℃的烘箱中保温1小时,取出冷却,比色(同NaHCO3溶性磷测定)。
颜色在2小时内可保持稳定。
5.4 NaOH-Na2CO3溶性磷(Fe-P型)的测定:将经NH4F溶液浸提过的土壤用饱和NaCL溶液洗两次(每次25mL,离心后弃去清液)。
然后加入NaOH-NaCO3(3.5)溶液50mL,振荡2小时,静置16小时,2再振荡2小时,离心(约4500转/分,8-10分钟)。
倾出上层清液于三角瓶中,并在浸出液中加入1.5mL浓HSO4 (在结果计算时应考虑加2SO4的体积),摇匀后过滤,以除去凝絮的有机质。
吸取适量滤入H2溶性磷测定)。
液(一般在5~20ml),比色测定磷(同NaHCO35.5 闭蓄态磷(O-P型)的测定:将经NaOH-Na2CO3溶液浸提过的土壤用饱和NaCI溶液洗两次(每次25mL,离心后弃去清液)。
然后加入柠檬酸钠溶液(3.6)40mL,充分搅碎土块,再加1g连二亚硫酸钠(保险粉),放入80~90℃的水浴中,待离心管内溶液温度和水浴温度平衡后,用电动搅拌机搅拌15分钟,再加入NaOH(3.7)10mL,继续搅拌10分钟,冷却后离心。
将上层清液倾入100mL容量瓶中。
土壤用饱和NaCL溶液洗两次(每次20mL),离心后上层清液一并倒入容量瓶中,用水定容。
吸取上述溶液10mL于50mL三角瓶中,加入三酸混合液10mL,瓶口上放一小漏斗,在电炉上消煮,逐步升高温度,待HNO3和HCIO4全部分解,瓶壁有H2SO4回流时即可取下。
冷却后成白色固体。
加入30mL水,煮沸,使固体全部溶解后,用水洗入50 mL容量瓶中,定容。
吸取30mL溶液于50mL容量瓶中,比色测定磷(同NaHCO3溶性磷测定)。
同时作试剂空白试验。
5.6 H2SO4溶性磷(Ca10-P型)的测定:浸提过O-P的土壤加入H2SO4溶液(3.10)50mL,振荡1小时,离心,倾出上层清液于三角瓶中。
吸取浸出液1~5ml于50ml容量瓶中,比色测定磷(同NaHCO3溶性磷的测定)。
6主要影响因素的讨论6.1试验样品的制备以甲方提供的样品作为试验样品,各种形态含量如下。
磷酸盐形态测定值M:PO4(M为金属离子)CaHPO4•2H2O 0.94:1Ca8H2(PO4)6•5H2O 1.32:1Ca10(PO4)6•F2 1.61:1FePO4•2H2O 0.99:1AlPO4•nH2O 0.81:16.2 NaHCO3浓度及pH值的影响:图一是pH8.5浓度从0.1M~0.5M的NaHCO3分别对各种磷酸盐试样进行的最大溶解量的测试结果。
浸提温度为20℃,振荡1小时(以下除另有注明外,均同)。
NaHCO3对Ca2-P(代表CaHPO4·2H2O,下同)的溶解量很高,且随着NaHCO3浓度的增加而递增,变幅大致在120-300ppmP2O5;对Ca8-P(代表Ca8H2(PO4)6·5H2O,下同)、Ca10-P(代表Ca10(PO4)6·F2,下同)和Al-P(代表AlPO4·nH2O,下同)的最大溶解量极低,而且基本保持平稳,最高量也只在6ppm以下;对Fe-P则随NaHCO3浓度的增加而增加,但最高溶解量也仅15ppm左右。
总的看,NaHCO3作为Ca2-P的专性浸提剂与其它磷酸盐的溶解量相比,应该是可以的。
图二是在图一的基础上,调控0.25M NaHCO3的PH对各种磷酸盐的最大溶解量的测试结果。
由图二可知,随着NaHCO3的PH的增大,Ca2-P的溶解量由190降至160ppm P2O5;而Al-P和Fe-P的溶解量随着PH的增大而增大,Ca8-P则相反。
从表观看,Ca2-P与其磷酸盐相比,溶解量大至差10倍以上。
6.3 NH4AC浓度及pH值的影响:图三是PH7.0浓度从0.1~0.5M的NH4AC对4种磷酸盐的测试结果,测试条件同NaHCO3。
结果表明,NHAC对Ca8-P的浸提量很高,且随NH4AC浓度的增加4-P、Al-P和Fe-P的最大而增加,变幅量大致在60~120ppm;对Ca10溶解量其绝对值均不超过1.3ppm。
图四是0.5M、PH4.0~7.0的NHAC的测试结果。
4-P溶解量显著增加,Ca8-P的最大溶解由图可知,PH降低,Ca8量与Ca-P的差距大致在200倍左右。
Al-P和Fe-P的溶解量不仅很10低,而且不受PH变化影响。
6.4 NaOH- Na2CO3浓度的影响:表三表明,在Na2CO3存在的情况下,CO3对Fe-P的浸提率都较低。
但无论是0.1M NaOH或者是0.5MNa20.1M NaOH-0.5MNa2CO3混合浸提液对Fe-P的浸提率,无论Na2CO3存在与否,两者基本吻合,而且比较理想,浸提率达95%。
这表明,在石灰性土壤中用0.1M NaOH浸提Fe-P时有严重的次生反应的干扰。
处理N aO H0.1N N a2CO30.5M N aO H0.1N-N a2CO30.5MFe-PFe-P+CaCaO393.473.448.648.997.494.8。