2021年氧化钙含量测定方法
- 格式:doc
- 大小:17.00 KB
- 文档页数:3


氧化钙和氢氧化钙混合后含量检测
氧化钙(CaO)和氢氧化钙(Ca(OH)2)混合后的含量检测是一个重要的化学分析问题。
首先,我们需要明确混合物中氧化钙和氢氧化钙的含量检测方法。
对于氧化钙,可以使用酸碱滴定法,将氧化钙溶解后与酸进行滴定来测定其含量。
而对于氢氧化钙,可以使用酸碱中和滴定法或者直接加热分解后测定氢氧化钙中的氢氧化钙含量。
其次,需要考虑混合物中氧化钙和氢氧化钙的质量比例。
通过化学计算,可以根据混合物中两者的质量比例,来确定混合物中氧化钙和氢氧化钙的含量。
另外,还可以利用仪器分析方法,比如X射线荧光分析仪、原子吸收光谱仪等,来对混合物中氧化钙和氢氧化钙进行定量分析。
最后,需要注意的是在进行含量检测时,要注意样品的制备和处理过程,确保样品的代表性和准确性。
另外,实验操作过程中要严格遵守安全操作规程,确保实验过程安全。
综上所述,氧化钙和氢氧化钙混合物的含量检测涉及到化学分
析方法、质量比例计算和仪器分析等多个方面,需要综合考虑并严格操作,才能准确地确定混合物中氧化钙和氢氧化钙的含量。

敞口放置的氧化钙测定其成分
敞口放置的氧化钙是指暴露在空气中的氧化钙样品。
氧化钙是
一种无机化合物,化学式为CaO。
在常温下,氧化钙会与空气中的
水和二氧化碳发生反应,形成氢氧化钙和碳酸钙。
因此,氧化钙的
成分主要包括氧化钙本身以及与空气中的水和二氧化碳发生反应后
生成的氢氧化钙和碳酸钙。
要测定氧化钙的成分,首先可以使用化学分析方法。
通过适当
的实验操作,可以将氢氧化钙和碳酸钙转化为其他化合物,然后通
过质量差异计算出氧化钙的含量。
另外,也可以利用仪器分析技术,如X射线衍射(XRD)或者红外光谱(IR)等方法对氧化钙样品进行分析,从而确定其中各种化合物的含量。
此外,还可以从应用角度来考虑氧化钙的成分。
比如,如果氧
化钙用于工业生产中,可以关注氧化钙样品中杂质的含量对产品质
量的影响。
另外,如果氧化钙用于环境保护或者建筑材料中,可以
关注样品中水和二氧化碳含量对材料性能的影响。
总的来说,测定氧化钙的成分需要综合运用化学分析方法和仪
器分析技术,同时也需要考虑样品的应用背景,以便全面准确地确定其成分。

关于粉煤灰中游离氧化钙含量测定的探讨摘要:介绍了测定粉煤灰中游离氧化钙的常规实验室方法,分析了由此衍生的蔗糖法、微波法、设备快速测定法的优势,供参考。
关键词:粉煤灰;游离氧化钙;实验室测量0.引言粉煤灰是指从煤燃烧后产生的烟气中收捕而来的细灰,是火力发电厂发电过程中产生的最主要的固体废物[1]。
近年来,随着环保理念逐渐深入人心,人们更认识到提高资源利用率的重要性。
如果在粉煤灰中存在过高含量的游离状氧化钙,则表明煤的燃烧还不够充分,而使用这样的粉煤灰制作含硫硅酸盐石膏等替代天然石膏的物品时,基于游离状氧化钙不稳定的特性,会导致应用安全问题。
故精确测量粉煤灰中游离状氧化钙含量至关重要。
1.最常用的粉煤灰中游离氧化钙含量实验室测定方法1.1原理解析向装有粉煤灰的烧杯中加入适量乙二醇溶液后,加热溶液,待其达到沸点后,乙二醇成分会与游离氧化钙发生化学反应,生成的物质为具备较强可溶性的乙二醇钙。
加入酚酞(用作指示剂),此时,向其中加入苯甲酸-无水乙醇标准滴定溶液,行滴定操作,便可测定出粉煤灰中的游离氧化钙含量。
1.2仪器设备及材料准备(1)游离氧化钙测量仪;(2)高温电阻炉(用于加热,最高温度可达1200℃);(3)容量达到1000ml的容量瓶1个、250ml的抽滤瓶和锥形瓶各1个、50ml的量筒1个、1000ml的量杯两个、50ml的酸式滴定管1个、用于搅拌玻璃棒的烧杯若干、用于转移溶液的移液管若干、自带胶塞的玻璃瓶若干。
(4)氢氧化钠分析纯(调节酸碱度至碱性环境用);(5)体积分数达到99%的乙二醇;(6)体积分数至少达到99.5%的乙醇(无水);(7)酚酞(用于指示剂作用);(8)苯甲酸分析纯。
1.3测定实验前的试剂配比准备(1)配置乙二醇-无水乙醇溶液。
配比剂量为2∶1。
具体方法为:①选择1000ml乙二醇,加入500ml无水乙醇后,使用玻璃棒进行搅拌;②向其中加入约0.2g的酚酞,混合均匀后备用。

专题21 流程图题1.(2021·湖南怀化市·中考真题)在实际生产中,常采用足量NaOH 溶液来“捕捉”(吸收)CO 2,部分流程图如下。
(1)大量CO 2直接排放到空气中会导致______的加剧,破坏人类生存的环境。
捕捉室内反应的化学方程式为______。
(2)操作①的名称______,所用到的玻璃仪器有烧杯、玻璃棒和______。
(3)往纯碱溶液中加入X 溶液,得到NaOH 溶液和CaCO 3,X 的化学式是______。
(4)整个流程中可以循环使用的物质是______。
(5)若要确认“捕捉”后的气体中CO 2含量已经降得很低,先分别取一瓶“捕捉”前和一瓶“捕捉”后的气体,接下来的实验操作是______。
【答案】(1)温室效应 22322NaOH+CO Na CO +H =O(2)过滤 漏斗(3)Ca(OH)2(4)氢氧化钠、氧化钙(5)加入等量澄清石灰水,观察变浑浊情况【详解】(1)大量CO 2直接排放到空气中会导致温室效应的加剧,破坏人类生存的环境。
由流程可知,捕捉室内反应为氢氧化钠和二氧化碳反应生成碳酸钠和水:22322NaOH+CO Na CO +H =O 。
(2)操作①为分离固液的操作,名称为过滤;所用到的玻璃仪器有烧杯、玻璃棒和漏斗。
(3)反应前后元素种类不变,往纯碱溶液中加入X 溶液,得到NaOH 溶液和CaCO 3,则X 为氢氧化钙Ca(OH)2。
(4)整个流程中氢氧化钠、氧化钙既是反应物也是生成物,故可以循环使用的物质是氢氧化钠、氧化钙。
(5)二氧化碳能使澄清石灰水变浑浊,若要确认“捕捉”后的气体中CO 2含量已经降得很低,先分别取一瓶“捕捉”前和一瓶“捕捉”后的气体,加入等量澄清石灰水,观察变浑浊情况。
2.(2021·湖南株洲市·中考真题)镁铝合金是重要的航天航空材料,下图是由废弃镁铝合金为原料来制备化工原料硫酸镁和硫酸铝的流程:(1)操作Ⅰ的名称为___________,操作Ⅰ的注意事项为___________。

蔗糖法测氧化钙含量有用氧化钙的测定有如下两种办法:蔗糖法道理,氧化钙在水中的消融度很小,20℃时消融度为 1.29g/参加蔗糖就可使之成消融度大的蔗糖钙,再用酸滴定蔗糖钙中的氧化钙的含量,反响如下:C12H22O11+CaO+2H2O─→C12H12O11CaO+2H2OC12H22O22O11CaO+2H2O+2HCl→C11H22O11+CaCl2+3H2O试剂:蔗糖:化学纯.酸:0.5mol/l尺度溶液.(0.5mol/LHCl溶液:量取45毫升盐酸,迟缓注入1000ml水.)酚酞指导剂.操纵:敏捷精确称取0.4~0.5g研成细粉的试样,置于250ml具有磨口玻塞的锥形瓶中,参加4g化学纯蔗糖及小玻球12~20粒,再参加新煮沸罢了冷却的蒸馏水40ml.塞紧瓶塞.动摇15min,以酚酞为指导剂,用0.5mol/l酸尺度溶液滴定至红色正好消掉,并在30s内不再现红色为止.盘算按下式盘算有用氧化钙的含量:式中:N──酸尺度溶液的浓度;V──滴准时所耗用的酸尺度液的量(ml);W──试样量(g)).留意事项测准时,不该使氧化钙生成碳酸钙,所以要用新煮沸过而尽量除去二氧化碳的蒸馏水,以免氧化钙溶于水后生成的氢氧化钙进一步与二氧化碳感化生成碳酸钙,使消费的酸尺度溶液量偏低.再者,因蔗糖只与氧化钙感化,而不与碳酸钙感化,所以称量试样要迅束,不然氧化钙会接收空气中的二氧化碳变成碳酸钙,导致成果偏低.酸量法测氧化钙含量酸量法道理有用氧化钙溶于水后生成氢氧化钙,可用酸滴定氢氧化钙,从而测出有用氧化钙的含量. 反响如下:CaO+H2O ─→Ca (OH )2Ca (OH )2+2HCl ─→CaCl2+2H2O试剂:0.1mol/l 酸尺度溶液.(0.1mol/L HCL 溶液:量取9毫升盐酸,迟缓注入1000ml 水.)酚酞指导剂.测定办法:精确称取研磨细的试样1g 阁下,置于烧杯内,参加刚煮沸过的蒸馏水约300ml,搅匀后全体转移至1000ml 的容量瓶中,将瓶加塞不时动摇,约20min 后冷却,再参加新煮沸已冷蒸馏水至刻度.混匀,过滤(过滤要敏捷).弃去最初100ml 滤液,汲取50ml 入锥形瓶中,以酚酞为指导剂,用0.1mol/l 酸尺度溶液滴定至红色消掉且30秒不再消失即为终点. 盘算:CaO(%)=50*W NV28×100试中各项意义同蔗糖法.留意事项所应用的蒸馏水必须从新煮沸过.过滤要敏捷,以免氢氧化钙接收空气中的二氧化碳变成碳酸钙,而使成果偏低。

2021.N〇.4杨飞,等:利用蒸汽动能磨中的过热蒸汽消解固硫灰中f-CaO的研究-5 -动能磨对固硫灰进行超细粉碎,得到如下结论:当分级轮转速为300 r/min和600 r/min时,固硫灰中的 f-CaO含量分别为3.84%和4.02%,蒸汽动能磨对固 硫灰中f-CaO的消解程度不大;当分级轮转速提升 至1200 r/min时,固硫灰中的f-CaO含量为0.丨1%,颗 粒粒度变细,f-CaO含量降低。
蒸汽动能磨中的高温 蒸汽在粉碎加工固硫灰的过程中能有效消解固硫灰 中的f-CaO,解决了固硫灰掺入水泥混凝土后由于 f-CaO造成的安定性不良的问题,为提高固硫灰的利 用提供了一种可行的方法。
参考文献:[1] ANTHONY E J. Fluidized bed combustion of alternative solid fuels;status, successes and problems of the technology [J]. Progress in Energy and Combustion Science, 1997,21(3): 239-268.[2] ANTHONY E J, GRANATSTEIN D L. Sulphation Phenomena in Fluidized Bed Combustion [J]. progress in energy and combustion science, 2001,27(2): 215-236.[3] PARK S M, SEO J H, LEE H K. Binder chemistry of sodium carbonate-activated CFBC fly ash [J]. Materials & Structures, 2018, 51[3] : 59.[4] PARK S M, LEE N K, LEE H K. Circulating fluidized bed combustion ash as controlled low-strength material (CLSM)by alkaline activation [J]. Construction & Building Materials, 2017, 156: 728-738. [5] SHENG G, QIN L, ZHAI J. Investigation on the hydration of CFBC fly ash [J]. Fuel, 2012,98: 61-66.[6]李端乐.掺超细循环流化床粉煤灰水泥的特性研究[D].北京:中国矿业大学,2018.p]陈德玉,陈鑫林,刘元正,等.固硫灰的膨胀及其控制m.四川大学学报(丁.程科学版),2015,47(2): 198-204+8.[8] CHENG C Y, YANG Y N, HUANG A N, et al. Steam hydration of CFBC bottom ashes in a rotary kiln [J]. Journal of the Taiwan Institute of Chemical Engineers, 2013,44(6):1060-1066.[9] CHEN X, GAO J, YAN Y, et al. Investigation of expansion properties of cement paste with circulating fluidized bed fly ash [J]. Construction & Building Materials, 2017, 157:1154-1162.[10] BURWELL S M, ANTHONY E J, BERRY E E. Advanced FBCash treatment technologies [M], 1995.[11] ZHAO Q Q, SCHURR G. Effect of motive gases on fine grindingin a fluid energy mill [J]. Powder Technology, 2002, 122(2):129-135. [12] ZHANG M X, CHEN H Y, et al. Steam jet mill-a prospective solution to industrial exhaust steam and solid waste [J]. Environmental Science & Pollution Research, 2018,25(18):1-13.[13] JUAN L, YU F, LIHUA H, et al. Preparation of a new high- performance calcium-based desulfurizer using a steam jet mill [J]. J Hazard Mater, 2020, 389.[14]杜君,刘家祥,李敏.乙二醇-EDTA滴定法与热解重量-示 差热分析法相结合测定钢渣中游离氧化钙含量m.理化检验(化学分 册),2013,49(8): 961-964.[15] WU Y, ANTHONY E J, JIA L. Experimental Studies on Hydration of Partially Sulphated CFBC Ash [J]. Canadian Journal of Chemical Engineering, 2003,81(6):1200-1214.[16]张志伟,钱觉时,张克,等.固硫灰渣中游离氧化钙测试方法 的影响因素研究[J].材料导报,2011,14: 122-125.[17]陈仕国,王群英,刘战礼,等.固硫灰中游离CaO分布与消解研 究[J].科学技术与工程,2016, 16(27): 270-274.(编辑胡如进)《水泥》杂志2021年选题与征稿启事2021年重点选题(但不限于):★水泥工业碳达峰、碳中和,碳减排,碳捕集、利用及封存技术,低碳生产技术,碳市场交易介绍等;★水泥窑协同处置技术应用实践(包括协同处置医疗垃圾、生活垃圾、市政污水污泥、污染土壤、垃圾焚烧底灰及飞灰等);★高性能水泥及特种水泥的生产与相关标准(如核电水泥、超轻水泥、大坝水泥及一些重大工程专用水泥等);★绿色工厂建设、生态水泥生产技术及绿色工厂评价等;★脱硫、脱硝、除尘等超低排放技术在水泥厂的应用实践;★5G技术与机器人等智能控制、物联网与互联网+在水泥行业的应用;★国内外新技术、新装备、新工艺(包括“两个二代”)介绍;★科研院所的新的研究成果及探索实践,优秀的毕业论文等;★新开辟"水泥与混凝土”栏目,适量报道有关砂石骨料与混凝土性能方面的文章。

2021年高考化学真题分项解析专题14《无机综合与推断》1.【xx新课标Ⅰ卷理综化学】(14分)硼及其化合物在工业上有许多用途。
以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:回答下列问题:(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式_____________。
为提高浸出速率,除适当增加硫酸浓度浓度外,还可采取的措施有_________(写出两条)。
(2)利用的磁性,可将其从“浸渣”中分离。
“浸渣”中还剩余的物质是______(写化学式)。
(3)“净化除杂”需先加H2O2溶液,作用是_______。
然后再调节溶液的pH约为5,目的是________。
(4)“粗硼酸”中的主要杂质是(填名称)。
(5)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为_______。
(6)单质硼可用于生成具有优良抗冲击性能硼钢。
以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程___________。
【答案】(1) Mg2B2O5·H2O+2H2SO42MgSO4+2H3BO3;减小铁硼矿粉粒径、提高反应温度。
(2) Fe3O4; SiO2和CaSO4;(3)将Fe2+氧化为Fe3+;使Al3+与Fe3+形成氢氧化物而除去。
(4)(七水)硫酸镁(5)(6) 2H3BO3 B2O3+3HO B2O3+3Mg 3MgO+2B【考点定位】元素及其化合物知识;化学工艺常识;物质结构。
本题是以化学工艺为素材,选材冷僻,试题难度为很难等级。
【名师点晴】我认为这道题是一道好题,层次分明,有区分度。
本题有考查“双基”——提速措施;四氧化三铁的磁性;制单质硼的反应。
也有考查知识综合运用能力——Mg2B2O5·H2O与硫酸反应;净化除杂两步实验操作的作用;两处成分的判断。
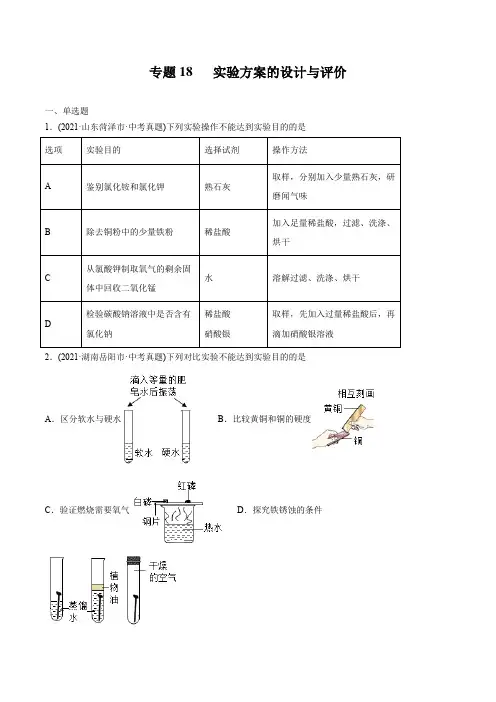
专题18 实验方案的设计与评价一、单选题1.(2021·山东菏泽市·中考真题)下列实验操作不能达到实验目的的是2.(2021·湖南岳阳市·中考真题)下列对比实验不能达到实验目的的是A.区分软水与硬水B.比较黄铜和铜的硬度C.验证燃烧需要氧气D.探究铁锈蚀的条件3.(2021·湖南岳阳市·中考真题)实验室常用以下装置来制取和收集气体。
下列说法正确的是A.实验室制取氧气时,可选用③或⑤作为收集装置B.检验④中CO2是否收集满:将燃着的木条伸入集气瓶内,看木条是否熄灭C.用①、⑤制取并收集气体完毕后,应先熄灭酒精灯,再将导管移出水面D.用锌粒和稀硫酸制取氢气,可选用②作为发生装置4.(2021·湖南岳阳市·中考真题)下列实验的现象和结论均正确的是①CO2溶解性实验②电解水实验③探究盐酸与氢氧化钠溶液是否反应④用小木棍蘸少量的浓硫酸5.(2021·江苏南京市·中考真题)某兴趣小组利用压强传感器研究氢氧化钠溶液吸收二氧化碳的情况。
用3个250mL的烧瓶收集满纯净的二氧化碳,连接压强传感器,同时采集数据,用注射器同时等速度分别注入三种不同浓度的氢氧化钠溶液各15mL,片刻后,同时振荡烧瓶,等待反应完成。
采集的数据如图所示。
下列说法正确的是A.0~t1段曲线呈现这种形态是因为注入氢氧化钠溶液后未进行振荡B.t1~t2段曲线呈现这种形态是因为注入氢氧化钠溶液后进行振荡C.a、b、c三种曲线所示的实验中,t3时烧瓶内压强由大到小的顺序是a>b>cD.a、b、c三种曲线所示的实验中,t3时被吸收的二氧化碳的体积由大到小的顺序是a>b>c 6.(2021·江苏南京市·中考真题)根据下列实验事实得出的结论不正确的是7.(2021·山西中考真题)设计实验方案,分析实验原理,解决实验问题,是化学独特的学科思想。

2021年道路工程试卷和答案(35)一、单选题(共35题)1.粗集料洛杉矶磨耗试验对水泥混凝土集料设定回转次数为()转。
A:250B:400C:500D:1000【答案】:C【解析】:粗集料洛杉矶磨耗试验对水泥混凝土集料设定回转次数为500转。
2.下述特点,不属于连续级配的特点有()。
A:内摩阻力相对较小B:温度稳定性好C:细集料多,粗集料较少D:空隙率较小,密实耐久【答案】:B【解析】:级配的特点:细集料多,粗集料较少,悬浮于细集料中,不能形成嵌挤骨架,空隙率较小。
连续级配混合料密实耐久、内摩阻力相对较小,高温稳定性较差。
3.沥青混合料车辙试验的评价指标为()。
A:稳定度B:残留稳定度C:动稳定度D:残留强度比【答案】:C【解析】:依据沥青混合料车辙试验(JTGE20-2011T0719),车辙试验的评价指标为动稳定度DS。
4.填石路基边线与边坡不应出现单向累计长度()的弯折。
上边坡也不得有危石。
A:超过20mB:超过30mC:超过50mD:超过60m【答案】:C【解析】:填石路基边线与边坡不应出现单向累计长度超过50m的弯折。
上边坡也不得有危石。
5.土工格栅的拉伸试验,每个试样至少为()宽,并具有足够长度。
A:100mmB:150mmC:300mmD:200mm【答案】:D【解析】:无纺类土工织物试样宽度为200mm±1mm(不包括边缘)。
6.采用真空法测定沥青混合料的理论最大相对密度,若抽气不干净或试样不干燥,测得的结果将分别()。
A:偏小、偏大B:偏小、偏小C:偏大、偏大D:偏大、偏小【答案】:A【解析】:依据沥青混合料理论最大相对密度试验(真空法)(JTGE20-2011T0711),若抽气不干净,残留的气体就计入了沥青混合料的理论体积中,测得的体积偏大,则测得的密度结果将偏小;若试样不干燥,说明试样中有水,测得的沥青混合料的质量就偏大了,则测得的密度结果将偏大。
7.《沥青喷洒法施工沥青用量测试方法》不能适用于检测()中的沥青材料数量。

绝密 启用并使用完毕前济南市2022年1月高一年级学情检测化学试题注意事项:1.答题前,考生先将自己的姓名㊁考生号㊁座号填写在相应位置,认真核对条形码上的姓名㊁考生号和座号,并将条形码粘贴在指定位置上.2.选择题答案必须使用2B铅笔(按填涂样例)正确填涂;非选择题答案必须使用0.5毫米黑色签字笔书写,字体工整㊁笔迹清楚.3.请按照题号在各题目的答题区域内作答,超出答题区域书写的答案无效;在草稿纸㊁试题卷上答题无效.保持卡面清洁,不折叠㊁不破损.可能用到的相对原子质量:H1㊀C12㊀N14㊀O16㊀M g24㊀S32㊀C l35.5㊀K39C a40㊀M n55㊀F e56㊀B a137㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀㊀一㊁选择题(本题包括20小题,每小题3分,共60分.每小题只有一个选项符合题意)1.碳中和是指C O2排放总量和减少总量相当.我国提出在2060年前实现碳中和,这对于改善环境实现绿色发展至关重要.下列措施中不能实现碳中和的是A.大规模开采南海可燃冰作为新能源B.以C O2和H2为原料生产碳氢合成燃料C.研发能够高效吸收和利用C O2的新型电池D.加大新技术在碳捕捉㊁应用与储存等领域的运用2.劳动成就梦想,创造美好生活.下列劳动实践中的原因解释错误的是选项实践项目原因解释A社区服务:宣传垃圾分类,倡导环保出行便于资源再利用,防止污染环境B兴趣活动:新榨果汁提取液可使酸性KM n O4溶液褪色果汁中含有还原性物质,能氧化高锰酸钾,使其褪色C家务劳动:用白醋清洗水壶中的水垢醋酸酸性大于碳酸D自主探究:加碘食盐溶液不能使淀粉溶液变色食盐中碘元素以化合态形式存在3.下列有关化学科学的成果,描述正确的是A.阿伏加德罗提出原子论,为近代化学发展奠定了基础B.波义耳提出了氧化学说,使近代化学取得了革命性的进展C.拉瓦锡最早发现了氯气的存在D.我国科学家屠呦呦发现并提取出了青蒿素,有效降低了疟疾患者的死亡率4.嫦娥五号将月壤等样本成功带回地球,科学家用充满氮气的人造水晶容器进行了保存.深入研究表明月壤富含F e㊁H e㊁S i O2㊁A l2O3㊁F e O㊁C a O等物质,下列说法错误的是A.氮气可保护月壤样品中低化合价的成分B.C a O属于碱性氧化物C.通过月壤样品组分推测,该样品中S i元素的含量最高D.科学家在分析月壤时,运用了观察㊁分类㊁实验㊁比较等方法5.如图所示,在蒸发皿中放一小块钠,加热至熔化成小球时,用玻璃棒蘸取少量无水C u S O4粉末与其接触,瞬间产生耀眼的火花,同时有红色物质生成.下列说法错误的是A.钠受热易熔成小球说明其熔点低B.钠与C u S O4粉末反应时放出大量热C.一定条件下,N a可与C u S O4反应生成C uD.将无水C u S O4粉末改为C u S O4溶液,反应现象相同6.下列实验室中试剂保存的方法错误的是A.钠通常保存在煤油中B.少量白磷储存在冷水中C.F e C l3溶液保存时,通常在溶液中加少量的单质铁D.硝酸银及高锰酸钾通常都保存在棕色试剂瓶中,防止其见光分解7.从实验安全的角度分析,下列做法正确的是A.金属钠着火时使用干粉(含碳酸氢钠)灭火器灭火B.验证碳酸氢钠固体热稳定性时,试管口应略向下倾斜C.浓硫酸溅到皮肤上,立即用稀氢氧化钠溶液冲洗,再用水冲洗D.向铜和浓硫酸反应后的试管中加入水,溶液显蓝色证明有硫酸铜生成8.某化学探究小组按如图所示进行H2燃烧实验时,发现烧杯中酸性KM n O4溶液褪色.若将烧杯中的溶液换成含有少量K S C N的酸性F e S O4溶液,溶液呈红色.据此判断下列说法中错误的是A.该条件下部分H2反应生成了H2O2B.H2本身有强还原性,可以使酸性KM n O4溶液褪色C.酸性F e S O4溶液中发生的离子反应为2F e2++H2O2+2H+=2F e3++2H2O9.下列实验操作正确或实验设计能达到实验目的的是A.制备氢氧化铁胶体B.除去二氧化碳中的氯化氢C.证明钠的密度小于水的密度但大于煤油的密度D.利用过氧化钠与水反应制备氧气,且随开随用㊁随关随停10.如图是N元素及其化合物的 价 类 二维图.下列说法中正确的是A.实验室采用向上排空气法收集AB.化合物B的水溶液能导电,证明B是电解质C.控制不同的反应条件,C与E也能相互转化D.两支玻璃棒分别蘸取B的浓溶液与D的浓溶液,靠近后会产生白雾11.硫和氮及其化合物对人类生存和社会发展意义重大,但硫氧化物和氮氧化物造成的环境问题也日益受到关注,下列说法正确的是A.N O2和S O2均为有刺激性气味的红棕色气体,是酸雨的主要成因B.汽车尾气中的主要大气污染物为N O㊁S O2㊁C O2和P M2.5C.植物直接吸收利用空气中的N O和N O2作为肥料,实现氮的固定D.工业废气中的S O2可采用生石灰法进行脱除12.将碳和浓H2S O4反应产生的气体X通入盛有足量B a C l2溶液的洗气瓶中(如图),有白色沉淀产生,下列说法正确的是A.洗气瓶中产生的沉淀是B a C O3和B a S O3的混合物B.洗气瓶中发生的离子反应可能为:S O2+H2O+B a2+=B a S O3ˌ+2H+C.Y处逸出的气体能使澄清石灰水变浑浊,说明反应产生了C O2D.若将B a C l2溶液改为煮沸后冷却的B a(N O3)2溶液,仍会有白色13.如图所示,向密闭容器内可移动活塞的两边分别充入C O 2㊁H 2和O 2的混合气体(已知C O 2体积占整个容器体积的1/5),将H 2和O 2的混合气体点燃引爆.活塞先左弹,恢复室温后,活塞右滑并停留于容器的中央.下列说法错误的是A.反应前,活塞左右两边气体原子数之比为3ʒ4B .活塞移动情况说明H 2㊁O 2燃烧放热,且该反应气体分子数减少C .反应后恢复到室温,活塞左右两边气体的物质的量相等D.原来H 2和O 2的体积之比可能为3ʒ1或1ʒ114.下列实验操作及现象与结论之间对应关系错误的是选项实验操作及现象结论A某气体通入到品红溶液中,溶液褪色该气体为S O 2B向某溶液中滴加足量N a O H 浓溶液并加热,生成的气体能使湿润的红色石蕊试纸变蓝该溶液中含N H +4C 灼热的玻璃棒接触长条状S 粉和F e 粉混合物一端,混合物燃烧,并能迅速蔓延至末端,产生黑色固体S 粉和F e 粉可以反应且放热D 向某澄清溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色气体该溶液不一定含有C O 2-315.下述实验中均有红棕色气体产生,对比分析所得结论错误的是①②③A.红棕色气体均为还原产物B .由实验①可推断浓硝酸不稳定,受热易分解C .实验②中红棕色气体不能表明木炭与浓硝酸发生了反应16.钱逸泰院士等以C C l4和N a为原料,在700ħ时反应制造出纳米级金刚石粉末和另一种化合物,该成果被科学家们高度评价为 稻草变黄金 .下列说法错误的是A.另一种化合物是N a C lB.纳米级金刚石粉末分散在水中可产生丁达尔效应C.该反应可以在空气中进行D.该反应利用了氧化还原反应实现了物质间的转化17.某兴趣小组发现某品牌矿泉水标签的部分内容如下,由表可知下列说法正确的是饮用矿物质水净含量:500m L㊀配料表:纯净水㊀硫酸镁㊀氯化钾㊀保质期:12个月主要离子成分:钾离子(K+)1.0~27.3m g L-1㊀镁离子(M g2+)0.1~4.8m g L-1㊀A.1m o lM g S O4的质量为120g m o l-1B.c(M g2+)最大值也可表示为0.2mm o l L-1C.若检测发现该矿泉水中c(C l-)为0.5m m o l L-1,则c(S O2-4)浓度最大值为0.4m m o l L-1D.实验室配制500m L0.2m o l L-1的M g S O4溶液时,必须用到的玻璃仪器只有玻璃棒㊁烧杯和胶头滴管.18.我国从2000年起逐步用C l O2替代氯气对水进行消毒,工业上常用2N a C l O3+H2S O4+S O2 2C l O2+2N a H S O4制备C l O2,下列说法错误的是A.每生成1m o l C l O2转移电子数为1N AB.反应中氧化产物与还原产物物质的量之比为1ʒ1C.该工业生产中的废气需用碱液处理后再排放D.还原产物相同时,相同质量下C l O2是C l2氧化能力的2.63倍19.某微型实验装置(夹持仪器已省略)如图所示,其中a棉球蘸有品红溶液,b棉球蘸有含酚酞的N a O H溶液,c棉球蘸有I2与淀粉的混合溶液.实验时将70%H2S O4滴入装有N a2S O3固体的培养皿中.下列说法错误的是A.a棉球会变白,微热后变红B.b棉球变为白色,离子反应为:S O2+2O H-=S O23-+H2OC.c棉球变为白色,说明S O2具有漂白性20.某企业排放的污水中含有H+㊁N H+4㊁F e2+㊁F e3+㊁H C O-3㊁S2-㊁S O2-4㊁C l-中的几种,取100m L浓缩后的污水,测得c(H+)=0.7m o l L-1,然后设计如下实验流程(气体X㊁Y均为无色,体积均在S T P下测定):根据以上的实验操作与现象,得出的结论错误的是A.一定不存在的离子有H C O-3㊁S2-B.原100m L溶液中含有C l-为0.9m o l L-1C.原100m L溶液中含有F e3+为0.3m o l L-1D.生成气体X的离子方程式为3F e2++N O-3+4H+=3F e3++N Oʏ+2H2O二㊁非选择题:本题共4小题,共40分21.(10分)新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用.下列是我们常见的几种消毒剂:① 84 消毒液;②H2O2(在水中一部分可以电离出阴㊁阳离子);③C l O2;④O3;⑤碘酒;⑥75%酒精;⑦过氧乙酸(C H3C O O OH);⑧高铁酸钠(N a2F e O4).回答下列问题:(1)上述杀菌消毒剂属于非电解质的是㊀㊀㊀㊀(填序号), 84 消毒液中有效成分的电离方程式为㊀㊀㊀㊀.(2)各类杀菌消毒剂使用时,必须严格按照使用说明.①巴西奥运会期间,由于工作人员将 84 消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿.一种可能的原因是N a C l O与H2O2反应产生O2促进藻类快速生长.该反应说明氧化性:N a C l O㊀㊀㊀㊀H2O2的(填 > 或 < ).当有0.1m o lO2生成时,反应中转移电子为㊀㊀㊀㊀m o l.②若混合使用 洁厕灵 (盐酸是成分之一)与 84 消毒液会产生氯气.原因是㊀㊀㊀㊀(用离子方程式表示).(3)工业上可在N a O H溶液中,用N a C l O氧化F e(O H)3的方法制备N a2F e O4.制备反应.22.(12分)物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角, C a O2与N a2O2都属于过氧化物.过氧化钙(C a O2)是一种难溶于水㊁可与水缓慢反应㊁能溶于酸的白色固体,广泛用于果蔬保鲜㊁空气净化㊁污水处理等方面.以下是一种制备过氧化钙的实验方法.已知:C a C l2+H2O2+2N H3+n H2O C a O2 n H2Oˌ+2N H4C l回答下列问题:(1)实验室中由熟石灰和氯化铵制备氨气的化学方程式为㊀㊀㊀㊀.(2)实验室中进行操作Ⅰ㊁Ⅱ时,用到的玻璃仪器有烧杯㊁㊀㊀㊀㊀.(3)流程中采用 冰浴 的目的,除了能够易于C a O2 n H2O析出,还能㊀㊀㊀㊀. (4)检验 洗涤 合格的方法是㊀㊀㊀㊀.(5)工业的无水过氧化钙通常含有部分C a O,实验室常采用以酸为介质,用高锰酸钾测定过氧化钙的含量.称取1.0g样品置于烧杯中,用稀硫酸溶解,滴加0.10m o l L-1的酸性KM n O4溶液,恰好完全反应时,消耗酸性KM n O4溶液的体积为40.00m L,则C a O2的质量分数为㊀㊀㊀㊀%.下列会导致C a O2的质量分数偏低的是㊀㊀㊀㊀(填序号). A.称量无水过氧化钙时,样品与砝码放反B.样品溶解前,烧杯壁有少量蒸馏水C.硫酸溶解过氧化钙时有少量气泡产生D.滴加酸性KM n O4溶液时,不小心有一滴洒出23.(8分)一定条件下,铁与空气接触时表面会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖:与金属接触的一侧是F e O,中间是F e3O4,与空气接触的一侧则是F e2O3.回答下列问题:(1)F e3O4是磁铁矿的主要成分,也是中国古代 四大发明 之一 司南 的指针材料.用A l 粉和F e3O4反应焊接钢轨的化学方程式为㊀㊀㊀㊀.(2)F e O可以合成补铁剂F e S O4.欲验证F e S O4超过保质期后已变质,可进行的操作是:取一定量样品加水溶解静置㊁取少许溶液于试管中,向其中加入㊀㊀㊀㊀溶液(填试剂名称),若液体出现红色,则证明该药物已变质.(3)某实验小组设计了如下实验步骤,利用部分变质的废弃F e C l2溶液制备F e2O3.框图中热空气的作用为㊀㊀㊀㊀,写出aңb的离子方程式㊀㊀㊀㊀,写出F e2O3的一种用.24.(10分)反应物相同,通过控制不同条件,可能得到不同的产物.某兴趣小组查阅资料发现:C l2与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐(杀菌消毒能力较差).他们利用如图装置以C l2制备N a C l O3和N a C l O.已知:3C l2+6N a O H>70ħN a C l O3+5N a C l+3H2O,回答下列问题:(1)a中盛放浓盐酸的仪器名称为㊀㊀㊀㊀;若没有b装置,会导致c中产生大量的副产物㊀㊀㊀㊀(填化学式).(2)a装置中发生反应的离子方程式为㊀㊀㊀㊀.(3)资料显示:工业上制备 84 消毒液时,采用的是从吸收塔下部通入C l2,从上部喷淋循环冷却的N a O H溶液(15~20%).N a O H需要循环冷却的目的是㊀㊀㊀㊀. (4)该兴趣小组在60ħ条件下,将一定量的C l2通入600m L1.00m o l L-1N a O H溶液中, N a O H恰好反应,得到产物中含有N a C l㊁N a C l O和N a C l O3,则参加反应C l2的物质的量为㊀㊀㊀㊀m o l.。
2021届高考化学小题必练13 酸碱中和滴定及应用年级:姓名:酸碱中和滴定是高中化学最重要的定量实验之一,是帮助学生养成科学态度和接受科学教育极好的实验课题,常常结合溶液中的水解平衡,物质定量测定,高考再现率高,而且考察角度不断创新,对学习化学有良好的导向作用。
1.【2020年浙江选考】室温下,向120.00mL 0.1000mol L -⋅盐酸中滴加0.1000mol/LNaOH 溶液,溶液的pH 随NaOH 溶液体积的变化如图。
已知lg50.7=。
下列说法不正确的是( )A .NaOH 与盐酸恰好完全反应时,pH=7B .选择变色范围在pH 突变范围内的指示剂,可减小实验误差C .选择甲基红指示反应终点,误差比甲基橙的大D .V(NaOH)30.00mL =时,pH=12.3【答案】C【解析】A .NaOH 与盐酸恰好完全反应时溶液中的溶质为NaCl ,呈中性,室温下pH=7,故A 正确;B .选择变色范围在pH 突变范围内的指示剂,可减小实验误差,B 正确;C .甲基橙的变色范围在pH 突变范围外,误差更大,故C 错误;D .V(NaOH)30.00mL =时,溶液中的溶质为氯化钠和氢氧化钠,且c(NaOH)=30mL0.1000mol/L 20mL 0.1000mol/L20mL 30mL ⨯-⨯+=0.02mol/L ,即溶液中(新高考)小题必练13:酸碱中和滴定及应c(OH−)=0.02mol,则c(H+)=5×10−13mol/L,pH=-lgc(H+)=12.3,故D正确;故答案为C。
【点睛】酸碱中和滴定实验,酸碱指示剂的选择,滴定终点的判断,及pH的计算。
【2020年全国I卷】以酚酞为指示剂,用0.1000mol·L−1的NaOH溶液滴定20.00mL 2.未知浓度的二元酸H2A溶液。
溶液中,pH、分布系数δ随滴加NaOH溶液体积V NaOH 的变化关系如图所示。
热点08 实验探究题之定量探究类【命题趋势】定量探究重点考查学生对化学基本方法、基本知识和基本技能的掌握程度和运用能力。
在考查初中化学核心概念并兼顾化学基础知识与理论覆盖率的基础上,将学生化学学科能力的考查放在首要位置,特别是突出考查学生在解决与化学相关的实际问题中分析、概括、归纳、判断、推理的化学思维能力和综合运用化学知识的能力。
定量实验是初中化学学科较为难的实验,是一般结合定性实验,除了干扰因素外,还要考虑进行化学定量的计算。
【满分技巧】1.认真读题,审清题意,确立探究课题。
2.根据课题,选择合适方法,提取相关化学知识,设计探究方案。
3.根据课题要求,将探究的问题与所学的知识进行整合与提炼,迁移到要解决的问题中来。
【热点内容】1.质量守恒定律;2.碳酸盐含量的测定;3.催化剂或催化效果的比较;4.金属氧化物含量的测定。
【限时检测】(建议用时:30分钟)1.(2021•长沙市模拟)足球比赛中让昏迷球员快速恢复意识会用到“嗅盐”,同学们对嗅盐产生了好奇,并对其成分进行如下探究。
【查阅资料】(1)嗅盐是由一种盐类物质和香料(不参与下列探究中的任何反应)组成,能释放出氨味气体,对人体神经会产生强烈的刺激作用,但过量吸入会危害健康。
(2)氯化钙稀溶液与碳酸氢铵溶液不发生反应。
(3)氨气极易溶于水,且能与硫酸化合生成硫酸铵。
【提出问题】嗅盐中盐类物质是什么?【实验探究】填写表中空格。
方案嗅盐与(填一种物质的俗名)混合研磨现象闻到刺激性气味且试纸变蓝有白色沉淀出现结论嗅盐中含有NH4+嗅盐中含有CO32-确认了小青的实验结论证明嗅盐中盐类物质是碳酸铵【质疑】小竹认为小青的实验结论不严谨。
小竹通过补做一个实验(方案见上表),进而确认了小青的结论。
小竹的实验目的是排除嗅盐中含有离子的可能性。
【继续探究】小湖同学利用如下图所示装置进一步测定嗅盐中碳酸铵的质量分数。
【实验主要操作步骤】①关闭止水夹,加入足量氢氧化钠溶液,充分反应。
2021年道路工程试卷和答案(29)一、单选题(共35题)1.沥青路面使用性能气候分区划分中,高温气候分区采用工地所处地最近30年内最热月份平均日最高气温的平均值作为气候分区的一级指标,并且划分了()个区。
A:2B:3C:4D:5【答案】:B【解析】:气候分区的高温指标:采用最近30年内年最热月的平均日最高气温的平均值作为反映高温和重载条件下出现车辙等流动变形的气候因子,并作为气候区划的一级指标。
按照设计高温分区指标,一级区划分为3个区,如下表:2.立方体抗压强度标准值是砼抗压强度总体分布中的一个值,强度低于该值的概率不超过()A:15%B:10%C:5%D:3%【答案】:C【解析】:立方体抗压强度标准值是指按标准方法制作和养护的边长为150mm的立方体试件,到28d龄期时,采用标准试验方式测得的抗压强度总体分布中的一个值,要求混凝土抗压强度低于标准值的百分率不超过5%(即具有95%保证率的抗压强度),以MPa(N/mm2)计。
3.沥青标号根据沥青的()的大小划定范围。
A:针入度B:软化点C:延度D:密度【答案】:A【解析】:沥青标号根据沥青的针入度的大小划定范围。
4.下列选项中,不属于检查井砌筑实测项目的是()。
A:砂浆强度B:中心点位C:沟底高程D:井盖与相邻路面高差【答案】:C【解析】:沟底高程是土沟的实测项目。
5.当路面温度超过20℃±2℃范围时,沥青面层厚度大于()的沥青路面,回弹弯沉值应进行温度修订。
A.8C.mB.4C.mA:10B:mC:5D:m【答案】:D【解析】:沥青路面的弯沉以路表温度20℃时为准,在其他温度(超过20℃±2℃范围)测试时,对厚度大于5cm的沥青路面,弯沉值应予温度修正。
温度修正有两种方法,查图法和经验计算法。
6.在表面用()测定时,所测定沥青面层的层厚应根据核子密度仪的性能确定最大厚度。
A:直接透射法B:散射法C:间接透射法D:穿透法【答案】:B【解析】:在表面用散射法测定时,所测定沥青面层的层厚应根据核子密度仪的性能决定最大厚度。
蔗糖法测氧化钙含量
欧阳光明(2021.03.07)
有效氧化钙的测定有如下两种方法:蔗糖法原理,氧化钙在水中的溶解度很小,20℃时溶解度为 1.29g/加入蔗糖就可使之成溶解度大的蔗糖钙,再用酸滴定蔗糖钙中的氧化钙的含量,
反应如下:
C12H22O11+CaO+2H2O─→C12H12O11CaO+2H2O
C12H22O22O11CaO+2H2O+2HCl→C11H22O11+CaCl2+3H2O
试剂:蔗糖:化学纯。
酸:0.5mol/l标准溶液。
(0.5mol/LHCl溶液:量取45毫升盐酸,缓慢注入1000ml水。
)
酚酞指示剂。
操作:
迅速精确称取0.4~0.5g研成细粉的试样,置于250ml具有磨口玻塞的锥形瓶中,加入4g化学纯蔗糖及小玻球12~20粒,再加入新煮沸而已冷却的蒸馏水40ml。
塞紧瓶塞。
摇动15min,以酚酞为指示剂,用0.5mol/l酸标准溶液滴定至红色恰好消失,并在30s 内不再现红色为止。
计算按下式计算有效氧化钙的含量:
CaO(%)=2.8NV/W
式中:N──酸标准溶液的浓度;
V──滴定时所耗用的酸标准液的量(ml);
W──试样量(g))。
注意事项测定时,不应使氧化钙生成碳酸钙,所以要用新煮沸过而尽量除去二氧化碳的蒸馏水,以免氧化钙溶于水后生成的氢氧化钙进一步与二氧化碳作用生成碳酸钙,使消耗的酸标准溶液量偏低。
再者,因蔗糖只与氧化钙作用,而不与碳酸钙作用,所以称量试样要迅束,否则氧化钙会吸收空气中的二氧化碳变成碳酸钙,导致结果偏低。
酸量法测氧化钙含量
酸量法原理有效氧化钙溶于水后生成氢氧化钙,可用酸滴定氢氧化钙,从而测出有效氧化钙的含量。
反应如下:
CaO+H2O─→Ca(OH)2
Ca(OH)2+2HCl─→CaCl2+2H2O
试剂:0.1mol/l酸标准溶液。
(0.1mol/LHCL溶液:量取9毫升盐酸,缓慢注入1000ml水。
)
酚酞指示剂。
测定方法:
准确称取研磨细的试样1g左右,置于烧杯内,加入刚煮沸过的蒸馏水约300ml,搅匀后全部转移至1000ml的容量瓶中,将瓶加塞不时摇动,约20min后冷却,再加入新煮沸已冷蒸馏水至刻度。
混匀,过滤(过滤要迅速)。
弃去最初100ml滤液,吸取50ml入锥形瓶中,以酚酞为指示剂,用0.1mol/l酸标准溶液滴定至红色消失且30秒不再出现即为终点。
计算:CaO(%)
=50*W NV
28×100
试中各项意义同蔗糖法。
注意事项所使用的蒸馏水必须重新煮沸过。
过滤要迅速,以免氢氧化钙吸收空气中的二氧化碳变为碳酸钙,而使结果偏低。