(医疗药品)治疗充血性心力衰竭的药物
- 格式:doc
- 大小:86.06 KB
- 文档页数:31



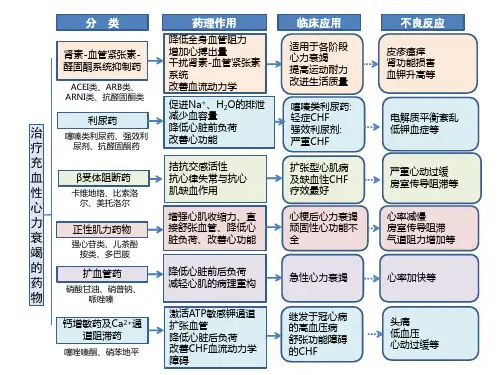
治疗慢性充血性心力衰竭(CHF)药物分类
根据药物作用及作用机制,治疗CHF的药物分一下几类:
1、肾素-血管紧张素-醛固酮系统(RASS)抑制药
(1)肾素血管紧张素I转换酶抑制药(ACE)卡托普利依那普利等
(2)肾素血管紧张素II受体(AT1)拮抗药氯沙坦缬沙坦厄贝沙坦等(3)醛固酮拮抗药螺内酯(是对抗醛固酮,排钠保钾利尿剂)
2、利尿药氢氯噻嗪、呋噻米、螺内酯等
3、B-受体阻断药美托洛尔、卡维地洛等
4、强心苷类药地高辛(毛花苷丙、毒毛花苷K ,需静脉给药,显效快,作
用短)
5、其他治疗CHF药物
(1)血管扩张药(降低心脏前后负荷)硝普钠、硝酸异山梨脂、肼屈嗪、哌唑嗪等
(2)非苷类正性肌力药米力农维司力农(抑制磷酸二脂酶,增加心肌细胞内c-AMP含量,激活蛋白激酶A,促进Ca内流增加心肌收缩力)等(3)长效钙通道阻滞药氨洛地平等(短效的钙通道阻滞药如硝苯地平、地尔硫卓、维拉帕米可使CHF症状恶化)。

治疗充血性心力衰竭的药物充血性心力衰竭(congestive heart failure,CHF) 或称慢性心力衰竭(chronic heart failure, CHF) 是一种临床综合征,本质上是一种超负荷的心肌病,也是各种病因所致心脏疾病的终末阶段的一种病理生理状态, 其症状复杂, 预后不良, 是心血管疾病中一大难题, 正日益受到广泛重视。
概述l CHF及其发病l CHF 时心脏结构的改变l CHF 时心脏功能的改变l CHF 时多种神经体液系统的变化l CHF 时心肌肥厚反应的信号转导l CHF 药物治疗的演变CHF及其发病l vCHF时心脏血流动力学的变化,是指在适量静脉回流的情况下,心脏不能排出足量的血液来维持机体组织代谢的需要。
l 主要由于心肌收缩性心脏排出量不足静脉系统淤血,动脉系统灌流久而久之发展成为CHF。
l CHF 的发病逐年增加。
发达国家罹患人数已超过总人口的1%, 且有上升趋势。
CHF 预后甚差, 估计5 年内病死率达30%~50% 。
病情严重者1年内病死率高达50% 以上, 病死者约一半为心律失常所致之猝死, 另一半死于进行性泵功能衰竭。
CHF 时心脏结构的改变——心肌细胞凋亡(apoptosis)多年来认为成人心肌细胞是最终分化细胞,不再增殖, 也不会凋亡。
近年发现心肌梗死、缺血和再灌, 压力超负荷及心律失常性右室心肌病时均可发生凋亡。
终末期心肌病时, 也发生心肌细胞凋亡。
人衰竭心肌中,P53 蛋白( 抑癌基因)的表达增加,促进细胞凋亡。
CHF 时心脏结构的改变——细胞外基质(extracellular matrix,ECM)细胞外包围着细胞的许多大分子物质,由各种纤维丝、胶原、纤维粘连蛋白、蛋白多糖等组成。
CHF 时心肌出现肥厚与纤维化, 此时ECM也发生变化,各种成分都增加、堆聚。
胶原堆聚将使心肌顺应性降低,导致心室舒张功能障碍。
肌纤维化减少心肌收缩单位,致使心肌收缩功能和舒张功能均遭损害。



硝普钠+芪苈强心胶囊治疗慢性充血性心力衰竭的临床疗效让我们来了解一下硝普钠和芪苈强心胶囊的特点。
硝普钠是一种短效硝酸酯类药物,可以扩张冠状动脉和周围血管,降低心脏前负荷和后负荷,从而减轻心脏负担,扩张血管,减轻心脏负担,降低心肌氧耗。
芪苈强心胶囊是一种中药复方制剂,主要成分有马钱子碱、羚羊角、当归等,具有扩张冠状动脉、增加冠脉血流量、改善心肌供血、减轻心脏负荷、增强心肌收缩力等作用。
硝普钠+芪苈强心胶囊在治疗慢性充血性心力衰竭的临床研究表明,该药物组合治疗慢性充血性心力衰竭的总有效率高达90%以上。
通过对患者症状、心功能等指标的观察,发现患者服用硝普钠+芪苈强心胶囊后,症状得到了显著改善,心功能也有所提升。
治疗后患者呼吸困难明显减轻,水肿明显缓解,体力恢复情况良好,运动耐力明显提高,心功能等级有所下降。
在临床实践中,硝普钠+芪苈强心胶囊也被证实具有较好的安全性和耐受性。
患者在服用该药物组合后,极少出现明显的不良反应,主要是轻度的头痛、头晕等症状。
而且,在治疗慢性充血性心力衰竭的过程中,硝普钠+芪苈强心胶囊也能够有效地控制血压,对心脏和肾脏功能的保护作用也得到了临床观察。
在使用硝普钠+芪苈强心胶囊时,患者仍需严格遵循医嘱,按时按量服用,并定期复诊,以便及时调整用药方案。
患者在治疗的还需遵循医嘱,合理饮食,适当锻炼,保持乐观心态,以达到更好的治疗效果。
在今后的临床实践中,我们期待进一步的多中心、大样本临床研究数据,以验证硝普钠+芪苈强心胶囊治疗慢性充血性心力衰竭的疗效和安全性。
相信随着科学技术的不断发展,硝普钠+芪苈强心胶囊这一治疗慢性充血性心力衰竭的药物组合会为更多的患者带来健康和幸福。


治疗充血性心力衰竭的药物充血性心力衰竭(congestiveheartfailure,CHF)或称慢性心力衰竭(chronicheartfailure, CHF)是一种临床综合征,本质上是一种超负荷的心肌病,也是各种病因所致心脏疾病的终末阶段的一种病理生理状态,其症状复杂,预后不良,是心血管疾病中一大难题,正日益受到广泛重视。
概述lCHF及其发病lCHF时心脏结构的改变lCHF时心脏功能的改变lCHF时多种神经体液系统的变化lCHF时心肌肥厚反应的信号转导lCHF药物治疗的演变CHF及其发病lvCHF时心脏血流动力学的变化,是指在适量静脉回流的情况下,心脏不能排出足量的血液来维持机体组织代谢的需要。
l主要由于心肌收缩性心脏排出量不足静脉系统淤血,动脉系统灌流久而久之发展成为CH F。
lCHF的发病逐年增加。
发达国家罹患人数已超过总人口的1%,且有上升趋势。
CHF预后甚差,估计5年内病死率达30%~50%。
病情严重者1年内病死率高达50%以上,病死者约一半为心律失常所致之猝死,另一半死于进行性泵功能衰竭。
CHF时心脏结构的改变——心肌细胞凋亡(apoptosis)多年来认为成人心肌细胞是最终分化细胞,不再增殖,也不会凋亡。
近年发现心肌梗死、缺血和再灌,压力超负荷及心律失常性右室心肌病时均可发生凋亡。
终末期心肌病时,也发生心肌细胞凋亡。
人衰竭心肌中,P53蛋白(抑癌基因)的表达增加,促进细胞凋亡。
CHF时心脏结构的改变——细胞外基质(extracellularmatrix,ECM)细胞外包围着细胞的许多大分子物质,由各种纤维丝、胶原、纤维粘连蛋白、蛋白多糖等组成。
CHF时心肌出现肥厚与纤维化,此时ECM也发生变化,各种成分都增加、堆聚。
胶原堆聚将使心肌顺应性降低,导致心室舒张功能障碍。
肌纤维化减少心肌收缩单位,致使心肌收缩功能和舒张功能均遭损害。
CHF时心脏结构的改变——心肌细胞骨架(cytoskeleton)心肌肥厚或CHF时,心肌细胞骨架的含量增加而其结构却遭破坏。
肌细胞负荷增加,加重心功能不全。
CHF时心脏结构的改变——心肌重构或肥厚l心肌肥厚是心脏腔室重量增加,伴有心室形态结构的改变和功能的减退,称此过程为重构。
是各种病因引起CHF时心脏形态结构的各种病理变化直至功能衰竭。
l重构时,心肌细胞肥大增生,而非肌细胞(成纤维细胞、胶原细胞、血管壁细胞)则发生增殖。
细胞数不增加,但每个细胞体积、重量增加而肥大,成为非生理性的不正常巨大细胞,终将凋亡。
CHF时心脏功能的改变——收缩功能障碍心肌收缩过程的物质基础有收缩蛋白和调节蛋白,并需ATP提供能量,Ca2+偶联兴奋-收缩过程,这些环节若出现障碍,会影响收缩功能。
lCHF时,左心室收缩功能出现障碍,心肌张力及张力上升最大速率下降,心肌收缩成分减少,能量的利用下降。
l治疗收缩功能障碍常用加强心肌收缩性的药物,如地高辛,也可用血管扩张药减轻心脏负荷,改善收缩功能。
CHF时心脏功能的改变——舒张功能障碍l舒张过程中的物质变化是胞浆中Ca2+浓度下降,并与肌钙蛋白脱离而使肌节松弛,心脏舒张。
此过程也需ATP供能。
舒张功能与心室壁顺应性(pliance)有关,舒张功能障碍表现为顺应性降低。
顺应性急剧下降见于急性心肌梗死时,肺循环淤血,引起呼吸困难甚至肺水肿,此即“舒张性心力衰竭”。
l治疗舒张功能障碍尚无特异直接的方法,但使用β受体阻断药、ACE抑制剂、钙拮抗剂有一定疗效。
CHF时心脏功能的改变——血流动力学某些参数的变化lCHF时血流动力学多项参数都有改变,且与病情严重程度相关,但因病因不同,其变化有差异。
l心排出量(CO)和心脏指数(CI):降低l射血分数(EF):下降l心房压(AP)和心室压(VP):不同原因的心衰,AP和VP变化不同。
一般二者多同时升高。
l左室舒张末压(LVEDP):CHF愈严重,LVEDP愈高,此时室壁肌张力愈大,耗能耗氧愈多,使心脏工作效率愈低。
临床测LVEDP困难,常用肺楔压(PCWP)代之。
CHF时心脏功能的改变——血流动力学某些参数的变化l右房压(RAP)和右室舒张末压(RVEDP):它们是右心衰竭的重要血流动力学指标。
.l心室dp/dtm:其中+dp/dtmax是指心室等容收缩期内压力上升的最大速率,反映了心室肌的收缩性,在CHF时是下降的。
-dp/dtmax是心室舒张后室内压力快速下降期的下降最大速率,反映心室舒张功能。
l动脉血压:CHF时动脉血压长期维持正常水平,保证了重要器官的血流供应,这是由神经体液系统的代偿功能所调控的。
CHF时神经体液系统的变化——交感神经系统是心血管系统最敏感的调节机制,其激活也是CHF发病中最常见的早期代偿表现。
在CHF发病早期与轻度阶段交感神经活性就已增高,血中NA浓度已提高2~3倍,且与预后相关,血中NE浓度升高有多种不良影响,对CHF的预后不利,浓度低者预后较好。
CHF时神经体液系统的变化——肾素血管紧张素系统(RAS)lRAS对循环系统的调节较慢,在中、重度CHF时被激活,肾素释放增加,血浆肾素活性升高,血中AngⅡ浓度亦升高。
lAngⅡ有多种作用:收缩全身小动脉,提高外周阻力及收缩出球小动脉,提高肾小球滤过压;增加NE、醛固酣、精氨酸加压素、内皮素等释放;促进水钠滞留;促进细胞生长,引起心肌及血管壁的重构与肥厚。
CHF时神经体液系统的变化——肾素血管紧张素系统(RAS)RAS的激活与交感神经激活相同,对CHF者,在一定时间内,对心功能有代偿作用,久之也因增加心肌负荷而使CHF恶化。
近还明确,心肌细胞自分泌、旁分泌所产生的AngⅡ也参与心肌及血管收缩的调节,并有促细胞生长作用,引起心室重构肥厚,终而导致进行性心功能障碍。
CHF时神经体液系统的变化——精氨酸加压素(AVP)lCHF患者血中AVP的量也随病情严重程度而增加。
AVP通过Vl受体,经第二信使IP3,DAG而收缩血管。
其特异的受体阻断药OPC21268等用于CHF患者,能扩张血管,改进左室功能。
CHF时神经体液系统的变化——内皮素(endothelin,ET)由内皮细胞合成分泌,其受体与不同G蛋白偶联而诱发不同效应,如促进血管收缩与细胞生长等。
CHF时,血中ET浓度随病情严重程度加剧而上升。
CHF时神经体液系统的变化——肿瘤坏死因子-α(tumornecrosisfactor-α,TNF-α) lTNF-α在CHF患者血中的浓度也是升高的,重度晚期患者上升最高。
高浓度可抑制心肌收缩性而致左室功能不良。
l负性肌力作用与TNF-α促增诱生型NO合酶(iNOS)活性,增加NO量有关。
长期应用T NF-α能伤害心肌,引起心肌结构改变、重构(肥厚)及凋亡。
CHF时神经体液系统的变化——利钠肽l现知有三种利钠肽:心房利钠肽(ANP)、脑利钠肽(BNP)及C型利钠肽(P),前二者产自心肌细胞,有较强的排钠利尿作用。
三种利钠肽尚有扩张血管、抗生长增殖,抑制NE、肾素、醛固酮、内皮素等的作用,在心室肌舒张过程的调控中起松弛作用。
lCHF早期无症状时,患者血中ANP、BNP浓度即己上升,随病情加重而上升更高。
ANP、BNP在患者血中浓度的增加程度能预示CHF严重程度及病死情况,也有诊断意义。
CHF时神经体液系统的变化——一氧化氮(nitdcoxide,NO)lCHF患者体内NO的产生和释放不足,患者的血管扩张反应减退,促进CHF多种症状形成。
NO具有抑制细胞增殖而抑制心室重构肥厚,防止CHF的恶化。
据此,设想给患者以外源性NO将有利于CHF的治疗和预后。
l临床已用的硝酸酯类就是NO的供体药,它们在体内代谢生成NO而能降低前负荷,增加左室射血分数。
对某些前、后负荷都增高的患者,合用肼屈嗪降低后负荷,则效果更好。
CHF时神经体液系统的变化——前列腺素I2、E2二者都有强大的血管扩张作用,能扩张冠状动脉及肾、肺、脑等动脉。
肾局部的PGI2能明显扩张肾血管,增加肾小球滤过率,减少肾小管对Na+的再吸收而排钠利尿。
lCHF患者血浆中PGI2、E2的浓度升高。
lCHF患者应用PGI2后,其前、后负荷下降,症状改善。
CHF时神经体液系统的变化——肾上腺髓质素(adrenomedullin,AM)l一种新发现的循环激素,广泛分布于肾上腺髓质、心、脑、肾、肺、胃肠道等器官中。
AM与其受体相结合,增加细胞内cAMP量,由后者介导而生效。
lAM的主要作用是扩张血管,降低血压,这一作用可能与NO的存在有关,并由其介导。
A M还有抗生长的作用,能抑制血管平滑肌细胞的有丝分裂和增殖。
CHF患者血浆中AM浓度上升,且与心衰严重程度相应。
CHF时神经体液系统的变化——其他体内物质l近知还有一些体内物质与CHF有关,可能也参与CHF的发病过程,其机制有待进一步研究。
l心脏肌钙蛋白(troponin)lP53蛋白l脂肪酸l免疫分子CHF时心肌肥厚反应的信号转导l心肌肥厚反应由细胞外肥厚刺激引发,经细胞内信号转导通路转入核内,促使基因表达改变,最终诱发心肌肥厚的表型变化。
CHF时心肌肥厚反应的信号转导——β受体下调l严重CHF患者心肌β1受体密度及数量较正常人为少。
β1受体下调,同时β2受体和α受体增加。
β1受体下调的原因是在高浓度NE长期作用下已被耗竭。
因此,β1受体下调对心脏是有保护意义,可使心脏免受过量NE之害。
CHF时心肌肥厚反应的信号转导——β受体与G蛋白脱偶联l在CHF早期已见β1受体与Gs蛋白脱偶联,使心脏对β1受体激动药的反应性降低。
脱偶联时,Gs蛋白数量减少,而抑制性Gi蛋白数量增多,Gs/Gi比值下降。
CHF时心肌肥厚反应的信号转导——腺昔酸环化酶(AC)活性下降lCHF时AC活性约降40%,这与上述Gs,Gi活性的变化有关。
与此相应,cAMP量减少。
——心肌细胞内Ca2+量减少lCHF时,胞内cAMP含量减少,PKA活性降低,继而L型钙通道开放率降低,Ca2+内流减少,胞内Ca2+量因而降低,使心肌收缩性下降。
CHF药物治疗的演变lCHF的药物治疗应用已久,短期疗效也还明显,但长年来多为经验性用药,进展缓慢,世界各地所用药物的品种,用药适应证,用药方法和剂量等,都互有差异,并无共识。
近代医学对此曾作广泛研究,在基础理论和临床实践都取得成绩,资料和经验积累丰富。
但CHF的药物治疗深受疾病“基本认识”的限制。
人们对CHF的基本认识迄今未明确肯定,历年变化甚大,主要是因CHF的发病发展过程较为复杂,难以全面的认识。
为此,CHF的药物治疗也难有效发展,20世纪以来,已有多次演变。
l20世纪50年代以前,治疗CHF的药物主要是洋地黄类强心苷,深受当时发病学上认为C HF的要害在于心肌收缩力衰退一说的影响(“心一心模式”说),重视应用能增强收缩力的药,重视强心苷的正性肌力作用。