003-00炒黄SOP
- 格式:doc
- 大小:38.50 KB
- 文档页数:3
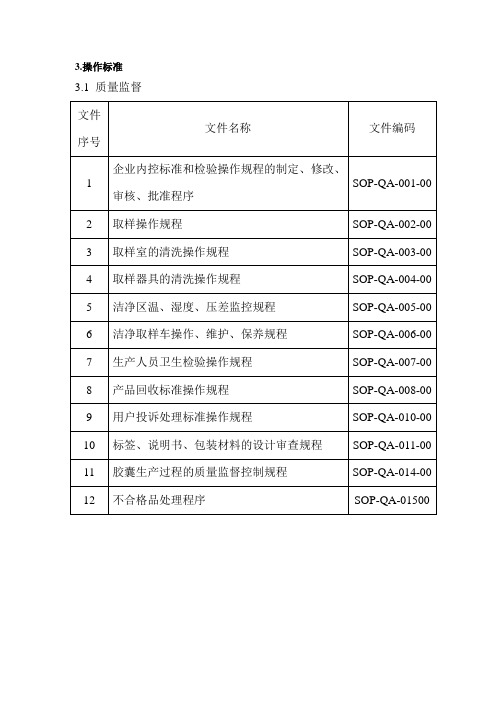
3.操作标准3.1 质量监督目的:为了确保药品质量,使公司生产的药品在法定标准的基础上进一步提高,特制定企业内控标准和检验操作规程的制定、修改、审核、批准规程。
范围:成品、中间产品、物料的内控标准和检验操作规程。
责任人:质管部、生产部、供销部。
内容:1、内控标准和检验操作规程由质管部门负责制定,制定的依据是法定标准及近两年来产品的质量情况统计分析表,并在此基础上有一定提高。
2、质管部门将制定的内控标准和检验操作规程草案会同生产部的技术人员进行讨论,提出修改意见,形成共同认可的公司内控标准和检验操作规程初步方案。
3、将已经过质管、技术、生产部门讨论修改过的内控标准方案交质管部部长审核,总经理批准, 检验操作规程初步方案由QA填写《检验方法变更情况表》(REC-QA-029-00)经质管部部长批准。
4、由质管部负责将批准生效的内控标准和检验操作规程以文件的形式发到公司有关部门,并规定新文件执行日期即旧文件作废日期。
目的:建立原料、辅料、包装材料、中间产品及成品的取样程序。
范围:适用于公司的所有原料、辅料、包装材料、中间产品及成品的取样。
责任人:QA检查员、仓库管理员、生产部相关人员内容:1、取样人员:QA(水质采样由QC除外)2、取样地点:直接入药的原辅料及直接接触药品的包装材料和聚乙烯袋的取样在仓库洁净取样车中进行;非直接接触药品的包装材料的取样在仓库待验区中进行;中间产品的取样在车间洁净区中进行;成品取样在车间外包工序包装封箱前进行。
3、取样工具和盛样器具。
3.1在洁净取样车和车间洁净区内的取样工具和盛样器具的卫生要求:直接接触药品的取样工具和盛样器具均不得与药品发生化学作用, 微生物限度检查用样品的取样工具和盛样器具须经灭菌处理,使用前必须严格按《取样器具的清洗操作规程》(SOP-QA-004-00)洗净消毒,并且在有效期内。
直接接触药品的取样工具在使用后,及时洗净,并按《取样器具的清洗操作规程》(SOP-QA-004-00)洗净消毒,放入无毒塑料袋包好,并贮存于仓库洁净取样车内备用。

信州区新久久大药房文件名中药饮片处方审核、调配、核对操作规程文件编号JJ-SOP-003-00版本号00 页码第 1 页共 2 页起草人审核人批准人起草日期审核日期批准日期发布日期生效日期1.目的:为依法经营,做好中药饮片处方审核、调配、核对和销售工作,特制定本规程。
2.范围:适用于本药房中药饮片处方的审核、调配、核对。
3.责任:质量负责人、处方审核人员对本规程的实施负责。
4.正文:4.1处方审核4.1.1处方审核人员接到处方后对处方进行审核审核内容包括处方有无患者的姓名、性别、年龄;有无药味、剂量、用法、剂数;有无医生签字、开方日期;有无配伍禁忌、妊娠禁忌药、超过规定剂量等问题;处方字迹是否清晰;是否存在错写药名、重味现象。
审核人员对以上项目审核无误后,在处方上签字并交调配人员进行调配。
4.1.2处方无医师签字、项目不齐、字迹辨认不清的,审核人员应拒绝调配,并告知患者找开方医生补齐或书写清楚。
4.1.3处方有配伍禁忌或超剂量的,审核人员应拒绝调配,并告知患者找开方医生更正或重新签字。
4.1.4处方应付药味本店短缺时,审核人员应拒绝调配,并告知患者找开方医生更换其它药味。
不得擅自更改或代用处方中的药味。
4.2处方调配4.2.1调剂人员根据审核人员签名的处方内容逐项调配,调剂人员配方时应认真、细致、准确。
4.2.2调剂人员称取药味应按处方所列顺序间隔平摆,不得混放一堆,以利核对。
调剂过程中必须按处方从上至下,从左到右进行调配。
4.2.3处方中要求先煎、后下、包煎、烊化、另煎、冲服等特殊煎法的药味,应进行单包并注明用法。
需要临时捣碎的药味应使用铜缸捣碎,铜缸在用后立即擦拭干净,文件名中药饮片处方审核、调配、核对操作规程文件编号JJ-SOP-003-00版本号00 页码第2页共 2 页不得残留粉末。
4.2.4调配处方完毕,调剂人员检查核对无误后在处方上签全名,将处方交处方审核人员复核。
4.3处方复核4.3.1处方审核人员按处方对照药味逐一进行复核。
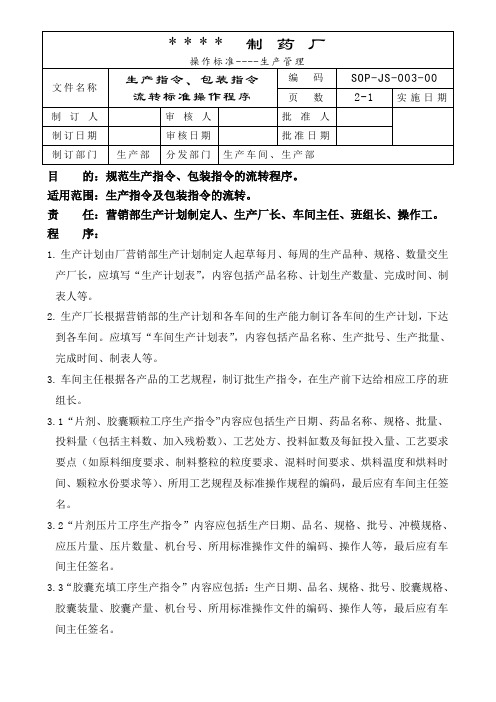
目的:规范生产指令、包装指令的流转程序。
适用范围:生产指令及包装指令的流转。
责任:营销部生产计划制定人、生产厂长、车间主任、班组长、操作工。
程序:1. 生产计划由厂营销部生产计划制定人起草每月、每周的生产品种、规格、数量交生产厂长,应填写“生产计划表”,内容包括产品名称、计划生产数量、完成时间、制表人等。
2. 生产厂长根据营销部的生产计划和各车间的生产能力制订各车间的生产计划,下达到各车间。
应填写“车间生产计划表”,内容包括产品名称、生产批号、生产批量、完成时间、制表人等。
3. 车间主任根据各产品的工艺规程,制订批生产指令,在生产前下达给相应工序的班组长。
3.1“片剂、胶囊颗粒工序生产指令”内容应包括生产日期、药品名称、规格、批量、投料量(包括主料数、加入残粉数)、工艺处方、投料缸数及每缸投入量、工艺要求要点(如原料细度要求、制料整粒的粒度要求、混料时间要求、烘料温度和烘料时间、颗粒水份要求等)、所用工艺规程及标准操作规程的编码,最后应有车间主任签名。
3.2“片剂压片工序生产指令”内容应包括生产日期、品名、规格、批号、冲模规格、应压片量、压片数量、机台号、所用标准操作文件的编码、操作人等,最后应有车间主任签名。
3.3“胶囊充填工序生产指令”内容应包括:生产日期、品名、规格、批号、胶囊规格、胶囊装量、胶囊产量、机台号、所用标准操作文件的编码、操作人等,最后应有车间主任签名。
3.4“片剂包衣工序生产指令”内容应包括:生产日期、品名、规格、批号、包衣数量、包衣锅编号、所用标准操作文件的编码等,最后应有车间主任签名。
4.对符合工艺规程要求,完成生产全过程并检验合格的中间产品,车间主任制订包装指令,在包装前下达给相应包装组的组长。
包装指令内容应包括品名、规格、批号、包装数量、包装方式、包装物使用数、采用标准操作文件的编码等,最后应由车间主任签名。
5. 班组长接到生产指令后,组织操作工凭生产指令向仓库限额领用原辅料、包装材料,并严格按生产指令的要求进行操作。

1.目的:建立偏差处理工作标准,使发生的偏差得到有效的调查和评估,并有适当的行动方案得到批准并有效实施。
2.范围:适用于与原料,产品,工艺过程,程序,标准,厂房设施,环境控制,计量校准,以及与质量相关的涉及 GMP和 SOP执行的所有偏差。
3.责任人:质量负责人、生产负责人、QA及各部门负责人。
4.内容:4.1.定义4.1.1偏差:任何与产品质量有关的异常情况,如:中间产品,成品检验结果超标、产品储存异常、设备故障、校验结果超标、环境监测结果超标、客户投诉等;以及与药品相关法律法规或已批准的标准、程序、指令不相符的意外/偏差事件。
4.1.2偏差的分级:严重:违反质量管理体系(QMS)质量政策或国家法规,危及产品安全及产品形象,导致或可能导致产品内/外在质量受到某种程度的影响,以致产品整批报废或成品收回等后果。
重大:导致或可能导致产品内/外在质量受到某种程度的影响,造成返工、回收等后果;严重违反GMP及 SOP的事件。
一般(Minor):不会影响产品质量,或临时性调整。
4.2.偏差的种类4.2.1检验结果超标:中间品,成品过程检验结果超出标准。
4.2.2物料平衡限度:超出合格范围。
跑料、标签、封口签、说明书等的实用数、残损数、退回数与领用数发生差额。
4.2.3工艺/SOP:违反工艺/SOP操作。
生产过程时间控制超出工艺规定范围。
4.2.4混淆:两种不同的产品/同种不同批号的产品,或同种/同批而用不同的包材的产品混在一起。
4.2.5异物(有形):在原辅料、包装材料、成品或生产包装过程中发现的异物。
4.2.6.潜在的污染:如不能正确清除,可能导致产品的污染。
4.2.7.过期的物料/设备:中间产品超过程序规定的储存期限;使用了超出校验期的设备。
4.2.8设备故障/过程中断:因设备故障导致产品质量缺陷或潜在威胁,生产中断;因动力原因(停电、汽、气、水)导致流程中断。
4.2.9环境:与药品生产相关的空调系统、厂房设施的防尘捕尘设施、防止蚊虫和其他动物进入设施、照明设施的故障,以及洁净区尘埃粒子检测超限,生产车间人员、空气、地面、墙面环境监测环控指标超限、温湿度控制超限、压差超限等偏差事件。

目录1. 药品名称 (1)1.1. 品名 (1)1.2. 汉语拼音 (1)2. 剂型 (1)3. 产品概述 (1)3.1. 性状 (1)3.2. 功能与主治 (1)3.3. 用法用量 (1)3.4. 规格 (1)3.5. 贮藏 (1)3.6. 有效期 (1)4. 处方和依据 (1)4.1. 处方 (1)4.2. 制法 (2)4.3. 标准依据 (2)4.4. 批准文号 (2)4.5. 生产处方 (2)5. 工艺流程图 (2)6. 操作过程及工艺要求 (4)6.1. 操作过程 (4)6.1.1. 原药材的前处理 (4)6.1.2. 配料 (4)6.1.3. 浸渍 (4)6.1.4. 渗漉 (4)6.1.5. 水提 (4)6.1.6. 浓缩 (5)6.1.7. 配液 (5)6.1.8. 灌装 (5)6.1.9. 灯检 (6)6.1.10. 包装 (6)6.2. 工艺要求 (6)6.2.1. 前处理 (6)6.2.2. 制剂 (7)6.3. 生产地点及生产设备 (8)6.3.1. 前处理 (8)6.3.2. 制剂 (9)7. 生产过程取样指南 (9)8. 生产过程质量控制 (9)8.1. 前处理 (9)8.2. 制剂 (10)9. 质量标准及检验方法 (10)10. 消耗定额 (11)10.1. 原料消耗定额 (11)10.2. 辅料消耗定额 (11)10.3. 包装材料消耗定额 (11)11. 物料平衡 (12)11.1. 技术指标 (12)11.2. 工序物料平衡 (12)11.3. 包装材料物料平衡 (12)12. 劳动组织与岗位定员、生产周期 (12)13. 技术安全及劳动保护 (13)14. 工艺卫生 (14)15. 综合利用和环境保护 (14)1.药品名称:1.1.品名:藿香正气水1.2.汉语拼音:Huoxiang Zhengqi Shui2.剂型:酊剂3.产品概述:3.1.性状:本品为深棕色的澄清液体(久贮略有浑浊);味辛、苦。

操作规程文件编号:SOP-003 版号:A/0
编制:审核:出厂检验规程批准:生效日期:
2020.3.1
1、目的
保证出厂产品进行了规定的检验和试验,达到有关技术标准和用户规定的
要求。
2、适用范围
适用于指导公司生产的所有通过出厂检验判定为成品的最终检验工作。
3、职责
质量管理部负责按本规程执行。
4、工作内容
4.1质量管理部负责编制检验作业指导书。
检验作业指导书应当确定成品需要
实施常规控制的验证/确认/监视/测量/检验/试验程序与要求,确保每批成品都
符合接收准则。
接收和拒收及其相关处置措施都应予以记录。
4.2产品的《出厂检验作业指导书》的内容原则上应当覆盖已注册或者备案的
产品技术要求中需要常规控制的检验项目和检验方法。
不能覆盖的,应当在产
品检验作业指导书中予以说明。
必要时,应当给出经过确认的替代解决方案。
4.3检验员按标准进行全检或抽样检验,并将检验情况记录在检验记录单上,
签字确认。
合格的成品按照《产品放行控制程序》执行交付;不合格成品按照《不合格品控制程序》执行。
5、相关文件
无
6、相关记录
7.1《出厂检验报告》QCP-25-QR-007
第 1 页共 1 页。
1 目的建立中药车间中药材粉碎岗位标准操作规程,规范本岗位操作人员的具体操作。
2 范围适用于中药车间中药材粉碎岗位的管理。
3 职责3.1中药车间中药材粉碎岗位操作人员负责实施。
3.2生产技术部、质量部负责监督。
4 内容4.1生产前准备4.1.1 生产操作人员必须按照《人员进出生产区更衣标准操作程序》进行更衣,才能进入生产操作间。
4.1.2 检查:操作间、设备及房间的清洁和状态标识牌;有无前次生产清场合格证正/副本,并在有效期内;设备有无“完好”标志和“已清洁”标志;计量器具有无“计量合格证”,并在有效期内;使用工具是否完好;容器具是否有“已清洁”标志。
检查岗位相关文件及生产记录是否齐全。
4.1.3 根据批生产指令、领料单到仓库领取待粉碎处理的中药材,领取时,认真核对品名、批号、数量、检验报告书以及物料放行审核记录,并放置于暂存间。
4.1.4到模具室领取生产指令规定目数和材质的罗。
并检查罗的完整性,发现破损不得使用。
山 东 百 维 药 业 有 限 公 司文件名称 中药车间中药材粉碎岗位标准操作规程文件编号:PM-SOP-003-00起 草 人: 起草日期: 部门:生产技术部审 核 人: 审核日期: 生产副总 页码 1/3 审 核 人: 审核日期: 质量部 版 本 号 00 批 准 人: 批准日期:质量副总生效日期颁发部门 质量部分发部门质量副总、生产副总、质量部、生产技术部、生产车间。
4.1.5 在器具暂存间领取在清洁效期内的不锈钢桶,并内衬洁净塑料袋。
4.1.6 在门前生产标识牌上填写生产品种的相关信息。
4.2 操作过程4.2.1 一切准备就绪,到物料暂存间领取待粉碎的中药材,按《ZKF-3型粉碎机标准操作规程》进行粉碎、过筛,粉碎间只能存放一种中药材,处理完一种中药才后须清场后再处理另一种中药材,将处理过的物料按规定扎口,放于编织袋内,包装内放交接单,外加标示标签:标明品名、规格、批号、数量、生产日期、操作人、复核人。
gmp文件目录生产管理、质量管理文件目录一、办公室文件目录二、质量技术部文件目录三、生产物控部文件目录四、工程部文件目录五、销售部文件目录六、验证文件目录办公室GMP文件目录序号文件编号文件名称1 SMP-AA-001-00 文件书写格式制度2 SMP-AA-002-00 文件分类管理规程3 SMP-AA-003-00 标准的起草、审核、批准、发放、修订和废除管理制度4 SMP-AB-001-00 部门职责5 SMP-AB-002-00 总经理岗位职责6 SMP-AB-003-00 办公室经理岗位职责7 SMP-AB-004-00 财务部经理岗位职责 8 SMP-AB-005-00 质量部经理岗位职责 9 SMP-AB-006-00 生产物控部经理职责10 SMP-AB-007-00 工程部经理岗位职 11 SMP-AB-008-00 销售部经理岗位职责 12 SMP-AB-009-00 QA岗位职责13 SMP-AB-010-00 QC岗位职责14 SMP-AB-011-00 质量部留样观察员岗位职责 15 SMP-AB-012-00 安全员岗位职责16 SMP-AB-013-00 卫生员岗位职责17 SMP-AB-014-00 采购员岗位职责18 SMP-AB-015-00 仓管员岗位职责19 SMP-AB-016-00 生产车间主任岗位 20 SMP-AB-017-00 生产车间操作工岗位职责 21 SMP-AB-018-00 生产车间技术员岗位职责 22 SMP-AB-019-00 空调系统岗位职责 23 SMP-AB-020-00 配电房岗位职责24 SMP-AC-001-00 档案管理规程25 SMP-AC-002-00 员工健康管理规程 26 SMP-AC-003-00 员工培训和教育管理制度 27 SMP-AC-004-00 人员招聘上岗管理规程 28 SMP-AD-001-00 厂区环境卫生、绿化管理制度 29 SMP-AD-002-00 卫生管理制度30 SMP-AE-001-00 劳动纪律管理条例及考核细则 31 SMP-AE-002-00 外来人、车辆、物资进出公司管理规程32 SMP-AE-003-00 文明办公管理规程质量部GMP文件目录序号文件编号文件名称1 SMP-CA-001-00 生产现场质量检查管理规程2 SMP-CA-002-00 技术、质量分析会管理规程3 SMP-CA-003-00 质量事故管理规程4 SMP-CA-004-00 物料、半成品、成品确认放行管理规程5 SMP-CA-005-00 不合格品管理规程6 SMP-CA-006-00 质量投诉管理规程7 SMP-CA-007-00 退货管理规程8 SMP-CA-008-00 产品收回管理规程 9 SMP-CA-009-00 用户访问管理规程 10 SMP-CA-010-00 GMP自检管理规程 11 SMP-CA-011-00 偏差处理管理规程 12 SMP-CA-012-00 称量管理规程13 SMP-CA-013-00 洁净厂房环境监测管理规程 14 SMP-CA-014-00 工艺用水的监测及管理规程 15 SMP-CA-015-00 留样观察管理规程 16 SMP-CA-016-00 物料供应商审计管理规程 17 SMP-CA-017-00 产品质量档案管理规程 18 SMP-CA-018-00 批记录管理规程19 SMP-CA-019-00 取样管理规程20 SMP-CA-020-00 标签管理规程21 SMP-CA-021-00 仓库监控管理规程 22 SMP-CA-022-00 物料检验管理规程23 SMP-CA-023-00 工艺规程的制(修)订、审批、发放管理规程24 SMP-CA-024-00 工艺查证管理规程 25 SMP-CB-001-00 实验室管理规程26 SMP-CB-002-00 试剂室管理规程27 SMP-CB-003-00 实验室温湿度控制管理规程 28 SMP-CB-004-00 质量检验管理规程 29 SMP-CB-005-00 检验原始记录管理规程 30 SMP-CB-006-00 检验报告单的管理规程31 SMP-CB-007-00 检验方法中技术参数和数据处理管理规程32 SMP-CD-001-00 化学试剂管理规程33 SMP-CD-002-00 标准溶液管理规程34 SMP-CD-003-00 标准品、对照品管理规程 35 SMP-CD-004-00 玻璃仪器管理规程36 SMP-CD-005-00 剧毒试剂管理规程37 SMP-CD-006-00 毒害废液、生物活性物质管理规程 38 SMP-CD-007-00 培养基管理规程39 SMP-CE-001-00 检验仪器设备管理规程STP-CF-001-00 XXXXXX工艺规程STP-CF-002-00 食品中水分测定法STP-CF-003-00 灰分测定法STP-CF-004-00 食品中铅的测定STP-CF-005-00 食品中汞的测定STP-CF-006-00 食品中砷的测定STP-CF-007-00 崩解时限检查法STP-CJ-001-00 洁净区(室)的洁净度监测标准SOP-CA-001-00 批生产记录审核操作规程SOP-CA-002-00 物料、半成品、成品审核放行操作规程SOP-CA-003-00 胶囊质量监控操作规程SOP-CA-004-00 清场检查操作规程SOP-CB-001-00 XX电子天平操作规程SOP-CB-002-00 XXX系列鼓风干燥箱操作规程SOP-CB-003-00 XXX型菌落计数器操作规程SOP-CB-004-00 XXX微波/烧烤炉操作规程SOP-CB-005-00 XXX恒温恒湿箱操作规程SOP-CB-006-00 XXX霉菌培养箱操作规程SOP-CB-007-00 XXXF净化工作台操作规程SOP-CB-008-00 ZB—1D型智能崩解仪操作规程SOP-CB-009-00 箱式电阻炉操作规程SOP-CB-010-00 YJ--A电动匀浆仪操作规程SOP-CB-011-00 XXX型立式自动压力蒸气灭菌器操作程序SOP-CC-001-00 盐酸滴定液配制与标定程序SOP-CC-002-00 硝酸银滴定液配制与标定程序SOP-CC-003-00 硫酸滴定液配制与标定程序SOP-CC-004-00 XXXX配制与标定程序SOP-CD-001-00 取样程序SOP-CE-001-00 玻璃仪器清洗程序SOP-CE-002-00 微生物玻璃器皿清洗消毒操作程序SOP-CE-003-00 微生物检验室使用清洁操作程序SOP-CE-004-00 洁净室工作服使用、清洁与灭菌程序SOP-CE-005-00 微生物检验室物品清洁、消毒和灭菌程序SOP-CE-006-00 取样工具及样品容器的清洗、灭菌、保存及传递程序SOP-CE-007-00 冰箱、冷柜的使用清洁程序SOP-CG-001-00 胶囊塑料瓶检验操作规程SOP-CG-002-01 纸盒、纸箱和纸张印刷品检验操作规程SOP-CG-003-01 洁净区域尘粒检测SOP-CG-004-01 洁净区域沉降菌检测生产物控部GMP文件目录序号文件编号文件名称1 SMP-EA-001-00 生产计划和调度管理规程2 SMP-EA-002-00 批生产指令管理规程3 SMP-EA-003-00 产品批号、生产日期和有效期管理规程4 SMP-EA-004-00 生产过程管理规程5 SMP-EA-005-00 物料平衡管理规程6 SMP-EA-006-00 生产车间状态标志和定置管理规程7 SMP-EA-007-00 生产记录管理规程8 SMP-EA-008-00 生产车间安全管理规程9 SMP-EA-009-00 模具间管理规程10 SMP-EA-010-00 生产废弃物的管理规程 11 SMP-EA-011-00 生产过程可利用物料管理规程 12 SMP-EA-012-00 车间新员工培训上岗管理规程 13 SMP-EA-013-00 外来人员进入生产区管理规程 14 SMP-EA-014-00 洁净服、洁净工作鞋管理规程 15 SMP-EA-015-00 一般生产区工作服、工作鞋管理规程 16 SMP-EA-016-00 生产事故处理管理规程 17 SMP-EB-001-00 物料采购管理规程18 SMP-EB-002-00 供应商档案管理规程 19 SMP-EB-003-00 印刷模具管理规程20 SMP-EC-001-00 标签库管理规程21 SMP-EC-002-00 仓库管理规程22 SMP-EC-003-00 物料报表和盘存管理规程 23 SMP-EC-004-00 不合格品库管理规程 24 SMP-EC-005-00 仓库虫鼠防范管理规程 25 SMP-ED-001-00 物料入库管理规程26 SMP-ED-002-00 物料发放、退库管理规程 27 SMP-ED-003-00 物料代号及编号管理规程 28 SMP-EE-001-00 清场管理规程29 SMP-EE-002-00 生产车间消毒管理规程 30 SMP-EE-003-00 乳胶手套、一次性口罩管理规程 31 SMP-EE-004-00 洁净区卫生管理规程 32 SMP-EE-005-00 一般生产区卫生管理规程 33 SMP-EE-006-00 洁净区洁净间管理规程 34 SMP-EE-007-00 一般生产区洁净间管理规程 35 SMP-EE-008-00 容器清洗存放室管理规程36 SMP-EE-009-00 除虫灭害管理规程37 SMP-EE-010-00 杀虫剂的使用管理规程38 SOP-EB-001-00 印字包材交付印刷程序 38 SOP-EC-001-00 仓库设备设施清洁维护规程 39 SOP-EC-002-00 人员进出危险品库操作程序 40 SOP-ED-001-00 标签寄入退库、存放、领发程序41 SOP-ED-002-00 请求补料标准操作程序 42 SOP-ED-003-00 物料寄库清洁程序43 SOP-ED-004-00 货位卡填写标准操作程序 44 SOP-ED-005-00 不合格标签的退库与销毁 45 SOP-EE-001-00 XXX产品岗位标准操作程序 46 SOP-EF-001-00 生产操作前检查标准操作程序 47 SOP-EF-002-00 称量岗位标准操作程序 48 SOP-EF-003-00 领退料标准操作程序 49 SOP-EF-004-00 胶囊制剂装量差异检查标准操作程序 50 SOP-EF-005-00 生产过程中紧急、异常情况处理标准操作程序51 SOP-EF-006-00 消毒剂配制和使用标准操作程序 52 SOP-EF-007-00 洁净区地漏消毒标准操作程序 53 SOP-EF-008-00 酒精配制标准操作程序 54 SOP-EF-009-00 传递窗使用程序55 SOP-EF-010-00 进入生产区标准操作程序 56 SOP-EF-011-00 进出洁净区标准操作程序 57 SOP-EF-012-00 车间物料进出洁净区程序 58 SOP-EG-001-00 XXX设备清洁标准操作程序 59 SOP-EH-001-00 公共操作间清洁标准操作程序工程部GMP文件目录序号文件编号文件名称1 SMP-FA-001-00 安全管理规程2 SMP-FA-002-00 安全事故报告管理规程3 SMP-FA-003-00 动火管理规程4 SMP-FA-004-00 消防器材管理规程5 SMP-FA-005-00 防尘、防毒、防职业病管理规程6 SMP-FA-006-00 三废排放管理规程7 SMP-FB-001-00 固定资产管理规程8 SMP-FB-002-00 锅炉、压力容器管理规程 9 SMP-FB-003-00 设备开箱验收管理规程 10 SMP-FB-004-00 设备档案管理规程11 SMP-FB-005-00 设备管理规程12 SMP-FB-006-00 动力设备管理规程13 SMP-FB-007-00 空调净化系统管理规程 14 SMP-FB-008-00 锅炉水质检测管理规程 15 SMP-FB-009-00 备品、备件管理规程 16 SMP-FB-010-00 设备的使用管理规程 17 SMP-FC-001-00 厂房、设施管理规程 18 SMP-FC-002-00 洁净区维修施工管理规程 19 SMP-FD-001-00 配电房管理规程20 SMP-FJ-001-00 计量器具管理规程21 SMP-FJ-002-01 计量器具统一编号管理规程 22 SMP-FJ-003-01 不合格计量器具管理规程 23 SMP-FN-001-00 停电、停汽、停水处理规程26 SOP-FB-001-00 XXX全自动胶囊填充机标准操作程序 27 SOP-FB-002-00 XXX全自动胶囊填充机维护保养程序 28 SOP-FB-003-00 XXXX型热风循环烘箱标准操作程序 29 SOP-FB-004-00 XXXX型热风循环烘箱维护保养程序 30 SOP-FB-005-00 XXXX封口机标准操作程序 31 SOP-FB-006-00 XXXX封口机维护保养程序销售部GMP文件目录序号文件编号文件名称1 SMP-GA-001-00 产品销售管理规程2 SMP-GA-002-00 成品验收、贮存、发放管理规程3 SOP-GA-001-00 成品入库操作规程4 SOP-GA-002-00 成品运输操作规程5 SOP-GA-003-00 成品出库操作规程6 SOP-GA-004-00 产品收回操作规程验证文件目录序号文件编号文件名称1 SMP-ZA-001-00 验证管理规程固体生产线HVAC系统验证 3 STP-ZA-002-004 STP-ZA-003-00 质检区HVAC系统验证5 STP-ZA-004-00 压缩空气系统验证6 STP-ZB-001-00 XX产品工艺验证STP-ZC-001-00 全自动胶囊填充机清洗验证 8XXX全自动胶囊充填机验证 9 STP-ZE-001-0010 STP-ZE-002-0011 STP-ZE-003-00XXXX型热风循环烘箱验证 12 STP-ZE-004-00XXXX封口机验证(DL-500E微电脑电磁感应封口机) 13 STP-ZE-005-00下面是赠送的合同范本,不需要的可以编辑删除~~~~~~教育机构劳动合同范本为大家整理提供,希望对大家有一定帮助。
质量管理标准操作规程(SOP)目录。
1.目的:明确原辅料取样的标准操作规程。
2.范围:原辅料的取样。
3.责任:QA检查员、仓库管理员。
4.内容:4.1 取样程序:4.1.1 QA检查员在接到仓库管理员的检验通知报告单后的两个工作日内,到仓库待验区,在仓库管理员的协助下进行取样操作。
4.1.2 取样前,QA检查员先根据检验通知报告单内容核对待验品的品名、批号、容器数,来源及原辅料供应商所提供的出厂检验报告单是否符合、一致。
4.1.3 QA检查员应先对待验的外包装进行检查是否无污染、水渍、虫蛀、霉变、混杂等情况,如不符合要求,应拒绝抽样,待原因调查清楚,经主管负责人批准后才可抽样。
4.1.4取样应用取样器具固体:不锈钢探子、不锈钢勺、不锈钢铲、不锈钢镊子液体:玻璃采样管、玻璃油提样品应置于标准容器中固体:具有封口装置的无毒塑料袋液体:具盖玻璃瓶,无毒塑料袋需取无菌样品时,以上相应器具均应无菌4.1.5由仓库管理员打开物料内外包装(注意:应穿清洁服、戴口罩、手套),由QA检查员检查外观(色泽、嗅味等)。
4.1.6取完一种物料的样品后,应先由仓库管理员将包装封好,再取下一种物料。
取不同种物料时,应更换一次性手套及取样工具以避免污染物料。
4.1.7确认所取样品的均一性,取样应具有代表性,并符合各有关测试标准的要求,所取样品应放在带盖瓶(或有色瓶或塑料袋)中。
4.1.8 取样时QA检查员与仓库管理员均必须换清洁服,并戴一次性口罩、手套。
避免交叉污染。
而且必要时应更换,以避免发生混药。
4.1.9取样工具必须洁净,使用前,用75%的酒精棉消毒;使用后,用清水反复冲洗数次,再用去离子水冲洗二遍,自然晾干后,保存在干燥、洁净、无污染的柜中,或包于无纤维脱落、无毒的塑料袋中。
4.1.10 取样后:在容器外标签上注明取样量、取样日期及取样人签字。
4.1.11取样时,如发现不同容器中所取样品外观有异常,或者某个包装有损坏,则应单独取样,以证实是否一致,并在标签的备注栏内清楚注明。
文件编号:SC-SOP-003-00 第 1 页共 3 页
1目的:建立本文件使炮制工序的整个生产过程标准化、规范化、合理化,以确保中药饮片生产质量,生产过程的人员安全与设备安全。
2范围:本文件适用于中药材的炒黄的生产操作。
3使用设备及操作标准
3.1操作人员按照《炒黄SOP》对其进行操作。
4职责
4.1操作人员:严格按本文件对中药饮片生产过程中需炒黄的生品饮片进行操作和控制。
4.2QA现场监控员:监督和检查炮制工序的操作是否规范化、标准化、合理化。
5内容
5.1生产用具的领取与班前检查
5.1.1由操作人员在容器存放间及其它相关辅助房间领取能满足生产需求的盛药器具(如
盛装用桶、口袋)、工具等,由中间站管理员发放,双方应核对领取物料的数量是否准确,盛药器具、工具是否为已清场物品与完好状况,与生产要求无误后填写《生产用具领发台帐》。
5.1.2操作人员将所领取的中药材和生产用具分别按管理要求放在炒药间规定位置。
5.1.3若需炒药前,则操作员将检查炒药间及与药材接触的炒药机、接料槽、凉药盘是否
为已清场。
5.1.4炒药操作人员将根据《中国药典》2000版一部、《全国中药炮制规范》、《广西中药炮
制规范》炮制要求对药材进行炮制。
5.1.5操作人员打开炒药间窗口内窗玻璃,并拉上沙窗,外窗保持关闭,以防蚊虫飞入炒
药操作间。
5.1.6检查房间电源情况,地漏通畅情况。
5.2开工检查:
文件编号:SC-SOP-003-00 第 2 页共 3 页5.2.1炮制工序长领到相应的生产记录后与本岗位操作人员、QA现场监控员一起进行下面
的开工检查项目,符合规定后方可进行生产。
5.2.2炮制工序应无与所生产批次无关的指令和记录。
5.2.3生产环境符合要求:
5.2.3.1炒药间挂有“已清场”标记。
5.2.4无与所生产批次无关的物料。
5.2.5炒药机挂有“完好”的状态标记。
5.2.6QA现场监控员检查符合上述规定后认可,准予生产。
5.2.7操作人员在“生产状态卡”上如实填写品名、批号、数量、开始生产时间、岗位负
责人后在操作间门上挂上“生产状态卡”,取下“已清场”状态标记。
5.3炮制工序物料的领取:
5.3.1炮制工序操作人员凭《批生产指令》在净药间领取生产饮片。
5.3.2领料时操作人员在领取时要与复核人、中间站管理员一起核对中药材的产品名称、
批号、净选程度。
核对包装情况是否符合密闭的原则且其外观无异常情况。
核对中药材重量、桶数是否与其外表面所贴的桶笺标示一致。
5.3.3三方核对无误后操作人员领取中药材并与中间站管理员一起填写《物料进出中间站
台帐》。
5.4炒黄操作法
5.4.1操作标准
5.4.1.1严格按照(CY-700型滚筒式液化气炒药机操作、维护保养SOP)检查炒药机气源、
电源、水处理装置等。
5.4.1.2启动电源,开启油箱气源,开启水处理装置,转动锅体,开始点火,在中火状态下
加热3分钟左右,使锅内较热(约50℃左右),将所需药材投入锅内,按照各品种《炮制工艺规程》要求的火力大小进行炒制。
5.4.2一般当药物表面呈黄色或较原色稍深,或发泡鼓起,或有爆裂声,溢出其固有气味
时,停止加热,开启出料开关,将药物倾倒于接料槽,平摊于凉药盘内。
5.4.2.1Q A现场监控员检查炒制火候。
5.4.2.2 继续中速正向转动锅体,待锅体温度降至较热时(约50℃左右)继续下一锅药材
文件编号:SC-SOP-003-00 第 3 页共 3 页的炒制;并继续将炒制药物平摊于凉药盘内,按《炒制、炙制混和SOP》进行混合均匀。
当炒制药物温度降至室温时(一般摊凉12小时),收集药物,称定重量,交接至中间站。
5.4.2.2当炒制工作结束,继续中速正向转动锅体,待锅体温度降至室温时,用软管加入饮
用水适量,清洗锅体,5分钟之后将洗锅水倾入接料槽,继续中速正转锅体加热1分钟左右,去除余水保持锅体干燥。
关闭电源和气源。
5.4.2.3摊凉完成后和干燥工序人员作好交接工作,由干燥工序人员将其转入筛选间进行筛
选。
5.5废弃物的处理:操作人员按照《剩余物料处理SOP》处理废弃物并在炒黄生产记录上
如实填写。
5.6清场
5.6.1严格执行《清场管理程序》,清场应涉及到人、机、料、法、环每个环节。
5.6.2将“生产状态”牌刷新;取下设备“运行中”标记,换上“未运行”状态标记;房
间挂上“待清洁”标记。
5.6.3严格按照相应清洁SOP对炒药机、地面、墙面、门窗等设备、设施进行清洁。
5.6.4清场后经QA现场监控员检查合格后在生产记录上签字认可后,操作人员在炒药房间
规定位置挂上“已清场”标记。
5.7生产指令与生产记录的填写与流转
5.7.1按照《生产记录发放、填写与整理SOP》对记录进行填写与整理。
5.7.2操作人员、复核人员与QA现场监控员均应在所涉及的生产记录上填写。
5.7.3生产记录的填写应及时、如实、同步填写。
5.8质量控制
5.8.1随时观察炒药火候和水处理装置的除尘效果。
生产过程如果出现偏差执行《偏差处理管理程序》。