高二化学金属晶体2
- 格式:pdf
- 大小:627.39 KB
- 文档页数:9



高二化学(沪科版2020选择性必修2 物质结构与性质)第三章晶体结构与性质3.1 金属晶体★基础过关练★1.下列关于晶体的说法中正确的是A.自然形成的水晶柱是晶体,从水晶柱上切削下来的粉末不是晶体B.晶胞中任何一个粒子都属于该晶胞C.玻璃制成的弹珠具有规则的几何外形,所以玻璃弹珠是晶体D.缺角的NaCl晶体在饱和NaCl溶液中慢慢变为完美的立方体块,体现了晶体的自范性【答案】D【详解】A.晶体形成后,其结构是有序性和可复制性,所以即使是粉末,其微观结构也是晶体的有序结构,描述错误,不符题意;B.晶胞的顶点、棱上、面上的离子均为多个晶胞共用,描述错误,不符题意;C.玻璃属于混合物,不是晶体,描述错误,不符题意;D.晶体的自范性能使结构有缺损的晶体结构在适当的环境中恢复晶体完整,描述正确,符合题意;综上,本题选D。
2.下列物质中,属于晶体的是A.玻璃B.石蜡和沥青C.塑料D.干冰【答案】D【详解】干冰属于分子晶体,玻璃、石蜡、沥青、塑料均属于非晶体,综上所述,D项正确;故选D。
3.关于晶体的自范性,下列叙述正确的是()A.破损的晶体能够在固态时自动变成规则的多面体B.缺角的氯化钠晶体在饱和NaCl溶液中慢慢变为完美的立方体块C.圆形容器中结出的冰是圆形的,体现了晶体的自范性D.由玻璃制成规则的玻璃球体现了晶体的自范性【答案】B【详解】晶体的自范性指的是在适宜条件下,晶体能够自发地呈现规则的多面体外形的性质,这一适宜条件一般指的是自动结晶析出的条件,A项所述过程不可能实现,错误;C项中的圆形并不是晶体冰本身自发形成的,而是受容器的限制形成的,错误;D项中玻璃是非晶体,错误。
4.下列叙述中,正确的是A.石英玻璃和水晶都是晶体B.具有各向异性的固体可能是晶体C.粉末状的固体肯定不是晶体D.晶体与非晶体的根本区别在于固体是否具有规则的几何外形【答案】B【详解】A.石英玻璃是非晶态(玻璃态)的SiO2,石英玻璃不是晶体,水晶是晶体,A项错误;B.晶体的许多物理性质,如强度、导热性、光学性质等会表现出各向异性,B项正确;C.许多粉末状的固体用肉眼看不到晶体外形,但在光学显微镜或电子显微镜下可观察到规则的晶体外形,说明这些粉末状的固体仍是晶体,C项错误;D.晶体与非晶体的根本区别在于粒子在微观空间是否呈周期性的有序排列,D项错误;答案选B。

化学金属晶体知识点总结一、金属晶体的基本概念金属晶体是由金属原子以一定规律排列组成的固体结构。
金属晶体具有一些特点,如具有金属典型的电性能、热性能和光学性能,同时还具有良好的延展性、韧性和导电性。
二、金属晶体的结构金属晶体的结构是由金属原子通过化学键相互连接而形成的。
金属晶体的结构有多种类型,其中最常见的是面心立方晶体结构和体心立方晶体结构。
金属晶体的结构对金属的性能具有重要影响,比如面心立方晶体结构使得金属具有优良的导电性和导热性,而体心立方晶体结构使得金属具有良好的韧性和延展性。
三、金属晶体的性能1. 导电性:金属晶体中的自由电子能够在晶体结构中自由传导,因此金属具有良好的导电性能。
2. 导热性:金属晶体中的自由电子能够在晶体结构中迅速传递热量,因此金属具有良好的导热性能。
3. 延展性:金属晶体中的金属原子之间的化学键相对较弱,因此金属具有良好的延展性能,可以被拉伸成细丝或者铺展成薄片。
4. 韧性:金属晶体中的金属原子之间的化学键相对较强,因此金属具有良好的韧性能,可以经受一定的外力而不易断裂。
5. 耐腐蚀性:金属晶体中的化学键特点使得金属具有一定的抗腐蚀性能,可以抵御外界腐蚀物质的侵蚀。
四、金属晶体的制备金属晶体的制备方法有多种,常见的包括熔融法、沉淀法、溶胶-凝胶法等。
熔融法是通过将金属加热至熔点后冷却凝固成固体晶体;沉淀法是通过将金属盐溶液中加入适量还原剂使金属物质析出,然后经过洗涤、干燥等处理制备金属晶体;溶胶-凝胶法是通过将金属盐加入溶液中形成凝胶后再经过热处理的方法制备金属晶体。
五、金属晶体的应用金属晶体广泛应用于工业生产中,主要包括金属材料、金属合金、金属催化剂等。
金属材料广泛用于航空航天、汽车制造、机械加工等领域;金属合金具有优异的物理性能和化学性能,用于制备高强度、高耐热、高耐腐蚀的材料;金属催化剂广泛用于化工生产中的有机合成、空气净化等领域。
总的来说,金属晶体是由金属原子组成的固体结构,在工业生产和科研领域有重要应用。

高山不爬不能到顶,竞走不跑不能取胜,永恒的幸福不争取不能获得。
想成为一名成功者,先必须做一名奋斗者。
《选修三第三章第三节 金属晶体》导学案(第2课时)高二 班 第 组 姓名 组内评价 教师评价_______【课标要求】1、能列举金属晶体的基本堆积模型2、了解金属晶体性质的一般特点3、理解金属晶体的类型与性质的关系 【重点难点】1、金属晶体的堆积方式 【新课导学】 二、金属晶体 1、金属晶体:(1)定义: 和 通过 形成的晶体。
(2)构成微粒: 。
(3)微粒间相互作用: 。
2、金属晶体的原子堆积模型Ⅰ、概念 ①紧密堆积:微粒之间的作用力,使微粒间尽可能地相互接近,使它们占有最小的空间 ②空间利用率:空间被晶格质点占满的百分数。
用来表示紧密堆积的程度 ③配位数:在晶体中,与离子直接相连的带异电荷的离子数称为配位数 Ⅱ、金属晶体的原子堆积模型(1) 金属原子在二维平面里有两种方式为非密置层和密置层__层,配位数为 _______层,配位数为 (2)金属原子在三维空间里有四种堆积方式①简单立方体堆积,非密置层排列的金属原子,在空间内可能的排列。
这种堆积方式形成的晶胞是一个 ,每个晶胞含 个原子,被称为 堆积。
这种堆积方式的空间利用率 ,只有金属钋采取这种堆积方式。
②体心立方(A 2型)堆积----钾型如果是非密置层上层金属原子填入下层的金属原子形成的凹穴中,每层均照此堆积,如下图:这种堆积方式所得的晶胞是一个含 个原子的立方体,一个原子在立方体的 ,另一个在立方体的 ,称为体心立方堆积,这种堆积方式的空间利用率( )显然比简单立方堆积的 多了,许多金属是这种堆积方式,如碱金属,简称为钾型。
③六方最密堆积(A 3)型和面心立方(A 1型)最密堆积对于密置层的原子按钾型堆积方式堆积,会得到两种基本堆积方式---- 和 ,即:镁型和铜型。
六方最密堆积如下图左侧,按 的方式堆积; 面心立方最密堆积如图右侧,按 的方式堆积.这两种堆积方式都是金属晶体的 堆积,配位数均为 ,空间利用率均为 ,但所得的晶胞的形式不同。

2023年高二化学教案金属晶体(精选3篇)教案1:金属晶体的特性及其影响因素【教学目标】1. 了解金属晶体的基本特性,包括密堆积、金属键、金属晶格等。
2. 分析金属晶体结构的影响因素,包括原子大小、电子数目等。
3. 能够运用金属晶体的特性解释金属的一些性质,如导电性、延展性等。
【教学内容】1. 金属晶体的基本特性:密堆积、金属键、金属晶格。
2. 金属晶体结构的影响因素:原子大小、电子数目等。
3. 金属晶体特性在金属性质中的应用。
【教学重点】1. 金属晶体的结构特性。
2. 金属晶体结构的影响因素。
3. 运用金属晶体特性解释金属性质。
【教学难点】1. 理解金属晶体的密堆积结构及金属键。
2. 分析金属晶体结构的影响因素。
【教学方法】讲授法、实验法、探究法、讨论法。
【教学过程】1. 导入:通过一些生活中常见的金属饰品,让学生观察其结构特点,引导学生思考金属晶体的结构。
2. 展示金属晶体的基本特性:密堆积、金属键、金属晶格,让学生了解其基本特点。
3. 分析金属晶体结构的影响因素,如原子大小、电子数目等,引导学生思考这些因素对金属晶格结构的影响。
4. 进行一些案例分析,让学生运用金属晶体的特性解释金属的一些性质,如导电性、延展性等。
5. 总结金属晶体的特性及其影响因素。
【教学评价】教师通过学生的观察和讨论,以及对应用题的解答情况,评价学生对金属晶体的特性和其影响因素的理解程度。
教案2:金属晶体的结构和性质【教学目标】1. 知道金属晶体的结构特点,如密堆积结构、金属键等。
2. 理解金属晶体结构对金属性质的影响,如导电性、延展性等。
3. 了解金属晶体在实际应用中的一些应用。
【教学内容】1. 金属晶体的结构特点:密堆积结构、金属键等。
2. 金属晶体结构对金属性质的影响。
3. 金属晶体在实际应用中的一些应用。
【教学重点】1. 金属晶体的结构特点。
2. 金属晶体结构对金属性质的影响。
【教学难点】1. 理解金属晶体结构对金属性质的影响。



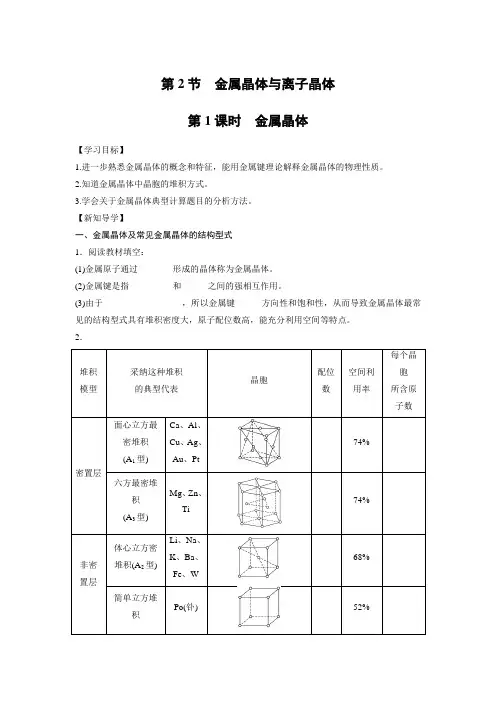
第2节金属晶体与离子晶体第1课时金属晶体【学习目标】1.进一步熟悉金属晶体的概念和特征,能用金属键理论解释金属晶体的物理性质。
2.知道金属晶体中晶胞的堆积方式。
3.学会关于金属晶体典型计算题目的分析方法。
【新知导学】一、金属晶体及常见金属晶体的结构型式1.阅读教材填空:(1)金属原子通过________形成的晶体称为金属晶体。
(2)金属键是指__________和______之间的强相互作用。
(3)由于__________________,所以金属键______方向性和饱和性,从而导致金属晶体最常见的结构型式具有堆积密度大,原子配位数高,能充分利用空间等特点。
2.、、、、【归纳总结】组成晶体的金属原子在没有其他因素影响时,在空间的排列大都服从紧密堆积原理。
这是因为在金属晶体中,金属键没有方向性和饱和性,因此都趋向于使金属原子吸引更多的其他原子分布于周围,并以密堆积方式降低体系的能量,使晶体变得比较稳定。
【活学活用】1.有四种不同堆积方式的金属晶体的晶胞如下图所示,有关说法正确的是()A.①为简单立方堆积,②为六方最密堆积,③为体心立方密堆积,④为面心立方最密堆积B.每个晶胞含有的原子数分别为①1个,②2个,③6个,④4个C.晶胞中原子的配位数分别为①6,②8,③8,④12D.空间利用率的大小关系为①<②<③<④2.Al的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。
若已知Al的原子半径为d,N A代表阿伏加德罗常数,Al的相对原子原子质量为M,请回答:(1)晶胞中Al原子的配位数为________,一个晶胞中Al原子的数目为________。
(2)该晶体的密度为__________(用字母表示)。
3.铜的堆积方式属于A1型紧密堆积,其晶胞示意图为______(填字母)。
晶胞中所含的铜原子数为______个。
金属铜晶胞为面心立方最密堆积,边长为a cm。
