品质体系简介共42页
- 格式:ppt
- 大小:1.63 MB
- 文档页数:42






ISO9000:2000质量管理体系基础与术语(doc 42页)GB 中华人民共和国国家标准GB/T 19000—2000Idt: ISO9000:2000质量管理体系标准Quality management system standards2000-12-28发布 2001-06-01实施国家质量技术监督局发布GB/T 19000-2000前言本标准等同采用ISO 9000:2000《质量管理体系基础和术语》。
本标准是GB/T 19000族标准之一。
标准中的“应”(shall)表示要求,“应当”(should)仅起指导作用。
由于两种语言上的差异,术语3.1.5capability与3.9.12competence 均译为“能力”,但其定义却不同。
在GB/T 19000族标准中,术语3.1.5能力(capability)特指组织、体系或过程的“能力”,而3.9.12能力(competence)则特指人员的“能力”。
某些定义下面所加的“注”,是为英文版国际标准的使用者所提供的附加信息(如3.2.6中的“注”,3.6.1中的“注2”,3.6.13中的“注”和3.7.2中的“注2”),为等同采用国际标准,本标准仍保留了这些内容。
本标准对GB/T 6583-1994作了技术性修订,故本标准发布时,代替GB/T 6583-1994。
本标准的附录A是提示的附录。
本标准由全国质量管理和质量保证标准化技术委员会(CSBTS/T C151)提出并归口。
本标准由中国标准研究中心负责起草。
本标准起草单位:中国标准研究中心、中国合格评定国家认可中心、上海市标准化研究院,航天科技集团七O八研究所、中国船级社、深圳市中兴通讯股份有限公司、中国天辰化学工程公司、中国新时代质量体系认证中心。
本标准主要起草人:李镜、徐有刚、陆关新、郭瑞霞、顾作甫、李溯、乔悦生、郑燕。
GB/T 19000-2000ISO前言国际标准化组织(ISO)是由各国标准化团体(ISO成员团体)组成的世界性联合会。


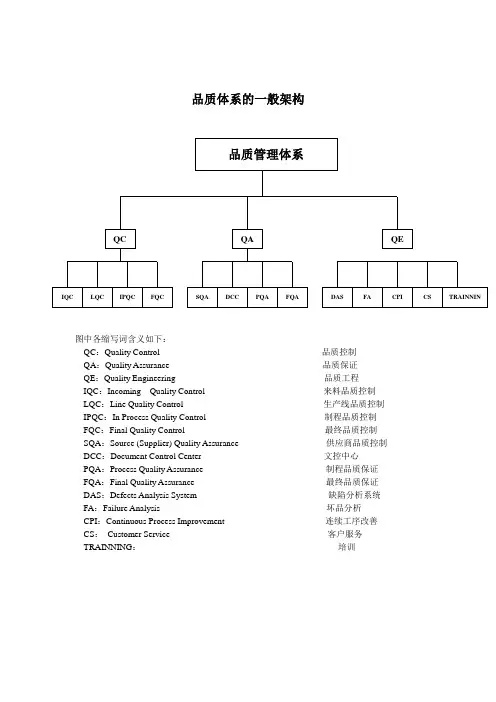
品质体系的一般架构图中各缩写词含义如下:QC:Quality Control 品质控制QA:Quality Assurance 品质保证QE:Quality Engineering 品质工程IQC:Incoming Quality Control 来料品质控制LQC:Line Quality Control 生产线品质控制IPQC:In Process Quality Control 制程品质控制FQC:Final Quality Control 最终品质控制SQA:Source (Supplier) Quality Assurance 供应商品质控制DCC:Document Control Center 文控中心PQA:Process Quality Assurance 制程品质保证FQA:Final Quality Assurance 最终品质保证DAS:Defects Analysis System 缺陷分析系统FA:Failure Analysis 坏品分析CPI:Continuous Process Improvement 连续工序改善CS:Customer Service 客户服务TRAINNING:培训一供应商品质保证(SQA)1.SQA概念SQA即供应商品质保证,识通过在供应商处设立专人进行抽样检验,并定期对供应商进行审核、评价而从最源头实施品质保证的一种方法。
是以预防为主思想的体现。
2.SQA组织结构3.主要职责1)对从来料品质控制(IQC)/生产及其他渠道所获取的信息进行分析、综合,把结果反馈给供应商,并要求改善。
2)耕具派驻检验远提供的品质情报对供应商品质进行跟踪。
3)定期对供应商进行审核,及时发现品质隐患。
4)根据实际不定期给供应商导入先进的品质管理手法及检验手段,推动其品质保证能力的提升。
5)根据公司的生产反馈情况、派驻人员检验结果、对投宿反应速度及态度对供应商进行排序,为公司对供应商的取舍提供依据。

质量体系医疗器械GBT19001ISO9001应用的专用要求(doc 42页)质量体系-医疗器械GB/T19001-ISO9001运用的公用要求前言 (3)0引言 (4)0.1总那么 (4)0.2进程方法 (4)0.3与其他规范的关系 (4)0.4与其它管理体系的相容性 (5)1范围 (5)1.1总那么 (5)1.2运用 (5)2援用规范 (6)3术语和定义 (6)4质量管理体系 (7)4.1总要求 (7)4.2文件要求 (8)5管理职责 (9)5.1管理承诺 (9)5.2 以顾客为关注焦点 (9)5.3 质量方针 (9)5.4 筹划 (10)5.5职责、权限和沟通 (10)5.6管理评审 (10)6资源管理 (11)6.1资源提供 (11)6.2人力资源 (11)6.3 基础设备 (12)6.4 任务环境 (12)7产品完成 (12)7.1产品完成的筹划 (12)7.2与顾客有关的进程 (13)7.3 设计和开发 (13)7.4推销 (15)7.5消费和效劳提供 (16)7.6监视和测量装置的控制 (18)8测量、剖析和改良 (19)8.1总那么 (19)8.2监视和测量 (19)8.3不合格品的控制 (20)8.4数据剖析 (20)8.5改良 (21)附录A (22)附录B (26)参考文献目录 (50)本规范同等采用ISO13485:2003«医疗器械质量管理体系用于法规的要求»本规范将取消并替代YY/T0287:1996和YY/T0288:1996。
过去运用YY/T0288:1996的组织可以依照1.2条,经过删减某些要求来运用本规范。
由于任何规范都会被修订,本规范出版时,本规范援用文件的最新的版本〔包括任何修正〕适用。
本规范是一个以GB/T19001为基础的独立规范,并遵照了ISO9001 GB/T19001的格式。
为了方便医疗器械行业的运用者,在本规范的注释中,与GB/T19001不同的内容采用黑色宋体字表示。

YY/T0287-2003质量体系-医疗器械GB/T19001-ISO9001应用的专用要求前言 (3)0引言 (4)0.1总则 (4)0.2过程方法 (4)0.3与其他标准的关系 (4)0.4与其它管理体系的相容性 (5)1范围 (5)1.1总则 (5)1.2应用 (5)2引用标准 (6)3术语和定义 (6)4质量管理体系 (7)4.1总要求 (7)4.2文件要求 (8)5管理职责 (9)5.1管理承诺 (9)5.2 以顾客为关注焦点 (9)5.3 质量方针 (9)5.4 策划 (10)5.5职责、权限和沟通 (10)5.6管理评审 (10)6资源管理 (11)6.1资源提供 (11)6.2人力资源 (11)6.3 基础设施 (12)6.4 工作环境 (12)7产品实现 (12)7.1产品实现的策划 (12)7.2与顾客有关的过程 (13)7.3 设计和开发 (13)7.4采购 (15)7.5生产和服务提供 (16)7.6监视和测量装置的控制 (18)8测量、分析和改进 (19)8.1总则 (19)8.2监视和测量 (19)8.3不合格品的控制 (20)8.4数据分析 (20)8.5改进 (21)附录A (22)附录B (26)参考文献目录 (50)本标准等同采用ISO13485:2003《医疗器械质量管理体系用于法规的要求》本标准将取消并代替YY/T0287:1996和YY/T0288:1996。
过去使用YY/T0288:1996的组织可以按照1.2条,通过删减某些要求来使用本标准。
由于任何标准都会被修订,本标准出版时,本标准引用文件的最新的版本(包括任何修改)适用。
本标准是一个以GB/T19001为基础的独立标准,并遵循了ISO9001 GB/T19001的格式。
为了方便医疗器械行业的使用者,在本标准的正文中,与GB/T19001不同的内容采用黑色宋体字表示。
本标准中所加的“注”是为英文版国际标准的使用者所提供的附加信息,为等同采用国际标准,本标准仍保留了这些内容。