高三化学物质的分类酸碱盐氧化物的相互关系教学案
- 格式:doc
- 大小:248.00 KB
- 文档页数:8

福建省漳州市芗城中学高中化学第一单元第二课时物质的分类及转化教案苏教版必修1学目标:1.能够说出常见物质的类别2.利用概念图的方法明确酸碱盐之间的转化关系3.能够对所给物质进行分类4.归纳常见反应类型的特征,并能举例说明5.能够用示例法初步了解复分解反应的条件6.根据化合价的变化判断反应是否属于氧化还原反应教学重点:1.根据物质的组成对物质进行分类。
2.酸、碱、盐、氧化物之间的相互转化关系。
3.四种化学反应类型与氧化还原反应的关系。
教学难点:引导学生从物质的宏观性质的学习和研究转入从微观角度分析研究问题。
学法指导:预习、讨论交流,实验操作。
教学用具:CAI课件教学过程:[导入新课]:我们知道,化学世界绚丽多彩,千姿百态,奥妙无穷。
请同学们我们在初中学过哪些种类的物质,我们是任何对它们行分类的?学生讨论回答:水、空气、食盐、酒精、蔗糖、甲烷、硫酸、烧碱、氢气、铁、铜……[板书]:物质的分类及转化一、物质的分类[交流与讨论]:请同学们根据课前预习的内容,将我们日常生活中经常接触的几种物质:空气、乙醇、硫酸铵、铜、碘酒、氢气、石墨、食盐水进行分类,(学生讨论交流、教师巡视、参与讨论、给予指导)[小结]:从存在状态分:固态----硫酸铵、铜、食盐、石墨;液态----食盐水、乙醇、碘酒;气态----空气、氢气。
从组成和性质分:混合物----空气、食盐水、碘酒;有机物----乙醇;单质----铜(金属)、氢气、石墨(非金属);盐----硫酸铵。
[交流与讨论]:根据物质组成的分类方法怎样判断单质和化合物有人说H2O2是由H2和O2组成的混合物,你同意吗?KClO3是不是氧化物?学生:思考讨论教师:在学生完成讨论后。
找学生回答,说明以下几点单质和化合物的区别是看组成物质的元素种类组成与构成的区别氧化物是指两种元素组成的化合物,其中一种为氧元素[归纳小结]:请同学们阅读教材第3页图1—2,熟悉按组成分类的概念关系图。
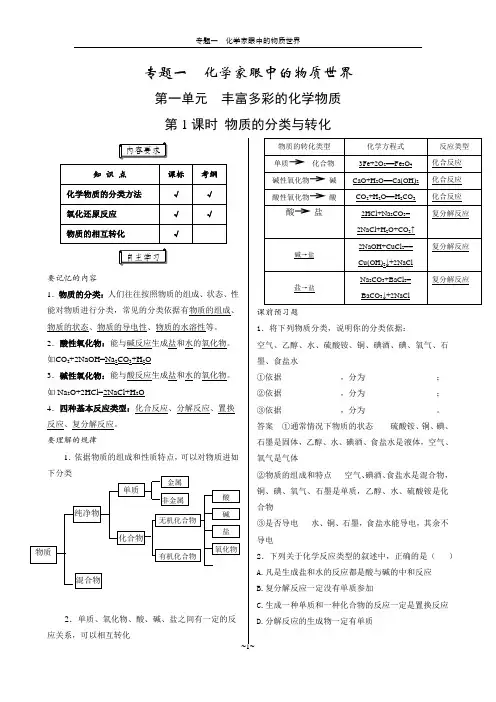
专题一化学家眼中的物质世界第一单元丰富多彩的化学物质第1课时物质的分类与转化要记忆的内容1.物质的分类:人们往往按照物质的组成、状态、性能对物质进行分类,常见的分类依据有物质的组成、物质的状态、物质的导电性、物质的水溶性等。
2.酸性氧化物:能与碱反应生成盐和水的氧化物。
如CO2+2NaOH=Na2CO3+H2O3.碱性氧化物:能与酸反应生成盐和水的氧化物。
如Na2O+2HCl=2NaCl+H2O4.四种基本反应类型:化合反应、分解反应、置换反应、复分解反应。
要理解的规律1.依据物质的组成和性质特点,可以对物质进如2.单质、氧化物、酸、碱、盐之间有一定的反应关系,可以相互转化课前预习题1.将下列物质分类,说明你的分类依据:空气、乙醇、水、硫酸铵、铜、碘酒、碘、氧气、石墨、食盐水①依据______________,分为_________________;②依据______________,分为_________________;③依据______________,分为_________________。
答案①通常情况下物质的状态硫酸铵、铜、碘、石墨是固体,乙醇、水、碘酒、食盐水是液体,空气、氧气是气体②物质的组成和特点空气、碘酒、食盐水是混合物,铜、碘、氧气、石墨是单质,乙醇、水、硫酸铵是化合物③是否导电水、铜、石墨,食盐水能导电,其余不导电2.下列关于化学反应类型的叙述中,正确的是()A.凡是生成盐和水的反应都是酸与碱的中和反应B.复分解反应一定没有单质参加C.生成一种单质和一种化合物的反应一定是置换反应D.分解反应的生成物一定有单质【例6】下列转化不能一步实现的是() A.CuO―→Cu(OH)2B.CuSO4―→CuC.CaCO3―→CaOD.MgSO4―→MgCl2解析CuO难溶于水,所以不会一步转化为Cu(OH) Fe能从CuSO4溶液中置换出Cu,高温分解CaCO3得到CaO,MgSO4和BaCl2反应可以生成BaSO4 MgCl2,所以答案为B。

第二章化学物质及其变化第一节物质的分类【学习目标】1、学会从多角度、依据不同标准对物质进行分类。
2、知道“交叉分类法〞和“树状分类法〞是两种常用的分类方法。
3、能根据化学反响的不同的情况对化学反响进行分类,初步认识各类物质之间的反响关系。
【学习重点】1、酸、碱、盐、氧化物等之间的转化关系。
2、会运用树状分类法和交叉分类法。
预习案【根底知识】阅读课本P24-25完成一、常见的分类法1、交含义根据不同的分类标准,〔〕进行多种分类的一种分类方法叉盐〔根据阳离子〕___分举例Na2CO3——盐〔根据阴离子〕类—盐〔根据溶解性〕树含义对〔〕事物按照某种属性进行〔〕的分类法状纯洁物---分举例物质类----------2、在不同的物质和它所属的类别之间进行连线K2SO4K2CO3Na2CO3Na2SO4钾盐钠盐硫酸盐碳酸盐二、分类方法的应用1、回忆初中化学知识对所学化学反响进行分类?2、常见物质之间的转化关系?总结以下转化关系Ca -------CaO --------Ca(OH)2----CaCO3C --------CO2--------- H2CO3------CaCO3预习自测1. 对以下物质分类全部正确的选项是〔〕(1〕纯碱〔2〕食盐水〔3〕石灰水〔4)氢氧化钠〔5〕液态氧〔6〕氯酸钾A碱——B纯洁物——C盐——D混合物——2.把以下的物质和分类用短线连起来物质分类BaSO4可溶NaOH难容Na2SO4盐Mg(OH)2碱3.图中,“——〞表示相连的物质间在一定条件下可以反响,“→〞表示丁在一定条件下可以转化为乙。
下面四组选项中,符合图示要求的是( )b5E2RGbCAP甲乙丁丙甲乙丙丁A H2SO4 Na2SO4 NaOH NaClB KCl K2CO3 KOH HClC O2 CO CuO CD Fe CuCl2 Zn HCl探究案一.金属、氧化物、酸、碱、盐之间的转化关系金属的化学通性2.氧化物的化学通性3.酸的通性4.碱的化学通性5.盐的化学通性【检测题】、分类法是一种行之有效,简单易行的科学方法,人们在认识事物时可以采取多种分类方法,以下关于“NaCO23〞的分类不正确的选项是〔〕p1EanqFDPwA、化合物B、氧化物C、碳酸盐D、钠盐2、无机化合物可根据其组成和性质进行分类无机化合物酸碱氧化物化物。
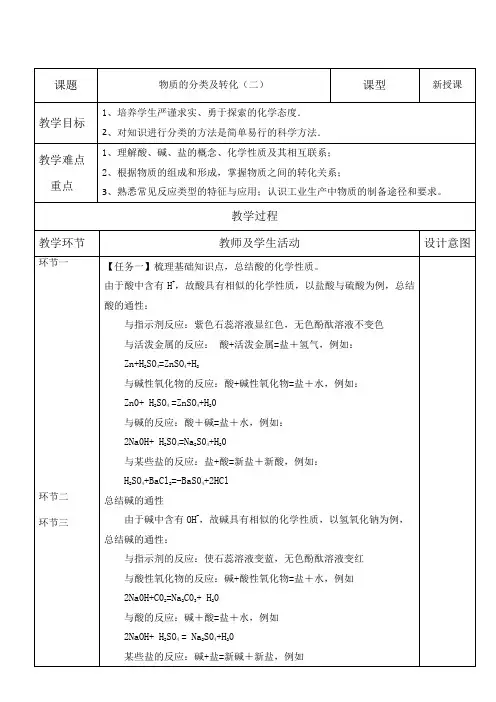
2NaOH+ CuSO4 = Cu(OH)2+ Na2S04总结盐的化学性质。
以碳酸钠、硫酸铜和碳酸氢钠溶液为例,总结盐的通性:硫酸盐与金属、碱的反应:CuSO4+Zn =ZnSO4+Cu;CuSO4+2Na0H=Cu(OH)2+Na2S04碳酸盐与酸、某些盐的反应:Na2C03+2HCl=NaCl+H20+C02;Na2C03+CaCl2=2NaCl+CaCO3碳酸氢盐与酸、某些盐的反应:NaHC03+HCl=NaCl+H20+C02;NaHC03+CaCl2=NaCl+ HCl+ CaCO3【任务二】根据酸、碱、盐的化学性质,自我总结酸性氧化物和碱性氧化物的化学性质。
【任务三】以钙转化为硫酸钙和碳转化为碳酸钠为例,带领学生写出每一步的化学方程式:【问题】对此例进行拓展,将钙元素换为钠元素,将碳元素换位硫元素,继续书写方程式。
【总结】酸性氧化物+碱=盐+水碱性氧化物+酸=盐+水某些酸性氧化物+某些碱性氧化物=盐碱性氧化物和水反应可以生成碱,但不是所有的碱性氧化物都可以,符合此规律的为强碱对应的氧化物,例如:氧化钙、氧化钠、氧化钡、氧化钾。
酸性氧化物和水反应可以生成酸,也并不是所有的酸性氧化物都可以,例如:七氧化二锰、三氧化铬、一氧化碳等。
【任务四】将物质的转化应用于生产生活中,通过物质的转化制备具体物质时,除了要考虑反应进行的可能性,还需要考虑原料来源、成本高低、设备要求等因素。
例如:工业制NaOH,原理:电解饱和食盐水:不采用Na2O和H2O反应制取的原因:氧化钠作为原料,来源少,成本高。

简单分类法及其应用精美句子1、善思则能“从无字句处读书”。
读沙漠,读出了它坦荡豪放的胸怀;读太阳,读出了它普照万物的无私;读春雨,读出了它润物无声的柔情。
读大海,读出了它气势磅礴的豪情。
读石灰,读出了它粉身碎骨不变色的清白。
2、幸福幸福是“临行密密缝,意恐迟迟归”的牵挂;幸福是“春种一粒粟,秋收千颗子”的收获. 幸福是“采菊东篱下,悠然见南山”的闲适;幸福是“奇闻共欣赏,疑义相与析”的愉悦。
幸福是“随风潜入夜,润物细无声”的奉献;幸福是“夜来风雨声,花落知多少”的恬淡。
幸福是“零落成泥碾作尘,只有香如故”的圣洁。
幸福是“壮志饥餐胡虏肉,笑谈渴饮匈奴血”的豪壮。
幸福是“先天下之忧而忧,后天下之乐而乐”的胸怀。
幸福是“人生自古谁无死,留取丹心照汗青”的气节。
3、大自然的语言丰富多彩:从秋叶的飘零中,我们读出了季节的变换;从归雁的行列中,我读出了集体的力量;从冰雪的消融中,我们读出了春天的脚步;从穿石的滴水中,我们读出了坚持的可贵;从蜂蜜的浓香中,我们读出了勤劳的甜美。
4、成功与失败种子,如果害怕埋没,那它永远不能发芽。
鲜花,如果害怕凋谢,那它永远不能开放。
矿石,如果害怕焚烧(熔炉),那它永远不能成钢(炼成金子)。
蜡烛,如果害怕熄灭(燃烧),那它永远不能发光。
航船,如果害怕风浪,那它永远不能到达彼岸。
5、墙角的花,当你孤芳自赏时,天地便小了。
井底的蛙,当你自我欢唱时,视野便窄了。
笼中的鸟,当你安于供养时,自由便没了。
山中的石!当你背靠群峰时,意志就坚了。
水中的萍!当你随波逐流后,根基就没了。
空中的鸟!当你展翅蓝天中,宇宙就大了。
空中的雁!当你离开队伍时,危险就大了。
地下的煤!你燃烧自己后,贡献就大了6、朋友是什么?朋友是快乐日子里的一把吉它,尽情地为你弹奏生活的愉悦;朋友是忧伤日子里的一股春风,轻轻地为你拂去心中的愁云。
朋友是成功道路上的一位良师,热情的将你引向阳光的地带;朋友是失败苦闷中的一盏明灯,默默地为你驱赶心灵的阴霾。

第一单元丰富多彩的化学物质第1课时物质的分类与转化学习目标:1.能根据物质的组成和性质对常见物质进行分类,并了解比较和分类对化学研究的作用。
2.掌握单质、氧化物、酸、碱、盐之间的转化关系,能从化合价升降的角度初步认识氧化还原反应,并了解通过化学反应实现物质转化的重要意义。
学习重、难点:学会从不同角度、不同的标准对物质及物质间的转化进行分类。
教学过程:一、导入新课教师讲解]阅读P2图片,思考化学与人类社会发展的关系。
强调]人类生活离不开各种各样的化学物质。
化学物质种类繁多,且新分子和新材料还在飞速增长。
展示]新分子和新材料的飞速增长过渡]世界上的物质如此繁多,为了简明有序地掌握其性质及变化规律,常采用的方法之一是进行分类研究。
那么,我们是如何来对不同物质进行分类的呢?板书] 物质的分类与转化二、推进新课教学环节一:物质的分类板书]一、物质的分类交流与讨论]在我们日常生活中,常会接触到下列物质:空气、乙醇、水、硫酸铵、铜、碘酒、碘、氧气、石墨、食盐水请你将上述物质进行分类,并说明分类的依据。
将你的分类结果与同学交流讨论。
归纳]分类标准:(1)混合物和纯净物;(2)单质和化合物;(3)导体和非导体;(4)气体、液体和固体;(5)易溶物、微溶物和难溶物。
板书]1. 研究物质常采用的方法之一是分类研究。
2. 对于若干种同样的物质,若分类的依据不同,则得到的分类结果不同。
对物质进行分类的常见依据有组成、状态、性能等。
化学上,根据组成对物质进行分类是最常用的方法。
思考]下图是根据物质的组成对物质进行分类的一种结果,试填写其中空格:提问]请说出上述概念“混合物、纯净物、单质、化合物”的含义。
问题解决]实验室中有下列物质,请根据物质的组成对它们进行分类。
①钠(Na);②氯气(Cl2);③氯化铁(FeCl3)溶液;④硫酸(H2SO4);⑤碳酸钙(CaCO3);⑥氧化钙(CaO);⑦氢氧化钠(NaOH);⑧葡萄糖(C6H12O6)。

第一章化学基本概念诸城二中王洪兵第一节物质的组成、性质和分类高考课标要求1.了解分子、原子、离子等概念的含义。
了解原子团的定义。
2.理解物理变化和化学变化的区别与联系。
3.理解混合物和纯净物。
单质和化合物、金属和非金属的概念。
4.理解酸、碱、盐、氧化物的概念及其相互联系。
回顾与思考1.焰色反应过程中,原子或离子中电子的运动状态发生了改变,属于化学变化;结晶水合物与对应的无水物是同一物质,因而结晶水合物脱水成无水物的变化是物理变化,上判断是否正确?2.下列物质中:(C6H10O5)n 、二甲苯、Na2SO3、Fe 、Na2O2、明矾福尔马林溶液哪些是纯净物?3.什么是酸性氧化物?酸性氧化物一定是非金属氧化物吗?4.什么是碱性氧化物?碱性氧化物一定是金属氧化物?整理归纳1.判断物理变化与化学变化的关键是2.如何判断纯净物3.将氧化物、两性氧化物、成盐氧化物、酸性氧化物、碱性氧化物、复杂氧化物、不成盐氧化物等按从属关系用表示出来,并将以下物质作为相应的例子CO、SO2、SiO2、Na2O 、CaO 、Mn2O7、Al2O3、Fe3O4、BeO、NO氧化物高考演练1.下列过程中,不涉及化学变化的是(2001年全国高考题)A.甘油加水作护肤剂B.用明矾净化水C.烹鱼时加入少量的料酒和食醋,可减少腥味,增加香味D.烧菜用过的铁锅,经放置常出现红棕色斑迹2.只含有一种元素的物质(05广东)A.可能是纯净物也可能是混合物B.可能是单质也可能是化合物C.一定是纯净物D.一定是一种单质3.下列俗称表示同一种物质的是(1999年上海高考)A.苏打、小苏打B.胆矾、绿矾C.三硝酸甘油酯、硝化甘油D.纯碱、烧碱知识与能力1.用化学方法不能实现的是()A.生成一种新分子B.生成一种新离子C.生成一种新原子D.生成一种新单质2.下列实验或生产操作:①蛋白质溶液中加入硫酸铵后形成沉淀;②除去混在氢氧化铁胶体中的氯化铁;③二氧化氮经加压凝成无色液体;④溴水滴入植物油中振荡褪色; ⑤水泥、砂子和水混合后硬化; ⑥照相底片感光。

《酸碱盐氧化物之间的关系》教案拾回桥中学金克芳教学目标1.通过对酸、碱、盐、氧化物性质的复习进一步掌握各类物质的性质及其相互关系。
2.巩固有关重要反应化学方程式的书写,并在此基础上进一步总结某些化学反应的规律。
学会运用金属活动顺序表判断某些置换反应能否发生;学会运用酸、碱、盐溶解性表判断复分解反应能否发生。
3.运用各类物质的性质及相互关系解决一些具体问题。
教学重点1.各类物质的通性及相互关系。
教学难点综合利用本章知识解决一些具体问题。
课时安排1课时教学过程一、运用金属活动顺序表判断某些置换反应能否发生,正确书写金属跟酸、金属跟盐反应的化学方程式。
(练习)判断下列反应能否发生?写出能发生反应的化学方程式,不能反应的说明理由。
(1)Mg+H2SO4 (2)Fe+HCl(3)Ag+H2SO4(稀) (4)Zn+HNO3(5)Zn+CuSO4 (6)Ag+ZnSO4(7)Cu+AgCl (8)Cu+Hg(NO3)2(讨论)可进行分组讨论,并小结置换反应能否发生的条件。
(小结)1.金属跟酸:(1)在金属活动性顺序表中,排在氢前的金属可置换出酸中的氢,排在氢以后的金属则不能置换出酸中的氢。
因此(1)、(2)可发生置换反应,生成相应的盐和氢气。
而(3)则不能发生置换反应。
(2)金属跟硝酸起反应时,由于硝酸的氧化性很强,一般不生成氢气。
如(4)不能发生置换反应。
2.金属跟盐:(1)在金属活动性顺序表中,排在前面的金属可以把排在后面的金属从它的盐溶液中置换出来。
因此(5)、(8)可以发生置换反应生成相应的盐和新的金属。
而(6)的反应中,Ag排在Zn的后面,反应不能发生。
(7)的反应不能发生是因为AgCl不溶于水。
(2)不要用钾、钙、钠置换盐溶液的金属。
由于钾、钙、钠化学性质极强。
它们与盐溶液的反应比较复杂。
如,钠跟硫酸铜溶液的反应为:2Na+2H2O=2NaOH+H2↑CuSO4+2NaOH=Cu(OH)2↓+Na2SO4四、运用酸、碱、盐溶解性表和复分解反应发生的条件判断某些复分解反应能否发生,正确书写有关复分解反应的化学方程式。
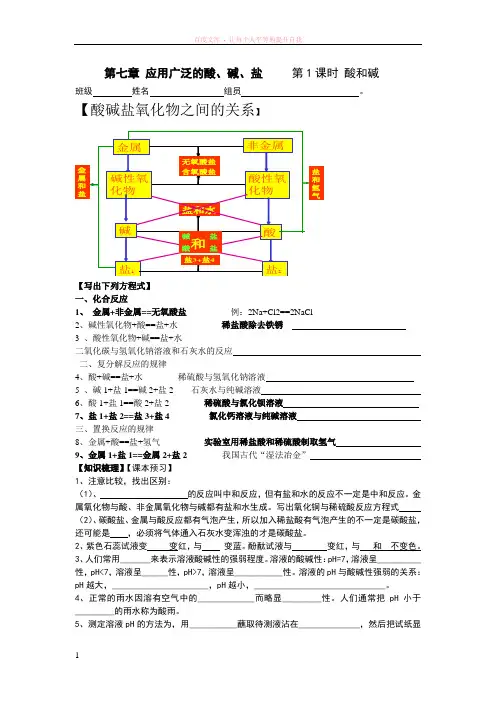
第七章应用广泛的酸、碱、盐第1课时酸和碱班级姓名组员。
【酸碱盐氧化物之间的关系】金属碱性氧化物碱盐1非金属酸性氧化物酸盐2无氧酸盐含氧酸盐盐和水盐3+盐4盐和氢气碱盐酸盐和金属和盐【写出下列方程式】一、化合反应1、金属+非金属==无氧酸盐例:2Na+Cl2==2NaCl2、碱性氧化物+酸==盐+水稀盐酸除去铁锈3 、酸性氧化物+碱==盐+水二氧化碳与氢氧化钠溶液和石灰水的反应二、复分解反应的规律4、酸+碱==盐+水稀硫酸与氢氧化钠溶液5 、碱1+盐1==碱2+盐2 石灰水与纯碱溶液6、酸1+盐1==酸2+盐2 稀硫酸与氯化钡溶液7、盐1+盐2==盐3+盐4 氯化钙溶液与纯碱溶液三、置换反应的规律8、金属+酸==盐+氢气实验室用稀盐酸和稀硫酸制取氢气9、金属1+盐1==金属2+盐2 我国古代“湿法冶金”【知识梳理】【课本预习】1、注意比较,找出区别:(1)、的反应叫中和反应,但有盐和水的反应不一定是中和反应。
金属氧化物与酸、非金属氧化物与碱都有盐和水生成。
写出氧化铜与稀硫酸反应方程式(2)、碳酸盐、金属与酸反应都有气泡产生,所以加入稀盐酸有气泡产生的不一定是碳酸盐,还可能是,必须将气体通入石灰水变浑浊的才是碳酸盐。
2、紫色石蕊试液变变红,与变蓝。
酚酞试液与变红,与和不变色。
3、人们常用_______来表示溶液酸碱性的强弱程度。
溶液的酸碱性:pH=7,溶液呈__________性,pH<7,溶液呈______性,pH>7,溶液呈___________性。
溶液的pH与酸碱性强弱的关系:pH越大,______________________,pH越小,______________________________。
4、正常的雨水因溶有空气中的_____________而略显_________性。
人们通常把pH小于_________的雨水称为酸雨。
5、测定溶液pH的方法为,用___________蘸取待测液沾在______________,然后把试纸显示的颜色与________________对照,就可以确定溶液的酸碱度。

第二讲物质分类【课程目标】1.认识混合物、纯净物、单质、化合物、氧化物的定义,并学会区别物质的类别。
2.学会判断酸、碱、盐等各类化合物。
3.理解判断有机物和无机物的依据。
【学海导航】一.物质的分类非金属氧化物:一般是酸性氧化物( SO2 CO2 HCl 等)金属氧化物:一般是碱性氧化物 (CuO Fe2O3 MgO等) (常见的中性氧化物:O2 H2 N2 CO 等)①和H2O反应相应的酸酸性氧化物②和碱反应盐和H2O氧化物的化学性质:①和H2O反应碱(必须是强碱)碱性氧化物②和酸反应盐和H2O三、综合知识1、复分解反应定义:两种化合物互相交换成分生成另外两种物质的反应。
范围:酸、碱、盐之间进行。
条件:有气体、水、沉淀生成的才能反应。
2NaOH + CuSO4 = Cu(OH ) 2↓+ Na2SO4NaOH + HCl = NaCl + H2OCaCO3 + 2HCl = CaCl2 + CO2↑+ H2O2、离子检验:①Cl–的检验:向溶液中滴加AgNO3溶液,产生白色沉淀,再加稀HNO3溶液,白色沉淀不溶解②SO42-的检验:向溶液中滴加BaCl2溶液,产生白色沉淀,再加稀HNO3溶液,白色沉淀不溶解③CO32-的检验:CO32-+酸(HCl/稀H2SO4)—冒气泡,将气体通入澄清的石灰水,石灰水变浑浊。
CO32-+Ca2+或Ba2+的可溶性盐或碱aq,产生白色沉淀1、紫色石蕊试液④ H+: 2、活泼金属——冒气泡,气体可燃3、CO32-———冒气泡,将气体通入澄清的石灰水,石灰水变浑浊。
4、不可溶的碱——沉淀溶解1、指示剂变色⑤OH–2、+Cu2+、Fe2+的可溶性盐溶液,产生蓝色、红褐色沉淀3、金属活动活动顺序:金属活动活动顺序表:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)Cu、Hg、Ag、Pt、Au应用:⑴只有排在H前面的金属才能够与酸反应生成氢气⑵只有排在前面的金属才能把排在后面的金属从其盐溶液里置换出来(K、Na、Ca除外)K、Na、Ca、Ba都可以直接与水反应生成相应的碱。
《1.1 物质的分类及转化》教案教师利用多媒体设备向学生投影出下面.教师:一、简单分类法及其应用1.分类:把某些特征相似的物体归类到一起的方法.2.目的和意义:能够提高人们工作、学习的效率,使人们更快更便捷的达到目的.3.简单分类法及其应用教师板书:交叉分类法讲述:好,我们对这四类盐进行分类,看看应该怎么分呢?对于Na2SO4,如果对于阳离子来说,她是属于钠盐,而对于阴离子来说,它是属于硫酸盐.Na2CO3也可以根据阳离子和阴离子来分,就可以分为钠盐和碳酸盐.同样的道理,K2SO4和K2CO3也可以以阴阳离子为标准进行分类.像这样的分类我们称之为交叉分类法.教师板书:树状分类法教师提问:将Ba(OH)2、NaHCO3、K2O、CuO、NaCl进行分类[问]很好,那我们发现树状分类法有什么优点吗?(树状分类法可以清楚地表示物质间的从属关系.)[教学推进]好,树状分类法和交叉分类法各有什么有点呢?我们看看,树状分类法就是对物质进行再分类,分类图看起来像一棵不断开枝的树,不断地对物质进行分类再分类.很明显我们的树状分类图很清晰很直观.所以,树状分类法的优点就是:清晰明了,一目了然.教师提问:同学们,化学反应的分类我们只是知道了很少的一部分,接下来的学习我们将会遇到很多根据不同的分类标准对化学反应再分类的,那是以后我们学习的任务.好,现在我们再来看看其他的分类.如果我们再继续分类的话,还可以怎么分?1.纯净物和混合物的区别(请学生回答)2.教师提问:再继续分类的话,单质还可以怎么分?(请学生回答):(单质可以分为金属和非金属,氧化物可以分为酸性氧化物、碱性氧化物和两性氧化物,酸可以分为一元酸、二元酸和多元酸,碱可以分为强碱和弱碱,盐可以分为正盐、酸式盐和碱式盐.)思考·交流:某物质经分析,只含一种元素,则此物质(A)一定是一种单质(B)一定是纯净物(C)一定是混和物(D)可能是纯净物,也可能是混和物3.教师提问:氧化物酸、碱、盐怎么分类?(请学生回答)(氧化物还可以分成金属氧化物和非金属氧化物,酸还可以分成含氧酸和无氧酸.)(碱可以分成可溶性碱和不溶性碱.)(盐可以分成含氧酸盐和无氧酸盐……思考·交流:(请学生回答)二、分类法的应用1.推断物质性质同类物质常常具有许多共性.因此可以通过物质所属类别,推测其具有的性质.思考交流(请学生回答)思考交流(请学生回答)2.确定转化关系(请学生回答)以钙为例,用化学方程式表示钙及其化合物之间的转化关系并指明反应类型.①_____________________,________;②_____________________,________;③_____________________,________;④_____________________,________;⑤_____________________,________;⑥_____________________,________.例题展示:下列不属于四种基本反应类型的是教师总结:单质、氧化物、酸、碱、盐之间的转化关系图活学活用:3.根据酸的通性,写出硫酸分别与镁及其氧化物、氢氧化物、碳酸盐反应生成硫酸镁的化学方程式.4.单质、氧化物、酸、碱和盐的相互关系,可以用图简单表示.限选择铁、碳、氧气、盐酸、氧化钙、二氧化碳、水、氢氧化钙8种物质作为反应物,将图中指定序号的转变用化学方程式表示(所写化学方程式不得重复).①C+O===CO22②_______________________________;③_______________________________;④_______________________________;⑤_______________________________;⑥_______________________________;⑦_______________________________.课堂达标教师:根据物质的分类,可以认识物质的性质、以及物质之间的转化关系,从而制备人类生活和生产需要的新物质.教师提问:那么,物质的性质是怎样的,物质之间的转换关系又是怎么样的呢?教师:引出本节课学习内容教师利用多媒体设备向学生投影出下面新课讲解:同类物质往往具有相似的性质教师:例如,盐酸和硫酸都是酸,他们都具有酸的性质,氢氧化钠和氢氧化钙都是碱,他们都具有碱的性质,碳酸钠和碳酸钾都是盐,他们都具有盐的性质.(展示图片)新课讲解:酸的主要化学性质教师:①酸可以与活泼金属反应②酸可以与碱性氧化物反应③酸可以与碱反应④酸可以与某些盐反应注意:“酸”是在水溶液中电离时产生的阳离子都是氢离子的化合物.思考讨论:根据酸的主要化学性质,可以有哪些反应实例呢?(展示表格)新课讲解:碱的主要化学性质教师:①碱可以与非金属氧化物反应②碱可以与酸反应③碱可以与某些盐反应④碱可以使酚酞试剂变红,使紫色石蕊试剂变蓝反应注意:“碱”是在水溶液中电离时产生的阴离子都是氢氧根离子的化合物.思考讨论:根据酸的主要化学性质,可以有哪些反应实例呢?(展示表格)新课讲解:盐的主要化学性质教师:①盐可以与金属反应②盐可以与酸反应③盐可以与碱反应④盐可以与某些盐反应注意:“盐”是在水溶液中电离时生成金属阳离子(或其他阳离子)和酸根阴离子的化合物.思考讨论:根据盐的主要化学性质,可以有哪些反应实例呢?(展示表格)思考讨论:①为什么不同的酸(或碱)具有相似的化学性质?答案:因为它们在组成上具有相似性.酸都含氢离子,碱都含氢氧根粒子,盐都含金属离子和酸根离子.思考讨论:②酸、碱、盐的主要化学性质中,涉及哪些反应类型?答案:从反应类型来看,初中学过的酸与金属、盐与金属的反应都属于置换反应,酸与碱、盐与酸、盐与碱、盐与盐之间的反应都属于复分解反应.思考讨论:教师:试着写出下列物质之间转化的化学方程式,体会由金属单质到盐、非金属到盐的转化关系.(展示图片)思考讨论:对于上述转化关系,从物质分类的角度看,你发现了什么规律?教师:金属单质和氧气反应生成碱性氧化物,碱性氧化物和水反应生成碱,碱和酸或酸性氧化物反应生成盐.教师:非金属单质和氧气反应生成酸性氧化物,酸性氧化物和水反应生成酸,酸和碱或碱性氧化物生成盐.思维启迪:制取某类物质的方法教师:根据物质的组成和性质,以及物质之间的转化关系,我们可以确定制取某类物质的方法.教师:例如,要想制取某种碱,通常可以采取两种方法:碱性氧化物与水发生反应;盐与另一种碱发生反应.思考讨论:工业生产中制取NaOH,是怎么做的呢?答案:工业上制取NaOH一般不采用Na2O与H2O反应,而主要采用电解饱和食盐水的方法.因为Na2O作为原料、来源少、成本高,因此不适用用批量生产NaOH.新课讲解:物质的转化教师:根据物质的组成和性质,通过化学变化可以实现物质之间的转化.在化学变化过程中,元素是不会改变的,这是考虑如何实现物质之间的转化时最基本的依据.在工业生产中要制取某种物质,除了要考虑反应进行的可能性,还要考虑原料来源、成本高低和设备要求等因素,以选取最适当的方法.思维启迪:化学科研工作者与化学工程师教师:化学科研工作者研究的是基本原理,例如怎么合成某种物质,某种物质的结构是什么样的,某种物质具有什么电子、光学、力学、磁学性质.教师:化学工程师研究的是怎么实现这些基本原理,例如怎么设计化工厂的反应器,选择反应的温度、压强、催化剂.教师:从基础知识来看,量子力学对化学科研工作者的重要性远远超过对化学工程师,流体力学对化学工程师的重要性远远超过对化学科研工作者.课堂达标1.下列物质分类正确的是().解析:“酸”是在水溶液中电离时产生的阳离子都是氢离子的化合物;“碱”是在水溶液中电离时产生的阴离子都是氢氧根离子的化合物;“盐”是在水溶液中电离时生成金属阳离子(或其他阳离子)和酸根阴离子的化合物;碱性氧化物是指与酸反应而成盐和水的氧化物;酸性氧化物是指与碱作用生成盐和水的氧化物.Na2CO3不是碱,NaOH不是盐,SO2不是碱性氧化物,选项A错误;CO不是酸性氧化物,选项B错误;CO不是碱性氧化物,选项C错误.因此选D.《1.1物质的分类及转化》导学案【学习目标】宏观辨识与微观探析:1.认识元素可以组成不同种类的物质,根据物质的组成和性质可以对物质进行分类。
清泉州阳光实验学校物质的分类第1课时教学设计一、物质的分类方法1.对物质进展分类,首先要确定分类的标准,然后按标准进展分类。
例如对以下化合物进展分类:①NaCl②HCl③CaCl2④CuO⑤H2O⑥Fe2O3(1)根据__________________为标准,可分为固体:________、液体:________、气体:________。
(2)根据物质的____________为标准,可分为氯化物:________、氧化物:________。
(3)根据物质的____________为标准,可分为酸:______、盐:______、氧化物:________。
2.试从不同的角度对以下各组物质进展分类,将其类别名称分别填在相应的空格内。
3.有以下十种物质:①草木灰②纯碱③金刚石④苛性钠⑤生石灰⑥硫酸⑦碘酒⑧食盐⑨金属钠⑩O2和O3的混合气体。
答复以下问题:(1)只有一种元素组成的是________;只有两种元素组成的是________。
(2)属于混合物的是________;属于纯洁物的是_______________________________________(3)属于单质的是________;属于化合物的是________。
(4)属于酸的是________;属于碱的是________;属于盐的是________。
总结归纳物质的分类方法(1)单一分类法:选定____________,对物质进展分类。
对于同一组物质,选用不同的分类标准,其分类结果________。
(2)穿插分类法:用____________的单一分类法对物质进展分类。
(3)树状分类法:采用树状形式对____________进展再分类。
如按照物质的组成和性质分类:物质【活学活用】1.请按以下线索提示画出Fe、Cu、S、H2、HCl、NaOH、H2SO4、Ba(OH)2、NaHCO3、K2O、CuO、NaCl的树状分类图:2.将以下Ⅰ中的物质与Ⅱ中的物质类型用短线连起来。
课时1 物质的分类及转化(教学案)学习目标:1、学会从不同的角度对常见物质进行分类。
掌握化学物质的分类方法,认识比较和分类等科学方法在化学研究中的作用(C)。
2、理解单质、氧化物、酸、碱、盐等物质之间的相互转化关系。
初步了解通过化学反应实现物质相互转化的重要意义(C)。
3、从化合价升降的角度,初步认识氧化还原反应(B)。
设计意图:先回忆初中所学的物质类别和反应类型,再交流、归纳出物质的分类方法和物质之间相互转化的规律,最后讨论,解决新问题。
重点难点:常见的物质分类方法、物质之间相互转化的规律。
互动课堂知识点一:物质分类的方法1、从物质组成分类:2、从物质的导电性分类:可将物质分成导体和绝缘体。
3、从物质的状态分类:可将物质分成固态、液态和气态。
4、从物质在水中的溶解能力分类:可将物质分为易溶、微溶、难溶、不溶等。
另外,还可以从物质的用途、物质来源等其他角度对以上八种物质进行分类。
知识点二:单质、氧化物、酸、碱、盐等物质之间的相互转化关系(“八圈图”)知识点三:化学反应的类型1、根据反应物和生成物的类别、种类多少分类(1)化合反应:A+B=AB;(2)分解反应:AB=A+B;(3)置换反应:AB+C=A+CB;(4)复分解反应:AB+CD=AD+CB。
2、根据反应中是否化合价的升降分类(1)氧化还原反应:是指元素化合价发生变化的反应。
(2)非氧化还原反应:是指元素化合价没有发生变化的反应。
3、四种基本反应类型和氧化还原反应之间的关系化合反应和分解反应不一定是氧化还原反应;置换反应一定是氧化还原反应;复分解反应一定不是氧化还原反应。
例题1、今有下列三组物质,每组中都有一种物质跟其他三种物质属于不同的类。
将挑出的物质(写化学式)和挑选依据(挑出的物质与其他物质不同之处)列在下面相应的表格内。
三组物质分别为:、H、C、N;(2)Fe、Na、Al、Si;(3)NO、CO、SO、Fe。
是无色无味的气体,它们之间的相互转化关系如下图:请回答:(1)写出下列物质的化学式:C:Fe,F:H2。
物质的分类酸碱盐氧化物的相互关系课程目标]1.了解阶段物质的简单分类方法2.掌握氧化物、酸、碱、盐的定义、制取方法及通性3.掌握金属活动顺序表的涵义及其应用4.熟练掌握酸、碱、盐、氧化物之间的相互关系5、了解化学反应的基本类型及其反应本质要点精析]一、物质的简单分类方法按组成分子是否相同纯净物按组成元素是否相同化合物有机化合物(含碳的化合物)(除CO、CO2、H2CO3、碳酸盐外)无机物酸无氧酸(HCl、H2S…)含氧酸(H2SO4、HNO3…)氧化物酸性氧化物(CO2、SO2…)碱性氧化物(Na2O、BaO…)两性氧化物(Al2O3、ZnO)不成盐氧化物(CO、NO)碱可溶性碱(NaOH、KOH、Ba(OH)2)等微溶性碱(Ca(OH)2)难溶性碱(Cu(OH)2、Fe(OH)3…)盐正盐(NaCl、CaCO3、CuSO4)酸性盐(NaHSO4 NaHCO3)碱式盐[Cu2(OH)2CO3]物质混合物单质金属非金属含稀有气另外,酸和碱按性质的强弱还可以分为强酸(碱)、弱酸(碱);按“元数”又可以分为一元酸(碱)、二元酸(碱)、三元酸(碱)等;化合物还有以下几种分类方法:按照组成和结构——离子化合物和共价化合物;按照在水溶液或在融化状态下是否导电——电解质和非电解质;按照化学反应中的表现——氧化剂和还原剂;混合物可以分为:固体混合物、液体混合物和气体混合物,其中按照分散质粒子的直径大小又可将液体混合物分为溶液、胶体和浊液。
思考题]:1.只含有一种元素的物质一定是纯净物吗?2.盐一定含有金属元素吗?3.金属氧化物一定是碱性氧化物吗?碱性氧化物一定是金属氧化物吗?4.非金属氧化物一定是酸性氧化物吗?酸性氧化物一定是非金属氧化物吗?5.Na2CO3·10H2O、盐酸是混合物还是纯净物?例1:下列物质中属于纯净物、化合物、无机化合物、盐、钙盐的是()A.石灰石B.Ca(OH)2C.CaCO3D.CH4解析:石灰石是混合物,主要成分是CaCO3;Ca(OH)2是碱;CH4是有机物。
答案:C。
二、氧化物的性质和制取三、酸的通性和制取四、碱的通性和制取五、盐的性质和制取难溶于水等弱电解质)弱电解质) 六、各类物质的相互关系思考题]化学中有“十大成盐规律”,你能写出以下成盐反应的化学方程式吗?(1)金属+酸→盐+H2 如:。
(2)金属1+盐1→金属2+盐2如:。
(3)酸+碱→盐+H2O如:。
(4)酸+碱性氧化物→盐+H2O如:。
(5) 碱+酸性氧化物→盐+H2O如:。
(6)酸1+盐1→酸2+盐2如:。
(7)碱1+盐1→碱2+盐2如:。
(8)盐1+盐2→盐3+盐4 如: 。
(9)金属+非金属→盐: 如: 。
(10)碱性氧化物+酸性氧化物→盐:如: 。
化学 反 应按物质组成形式划分化合反应 A + B = AB 分解反应AB = A + B置换反应AB + C = CB + A复分解反应 AB+CD = AD+CB 按有无电子转移 (化合价升降)划分 氧化还原反应 非氧化还原反应 按是否有离子参加划分离子反应分子反应 按反应进程划分可逆反应不可逆反应 按反应的热效应划分吸热反应(△H > 0)放热反应(△H < 0)强化训练]一、选择题(以下各题均只有1个选项符合题意)1.Na 2CO 3俗名纯碱,下面是对纯碱采用不同分类法的分类,不正确的是( )A .Na 2CO 3是碱B .Na 2CO 3是盐C .Na 2CO 3是钠盐D .Na 2CO 3是碳酸盐2.下列物质中虽不属于碱性氧化物,但与酸反应却能够生成盐和水的是 ( )A .Na 2OB .Na 2O 2C . NaD .CuO3.在混有少量CuO 的铁粉中加入一定量的稀盐酸,充分反应后过滤,再向滤液中放入一枚洁净的铁钉,足够长时间后取出,铁钉表面无变化,下列判断正确的是( )A .过滤出的不溶物只有铜B .过滤出的不溶物只有铁C .过滤出的不溶物中一定含有铜,可能含有铁D .滤液中一定含有氯化亚铁,可能含有氯化铜4.由以下五种元素给定价态的原子:H +1、S +6、O -2、K +1、Na +1,最多可以组成( )种化合物A .9B .10C .11D .12 5.下列物质属于纯净物的是( )A .稀硫酸B .烧碱C .水玻璃D .天然气6.食品卫生与身体健康密切相关.下列做法会导致食品对人体产生危害的是( ) ①用石灰水保存鲜蛋 ②为保持肉制品鲜美,在香肠中添加过量亚硝酸钠 ③做馒头时加入适量纯碱④为了让猪长得瘦,用“瘦肉精”饲养生猪A.①②B.①③C.②③D.②④7.某工厂排出的废水经检验pH<7,并含有较多的Cu2+,它们对人体、牲畜和农作物都有害,从回收利用和环境保护的角度考虑,切合实际的合理方案是加入()。
A. NaCl和HCl B.Na2SO4和MgCl2 C.CaO和铁粉D.石灰石和Ag 8.以下是一些食物的近似pH:(1)苹果3.3~4.5、(2)鸡蛋清7.6~8.0、(3)番茄4.0~4.4、(4)玉米粥6.8~8.0、(5)柑橘汁3.4~4.2,患胃痛、胃胀病的人宜经常食用的是()A.(1)(4)B.(4)(5) C.(2)(4)D.(3)(5)9.某种消化药片的有效成分氢氧化镁,能减缓因胃酸过多引起的疼痛。
在氢氧化镁与胃酸作用的过程中,胃液pH变化的情况是()t t tA B C D10.下列生产实践中不宜用熟石灰的是()A.建筑工业上制三合土 B.降低土壤的酸性,改良土壤C.处理呈酸性的工业废水 D.干燥气体11.对于化学反应A+B=C+D,下列说法中正确的是()A.若生成物C、D中有一种为单质,则该反应一定是置换反应B.若生成物C和D分别为两种沉淀,A、B有可能为盐和碱C.若C、D是盐和水,A、B一定是酸和碱,D.若A、B为两种化合物,C、D也一定为化合物12.下列每组物质的名称、俗名、化学式三者不能表示同一种物质的是()A.甲烷、沼气、CH4 B.氢氯酸、盐酸、HClC.氢氧化钠、火碱、N aOH D.氧化钙、熟石灰、CaCO313蚊子、蜂、蚂蚁等昆虫叮咬人时,会向人体射入一种叫蚁酸的物质,使皮肤红肿、瘙痒。
要消除这种症状,可在叮咬处涂抹下列物质中的A.牙膏或肥皂水 B.食盐水 C.火碱液 D.食醋14.某工厂的废渣中混有少量锌粉和氧化铜(其它成分不跟酸反应)跟大量的废盐酸接触形成污水,产生公害。
若向污水中撒入铁粉,且反应完,铁粉有剩余,此时污水中一定含有的金属离子是()A.Fe2+、Cu2+ B.Cu2+、H+ C.Fe2+、Zn2+ D.Zn2+、H+15.如图所示,广口瓶中盛有气体X ,胶头滴管中盛有液体Y ,若挤压胶头滴管使液体滴入瓶中,振荡,一段时间后可见小球a 膨胀鼓起.下表中的各组物质不出现上述现象的是 ( )X Y A CO Ca (OH )2 B CO 2 NaOH C HCl Ba (OH )2 DSO 2NaOH二、填空题16.某校化学兴趣小组对附近一化工厂排出的污水进行监测。
发现污水中含某些金属离子对水质和环境造成了严重污染。
他们曾对该厂排出的污水取样、过滤,对滤液进行了多次检测,其中有三次检测结果发现有如下物质:①CuCl FeCl MgSO H SO 23424、、、;②()CuSO MgCl Fe SO HCl 42243、、、;③CuSO AgNO FeCl HCl 433、、、。
试回答:(1)三次检测的结果中第________次检测的结果不正确。
(2)研究小组根据检测结果,向化工厂提出建议:用一种含钠离子的化合物来处理污水,就可以同时除去检测出的金属离子。
这种化合物是_____________。
(3)在检测时,为了确定滤液中是否存在硫酸根离子和氯离子,同学们将滤液酸化后,首先向滤液中加入过量的_____________溶液,将反应后的混合物过滤,再向得到的滤液中加入_____________溶液。
17.自从非典型肺炎在我国部分地区发现以来,一些医用消毒剂走进了百姓家。
请阅读下面材料,并回答相关问题:消毒剂化学式性质和用途备注 过氧乙酸 CH 3COOOH过氧乙酸易挥发、易分解,其分解产物是醋酸和氧气。
过氧乙酸具有很强的消毒刹菌能力,可以迅速杀灭各种微生物、病毒和细菌等。
醋酸对皮肤有腐蚀性双氧水H 2O 2 过氧化氢俗称双氧水,是一种无色液体,容易分解,其分解产物是水和氧气。
双氧水具有较强的消毒杀菌能力。
(1)对“非典”患者的用品、住过的房间消毒,应用的消毒剂为__________。
(2)外伤患者的伤口消毒,选用更合适的消毒剂为________________,理由是_____________。
(3)如果两瓶消毒剂的标签都没有了,你如何用化学方法去检验此消毒剂是双氧水还是过氧乙酸?第五课:1.A 2.B 3.C 4.C 5.B 6. D 7.C 8.C 9.B 10.D 11.B 12.D 13.A 14.C 15.A16.(1)③;(2)NaOH;(3)()Ba NO AgNO323;;17.(1)过氧乙酸;(2)双氧水;因为双氧水有消毒杀菌作用,且分解产物是水,对伤口无刺激作用。
(3)取少量的样品,加入少量的水稀释后分置于两支试管中,然后分别加入少量紫色石蕊试液,观察是否变红。