湖大物理化学(工科)考试大纲
- 格式:pdf
- 大小:212.07 KB
- 文档页数:8

《物理化学(甲)》考试大纲一、内容:涵盖物理化学(占80%左右)和结构化学(占20%左右)。
二、物理化学大纲1. 气体的PVT关系基本内容:理想气体状态方程;分压定律和分体积定律;理想气体的微观模型;气体的液化;范德华方程与维里方程;临界性质;对应状态原理;压缩因子图。
2. 热力学第一定律基本概念:重要热力学概念;热力学第一定律;热、功;内能;焓;热容;可逆体积功;相变焓;反应焓;节流膨胀。
基本内容:热力学基本概念及术语;热力学第一定律的表述与数学表达式;Qv=ΔU,Qp=ΔH及H的定义;过程热的计算;Cp与Cv的关系;由Cp计算Qp和ΔH;理想气体的等温可逆过程与绝热可逆过程功的计算;其他常见过程功的计算;相变焓、相变过程、相变热的计算;化学变化过程、化学反应热效应的计算;化学反应进度;标准热力学函数的计算。
3.热力学第二定律基本概念:卡诺循环,过程可能性判据,热力学第二定律,熵及熵变,第三定律,吉布斯自由能,亥姆霍兹自由能,热力学基本方程及麦克斯韦关系式,特性函数,克-克方程。
基本内容:卡诺循环;自发过程的共同特征;卡诺定理与热力学第二定律,熵增原理;熵函数,熵判据;各种典型过程熵变的计算;热力学第三定律,规定熵与标准熵;亥姆霍兹函数与吉布斯函数;ΔA与ΔG判据;一些基本过程ΔG的计算与应用;热力学基本方程与麦克斯韦关系式;吉布斯—亥姆霍兹方程;克拉贝龙方程及其应用。
4.多组分系统热力学基本概念:偏摩尔量,化学势,化学势判据,拉乌尔定律,亨利定律,理想液态混合物,理想稀溶液,稀溶液的依数性,逸度与逸度因子,活度与活度因子,热力学标准态。
基本内容:偏摩尔量与摩尔量;偏摩尔量的集合公式;Gibbs-Duhem方程;化学势的定义与各类系统化学势的表示式;化学势判据;拉乌尔定律与享利定律;理想液态混合物的定义及其特征;稀溶液的定义及其依数性;逸度与逸度因子的计算;活度和活度因子的计算;标准态选择与活度的关系;简单汽液平衡计算。

物理化学(科目代码807)考试大纲I、考查范围热力学第一定律、热力学第二定律约30%,多组分系统热力学10%,化学平衡和相平衡15%,电化学10%,化学动力学20%,表面现象和胶体15%。
II、考查要求要求考生系统掌握有机化学,分析化学,无机化学和物理化学的基本原理和基本知识,以及利用相关知识解决药学实际问题的能力。
III、考查形式及试卷结构1.考试方式:闭卷,笔试2.考试时间:180分钟3.试卷分值:满分150分4.题型结构:选择题(A型题)约占25%名词解释/填空约占20%简答约占30%论述题/计算题约占25%IV、考查内容物理化学(一)热力学第一定律【考试目标】1. 掌握体系与环境、强度性质与容量性质、状态与状态函数、过程与途径、热力学平衡态、可逆过程与不可逆过程、内能与标准生成焓等概念,掌握功、热、焓、恒压热容、恒容热容、焦耳-汤姆逊系数等定义;2. 掌握功和热都是与过程相联系的物理量,内能、焓则为状态函数;3. 掌握状态函数的全微分性质及其应用;4. 掌握热力学第一定律,并能熟练地计算体系在相变过程、理想气体在自由膨胀过程、等温过程、等容过程、绝热过程、循环过程中的ΔU、ΔH、Q及W 的值;5. 掌握可逆过程概念与意义;6. 掌握计算化学反应热效应的方法;7. 了解热力学第一定律对实际气体的应用。
【考试内容】基本概念:体系与环境、强度性质与容量性质、状态与状态函数、过程与途径、热力学的平衡态;状态函数及其全微分的性质;功的定义、体积功与非体积功的计算;热和热容的定义、热量的计算;可逆过程与不可逆过程的概念;热力学第一定律;第一定律对理想气体的应用;理想气体的绝热可逆过程的过程方程式;第一定律对实际气体的应用;热化学。
(二)热力学第二定律【考试目标】1.掌握从卡诺原理得出克劳修斯原理和熵函数的逻辑推理,从而理解克劳修斯不等式的重要性与熵函数概念,明确熵与热温商的区别和联系;2.掌握每一热力学函数只是在各自特定条件下才能作为过程进行方向与限度的判据,并学会使用熵判据和吉布斯自由能判据;3.熟悉并理解亥姆霍兹自由能F、吉布斯自由能G的定义;4.熟悉计算一些简单过程的ΔS、ΔG与ΔF值,并正确理解ΔG与ΔF在特定条件下的物理意义;5.熟悉热力学基本关系式,能熟练地运用吉布斯-亥姆霍兹公式;6.了解自发过程的共同特征,正确理解第二定律的几种说法,明确热力学第二定律的意义;7.了解热力学第三定律的基本内容,明确规定熵、标准熵的概念及其计算、应用;8.了解熵的统计意义。

《物理化学》(工科)考试大纲本考试大纲适用于报考湖南大学研究生院化工与应化学类专业的硕士研究生入学考试。
《物理化学》是大学本科化工与应化专业的一门重要基础理论课。
它是从物质的物理现象和化学现象的联系入手探求化学变化基本规律的一门科学。
物理化学课程的主要内容包括化学热力学、化学动力学、电化学、界面化学与胶体化学等。
要求考生熟练掌握物理化学的基本概念、基本原理及计算方法,并具有综合运用所学知识分析和解决实际问题的能力。
一、指导思想及大纲依据1、指导思想为正确、客观、真实、公平的考核研究生入学前本科层次的物理化学基础,为研究生入学选拔和今后的研究生教育提供依据,采用此大纲对考生进行物理化学知识水平考试。
2、大纲依据(1)天津大学物理化学教研室编,物理化学(第五版)。
高等教育出版社出版:北京,2009年(2)中华人民共和国国家标准GB3102·8物理化学和分子物理学的量和单位。
二、考试题型主要题型可能有:是非题、选择题、填空题、简答题、计算题、综合题、作图与析图题等。
三、考试方式、考试所需时间和改卷方式1、考试方式:书面笔答形式。
2、卷面总分:150分。
3、考试时间:3小时。
4、改卷方式:封闭流水改卷。
四、考试内容(一)热力学第一定律及其应用1、热力学概论2、热力学第一定律3、准静态过程与可逆过程4、焓5、热容6、热力学第一定律对理想气体的应用7、实际气体8、热化学9、赫斯定律10、几种热效应11、反应热和温度的关系—基尔霍夫定律(二)热力学第二定律1、自发过程的共同特征—不可逆性2、热力学第二定律3、卡诺定理4、熵的概念5、克劳修斯不等式与熵增加原理6、熵变的计算7、热力学第二定律的本质和熵统计意义8、亥姆霍兹自由能和吉布斯自由能9、变化的方向和平衡条件10、 G的计算示例11、几个热力学函数间的关系12、单组分体系的两相平衡—热力学对单组分体系的应用13、多组分体系中物质的偏摩尔量和化学势14、热力学第三定律与规定熵(三)溶液—多组分体系热力学在溶液中的应用1、溶液组成的表示法2、稀溶液中的两个经验定律3、混合气体中各组分的化学势4、理想溶液的定义、通性及各组分的化学势5、稀溶液中各组分的化学势6、理想溶液和稀溶液的微观说明7、稀溶液的依数性8、非理想溶液9、分配定律—溶质在两互不相溶液相中的分配(四)相平衡1、多相体系平衡的一般条件2、相律3、单组分体系的相图及其应用4、二组分体系的相图及其应用(五)化学平衡1、化学反应的平衡条件和化学反应的亲和势2、化学反应的平衡常数与等温方程式3、平衡常数的表示式4、复相化学平衡5、平衡常数的测定和平衡转化率的计算6、标准生成吉布斯自由能7、温度、压力及惰性气体对化学平衡的影响8、同时平衡9、反应的耦合(六)电解质溶液1、电化学的基本概念与法拉第定律2、离子的电迁移和迁移数3、电导4、强电解质溶液理论简介(七)可逆电池的电动势及其应用1、可逆电池和可逆电极2、电动势的测定3、可逆电池的书写方法及电动势的取号4、可逆电池热力学5、电动势产生的机理6、电极电势和电池的电动势7、浓差电池和液体接界电势的计算公式8、电动势测定的应用9、生物电化学(八)电解与极化作用1、分解电压2、极化作用3、电解时电极上的反应4、金属的电化学腐蚀、防腐与金属的钝化5、化学电源(九)化学反应动力学基础1、化学反应速率表示法和速率方程2、具有简单级数的反应3、几种典型的复杂反应4、温度对反应速率的影响5、链反应6、拟定反应历程的一般方法7、碰撞理论8、过渡态理论9、单分子反应理论10、溶液中进行的反应11、光化学反应12、催化反应动力学(十)界面现象1、表面吉布斯自由能和表面张力2、弯曲表面下的附加压力和蒸气压3、液体界面的性质4、不溶性表面膜5、液-固界面现象6、表面活性剂及其作用7、固体表面的吸附8、吸附速率—吸附和解吸速率方程式9、气-固相表面催化反应(十一)胶体分散体系和大分子溶液1、胶体和胶体的基本特性2、溶胶的制备和净化3、溶胶的动力性质4、溶胶的光学性质5、溶胶的电学性质6、溶胶的稳定性和聚沉作用7、乳状液8、大分子概说9、大分子的相对分子质量10、唐南平衡11、天然大分子五、考试要求(一)热力学第一定律及其应用明确热力学的一些基本概念,如体系、环境、功、热、变化过程等。

第一章 气体自测题1. 在温度恒定为25℃,体积恒定为25 dm 3的容器中,含有0.65 mol 的理想气体A , 0.35 mol的理想气体B ;若向容器中再加人0.4 mol 的理想气体D , 则B 的分压力B p ( ),分体积*B V ( )。
(A) 变大;(B) 变小;(C) 不变;(D) 无法确定。
2. 由A(g )和B(g )形成的理想气体混合系统,总压p =p A +p B ,体积V =*A V +*B V ,n =n A +n B 下列各式中,只有式( )是正确的。
(A) *B B B p V n RT =;(B) *A pV nRT =;(C) B B p V n RT =;(D) *A A A p V n RT =。
3. (1)在一定的T ,p 下(假设高于波义耳温度T B ):V m (真实气体)( )V m (理想气体) (2)在n ,T ,V 皆为定值的条件下:p (范德华气体)( )p (理想气体) (3)在临界状态下,范德华气体的压缩因子c Z ( )1 (A)>;(B)=;(C)<;(D)不能确定。
4. 已知A(g )和B(g )的临界温度之间的关系为:c c (A)(B)T T >;临界压力之间的关系为:c c (A)(B)p p <。
则A ,B 气体的范德华常数a 和b 之间的关系必然是:a (A)( )a (B);b (A)( )b (B)。
(A)>;(B)<;(C)=;(D)不能确定。
5. 在一个密闭的容器中放有足够多的某纯液态物质,在相当大的温度范围内皆存在气(g )、液(l )两相平衡。
当温度逐渐升高时液体的饱和蒸气压*p 变大,饱和液体的摩尔体积V m(1) ( );饱和蒸气的摩尔体积V m (g )( );m m m =()()V V g V l Δ−( )。
(A)变小;(B)变大;(C)不变;(D)无一定变化规律。
6. 在t =−50℃,V =40 dm 3的钢瓶内纯H 2的压力p =12.16 × 106 Pa 。

《物理化学》课程考试大纲(三年制专科. 试行)课程编号:0322208课程性质:必修课适用专业:化学教育开设学期:第5、6学期考试方式:闭卷笔试一总要求学生应按本大纲的要求,了解或理解物理化学中的一些基本概念、基本内容与基本理论;学会、掌握或熟练掌握上述各部分的基本方法。
尤其是应注意各部分知识的结构及知识的内在联系,运用有关的基本概念、基本理论和基本方法,进行一定的计算,解决一些简单的实际问题。
本大纲对内容的要求由低到高,对概念和理论分为“了解”和“理解”两个层次;对方法和运用分为“会”、“掌握”、和“熟练掌握”三个层次。
二教材与参考书目1.教材:《物理化学》印永嘉等编高等教育出版社 1992年第三版2.参考书目:《物理化学》上海师范大学等五校编高等教育出版社 1989年第三版三课程的内容和考核目标(一) 热力学第一定律1.考核知识点(1)热力学的一些基本概念(2)热力学第一定律(3)体积功、热、内能和焓(4)热容、理想气体的绝热过程(5)热力学第一定律对理想气体的应用(6)热化学等2. 考核要求(1)掌握热力学的一些基本概念,能了解状态函数的特点等。
(2)明确内能(U)和焓(H)都是状态函数。
热(Q)和功(W)都是与过程相联系的物理量。
(3)掌握可逆过程的特点(4)掌握热力学第一定律的表达式。
并能较熟练地掌握理想气体在等温、等压、等容及绝热过程中的⊿U、⊿H、Q及W 的计算。
(5)理解热力学第一定律与盖斯定律的关系,熟悉盖斯定律的应用,熟练掌握和运用生成热、燃烧热的数据计算化学反应热效应的方法等。
(二) 热力学第二定律1. 考核知识点(1)自发过程的特征、卡诺循环与卡诺原理及热力学第二定律经典表述(2)亥姆霍兹自由能(A)和吉布斯自由能(G)、过程的热温商与熵函数(3)过程方向与限度的判据(4)熵的统计意义(5)熵变的计算与熵判据的应用(6)热力学第三定律(7)等温过程的⊿G的计算与应用(8)热力学关系式2. 考核要求(1)了解自发过程的共同特征,掌握热力学第二定律的经典表述。

物理化学考试大纲一、考试科目基本要求及适用范围本考试大纲适用于报考吉林大学化学学院硕士研究生入学考试。
要求考生全面系统地掌握物理化学的基本概念、基本原理和方法。
二、考试形式闭卷考试,笔试,总分75分。
三、试卷结构选择题和计算题四、参考书1. 杨永华主编,物理化学,高等教育出版社,2017(2版)。
2. 杨桦主编,物理化学教学笔记,高等教育出版社,2018。
3. 杨永华主编,物理化学题解,高等教育出版社,2017(2版)五、考试内容主要是热力学第一定律、热力学第二定律、多组分系统热力学、相平衡、化学平衡、动力学和电化学。
具体内容如下:(一)热力学第一定律1 绪论,热力学基本概念,热、功、热力学能关系2 热力学第一定律表述及计算式3 可逆过程,热力学能及焓变的计算4 热化学,热效应,生成热等(二)热力学第二定律1 自发过程,第二定律表述2 熵函数的概念,判据及计算3 ΔA、ΔG判据及计算4 热力学基本方程(三)多组分体系热力学-溶液1 偏摩尔量、化学势2 理想液体混合物热力学性质3 稀溶液热力学性质及依数性(四)相平衡1 相律2 单组份系统的相图,克-克方程3 二组份系统的气-液平衡相图4 二组份系统的液-液平衡相图5 二组份系统的固-液平衡相图(五)化学平衡1 平衡常数及表示式2 化学平衡等温式3 气态及液态化学反应平衡常数计算4 温度对平衡常数影响(六)化学动力学1 化学动力学基本概念2 典型反应动力学方程3 复杂反应4 速率常数与温度的关系5 基元反应的速度理论:过渡态理论(七)电化学1 电解质溶液2 可逆电池的热力学,能斯特方程3 不可逆电池。

《物理化学》考试大纲学院(盖章):负责人(签字):专业代码:070304 专业名称:物理化学考试科目代码:615 考试科目名称:物理化学(一)考试内容物理化学是化学类(理科)专业和化工类(工科)的一门必修基础理论课。
该学科综合运用数学、物理等基础科学的理论和实验方法来研究化学过程(包括化学变化、相变化和pVT 变化)中的平衡规律和速率规律,也为后续专业课程学习奠定基础。
试题重点考查的内容:一、理想气体的状态方程1.掌握理想气体的状态方程及其计算2.掌握分压定律和分体积定律3.掌握真实气体及饱和蒸汽压的概念二、热力学第一定律1. 理解系统与环境、三大系统、状态、过程、状态函数与途径函数等基本概念2. 掌握热力学第一定律文字表述和数学表达式3. 理解功、热、热力学能、焓、热容、标准摩尔生成焓、标准摩尔燃烧焓等概念4. 掌握热、功、焓、内能的计算三、热力学第二定律1. 掌握自发过程、卡诺循环、卡诺定理2. 掌握热力学第二定律的文字表述和数学表达式3. 掌握熵增原理、熵判据、亥姆霍兹函数判据、吉布斯函数判据4. 掌握熵、吉布斯函数、亥姆霍兹函数的计算四、化学平衡1.掌握标准平衡常数的运用及其和吉布斯函数的关系2.判断温度、压力、组成等因素对化学反应可能进行的方向的影响五、多组分系统热力学及相平衡1.了解混合物与溶液的区别,会各种组成表示之间的换算2. 理解拉乌尔定律、享利定律,掌握其有关计算3.理解理想液态混合物的定义,理解混合物的性质4. 了解偏摩尔量与化学势的概念,会运用分配定律作简单计算5. 理解相律的意义、推导,掌握用杠杆规则进行分析与计算6. 掌握单组分系统、二组分气―液平衡系统和二组分凝聚系统典型相图的分析和应用六、电化学1. 掌握电池电动势与热力学函数的关系及其计算2. 掌握常用电极符号、电极反应及其电极电势的计算,掌握电池电动势的计算及其应用七、表面现象1. 理解表面张力及表面吉布斯函数的概念,理解亚稳状态与新相生成的关系2. 理解物理吸附与化学吸附的概念,了解兰格缪尔单分子层吸附理论及吸附等温式。

湖南大学研究生院硕士研究生入学考试《物理化学》(工科)考试大纲本考试大纲适用于报考湖南大学研究生院化工与应化学类专业的硕士研究生入学考试。
《物理化学》是大学本科化工与应化专业的一门重要基础理论课。
它是从物质的物理现象和化学现象的联系入手探求化学变化基本规律的一门科学。
物理化学课程的主要内容包括化学热力学、化学动力学、电化学、界面化学与胶体化学等。
要求考生熟练掌握物理化学的基本概念、基本原理及计算方法,并具有综合运用所学知识分析和解决实际问题的能力。
一、指导思想及大纲依据1、指导思想为正确、客观、真实、公平的考核研究生入学前本科层次的物理化学基础,为研究生入学选拔和今后的研究生教育提供依据,采用此大纲对考生进行物理化学知识水平考试。
2、大纲依据(1)天津大学物理化学教研室编,物理化学(第五版)。
高等教育出版社出版:北京,2009年(2)中华人民共和国国家标准GB3102·8物理化学和分子物理学的量和单位。
二、考试题型主要题型可能有:是非题、选择题、填空题、简答题、计算题、综合题、作图与析图题等。
三、考试方式、考试所需时间和改卷方式1、考试方式:书面笔答形式。
2、卷面总分:150分。
3、考试时间:3小时。
4、改卷方式:封闭流水改卷。
四、考试内容(一)热力学第一定律及其应用1、热力学概论2、热力学第一定律3、准静态过程与可逆过程4、焓5、热容6、热力学第一定律对理想气体的应用7、实际气体8、热化学9、赫斯定律10、几种热效应11、反应热和温度的关系—基尔霍夫定律(二)热力学第二定律1、自发过程的共同特征—不可逆性2、热力学第二定律3、卡诺定理4、熵的概念5、克劳修斯不等式与熵增加原理6、熵变的计算7、热力学第二定律的本质和熵统计意义8、亥姆霍兹自由能和吉布斯自由能9、变化的方向和平衡条件10、 G的计算示例11、几个热力学函数间的关系12、单组分体系的两相平衡—热力学对单组分体系的应用13、多组分体系中物质的偏摩尔量和化学势14、热力学第三定律与规定熵(三)溶液—多组分体系热力学在溶液中的应用1、溶液组成的表示法2、稀溶液中的两个经验定律3、混合气体中各组分的化学势4、理想溶液的定义、通性及各组分的化学势5、稀溶液中各组分的化学势6、理想溶液和稀溶液的微观说明7、稀溶液的依数性8、非理想溶液9、分配定律—溶质在两互不相溶液相中的分配(四)相平衡1、多相体系平衡的一般条件2、相律3、单组分体系的相图及其应用4、二组分体系的相图及其应用(五)化学平衡1、化学反应的平衡条件和化学反应的亲和势2、化学反应的平衡常数与等温方程式3、平衡常数的表示式4、复相化学平衡5、平衡常数的测定和平衡转化率的计算6、标准生成吉布斯自由能7、温度、压力及惰性气体对化学平衡的影响8、同时平衡9、反应的耦合(六)电解质溶液1、电化学的基本概念与法拉第定律2、离子的电迁移和迁移数3、电导4、强电解质溶液理论简介(七)可逆电池的电动势及其应用1、可逆电池和可逆电极2、电动势的测定3、可逆电池的书写方法及电动势的取号4、可逆电池热力学5、电动势产生的机理6、电极电势和电池的电动势7、浓差电池和液体接界电势的计算公式8、电动势测定的应用9、生物电化学(八)电解与极化作用1、分解电压2、极化作用3、电解时电极上的反应4、金属的电化学腐蚀、防腐与金属的钝化5、化学电源(九)化学反应动力学基础1、化学反应速率表示法和速率方程2、具有简单级数的反应3、几种典型的复杂反应4、温度对反应速率的影响5、链反应6、拟定反应历程的一般方法7、碰撞理论8、过渡态理论9、单分子反应理论10、溶液中进行的反应11、光化学反应12、催化反应动力学(十)界面现象1、表面吉布斯自由能和表面张力2、弯曲表面下的附加压力和蒸气压3、液体界面的性质4、不溶性表面膜5、液-固界面现象6、表面活性剂及其作用7、固体表面的吸附8、吸附速率—吸附和解吸速率方程式9、气-固相表面催化反应(十一)胶体分散体系和大分子溶液1、胶体和胶体的基本特性2、溶胶的制备和净化3、溶胶的动力性质4、溶胶的光学性质5、溶胶的电学性质6、溶胶的稳定性和聚沉作用7、乳状液8、大分子概说9、大分子的相对分子质量10、唐南平衡11、天然大分子五、考试要求(一)热力学第一定律及其应用明确热力学的一些基本概念,如体系、环境、功、热、变化过程等。
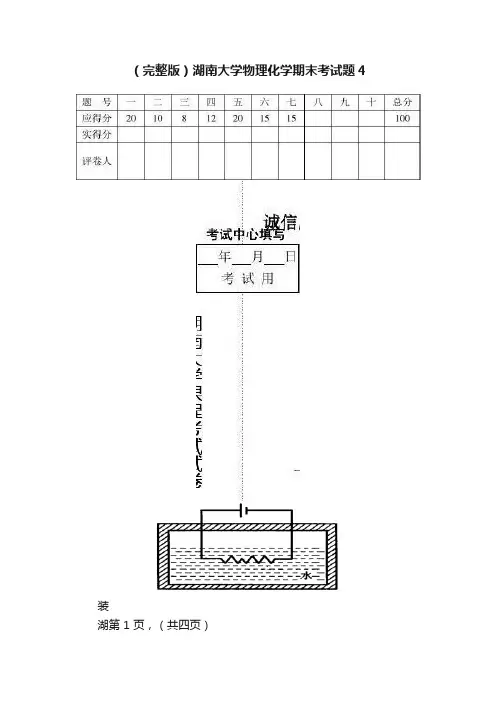
(完整版)湖南大学物理化学期末考试题4装湖第 1 页,(共四页)第 2 页,(共四页)订钱(答案不得超过此线)南大学教务处考试中心,考试作弊将带来严重后果!湖南大学课程考试试卷课程名称:物理化学(1);课程编码:试卷编号: A ;考试时间:120分钟(每题1分,共20分)1.若在高温高压下,某实际气体的分子所占有的空间的影响用体积因子b 来表示,则描述该气体较合适的状态方程是()A. pV m = RT + bB. pV m = RT + BT 2C. pV m = RT + bpD. pV m = RT + bTp2. 已知气体A 和B 的临界温度T c (A) > T c (B),临界压力p c(A) < p c (B),则这两种气体的van der Waals 常数关系是( )A. a (A)>a (B),b (A)>b (B)B. a (A)C. a (A)>a (B),b (A)D. a (A)b (B)3. 如图所示,在绝热盛水容器中,浸有电阻丝,通电后水与电阻丝的温度均升高统的?U 值的符号为。
如以电阻丝为系统,则上述过程的Q 、W 和系统的?U 值的符号为( )A. W =0,Q <0,?U <0B. W >0,Q <0,?U >0C. W =0,Q >0,?U >0D. W <0,Q =0,?U >04. 苯在一个刚性的绝热容器中燃烧,()()()()6622215C H l +O g = 6CO g +3H O g 2下列各关系式正确的是()A. △U =0,△H < 0,Q = 0B. △U =0,△H = 0,Q = 0C.△U =0,△H > 0,W = 0D. Q < 0,W = 0,△U < 05.实际气体经节流膨胀后,()A 、Q <0, d H =0, d p <0B 、Q =0, d H =0, d T <0C 、Q =0, d H <0, d p <0D 、Q =0, d H =0, d p <06. 1 mol 单原子理想气体,从273K 、202.65 kPa ,经pT =常数的可逆途径压缩到405. 3 kPa 的终态,该过程的?U 是( )A. 1702 JB. -406.8 JC. 406.8 JD. -1702 J7. △H = Q p 适用于下列哪个过程( )A. 理想气体从l ?10-7 Pa 反抗恒定的压力l ?10-5 Pa 膨胀到l ?10-5 PaB. 0 ℃、101325 Pa 下冰融化成水C. l0l325 Pa 下电解CuSO 4水溶液D. 气体从298 K 、101 325 Pa 可逆变化到373 K 、101 32.5 Pa8.下列宏观过程:()(1)101325Pa ,273.15 K 下冰融化为水;(2)电流通过金属发热;(3)往车胎内打气;(4)水在101325Pa ,373.15K 下蒸发;可看作可逆过程的是:( )(A )(1),(4)(B )(2),(3)(C )(1),(3)(D )(2),(4)9. 理想气体与温度为T 的大热源接触作等温膨胀,吸热Q ,所做的功是变到相同终态的最大功的20 %,则系统的熵变为 ( ) A. Q /T B. -Q /T C. 5Q /T D. -5Q /T10. 常温常压下2 mol H 2和2 mol Cl 2在绝热钢筒内反应生成HCl 气体,则( )A. ?r U =0,?r H =0,?r S >0,?r G<0B. ?r U <0,?r H <0,?r S >0,?r G<0C. ?r U =0,?r H >0,?r S >0,?r G<0D. ?r U >0,?r H >0,?r S =0,?r G>011. 恒压下,纯物质当温度升高时期Gibbs 自由能()A.增加B.下降C.不变D.难以确定 12. 对物质的量为n 的理想气体,()/s T p ??应等于( )A. V /RB. V /(nR )C. V /C VD. V /C p13. 某气体的状态方程为:=f (),f ()p V T V ?仅表示体积V 的函数,恒温下该气体的熵随体积V 的增加而 ( )A 增加B 下降C 不变D 难以确定14. 1 mol 理想气体在等温条件下,经恒外压压缩至稳定,环境和体系的熵如何变化?()A. ΔS 体 > 0,ΔS 环 > 0B. ΔS 体 < 0 ,ΔS 环 > 0C. ΔS 体< 0,ΔS 环 < 0D. ΔS 体 > 0 ,ΔS 环 < 015. 恒温时,B 溶解于A 中形成溶液,若纯B 的摩尔体积大于溶液中B 的偏摩尔体积,则增加压力将使B 在A 中溶解度如何变化()A. 增大B. 减小C. 不变D. 不一定16. 两只烧杯各有1 kg 水,向A 杯中加入0.01 mol 蔗糖,向B 杯中溶入0.01 mol NaCl ,两只烧杯按同样速度冷却降温,则有( )A. A 杯先结冰B. B 杯先结冰C. 两杯同时结冰D. 两杯都不会结冰17. 关于偏摩尔量,下面的叙述中不正确的是()A. 偏摩尔量可以是正数、负数和零B. 溶液中每一种广度性质都有偏摩尔量,而且都不等于其摩尔量C. 除偏摩尔吉布斯(Gibbs )自由能外,其它偏摩尔量都不等于化学势D. 溶液中个组分的偏摩尔量之间符合吉布斯-杜亥姆关系式湖湖第页,(共四页)第页,(共四页))南大学课程考试试卷南大学教务处考试中心18. 在598.15 K 时,与汞的摩尔分数为0.497的汞齐呈平衡的气相中,汞的蒸气压为纯汞在该温度下的饱和蒸气压的43.3%,汞在该汞齐中的活度系数γ(Hg)为( )A. 1.15B. 0.87C. 0.50D. 0.4319. 298 K 时,饱和的蔗糖水溶液与冰共存的独立组分数、相数、自由度数是 ( )A . C =2,Φ =2,f * =1B .C =2,Φ =2,f * =2 C . C =2 ,Φ =1,f * =2 D. C =2,Φ =1,f * =320. 101.3 kPa 下,用水蒸气蒸馏法提纯某不溶于水的有机物时,系统的沸点 ( )A .低于373.2 K B. 高于373.2 KC .取决于水与有机物的相对数量 D. 取决于有机物的相对分二、填空题(每空1分,共10分)1. 与298K ,1?105 Pa 下的H 2(g)处于相同对比状态时的NH 3(g)的压力为。

《物理化学》课程考试大纲一、课程的性质与考试目的本课程为专业根底课。
本课程是学习物理化学的根本原理,掌握化学反响平衡规律和速率规律。
通过本课程的学习,学生应该掌握必需的物理化学根本原理,并能用以分析和解决与化学有关的实际问题,为学习药学专业课程打下根底。
通过本课程的学习,为后续课程做好理论打算,增强学习化学的兴趣,培养尊重事物的科学态度,进一步深化学习化学的学习方法,使学生初步具有探究事物本质的勇气和精神。
二、考试的内容与要求第一章热力学第肯定律考试内容:系统与环境、系统的性质、热力学平衡态, 掌握状态函数法和状态方程、过程和途径、热和功等根本概念、热力学第肯定律, 最大体积功等一些重要概念的理解和应用;热力学第肯定律,盖斯定律、生成焓,燃烧焓,了解键焓估算的反响热、离子摩尔生成焓、溶化热和稀释热,掌握基希霍夫公式考试要求;1. 理解系统与环境、系统的性质、热力学平衡态, 掌握状态函数法和状态方程、过程和途径、热和功;2. 掌握热力学第肯定律、热力学能、热力学第肯定律的数学表达式;掌握热力学第肯定律在理想气体中的应用, 了解热力学第肯定律在实际气体中的应用;3. 理解盖斯定律、生成焓,燃烧焓,了解键焓估算的反响热、离子摩尔生成焓、溶化热和稀释热,掌握基希霍夫公式;第二章热力学第二定律考试内容:热力学第二定律;熵、熵变的计算;亥姆霍兹能、吉布斯能考试要求:1、理解热力学第二定律。
2、掌握环境和系统的熵变的计算。
3、掌握热力学第肯定律和第二定律的联合公式; 掌握亥姆霍兹能、吉布斯能能;理解自发过程的方向和限度4、掌握理想气体的简单状态,相变化和化学变化的ΔG的计算。
第三章多组分系统热力学考试内容:偏摩尔量、化学势;稀溶液中的两个经验定律、气体组分中各组分的化学势、液态混合物,稀溶液,真实溶液中组分的化学势考试要求:1. 识记偏摩尔量的物理, 了解偏摩尔量的集合公式和吉布斯-杜亥姆方程2. 理解化学式;3. 了解拉乌尔定律和亨利定律的微观解释,掌握拉乌尔定律和亨利定律;4. 气体组分中各组分的化学势;5、了解液态混合物,稀溶液,真实溶液中组分的化学势;第四章化学平衡考试内容:化学反响等温式和平衡常数;平衡常数的测定和反响限度的计算、标准反响吉布斯能的变化及化合物的标准生成吉布斯能;温度对平衡常数的影响考试要求:1. 掌握化学反响等温式和平衡常数;2. 掌握平衡常数的测定和反响限度的计算;3. 掌握标准反响吉布斯能的变化及化合物的标准生成吉布斯能;4. 了解反响吉布斯能随温度的变化和范特霍夫方程;第五章相平衡考试内容:相律;单组分系统;单组分系统考试要求;1. 了解相律的推导,理解相、自由度、组分数、物种数、相平衡的概念,掌握相律及其应用;2. 掌握单组分的相图和克劳修斯-克拉伯龙方程;3. 掌握理想的完全互溶双液系, 掌握杠杆规则, 理解非理想的完全互溶双液系;了解蒸馏和精馏第六章电化学考试内容:电化学的根本概念、电解质溶液电导的测定及应用、电池电动势与电极电势;电池中各物质活度对电池电动势的影响;可逆电池的电动势测定及其应用。

《物理化学》课程考试大纲考试内容及要求涉及下列范围,不指定教材,下列各章标题系参考:傅献彩,沈文霞,姚天扬等编:《物理化学》(第五版),高等教育出版社,2006年,但不限于此教材。
第二章 热力学第一定律1.了解热力学的内容、方法和特点。
2.理解并掌握热力学的基本概念:体系、环境、热力学平衡态、状态函数、过程与途径、体系的性质、功、热、能等。
3.明确体系的内能、焓、热容的意义。
4.明确热力学第一定律的意义及其表示法:熟知功与热的符号惯例,从微观上了解热力学第一定律的本质。
5.明确准静态过程,可逆过程和热力学平衡态的意义,以及最大功的概念。
6.较熟练地应用热力学第一定律计算理想气体在等温、等压、等容、绝热等过程和卡诺循环的ΔU、ΔH、W和Q。
7.能较熟练地应用生成焓、燃烧焓来计算反应热,学会用键焓估算反应热的方法;8.明确Hess定律与Kirchhoff定律的意义,并学会这两个定律的应用;9.了解Carnot循环的意义以及理想气体在诸过程中热、功的计算。
第三章 热力学第二定律1.了解自发过程的特征,明确热力学第二定律的意义及其表述;2.了解热力学第二定律与Carnot定理的联系,理解从卡诺定理定理导出熵函数的逻辑推理和克劳修斯不等式的重要意义;3.明确熵函数概念及其微观统计意义,并熟记G和A的定义;4.了解体系各热力学函数间的基本关系;5.较熟练地计算一些简单过程的ΔS、ΔH、ΔA和ΔG;6.明确熵判据和吉布斯自由能判据的条件及它们之间的关系;7.学会处理ΔG与温度的关系;8.了解热力学第三定律的基本内容,明确规定熵的意义、计算及其运用;9.初步了解不可逆过程关于熵流和熵产生等基本知识。
第四章 多组分体系热力学及其在溶液中的应用1.熟悉溶液组成的各种表示法及其相互关系;2.明确偏摩尔量和化学势的意义及其区别,了解这两个概念在多组分体系重要性;3.理解拉乌尔定律和亨利定律,认识它们在溶液热力学中的作用;4.理解理想液态混合物的意义,熟悉理想液态混合物的特性;5.了解逸度与活度的概念,学会运用蒸汽压法求活度和活度系数;6.熟悉气体、溶液各组分化学势的公式;7.熟悉物质在混合气体、溶液中标准态和参考态的选取,认识相对活度与标准态或参考态的关系;8.认识稀溶液的依数性,理解各依数性公式的推导方法;9. 了解分配定律的热力学基础及其应用。