胶体的电动现象
- 格式:ppt
- 大小:554.50 KB
- 文档页数:23

深圳大学实验报告课程名称:物理化学实验(2)实验项目名称:演示实验胶体的电动现象实验学院:化学与化工学院专业:指导教师:报告人:学号:班级:实验时间:2012.12.21实验报告提交时间:2012.12.27教务部制Ⅰ、目的要求1、了解胶体粒子的结构,了解电泳及电动现象的概念,掌握电动电势的意义。
2、 掌握应用电泳技术测定胶体溶液ζ电势的原理和技术。
Ⅱ、实验原理在外电场作用下,胶体粒子在分散介质中作定向移动称为电泳。
根据扩散双电层的物理模型,得到胶粒的ζ电势由下式表示,(XX-1)式中:ζ为电动电势,伏特;K 为无量纲常数,球状胶粒K=6,棒状胶粒K=4;η为介质的粘度,Pa.s ;u 为胶粒相对移动速率,ms -1;ε=εr ε0为介质的介电常数,Fm -1;E 为电势梯度,Vm -1。
对于电泳, 0(p316,8-28)r uEηζεε=印永嘉式中,εr 是介质相当于真卡的介电常数,本实验取81; ε0是真空的介电常数,8.85×10-12Fm -1; η是介质的黏度,本实验取0.001 Pa.s ; E 是电势梯度,Vm -1; u 是电泳速率,ms -1.Ⅲ、实验仪器和实验试剂EuKV επηζ=/Ⅳ、实验操作步骤(一)Fe(OH)3溶胶的制备和净化1、将0.5g无水FeCl3溶于20mL蒸馏水中,在搅拌的情况下将上述溶液滴入200mL沸水中(控制在4min~5min内滴完),然后再煮沸1min~2min,即制得Fe(OH)3溶胶。
2、溶胶净化半透膜袋的制备:将约20mL火棉胶液倒入干净的250mL锥形瓶内,小心转动锥形瓶使瓶内壁均匀铺展一层胶膜,倾出多余的棉胶液,将锥形瓶倒置于铁圈上,待溶剂挥发完(此时胶膜已不沾手),用蒸馏水注入胶膜与瓶壁之间,使胶膜与瓶壁分离,将其从瓶中取出,浸入蒸馏水中待用。
3、溶胶的净化:将冷至约50℃的Fe(OH)3溶胶转移至半透膜袋中,袋外用约50℃的蒸馏水渗析净化,约10min换水1次,共渗析5次,或者渗析到用AgNO3溶液测定渗析纯化液中不再含有氯离子为止。

实验五电泳电渗二、原理电渗属于胶体的电动现象。
电动现象是指溶胶粒子的运动与电性能之间的关系。
一般包括电泳、电渗、流动电位与沉降电位。
电动现象的实质是由于双电层结构的存在,其紧密层和扩散层中各具有相反的剩余电荷,在外电场或外加压力下,它们发生相对运动。
电渗是指在电场作用下,分散介质通过多孔膜或极细的毛细管而定向移动的现象。
若知道液体介质的粘度,介电常数,电导率,只要测定在电场作用下通过液体介质的电流强度I,和单位时间内液体流过毛细管的流量v,可根据下式求出电势。
操作步骤:(一)具体操作方法1按照实验装置图所示安装电渗仪。
2测定电渗时液体的流量v和电流强度I。
反复测量正、反向电渗时的流量v值各三次,同时记录各次的电流值。
3测定液体的电导率。
(二)注意事项计算SiO2对水的电势时,注意各物理量的单位。
在法定计量单位实行之后,计算公式中不应有4。
(三)提问:固体粉末样品粒度太大,电渗测定的结果重现性差,其原因何在?四、总结(一)数据处理计算各次电渗测定的v/I值,取其平均值,将液体的电导率和v/I的平均值代入上式,可求得SiO2对水的电势。
1.实验目的(1)掌握电泳法测定ζ电势的原理与技术;(2)加深理解电泳是胶体中液相和固相在外电场作用下相对移动而产生的电性现象。
(3)通过电渗法测定SiO2对水的电势,掌握电渗法测定电势的基本原理和技术。
2加深理解电渗是胶体中液相和固相在外电场作用下相对移动而产生的电性现象。
2.实验原理胶体溶液是一个多相体系,分散相胶体和分散介质带有数量相等而符号相反的电荷,因此在相界面上建立了双电层结构。
但在外电场的作用下,胶体中的胶粒和分散介质反向相对移动。
就会产生电位差,此电位差称为ζ电势。
ζ电势和胶体的稳定性有密切关系。
∣ζ∣越大,表明胶体的荷电越多,胶体之间的斥力越大,胶体越稳定。
反之,则不稳定。
当ζ等于零时,胶体的稳定性最差,此时可观察到聚沉的现象。
因此无论制备或破坏胶体,均需要了解所研究胶体的ζ电势。
![胶体的电学性质[业界优制]](https://uimg.taocdn.com/cd35b8729ec3d5bbfd0a74e1.webp)

胶体电泳现象和原理
胶体电泳现象是指在电场作用下,胶体颗粒会在电场中发生移动的现象。
胶体电泳的原理是靠电场力驱动胶体颗粒的运动。
在电场作用下,胶体颗粒表面的电荷会受到电场力的作用,从而产生电荷分布不均匀,即在胶体颗粒表面形成正负电荷的电层。
当外加电场方向与胶体颗粒表面电层中的电离离子移动方向相同时,正离子会向胶体颗粒的负电荷一侧移动,负离子则向胶体颗粒的正电荷一侧移动,从而形成了电双层。
电场力使得离子迁移速率大于胶体颗粒的运动速率,导致胶体颗粒在电场作用下发生移动。
胶体电泳的原理还涉及到电渗流的效应。
胶体颗粒的运动会引起周围液体的移动,形成了电渗流。
电渗流产生的剪切力与离子迁移速率不同,会影响胶体颗粒的移动速度,进而改变胶体的运动方向和速率。
值得注意的是,胶体电泳还受到胶体颗粒的形状、尺寸、表面电荷密度、溶液浓度等因素的影响,这些因素会对胶体颗粒的移动速度和方向产生影响。

胶体带电的主要原因胶体颗粒带电的主要原因可以归结为以下几个方面:1.电双层效应:在溶液中,胶体颗粒表面一般带有电荷,这是由于介质中存在大量的溶质离子和胶体颗粒表面活性基团之间的相互作用。
当溶剂中存在电解质时,正负电离子会围绕着胶体颗粒的表面聚集形成电双层,其中正离子(如Na+)排列在胶体颗粒表面附近,而负离子(如Cl-)则位于电双层外部。
这种电双层的形成使得胶体颗粒带有电荷。
2.界面离子化:胶体颗粒的表面活性基团可以与溶液中的离子发生化学反应,形成表面电荷。
例如,胶体颗粒表面的羟基(-OH)基团可以与酸或碱反应,产生正负电荷。
这种界面离子化的过程也是胶体带电的重要原因之一3.胶体颗粒大小和形状:胶体颗粒的大小和形状对其带电性也有一定影响。
通常情况下,较小的颗粒更容易带电,并且球形颗粒带电更多。
这是因为小颗粒具有比大颗粒更大的表面积,从而使得电荷在其表面分布更加密集。
4.pH值的影响:溶液的pH值对胶体颗粒的带电性有很大影响。
在不同的pH值条件下,溶液中的溶解离子浓度会发生变化,从而改变了电双层的结构和电荷性质。
例如,在低pH值条件下,溶液中的氢离子浓度增加,会导致正离子浓度增加,进而使胶体颗粒带正电荷;而在高pH值条件下,溶液中的氢离子浓度降低,会导致负离子浓度增加,使胶体颗粒带负电荷。
总之,胶体带电的主要原因是由于其颗粒表面的活性基团与溶液中的离子发生化学反应或形成电双层效应。
胶体的带电性对于其稳定性和相互作用具有重要影响,在许多领域如胶体科学、药物输送和环境污染等领域中具有广泛的应用价值。


常见胶体及胶粒带电的原因胶体是由两种或多种物质组成的混合体系,其中至少有一种物质为微细颗粒状悬浮于另一种物质中。
常见的胶体包括乳液、乳胶、溶胶、泡沫等。
胶体颗粒的带电状态是胶体体系中的重要特征。
其带电性是由于胶体颗粒表面存在电离物种或官能团引起的,主要有以下几种原因:1. 浸润膜某些情况下,胶体颗粒表面会被一层称为浸润膜的物质包裹,使得颗粒带有电荷。
例如,乳液是由液滴悬浮于另一种液体中,液滴表面被薄膜包裹。
该膜通常由溶剂分子、表面活性剂或吸附层组成,这些物质可以带电离物种,从而使得颗粒带电。
2. 静电效应当两种不同材料接触时,若一个材料具有较高的电导率,而另一个材料则具有较低的电导率,电荷会在两者之间产生迁移和分离,从而在两个材料之间产生静电。
在胶体中,可以通过在颗粒表面引入电离物种,从而在胶体颗粒表面形成静电效应,使颗粒带电。
例如,通过在聚合物颗粒表面引入带电离物种,可以使胶体颗粒带有正负电荷。
3. 动态离子吸附在溶液中,胶体颗粒表面通常会吸附带电离子。
这些离子可以来自于胶体颗粒周围的电解质溶液,也可以是在胶体颗粒自身溶解时释放出的离子。
通过选择适当的电解质浓度和性质,可以控制胶体颗粒表面带电物种的种类和数量,从而调节颗粒的带电性质。
4. 质子化/脱质子化反应某些物质的带电性质可以通过质子化(化学反应中的质子(H+)转移)或脱质子化(化学反应中的质子(H+)捐赠)反应产生。
例如,聚酸胶体在酸性环境下会失去质子而产生负电荷,而在碱性环境下会重新获得质子而失去电荷。
总之,胶体颗粒带电的原因主要包括浸润膜、静电效应、动态离子吸附以及质子化/脱质子化反应。
这些带电物种的存在使得胶体颗粒之间相互吸引或排斥,从而影响胶体体系的性质和行为。
对于理解和应用胶体科学具有重要意义。

常见的胶体的带电情况:1.胶粒带正电荷的胶体有:金属氧化物、金属氢氧化物。
例如Fe(OH)3、Al(OH)3等。
2.胶粒带负电荷的胶体有:非金属氧化物、金属硫化物、硅酸胶体、土壤胶体。
3.胶粒不带电的胶体有:淀粉胶体。
4.特殊的,AgI胶粒随着AgNO3和KI相对量不同,而带正电或负电。
若KI过量,则AgI胶粒吸附较多I-而带负电;若AgNO3过量,则因吸附较多Ag+而带正电。
注意:胶体不带电,而胶粒可以带电。
胶体电性(1)正电:一般来说,金属氢氧化物、金属氧化物的胶体粒子带正电荷,如Fe(OH)3 ,Al(OH)3 ,Cr(OH)3 ,H2TiO3 ,Fe2O3 ,ZrO2 ,Th2O3(2)负电:非金属氧化物、金属硫化物的胶体粒子带负电荷,如As2S3 ,Sb2S3 ,As2O3 ,H2SiO3 ,Au ,Ag ,Pt.(另外土壤胶粒子也带负电)(3)不带电:像淀粉溶液,蛋白质溶液一类的高分子胶体粒子是不带电的.(4)胶体粒子可以带电荷,但整个胶体呈电中性聚沉(Coagulation).胶体稳定的原因是胶粒带有某种相同的电荷互相排斥,胶粒间无规则的布朗运动也使胶粒稳定.因此,要使胶体聚沉、其原理就是:中和胶粒的电荷或加快其胶粒的热运动以增加胶粒的结合机会金属氧化物和金属氢氧化物胶体微粒一般带正电荷,非金属氧化物和金属硫化物胶体微粒一般带负电荷,很多有机物胶体微粒带负电荷,硅酸胶体带负电荷Soul丶0152 2014-09-29追问:那氢氧化铁为什么带负电追答:氢氧化铁带的是正电追问:我们答案上说氢氧化铁胶体带负电追答:胶体粒子的电性判断没有绝对的标准,咱说的都是一般情况,氢氧化铁胶体一般都是带正电,你说的这个题是不是有特别说明在什么样的溶液中,或者其他条件胶体粒子的带电:胶体粒子吸附溶液中的离子而带电,当吸附了正离子时,胶体粒子荷正电,吸附了负离子则荷负电。
不同情况下胶体粒子容易吸附何种离子,与被吸附离子的本性及胶体粒子表面结构有关。

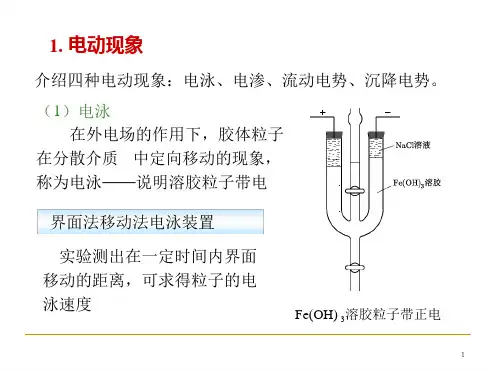

一、实验目的1. 理解电渗现象的基本原理和电动现象的基本概念。
2. 掌握电渗实验的基本操作和测量方法。
3. 通过实验观察电渗现象,加深对胶体电学性质的理解。
4. 计算并分析电渗过程中产生的电动电势(ζ电势)。
二、实验原理电渗是胶体常见的电动现象之一,指的是在外加电场作用下,液体介质通过多孔固体表面时产生的相对运动。
这种现象的产生是由于多孔固体表面吸附了离子或自身电离而带电荷,而液体介质则带相反的电荷。
在外电场的作用下,液体介质会通过多孔固体隔膜的毛细管定向移动,从而形成电渗现象。
电渗过程中,液体介质的流动速度与电场强度、毛细管半径、固液界面处的吸附层厚度以及介质的电导率等因素有关。
通过实验测量液体介质的流动速度和通过的电流,可以计算出电动电势(ζ电势),进而了解多孔固体表面吸附层的性质。
三、实验材料与仪器1. 实验材料:SiO2多孔固体、蒸馏水、电解质溶液、电极、毛细管、电源、电压表、电流表、计时器等。
2. 实验仪器:电渗实验装置、电子天平、温度计、pH计等。
四、实验步骤1. 准备实验装置,将SiO2多孔固体放入毛细管中,用蒸馏水冲洗干净,确保毛细管内部无杂质。
2. 将毛细管两端连接到电极上,将电极插入电解质溶液中,形成闭合回路。
3. 打开电源,调节电压,使电场强度在一定范围内变化。
4. 观察并记录液体介质的流动速度和通过的电流,记录实验数据。
5. 改变毛细管半径、电解质浓度等参数,重复实验,记录数据。
6. 根据实验数据,计算电动电势(ζ电势)。
五、实验结果与分析1. 实验结果显示,随着电场强度的增加,液体介质的流动速度逐渐加快。
这符合电渗现象的基本原理,即在外加电场作用下,液体介质会通过多孔固体表面定向移动。
2. 实验结果显示,随着毛细管半径的减小,液体介质的流动速度逐渐加快。
这是因为毛细管半径越小,毛细管内的压力差越大,从而加快了液体介质的流动速度。
3. 实验结果显示,随着电解质浓度的增加,液体介质的流动速度逐渐加快。
胶体带电的原因主要有两个方面:
一方面,胶体微粒的表面积较大,因此具有较强的吸附能力,能吸附溶液中的阴离子或阳离子,导致胶体粒子带电。
另一方面,有些胶体溶液是通过表面基团的电离而产生电荷的。
例如,硅酸溶液中的胶体粒子是由许多硅酸分子缩合而成的,表面上的硅酸分子可以电离出离子,在胶体粒子表面留下离子,从而使胶体粒子带负电荷。
胶体粒子带电而胶体不带电,金属氧化物、氢氧化物的胶粒带正电,非金属氧化物、金属硫化物的胶粒带负电。
希望以上信息对您有帮助。