有机人名反应(3)
- 格式:ppt
- 大小:1.59 MB
- 文档页数:50

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R′I >R′Br >R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或 b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷 R'X 的烷基和亚磷酸三烷基酯 (RO)3P 的烷基相同(即 R' = R),则Arbuzov 反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯 RP(OR')2和次亚膦酸酯 R2POR' 也能发生该类反应,例如:反应机理2 进行的分子内重排反应:一般认为是按 SN反应实例二、Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer----Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R′I >R′Br >R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷R'X 的烷基和亚磷酸三烷基酯(RO)3P 的烷基相同(即R' = R),则Arbuzov 反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2和次亚膦酸酯R2POR' 也能发生该类反应,例如:反应机理2 进行的分子重排反应:一般认为是按SN反应实例二、Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer----Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。

有机合成常用人名反应有机合成是化学领域中的一个重要分支,它研究有机化合物的合成方法和反应过程。
在有机合成中,常常会使用一些常用的人名反应,这些反应以人名命名,代表了该反应的发现者或者重要贡献者。
本文将介绍一些常用的人名反应,并对其原理和应用进行阐述。
一、格氏反应(Gattermann Reaction)格氏反应是一种用于合成醛的重要反应。
它是由德国化学家格氏(Gattermann)于1898年发现的。
格氏反应通过在芳香化合物上引入氰基,然后将其加氢还原,得到相应的醛。
格氏反应是一种重要的合成醛的方法,广泛应用于有机合成领域。
二、斯特雷克反应(Strecker Reaction)斯特雷克反应是一种合成α-氨基酸的方法,由德国化学家斯特雷克(Strecker)于1850年发现。
该反应通过使用醛、氰化物和胺,经过缩合和水解反应,合成出具有氨基酸结构的化合物。
斯特雷克反应是合成氨基酸的重要方法之一,广泛应用于生物化学和药物化学领域。
三、沃尔夫-克尼希反应(Wolf-Kishner Reduction)沃尔夫-克尼希反应是一种将醛或酮转化为对应的烷烃的方法。
该反应由德国化学家沃尔夫(Wolf)和克尼希(Kishner)于1912年发现。
沃尔夫-克尼希反应通过使用氨水和氢醇钠,将醛或酮转化为相应的烷烃。
这种还原反应在有机合成中具有重要的应用价值。
四、格里格纳德试剂(Grignard Reagent)格里格纳德试剂是一类由法国化学家格里格纳德(Grignard)于1900年发现的有机金属试剂。
格里格纳德试剂可以与卤代烃反应,生成烷基镁试剂。
这些烷基镁试剂可以与酮、醛、酸等化合物发生加成反应,合成出复杂的有机分子。
格里格纳德试剂是一种重要的有机合成试剂,在有机合成中具有广泛的应用。
五、费舍尔试剂(Fisher Reagent)费舍尔试剂是一种用于合成酮的试剂,由德国化学家费舍尔(Fisher)于1895年发现。

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯与一个新得卤代烷:卤代烷反应时,其活性次序为:R′I >R′Br 〉R′Cl.除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a—或b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总就是先脱除含碳原子数最少得基团。
本反应就是由醇制备卤代烷得很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用得卤代烷R’X得烷基与亚磷酸三烷基酯(RO)3P得烷基相同(即R'=R),则Arbuzov反应如下:这就是制备烷基膦酸酯得常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2与次亚膦酸酯R2POR'也能发生该类反应,例如:反应机理一般认为就是按SN2 进行得分子内重排反应:反应实例二、Arndt—Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer——--Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上得一个烃基带着一对电子迁移到—O-O-基团中与羰基碳原子直接相连得氧原子上,同时发生O-O键异裂.因此,这就是一个重排反应具有光学活性得3-—-苯基丁酮与过酸反应,重排产物手性碳原子得枸型保持不变,说明反应属于分子内重排:不对称得酮氧化时,在重排步骤中,两个基团均可迁移,但就是还就是有一定得选择性,按迁移能力其顺序为:醛氧化得机理与此相似,但迁移得就是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应得酯,其中三氟过氧乙酸就是最好得氧化剂。
这类氧化剂得特点就是反应速率快,反应温度一般在10~40℃之间,产率高。

有机化学中国人名反应中国人名反应是指以中国有机化学家的名字命名的有机化学反应。
这些反应通常是由这些化学家发现或发展,并且对有机化学领域的发展做出了重要贡献。
以下将介绍几个著名的中国人名反应。
1. 曾光明反应曾光明反应是由中国有机化学家曾光明教授于1981年首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将酮类化合物与硅醚反应,形成相应的醇类化合物。
曾光明反应在有机合成中具有广泛的应用,可以高效地构建C-O键,是合成醇类化合物的重要工具。
2. 毛宗回反应毛宗回反应是由中国有机化学家毛宗回教授于1978年首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将酮类化合物与有机硅化合物反应,生成相应的醇类化合物。
毛宗回反应在有机合成中广泛应用,具有高效、高选择性和环境友好等优点,被广泛用于合成复杂有机分子。
3. 李盛骏反应李盛骏反应是由中国有机化学家李盛骏教授于20世纪80年代中期首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将炔烃与醛类化合物反应,形成相应的α,β-不饱和醛类化合物。
李盛骏反应在有机合成中具有重要的应用价值,可以高效地构建C-C键和C=O键,是合成复杂有机分子的重要工具。
4. 王立群反应王立群反应是由中国有机化学家王立群教授于1992年首次报道的一种重要的合成方法。
该反应以过渡金属催化剂为催化剂,能够将酮类化合物与炔烃反应,形成相应的烯醇类化合物。
王立群反应在有机合成中具有广泛的应用,可以高效地构建C-C键和C-O键,是合成天然产物和药物分子的重要工具。
5. 陈茵反应陈茵反应是由中国有机化学家陈茵教授于20世纪70年代末首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将酮类化合物与酸类化合物反应,形成相应的酯类化合物。
陈茵反应在有机合成中具有重要的应用价值,可以高效地构建C-C键和C-O键,是合成酯类化合物的重要工具。

一、Arbuzov 反响亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反响时,其活性次序为:R′I >R′Br >R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或b-卤代酸酯、对甲苯磺酸酯等也可以进行反响。
当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反响是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反响制得:如果反响所用的卤代烷R'X 的烷基和亚磷酸三烷基酯(RO)3P 的烷基相同〔即R' = R〕,则Arbuzov 反响如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2和次亚膦酸酯R2POR' 也能发生该类反响,例如:反响机理一般认为是按S N2 进行的分子内重排反响:反响实例二、Arndt-Eister 反响酰氯与重氮甲烷反响,然后在氧化银催化下与水共热得到酸。
反响机理重氮甲烷与酰氯反响首先形成重氮酮〔1〕,〔1〕在氧化银催化下与水共热,得到酰基卡宾〔2〕,〔2〕发生重排得烯酮〔3〕,〔3〕与水反响生成酸,假设与醇或氨〔胺〕反响,则得酯或酰胺。
反响实例三、Baeyer----Villiger反响反响机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反响具有光学活性的3---苯基丁酮和过酸反响,重排产物手性碳原子的枸型保持不变,说明反响属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有肯定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反响实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。

有机化学人名反应总结是研究碳及其化合物的科学,其中许多反应被命名以纪念其首位发现者或发展者。
这些人名反应不仅对于的发展起到了巨大的推动作用,也源自于对科学家们的敬意和对他们贡献的赞扬。
在本文中,将总结几个人名反应,了解它们的原理和应用。
一、丁基锂合成反应(BuLi 生成反应)丁基锂是一种有机锂化合物,它的生成反应是通过将溶于正丁脱氢剂(n-BuLi)加入至正丁锂反应(floats-buLi)中得到的。
正丁锂反应是以但钾为催化剂,会使其在高压下进行。
该反应的关键是高温和高压条件下n-BuLi和粉末锂(floats-Li)之间的快速反应。
这个反应的应用十分广泛,可以用来合成各种有机锂试剂,如烃基锂、脂基锂,进而合成复杂的有机化合物。
二、格氏试剂合成反应 (Grignard 试剂生成反应)格氏试剂是有机锂试剂的后继者,由法国化学家弗朗索瓦·格里尼亚(francois auguste)发明并得名。
该反应以季碳基物质镁为催化剂,与卤化烃或卤化芳烃发生取代反应得到格氏试剂。
格氏试剂常用于合成范围广泛的有机化合物,主要反应机制类似于亲核取代反应,并使其非常重要的有机合成试剂之一。
三、斯托茨勒合成(Storz reaction)斯托茨勒合成反应是醛、酮与硫酸钠或硫酸食盐反应,生成酯的方法。
该反应是由俄罗斯化学家弗拉基米尔·利奥诺维奇·斯托茨(Vladimir Leontievich Stotsky)发现并命名的。
通过控制反应条件和底物的选择,可以合成具有多种不同结构的酯。
四、诺贝尔-加斯基诺反应 (Nobel-Gassman 试剂生成反应)诺贝尔-加斯基诺反应是一种用于合成β-哌啶酮的方法,是由德国化学家赫尔曼·斯图尔特·诺贝尔(Herman Staudinger)和法国化学家约瑟夫·加斯奥诺(Joseph Köck)合作发现的。
这个反应的关键是氰甲酸酯的转化,通过底物的选择,可以合成出不同结构的β-哌啶酮,具有广泛的应用前景。

有机人名反应讲解有机人名反应是一种基于人名命名的有机化学反应,通常是由某个化学家或科学家首次发现和提出的。
这些反应在有机化学中非常重要,因为它们是构建复杂有机分子的重要工具。
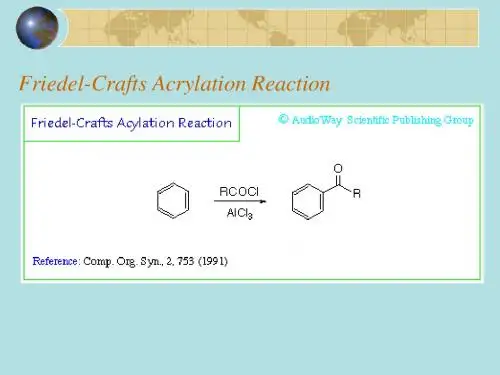
以下是一些著名的有机人名反应的讲解:1. 付克(傅瑞德尔)反应 (Friedel-Crafts Reaction):这是一个在路易斯酸(如氯化铝)催化下,在芳香烃中引入卤素和硝基等基团的过程。
这个反应由法国化学家查尔斯·傅瑞德尔和美国化学家詹姆斯·E·克雷夫特在19世纪末和20世纪初发现。
2. 珀金反应 (Perkin Reaction):这是一个由英国化学家威廉·珀金在19世纪末发现的反应,涉及芳香醛和酸酐在酸催化下缩合生成酯,并伴随有烯烃的生成。
3. 沃尔夫-凯惜纳-梅尔斯反应 (Wolff-Kishner-Mellor Reaction):这个反应由德国化学家卡尔·沃尔夫、美国化学家赫尔曼·梅尔斯和英国化学家约翰·凯惜纳在20世纪初发现。
它涉及将醛或酮的羰基转化为醇或烃的过程,通常使用氢氰酸和硫酸作为反应试剂。
4. 布特列洛夫反应 (Butlerov Reaction):这是由俄国化学家亚历山大·布特列洛夫在19世纪末发现的反应,涉及将醛或酮与醇在酸催化下缩合,生成环状酯的反应。
5. 迪尔斯-阿尔德反应 (Diels-Alder Reaction):这是一个由德国化学家奥托·迪尔斯和英国化学家罗纳德·奥多·阿尔德在20世纪初发现的反应,涉及共轭二烯烃和烯酮之间的环加成反应,生成一个四环化合物。
6. 霍夫曼消除反应 (Hofmann Elimination):这是由德国化学家阿道夫·霍夫曼在19世纪末发现的反应,涉及季铵碱加热时消除氢氧化铵的反应,生成烯烃。
7. 柏金反应 (Perkin Reaction):这个反应类似于珀金反应,但使用了不同的酸酐和酚类化合物作为反应物,生成相应的酯和酮类化合物。

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R′I 〉R′Br〉R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a—卤代醚、a- 或b-卤代酸酯、对甲苯磺酸酯等也可以进行反应.当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷R’X的烷基和亚磷酸三烷基酯(RO)3P 的烷基相同(即R' = R),则Arbuzov 反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2和次亚膦酸酯R2POR' 也能发生该类反应,例如:反应机理一般认为是按S N2 进行的分子内重排反应:反应实例二、Arndt-Eister反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸.反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer--—-Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O—O键异裂.因此,这是一个重排反应具有光学活性的3-—-苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸.反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。
这类氧化剂的特点是反应速率快,反应温度一般在10~40℃之间,产率高。

一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯与一个新的卤代烷:卤代烷反应时,其活性次序为:R′I >R′Br >R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总就是先脱除含碳原子数最少的基团。
本反应就是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷R'X 的烷基与亚磷酸三烷基酯(RO)3P 的烷基相同(即R' = R),则Arbuzov 反应如下:这就是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2与次亚膦酸酯R2POR' 也能发生该类反应,例如:反应机理一般认为就是按S N2 进行的分子内重排反应:反应实例二、Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer----Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这就是一个重排反应具有光学活性的3---苯基丁酮与过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但就是还就是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的就是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸就是最好的氧化剂。
1.Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R'I >R'Br >R'Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或 b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷 R'X 的烷基和亚磷酸三烷基酯 (RO)3P 的烷基相同(即 R' = R),则Arbuzov 反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯 RP(OR')2和次亚膦酸酯 R2POR' 也能发生该类反应,例如:反应机理一般认为是按 S N2 进行的分子内重排反应:反应实例2.Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例3.Baeyer----Villiger 反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。
1. Arndt-Eistert 反应醛、酮与重氮甲烷反应,失去氮并重排成多一个CH2 基的相应羰基化合物,这个反应对于环酮的扩环反应很重要。
2. Baeyer-Villiger 氧化应用过氧酸使酮氧化成酯。
反应中在酮的羰基和相邻的碳原子之间引人一个氧原子。
如由樟脑生成内酯:有时反应能生成二或多过氧化物,但环状酮转变为内酯能得到单一的预期产物。
合适的酸为过硫酸(Caro’s 酸)、过氧苯甲酸、三氟过氧乙酸。
除环酮外,无环的脂肪、芳香酮也可发生此反应。
二酮生成酸酐类、α、β-不饱和酮得到烯醇酯类。
3. Bechamp 还原(可用于工业制备)在铁、亚铁盐和稀酸的作用下,芳香族硝基化合物能还原成相应的芳香胺。
当某些盐(FeCl2、FeCl3、FeSO4、CaCl2 等)存在时,所用酸无论是过量还是少量,甚至在中性溶液中都能够进行这种还原。
此方法适用于绝大部分各种不同结构的芳香族化合物,有时也用来还原脂肪族硝基化合物。
4. Beckmann 重排醛肟、酮肟用酸或路易斯酸处理后,最终产物得酰胺类。
单酮肟重排仅得一种酰胺,混酮肟重排得两种混合酰胺。
但一般质子化羟基的裂解和基团R 的转移是从相反的位置同时进行的。
无论酯酮肟和芳酮肟都会发生此反应。
环酮肟重排得内酰胺,这在工业生产上很重要,利用此反应可帮助决定异构酮肟的结构。
5. Beyer 喹啉类合成法芳香伯胺与一分子醛及一分子甲基酮在浓盐酸或ZnCl2 存在下,反应生成喹啉类化合物。
这是对Doebner-Miller 喹啉合成法的改进。
Doebner-Miller 合成法由芳胺和不饱和醛或酮反应得到喹啉衍生物。
6. Blanc 氯甲基化反应芳香族化合物苯、萘、蒽、菲、联苯及衍生物,在ZnCl2(或NH4Cl、AlCl3、SnCl4、H2SO4、H3PO4 )存在下,用甲醛和极浓盐酸处理,发生芳香化合物的氯甲基化反应。
对于取代烃类,取代基的性质对反应能力影响很亲电取代,烷基,烷氧基一般使反应速度增加,而卤素、羧基特别是硝基用乙醛得到氯乙基化。
基础有机化学人名反应在有机化学领域,有许多重要的反应被以其发现者的名字命名,这些被称为人名反应。
这些反应在有机合成中起着关键的作用,帮助化学家们合成各种有机化合物并推动了该领域的发展。
本文将介绍几个代表性的基础有机化学人名反应。
1. 邻菲罗啉重排反应(Friedel-Crafts重排反应)邻菲罗啉重排反应是以法国化学家Charles Friedel和美国化学家James Crafts的名字命名的。
该反应可以将芳香烃转化为更高反应活性的中间体,如芳香醇、醛、酮等。
这个反应通常发生在有氯化铝或氯化铟等路易斯酸催化剂的存在下。
邻菲罗啉重排反应在有机合成中非常重要,可用于合成多种重要有机化合物,如苯甲酸、乙酸苯酯等。
2. 斯内夫反应(SnCl4催化的醇醚缩合反应)斯内夫反应以德国化学家Heinrich Snethlage的名字命名。
该反应是一种使用SnCl4作为催化剂,在醇和醚之间发生的缩合反应。
斯内夫反应广泛用于有机合成中,可用于合成醚、酯等化合物。
此外,其他的Sn催化剂也可以用于不同类型的醇醚缩合反应。
3. 阿尔金反应(AlCl3催化的醛酮缩合反应)阿尔金反应是以德国化学家Heinrich Alkohol的名字命名。
该反应是一种醛和酮之间的缩合反应,使用AlCl3作为催化剂。
阿尔金反应在有机合成中被广泛应用于合成α,β-不饱和酮、羧酸等化合物。
4. 卡巴列罗反应(Gabriel合成)卡巴列罗反应以德国化学家Siegmund Gabriel的名字命名。
该反应是一种通过使用氨和HCl与马来酰亚胺反应,生成胺的方法。
这个反应被广泛用于制备一级胺,并且在药物合成中具有重要的应用。
5. 罗宾森环化反应(Robinson环化反应)罗宾森环化反应是以英国化学家Sir Robert Robinson的名字命名。
这个反应可以将某种具有共轭体系的化合物环化为具有更稳定的环形结构。
罗宾森环化反应在天然产物合成和人工合成中都有广泛的应用。
有机化学人名反应取代反应:1,加特曼反应:加特曼(GattermannL)发现:用催化量的金属铜代替氯化亚铜或溴化亚铜作催化剂,也可使重氮盐与盐酸或氢溴酸反应制得芳香氯化物或溴化物。
这样进行的反应叫做加特曼反应。
2,加特曼-科赫反应:苯、一氧化碳和氯化氢反应生成苯甲醛,此反应称为加特曼-科赫反应。
3,傅-克反应:芳香化合物芳环上的氢被烷基取代的反应称为傅-克烷基化反应;芳香化合物芳环上的氢被酰基取代的反应称为傅-克酰基化反应;统称傅-克反应。
4,布赫尔反应:萘酚在亚硫酸氢钠存在下与氨作用,转变成相应萘胺的反应称为布赫尔反应。
5,齐齐巴宾反应:吡啶与氨基钠反应,生成-氨基吡啶,如果位已被占据,则得-氨基吡啶,但产率很低。
这个反应称为齐齐巴宾(Chichibabin)反应。
6,刚穆伯—巴赫曼反应:芳香重氮盐中的芳基在碱性条件下与其它芳香族化合物偶联成联苯或联苯衍生物的反应称为刚穆伯(Gomberg)—巴赫曼(Bachmann)反应。
7,柯尔伯—施密特反应:干燥的酚钠或酚钾与二氧化碳在加温加压下生成羟基苯甲酸的反应称为柯尔伯—施密特(Kolbe-Schmitt)反应。
8,威廉森合成法:在无水条件下,醇钠和卤代烷作用生成醚的反应称为威廉森(WilliamonAW)合成法。
9,席曼反应:芳香重氮盐和氟硼酸反应,生成溶解度较小的氟硼酸盐,后者加热分解产生氟苯,这称为席曼(Schiemann)反应。
10,桑德迈耳反应:1884年,桑德迈耳(SandmeyerT)发现:在氯化亚铜或溴化亚铜的催化下,重氮盐在氢卤酸溶液中加热,重氮基可分别被氯或溴原子取代,生成芳香氯化物或溴化物。
这一反应称为桑德迈耳反应。
11,普塑尔反应:一些重氮盐在碱性条件下或稀酸的条件下可以发生分子内的偶联反应。
这个反应是普塑尔(PchorrR)在寻找合成菲环的新方法中首先发现的,故称为普塑尔反应。
12,瑞穆尔—悌曼反应:酚与氯仿在碱性溶液中加热生成邻位及对位羟基醛的反应称为瑞穆尔—悌曼(Reimer—Tiemann)反应。
有机化学人名反应1.拜耳维利格Baeyer----Villiger 反应(p317)反应机理(不要求)过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例2.康尼查罗Cannizzaro 反应(p321)凡α位碳原子上无活泼氢的醛类和浓NaOH或KOH水或醇溶液作用时,不发生醇醛缩合或树脂化作用而起歧化反应生成与醛相当的酸(成盐)及醇的混合物。
此反应的特征是醛自身同时发生氧化及还原作用,一分子被氧化成酸的盐,另一分子被还原成醇:脂肪醛中,只有甲醛和与羰基相连的是一个叔碳原子的醛类,才会发生此反应,其他醛类与强碱液,作用发生醇醛缩合或进一步变成树脂状物质。
具有α-活泼氢原子的醛和甲醛首先发生羟醛缩合反应,得到无α-活泼氢原子的β-羟基醛,然后再与甲醛进行交叉Cannizzaro反应,如乙醛和甲醛反应得到季戊四醇:反应机理醛首先和氢氧根负离子进行亲核加成得到负离子,然后碳上的氢带着一对电子以氢负离子的形式转移到另一分子的羰基不能碳原子上。
反应实例3.克莱森许密特Claisen—Schmidt 反应(交叉羟醛缩合)(p314)一个无氢原子的醛与一个带有氢原子的脂肪族醛或酮在稀氢氧化钠水溶液或醇溶液存在下发生缩合反应,并失水得到不饱和醛或酮:反应机理反应实例3.Claisen 重排烯丙基芳基醚在高温(200°C)下可以重排,生成烯丙基酚。
当烯丙基芳基醚的两个邻位未被取代基占满时,重排主要得到邻位产物,两个邻位均被取代基占据时,重排得到对位产物。
一、Arbuzov 反应亚磷酸三烷基酯作为亲核试剂与卤代烷作用,生成烷基膦酸二烷基酯和一个新的卤代烷:卤代烷反应时,其活性次序为:R′I >R′Br >R′Cl。
除了卤代烷外,烯丙型或炔丙型卤化物、a-卤代醚、a- 或b-卤代酸酯、对甲苯磺酸酯等也可以进行反应。
当亚酸三烷基酯中三个烷基各不相同时,总是先脱除含碳原子数最少的基团。
本反应是由醇制备卤代烷的很好方法,因为亚磷酸三烷基酯可以由醇与三氯化磷反应制得:如果反应所用的卤代烷R'X 的烷基和亚磷酸三烷基酯(RO)3P 的烷基相同(即R' = R),则Arbuzov 反应如下:这是制备烷基膦酸酯的常用方法。
除了亚磷酸三烷基酯外,亚膦酸酯RP(OR')2和次亚膦酸酯R2POR' 也能发生该类反应,例如:反应机理一般认为是按S N2 进行的分子内重排反应:反应实例二、Arndt-Eister 反应酰氯与重氮甲烷反应,然后在氧化银催化下与水共热得到酸。
反应机理重氮甲烷与酰氯反应首先形成重氮酮(1),(1)在氧化银催化下与水共热,得到酰基卡宾(2),(2)发生重排得烯酮(3),(3)与水反应生成酸,若与醇或氨(胺)反应,则得酯或酰胺。
反应实例三、Baeyer----Villiger反应反应机理过酸先与羰基进行亲核加成,然后酮羰基上的一个烃基带着一对电子迁移到-O-O-基团中与羰基碳原子直接相连的氧原子上,同时发生O-O键异裂。
因此,这是一个重排反应具有光学活性的3---苯基丁酮和过酸反应,重排产物手性碳原子的枸型保持不变,说明反应属于分子内重排:不对称的酮氧化时,在重排步骤中,两个基团均可迁移,但是还是有一定的选择性,按迁移能力其顺序为:醛氧化的机理与此相似,但迁移的是氢负离子,得到羧酸。
反应实例酮类化合物用过酸如过氧乙酸、过氧苯甲酸、间氯过氧苯甲酸或三氟过氧乙酸等氧化,可在羰基旁边插入一个氧原子生成相应的酯,其中三氟过氧乙酸是最好的氧化剂。