第十三章电位分析法
- 格式:ppt
- 大小:1.02 MB
- 文档页数:15

十三章电化学分析导论13-1为什么不能测定电极的绝对电位,我们通常使用的电极电位是如何得到的?答:不能。
电池都是至少有两个电极组成的,根据它们的电极电位,可以计算出电池的电动势。
但是目前还无法测量单个电极的电位绝对值,而只能使用另一个电极标准化,通过测量电池的电动势来获得其相对值。
我们使用的电极电位是以标准氢电极作为标准,即人为规定起电极电位为零,将它与待测电极组成电池,所测得的电池电动势即为该电极的电极电位。
应该注意的是,当测量的电流较大或溶液电阻较高时,一般测量值中常包含有溶液的电阻所引起的电压降iR,所以应当加以校正。
13-2能否通过测定电池电动势求得弱酸或弱碱的电离常数、水的离子积、溶解积和络合物的稳定常数?试举例说明。
答:可以。
例如:已知下列半反应以及其标准电极电位为Cu2++I-+e-=CuI (1) E⊙(1)=0.86vCu2+ + e- = Cu+ (2) E⊙(2)=0.159v计算CuI的溶度积。
解E Cu2+/Cu+= E⊙Cu2+/Cu++ 0.059lg[Cu2+]/[ Cu+]∵Cu++I-+e-=CuI∴[Cu+][I-]=K SPCuI即[Cu+]= K SPCuI/[I-]E Cu2+/Cu+= E⊙Cu2+/Cu++ 0.059lg[Cu2+]*[I-]/K SPCuI当[Cu2+]=[I-]=1mol*L-1E= E⊙(1)=0.86vE⊙Cu2+/Cu+= E⊙(2)=0.159v0.86=0.159+0.159lg1/K SPCuIK SPCuI=1.4*10-1213-3电化学中的氧化还原反应与非电化学的氧化还原反应有什么区别?答:电化学的氧化还原是电子在电极上发生转移,有电流通过,方程式可写成两极的反应;而非电化学的氧化还原没有电流,方程式不能拆开写.13-4充电电流是如何形成的?它与时间的关系有何特征?能否通过降低和消除充电电流来发展灵敏的电分析方法?答:电极表面双电层类似一个电容器,当向体系施加电扰动的时,双电层所负载的电荷会发生相应该变,导致电流的产生,这一部分电流称为充电电流.当施加一个电位阶跃,充电电流随时间成指数衰减,时间常数为RC,不能通过降低或消除充电电流来发展灵敏的电分析方法。

电化学智慧树知到课后章节答案2023年下浙江大学浙江大学第一章测试1.若电极反应Cu–2e- → Cu2+ 在某一阴极电位下的净反应电流密度为i(mA/cm2),则Cu金属的溶解速度为答案:(1/2)i/F (mmol·cm-2·s-1)2.下述是“II类导体”的是答案:熔融的CaCl23.在I/II类导体界面上发生了答案:其他电化学现象;离子与电子间的电荷转移;相关电荷的积累;电化学反应4.电化学反应是异相反应答案:对5.离子在离子导体中的运动速度与溶剂无关错第二章测试1.双电层的厚度一般为()左右答案:1nm2.()认为双电层是由内层的紧密层和外层的分散层两部分组成的答案:Stern理论3.以下哪些双电层模型()考虑了溶液中离子的热运动答案:Stern理论;Gouy-Chapman理论4.电化学反应既不在电子导体相也不在离子导体相中进行,而是在两相界面的很窄范围物理空间中进行答案:对5.过剩离子双电层是金属晶格中的金属离子受晶格中的电子和溶液相中的水化作用力不同导致电荷分离而造成的的。
对第三章测试1.金属/金属间的相间电位也叫作___答案:接触电位2.绝对电极电位指的是答案:金属/溶液间的相间电位3.关于相间电位的描述,正确的为____答案:相间电位为两相内电位的差值,所以是电压。
;金属/溶液间的相间电位就是常说的电极体系的电极电位;溶液/溶液间的详见电位也称液接电势4.电化学测量中一般要求在参比电极与测试溶液间采用盐桥相连,主要目的是为了防止参比电极内的溶液与测试溶液间的相互沾污答案:错5.电极电位是金属/溶液间的相间电位,实质上是电压,所以它的绝对数值是可测的答案:错第四章测试1.若如下阴极反应O+ne®R有净反应发生,则电极电位与平衡电极相比()答案:减小2.电化学反应发生平衡的基本热力学条件为答案:氧化态物种加上电子的电化学位等于还原态物种的电化学位3.下述关于某一电化学反应的描述正确的是答案:正向反应的绝对速度与逆向反应的绝对速度均为正值;电化学反应的净速度为正、逆向反应的绝对速度的代数和;任一电化学反应均发生在电子导体(或狭义上说的电极)与离子导体间的界面上;同一电化学反应均存在正向、逆向两个反应方向4. Nernst方程只适用于平衡或准平衡电极反应答案:对5.两个电子导体界面处于平衡的基本条件是电子在两个金属相中的化学位相等。

第十三章电化学分析法一、选择题1. 下列( )不是玻璃电极的组成部分。
A.Ag-AgCl 电极 B.一定浓度的HCl 溶液C.饱和KCl溶液 D .玻璃管2.测定溶液PH值时,所用的指示电极是: ( )A.氢电极 B.铂电极 C.氢醌电极 D.玻璃电极3.测定溶液PH时,所用的参比电极是: ( )A.饱和甘汞电极 B.银-氯化银电极 C.玻璃电极 D.铂电极4.在电位滴定中,以△E/△V为纵坐标,标准溶液的平均体积V为横坐标,绘制△E/△V~ V曲线, 滴定终点为:( )A.曲线的最高点 B. 曲线的转折点C.曲线的斜率为零时的点 D. △E/△V=0对应的5.在电位法中离子选择性电极的电位应与待测离子的浓度()A.成正比 B.的对数成正比C.复合扩散电流公式 D. 符合能斯特方程式6.玻璃电极使用前一定要在水中浸泡24h以上, 其目的是( )A.清洗电极 B.活化电极C.校正电极 D.检查电极好坏7.25℃时, 标准溶液与待测溶液的pH值变化一个单位,电池电动势的变化为( ) A.0.058V B.58V C.0.059V D.59V8.pH玻璃电极膜电位的产生是因为( )A.电子得失 B. H+穿过玻璃膜C.H+被还原D. 溶液中H+和玻璃膜水合层中的H+的交换作用9.在离子选择性电极分析法中,( )说法不正确。
A. 参比电极电位恒定不变B.待测离子价数愈高,测定误差愈大C.指示电极电位与待测离子浓度呈能斯特响应D.电池电动势与待测离子浓度成线性关系。
10.电位滴定与容量滴定的根本区别在于()。
A.滴定仪器不同B.指示终点的方法不同C.滴定手续不同D.标准溶液不同11.永停滴定法采用()方法确定滴定终点。
A.电位突变B.电流突变C.电阻突变D.电导突变12.pH玻璃电极使用前应在()中浸泡24h以上。
A.蒸馏水B.酒精C.浓NaOH溶液D.浓HCl溶液13.用酸度计以浓度直读法测试液的pH,先用与试液pH相近的标准溶液()。


《仪器分析》课程标准一、课程概述仪器分析是分析化学最为重要组成部分,是食品分析和研究一门重要技术,也是分析化学发展方向。
本课程教学目是使学生通过本课程学习,牢固掌握各类仪器分析方法基本原理以及仪器各重要组成部分,对各仪器分析方法应用对象及分析过程要有基本了解。
此外,通过本课程教学,让学生对当今世界各类分析仪器及分析方法及发展趋势有一些初步了解,从而为其今后工作及更深一步地学习作必要铺垫。
在完成该课程学习之后,要求学生在掌握了仪器分析基本原理等知识前提下,可以根据样品性质、分析对象选择最为合适分析仪器及分析方法。
二、课程目标现代仪器分析是以测量物质物理性质为基础分析方法。
随着科学技术发展,分析化学在方法和实验技术方面都发生了深刻变化,从而使仪器分析在分析化学中所占比例不断增大,并成为现代实验化学重要支柱。
仪器分析一些基本原理和实验技术,已成为食品研究人员所必须掌握基础知识和基本技能,是培养学生综合素质重要环节。
课程基本任务是使学生掌握基本仪器分析方法和原理,能根据实际任务合理选择分析方法和测试条件,解决生产和科研中测试问题。
三.课程主要内容第一章绪论通过本章学习,了解仪器分析在分析化学中所占地位,了解现代仪器分析方法分类。
仪器分析方法特点;仪器分析在食品科学中作用;仪器分析发展趋势。
第二章原子发射光谱法一、学习目与要求通过本章学习, 掌握原子发射光谱分析法基本原理、原子发射光谱分析法基本装置以及原子发射光谱分析法新发展。
二、考核知识点与考核目标(一)电磁辐射不同区域(一般)识记:电磁辐射不同区域。
(二)光学分析法分类(一般)识记:光学分析法分类。
(三)原子发射光谱分析法基本原理(重点)识记:原子光谱是线状光谱原因。
理解:原子发射光谱分析法基本原理。
(四)光谱分析仪器主要组成及其作用(重点)识记:光谱分析仪器基本装置。
理解:光谱分析仪器主要组成(光源、光谱仪、观测设备)作用。
(五)光谱定性分析基本原理(重点)识记:光谱定性分析基本术语:灵敏线、最后线、共振线、分析线。
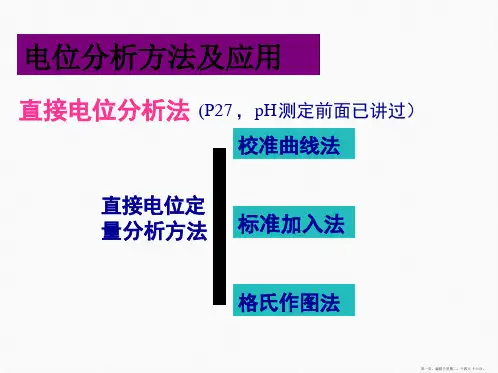


仪器分析仪器分析课程组第十三章电化学分析法导论第十三章电化学分析法导论13.3 电极类型1. 根据电极上是否发生电化学反应分类2. 根据电极在电分析化学中的作用分类1. 根据电极上是否发生电化学反应分类•金属基电极(特点:电极上有电子交换反应)第一类电极第二类电极第三类电极第零类电极•离子选择性电极(膜电极)•第一类电极第一类电极例•第二类电极•第三类电极•由金属,该金属的难溶盐(或难离解的络离子),与此难溶盐具有共同阴离子的另一难溶盐(或难离解的络离子)和与此难溶盐具有相同阳离子的电解质溶液组成。
M|MY, M’Y, M’n+第三类电极例O4(s),CaC2O4(s),Ca2+•Zn|ZnC2C2O4(s),CaC2O4(s),Ca2+•Ag|Ag2•Hg|HgY,CdY,Cd2+(Y=EDTA)第三类电极例•零类电极•将一种惰性金属(如铂或金)浸入氧化态和还原态同时存在的溶液中所构成的体系。
•特点:–金属不参与电极反应,仅起传递电子的作用–指示溶液中氧化态和还原态的比值零类电极例•离子选择性电极(膜电极)•20世纪60年代发展起来的一类新型电化学传感器。
•它能选择性地响应待测离子的浓度(活度)而对其他离子不响应或响应很弱,其电极电位与溶液中待测离子活度的对数有线性关系•响应机理:相界面上发生了离子交换和扩散,而非电子转移。
2. 根据电极在电分析化学中的作用分类•指示电极•参比电极•工作电极•辅助电极或对电极•指示电极•电极电位随被测电活性物质活度变化的电极称为指示电极。
(通常无电流通过)•如:pH 玻璃电极、离子选择性电极等•参比电极•在恒温恒压条件下,电极电位不随溶液中被测离子活度的变化而变化,具有基本恒定电位值的电极称为参比电极。
•常用的参比电极–甘汞电极(calomel electrode)–银-氯化银电极甘汞电极甘汞电极的能斯特方程表达式KCl浓度不同时,甘汞电极的电极电位25℃, 相对于SHEc(KCl)/(mol/L) 0.1 1.0 饱和φ/V +0.3356 +0.2828 +0.2443其中饱和甘汞电极(SCE)最为常用银-氯化银电极由一根表面镀有AgCl的银丝插入到用AgCl饱和的KCl溶液中构成。

课后习题答案第一章:绪论1.解释下列名词:(1)仪器分析和化学分析;(2)标准曲线与线性范围;(3)灵敏度、精密度、准确度和检出限。
答:(1)仪器分析和化学分析:以物质的物理性质和物理化学性质(光、电、热、磁等)为基础的分析方法,这类方法一般需要特殊的仪器,又称为仪器分析法;化学分析是以物质化学反应为基础的分析方法。
(2)标准曲线与线性范围:标准曲线是被测物质的浓度或含量与仪器响应信号的关系曲线;标准曲线的直线部分所对应的被测物质浓度(或含量)的范围称为该方法的线性范围。
(3)灵敏度、精密度、准确度和检出限:物质单位浓度或单位质量的变化引起响应信号值变化的程度,称为方法的灵敏度;精密度是指使用同一方法,对同一试样进行多次测定所得测定结果的一致程度;试样含量的测定值与试样含量的真实值(或标准值)相符合的程度称为准确度;某一方法在给定的置信水平上可以检出被测物质的最小浓度或最小质量,称为这种方法对该物质的检出限。
第三章光学分析法导论1.解释下列名词:(1)原子光谱和分子光谱;(2)原子发射光谱和原子吸收光谱;(3)统计权重和简并度;(4)分子振动光谱和分子转动光谱;(5)禁戒跃迁和亚稳态;(6)光谱项和光谱支项;(7)分子荧光、磷光和化学发光;(8)拉曼光谱。
答:(1)由原子的外层电子能级跃迁产生的光谱称为原子光谱;由分子的各能级跃迁产生的光谱称为分子光谱。
(2)当原子受到外界能量(如热能、电能等)的作用时,激发到较高能级上处于激发态。
但激发态的原子很不稳定,一般约在10-8s内返回到基态或较低能态而发射出的特征谱线形成的光谱称为原子发射光谱;当基态原子蒸气选择性地吸收一定频率的光辐射后跃迁到较高能态,这种选择性地吸收产生的原子特征的光谱称为原子吸收光谱。
(3)由能级简并引起的概率权重称为统计权重;在磁场作用下,同一光谱支项会分裂成2J+1个不同的支能级,2J+1称为能级的简并度。
(4)由分子在振动能级间跃迁产生的光谱称为分子振动光谱;由分子在不同的转动能级间跃迁产生的光谱称为分子转动光谱。
《仪器分析》课程教学大纲()【课程代码】【课程修习类型】必修(平台课程)【开课学院】材料与化学化工学院【适用专业】化学【学分数】【学时数】总学时学时【建议修读学期】二秋【先修课程】无机化学、物理、高等数学、分析化学、有机化学一、课程说明.课程介绍(中、英文)仪器分析是化学专业的专业核心课,应化及制药工程专业的专业选修课之一。
它是研究物质的化学组成、结构和状态的分析测试方法,也是其它学科取得化学信息的研究手段,在许多领域发挥着重要的作用。
课程涉及的知识面广且综合性强,包括各种现代仪器分析方法的物理和化学的原理、特点、仪器的结构原理、定性定量分析原理、方法及其应用范围。
本课程主要讲解原子发射光谱、原子吸收光谱、分子发光分析法、电位分析法、电解库仑分析法、伏安与极谱法、气相色谱、液相色谱及毛细管电泳等分析方法。
通过本课程的学习,使学生能够基本掌握主要仪器分析方法的原理及应用领域,掌握应用合适的方法进行实际样品分析,并解决相应分析化学问题的能力。
仪器分析在工业、农业、环境、医药、健康、食品及科学研究等方方面面都有着广泛的应用。
掌握各种仪器分析方法,不仅有利于学生提高化学及相关学科的学习和研究能力,而且能更快更好地与社会接轨,提高他们的就业竞争力。
因此,仪器分析课程在化学及相关专业的人才培养过程中起到承前启后的作用。
. , , . . , , , , , , , , , ,, , .. ., , , , , . , . ..课程的主要内容及课时安排:.课程教学目标:()课程教学目标:通过本课程的教学,使学生在知识、能力和素质等方面达到如下教学目标。
)知识方面目标:掌握光学分析法、电化学分析法、色谱分析法的基本原理、仪器的基本构成。
理解仪器各部分的物理原理,各种仪器的应用情况。
了解各类仪器分析方法的最新发展情况。
目标:掌握原子发射光谱、原子吸收光谱、分子发光分析法、电位分析法、电解库仑分析法、伏安与极谱法、气相色谱、液相色谱等主要仪器分析方法的仪器基本结构及其工作原理,主要部件的功能,条件选择及干扰消除、定性及定量方法原理,应用范围等。
课后习题答案第一章:绪论1.解释下列名词:(1)仪器分析和化学分析;(2)标准曲线与线性范围;(3)灵敏度、精密度、准确度和检出限。
答:(1)仪器分析和化学分析:以物质的物理性质和物理化学性质(光、电、热、磁等)为基础的分析方法,这类方法一般需要特殊的仪器,又称为仪器分析法;化学分析是以物质化学反应为基础的分析方法。
(2)标准曲线与线性范围:标准曲线是被测物质的浓度或含量与仪器响应信号的关系曲线;标准曲线的直线部分所对应的被测物质浓度(或含量)的范围称为该方法的线性范围。
(3)灵敏度、精密度、准确度和检出限:物质单位浓度或单位质量的变化引起响应信号值变化的程度,称为方法的灵敏度;精密度是指使用同一方法,对同一试样进行多次测定所得测定结果的一致程度;试样含量的测定值与试样含量的真实值(或标准值)相符合的程度称为准确度;某一方法在给定的置信水平上可以检出被测物质的最小浓度或最小质量,称为这种方法对该物质的检出限。
第三章光学分析法导论1.解释下列名词:(1)原子光谱和分子光谱;(2)原子发射光谱和原子吸收光谱;(3)统计权重和简并度;(4)分子振动光谱和分子转动光谱;(5)禁戒跃迁和亚稳态;(6)光谱项和光谱支项;(7)分子荧光、磷光和化学发光;(8)拉曼光谱。
答:(1)由原子的外层电子能级跃迁产生的光谱称为原子光谱;由分子的各能级跃迁产生的光谱称为分子光谱。
(2)当原子受到外界能量(如热能、电能等)的作用时,激发到较高能级上处于激发态。
但激发态的原子很不稳定,一般约在10-8 s内返回到基态或较低能态而发射出的特征谱线形成的光谱称为原子发射光谱;当基态原子蒸气选择性地吸收一定频率的光辐射后跃迁到较高能态,这种选择性地吸收产生的原子特征的光谱称为原子吸收光谱。
(3)由能级简并引起的概率权重称为统计权重;在磁场作用下,同一光谱支项会分裂成2J+1个不同的支能级,2J+1称为能级的简并度。
(4)由分子在振动能级间跃迁产生的光谱称为分子振动光谱;由分子在不同的转动能级间跃迁产生的光谱称为分子转动光谱。
第十三章杂环类药物的分析(五)杂环类药物的分析1.异烟肼异烟肼的鉴别方法、杂质检查项目和方法、含量测定方法2.硝苯地平硝苯地平的鉴别方法、特殊杂质检查方法、含量测定方法3.左氧氟沙星(1)左氧氟沙星的物理常数测定法、鉴别方法.杂质检查项目和方法、含量测定方法(2)左氧氟沙星片的检查项目和方法、含量测定方法4.盐酸氯丙嗪(1)盐酸氯丙嗪的鉴别方法、杂质检查项目和方法、含量测定方法(2)盐酸氯丙嗪片和注射液的含量测定方法5.地西泮(1)地西泮的鉴别方法、杂质检查项目和方法、含量测定方法(2)地西泮片和注射液的鉴别、检查项目和方法、含量测定方法6.氟康唑(1)氟康唑的物理常数测定法、鉴别方法、检查项目和方法、含量测定方法(2)氟康唑片和胶囊的鉴别和含量测定方法杂环化合物:指环状有机化合物的碳环中夹杂有非碳元素原子(如O、S、N等)的化合物第一节异烟肼的分析重点:游离肼的检查及含量测定方法一、结构特点及鉴别特征1.含有吡啶环,N原子具有弱碱性——非水碱量法含量测定或重金属离子沉淀反应鉴别2.γ位上有酰肼基取代还原性——鉴别或氧化还原滴定法含量测定可与某些羰基试剂发生缩合反应——鉴别3.酰胺键易水解引入特殊杂质——游离肼二、鉴别1.与氨制硝酸银试液的反应——酰肼基的还原性异烟肼的酰肼基具有还原性,与硝酸银反应,生成气泡与黑色浑浊,并在试管壁上生成银镜。
异烟肼+AgNO3→Ag(黑色↓、银镜)+N2↑2.红外光谱法3.高效液相色谱法利用保留时间进行鉴别三、检查1.一般杂质检查:“干燥失重”、“炽灼残渣”和“重金属”2.酸度:PH测定法3.溶液的颜色与澄清度游离肼的检查薄层色谱法,对二甲氨基苯甲醛试液显色。
要求在供试品主斑点前方与对照品溶液主斑点相应的位置上,不得显黄色斑点。
控制限量为0.02%。
5.有关物质:高效液相色谱法四、含量测定高效液相色谱法(注意与以往的讲义不同)(氧化还原滴定法)历年考点:含量测定方法A.硫酸铜试液B.溴化钾试液C.醋酸铅试液D.茚三酮E.氨制硝酸银试液以下药物鉴别所使用的试液是1.盐酸利多卡因【答案】A2.异烟肼【答案】E3.硫喷妥钠【答案】C4.磺胺甲噁唑【答案】A解析:考察药物的鉴别方法,将不同类型的药物以配伍选择题的形式出现。