铁盐的性质
- 格式:doc
- 大小:155.00 KB
- 文档页数:4

铁的氢氧化物和铁盐的性质实验报告一、实验名称:铁的氢氧化物和铁盐的性质二、实验目的:1.掌握氢氧化铁、氢氧化亚铁的制备。
2.认识铁盐和亚铁盐之间的转化及其检验。
三、实验准备:四、实验步骤:五、实验现象:【反思交流】1、有什么方法是氢氧化钠与硫酸亚铁反应的现象更明显?2、检验二价铁和三价铁离子,还有哪些方法?2021届新高考化学模拟试卷一、单选题(本题包括15个小题,每小题4分,共60分.每小题只有一个选项符合题意)1.设N A为阿伏加德罗常数的值,下列说法正确的是()A.标准状况下,11.2LSO3中含有原子数为2N AB.用浓盐酸分别与MnO2、KClO3反应制备1molCl2,均转移电子2N AC.将0.1molNH4NO3溶于适量的稀氨水,溶液恰好呈中性,溶液中NH4+数目小于0.1N A D.2molNO和1molO2充分反应后,所得混合气体的分子数小于2N A2.已知2FeSO4高温Fe2O3+SO2↑+SO3↑,某同学设计利用如图装置分别检验产物中的气体。
下列有关表述错误的是()A.用装置甲高温分解FeSO4,点燃酒精喷灯前应先向装置内通一段时间N2 B.用装置乙可检验分解产生的SO2,现象是石蕊试液先变红后褪色C.按照甲→丙→乙→丁的连接顺序,可用装置丙检验分解产生的SO3D.将装置丁中的试剂换为NaOH溶液能更好的避免污染环境3.改变下列条件,只对化学反应速率有影响,一定对化学平衡没有..影响的是A.催化剂B.浓度C.压强D.温度4.室温下,下列各组离子在指定溶液中能大量共存的是()A.能使甲基橙变红的溶液:Na+、Ca2+、Br-、HCO3-B.+-c(H)c(OH)=1×10-12的溶液:K+、Na+、CO32-、AlO2-C.0.1 mol·L-1KFe(SO4)2溶液:Mg2+、Al3+、SCN-、NO3-D.0.1 mol·L-1Ca5NH4(NO3)11溶液:H+、Fe2+、Cl-、SO42-5.设NA为阿伏加德罗常数值。

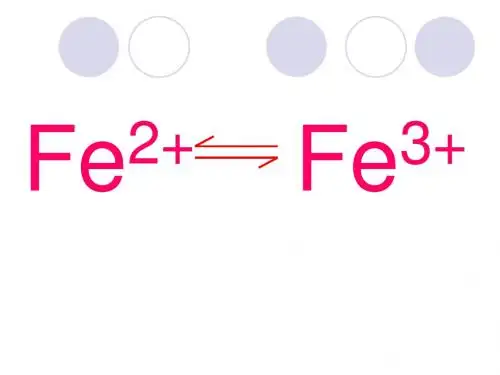


亚铁盐和铁盐亚铁盐:组成中含有Fe2+的盐,如FeCl2、FeSO4·7H2O(绿矾)、(NH4)2SO4·FeSO4·6H2O(硫酸亚铁铵或莫尔盐)、Fe(NO3)2等。
铁盐:组成中含有Fe3+的盐,如FeCl3、Fe2(SO4)、Fe(NO3)3等。
3教材P83活动·探究亚铁盐和铁盐的性质方法导引研究物质性质的两个基本角度在研究物质的性质时,可以从物质类别、物质所含核心元素的化合价这两个基本角度预测物质可能具有的性质,并通过实验进行验证。
Fe3+的检验依据Fe3+与SCN-反应使溶液显红色的性质,可以用KSCN溶液检验Fe3+的存在,发生反应的离子方程式为:Fe3++3SCN-===Fe(SCN)3。
1 铁盐的性质【实验目的】以FeCl3为例,通过实验探究铁盐的性质。
【性质预测】【实验试剂】FeCl3溶液,NaOH溶液,KSCN溶液,KI溶液,淀粉溶液,铁粉,铜片。
【实验方案设计及实施】2 亚铁盐的性质【实验目的】以FeSO4为例,通过实验探究亚铁盐的性质。
【性质预测】【实验试剂】FeSO4溶液,酸性KMnO4溶液,氯水,KSCN溶液,NaOH溶液,锌片。
【实验方案设计及实施】教材延伸Fe2+的检验方法可用先加KSCN溶液再加新制氯水的方法检验Fe2+的存在:发生反应的离子方程式为2Fe2++Cl2===2Fe3++2Cl-、Fe3++3SCN-===Fe(SCN)3。
检验补铁保健品是否变质的方法补铁剂或补铁片的有效成分是亚铁盐,若补铁片的糖衣破裂,其可能已经变质而失去补铁作用,可以采用研碎、溶解、滴加KSCN溶液的方法检验补铁片是否变质。
名师提醒(1)实验室在配制和保存亚铁盐(Fe2+)时,通常加入铁粉或铁钉,防止Fe2+被氧化成Fe3+。
(2)工业上常用FeCl3溶液腐蚀覆盖在绝缘板上的铜箔制造印刷电路板,发生反应的化学方程式为2FeCl3+Cu===CuCl2+2FeCl2,说明Fe3+的氧化性强于Cu2+。


《铁盐和亚铁盐的性质与转变》教学设计
铁盐和亚铁盐是我国化学教育中重要的两个概念,它们的性质和转变与我们日常生活息息相关。
因此,根据教育部《高等学校化学教学大纲》的规定,对此两种重要的物质的性质和转化应该进行详细的教学设计和讲解。
第一部分要讲述的是铁盐的性质。
铁盐是一种由铁元素组成的盐,据化学实验结果显示,其晶体性质大多可以溶于水。
因而,多数时候,铁盐表现出溶解度高、沉淀不完全性等特点。
在一定温度和压力下,铁盐也易于发生变化,其中包括氧化-还原反应和消去反应等。
第二部分主要讲述的是亚铁盐的性质。
亚铁盐是一种有metaloid属性的混合盐,里面包含有 iron-III,它的合成是通过催分水解法进行的。
此外,它还具备机械强度高、热稳定性好等特性。
同时,亚铁盐可以发生氢化-还原反应和溶剂形成反应,并且可以通过改变溶液的种类或变化水浓度而迅速失去水分。
最后,本文还将概括铁盐和亚铁盐的转变过程,具体而言,铁盐的氧化-还原反应和消去反应可以使晶体结构稳定,而亚铁盐的氢化-还原反应、溶剂形成反应可以使其扩散性变的更强。
通过对这些反应的详细分析,可以更好地了解物质的性质和转变,从而为下一步的学习和实验服务。




亚铁盐与铁盐的相互转化亚铁盐与铁盐的相互转化导语:亚铁盐和铁盐是我们在化学实验和工业生产中经常接触到的物质。
它们之间的相互转化在化学反应中起着重要作用。
本文将深入探讨亚铁盐和铁盐的相互转化,包括它们的性质、反应条件和应用领域。
让我们一起来了解这一有趣的化学现象吧!一、亚铁盐和铁盐的性质及区别1. 亚铁盐的性质:亚铁盐,通常是指氯化亚铁(FeCl2)和硫酸亚铁(FeSO4)。
它们的共同特点是含有2价的铁离子(Fe2+)。
亚铁盐多数为淡绿色或淡蓝色的晶体,易溶于水,在空气中容易被氧化而发生颜色变化。
由于亚铁离子具有较强的还原性,因此亚铁盐在一些还原反应中起到了重要的催化剂的作用。
2. 铁盐的性质:铁盐主要指氯化铁(FeCl3)和硫酸铁(Fe2(SO4)3)。
与亚铁盐不同的是,铁盐中铁的氧化态为3+,即含有3价的铁离子(Fe3+)。
铁盐呈现出红褐色或黄褐色的颜色,也易溶于水。
铁盐在一些氧化反应和络合反应中发挥着重要的作用。
3. 区别与联系:亚铁盐和铁盐的区别主要在于铁的氧化态不同,导致了不同的性质和催化活性。
亚铁盐中的2价铁离子较于3价铁离子在电子构型上更不稳定,因此更容易参与化学反应。
在一些氧化还原和复合反应中,亚铁盐常常被氧化成铁盐。
相反的,铁盐可以通过还原反应转化为亚铁盐。
二、亚铁盐与铁盐的相互转化反应1. 亚铁盐氧化为铁盐:亚铁盐的氧化过程是亚铁离子被氧气氧化为3价的铁离子的过程。
这个反应通常发生在潮湿的空气中。
亚铁盐溶液接触到空气中的氧气后,亚铁离子会被氧化成铁离子。
这个反应可以用如下的反应方程式表示:2Fe2+ + O2 → 2Fe3+。
2. 铁盐还原为亚铁盐:铁盐的还原过程是3价铁离子被还原成2价铁离子的过程。
这个反应通常发生在还原剂的作用下。
在硫酸铁溶液中加入铁粉,铁粉会与铁离子发生反应,并将铁离子还原成亚铁离子。
这个反应可以用如下的反应方程式表示:Fe3+ + Fe → 2Fe2+。
《铁盐》导学案一、学习目标1、了解铁盐的主要性质,包括氧化性、水解性等。
2、掌握铁盐的检验方法。
3、理解铁盐在生产生活中的应用。
二、知识回顾1、铁元素在周期表中的位置:位于第____周期第____族。
2、铁常见的化合价有:____、____、____。
3、写出铁与盐酸反应的化学方程式:____________________。
三、铁盐的定义铁盐是指含有铁离子(Fe³⁺)的盐类化合物,常见的铁盐有氯化铁(FeCl₃)、硫酸铁Fe₂(SO₄)₃等。
四、铁盐的性质1、氧化性Fe³⁺具有较强的氧化性,可以氧化一些还原性物质,如铜:2Fe³⁺+ Cu = 2Fe²⁺+ Cu²⁺2、水解性Fe³⁺在水溶液中容易发生水解反应,使溶液显酸性。
Fe³⁺+ 3H₂O ⇌ Fe(OH)₃+ 3H⁺五、铁盐的检验1、观察溶液颜色:含 Fe³⁺的溶液呈黄色。
2、加入 KSCN 溶液:若溶液变成血红色,则含有 Fe³⁺。
六、铁盐的制备1、以氧化铁为原料制备氯化铁Fe₂O₃+ 6HCl = 2FeCl₃+ 3H₂O2、以铁粉和氯气为原料制备氯化铁2Fe + 3Cl₂= 2FeCl₃(条件:点燃)七、铁盐的用途1、在净水方面铁盐在水中水解生成氢氧化铁胶体,能吸附水中的悬浮杂质,起到净水作用。
2、在印刷电路板制作中的应用利用 FeCl₃溶液与铜的反应来制作印刷电路板。
3、在医疗领域某些铁盐可用于治疗缺铁性贫血。
八、课堂练习1、下列能检验出溶液中含有 Fe³⁺的是()A 加入铁粉B 滴入 NaOH 溶液C 通入氯气D 加入 KSCN 溶液2、为了除去氯化铁溶液中的少量氯化亚铁杂质,可加入的试剂是()A 氯气B 铁粉C 铜粉D 稀盐酸3、写出氯化铁溶液中加入铁粉的离子方程式:____________________。
九、课后作业1、总结铁盐的性质和用途。
第三章铁金属材料第一节铁及其化合物3.1.3 铁盐和亚铁盐板块导航01/学习目标明确内容要求,落实学习任务02/思维导图构建知识体系,加强学习记忆03/知识导学梳理教材内容,掌握基础知识04/效果检测课堂自我检测,发现知识盲点05/问题探究探究重点难点,突破学习任务06/分层训练课后训练巩固,提升能力素养1.知道Fe3+、Fe2+的检验原理、试剂的选择及用显色法检验Fe2+时试剂加入的顺序。
2.知道Fe2+的强还原性、Fe3+的强氧化性,能依据氧化还原反应原理选择适当的物质实现两者间的相互转化。
3.依据氧化还原反应原理理解Fe、Fe2+、Fe3+的转化关系及应用。
重点:Fe3+、Fe2+的检验,铁盐与亚铁盐之间相互转变。
难点:铁盐与亚铁盐之间相互转变。
一、亚铁盐的性质及应用1.弱氧化性(1)Mg、Al、Zn与亚铁盐溶液发生反应①Fe2++Zn Fe+Zn2+①Fe2++Mg Fe+Mg2+①3Fe2++3Al3Fe+2Al3+(2)K、Ca、Na与亚铁盐溶液反应①先与反应:2Na+2H2O2NaOH+H2↑①与亚铁盐反应:Fe2++2OH-Fe(OH)2↓2.强还原性(1)能够被Cl2、Br2氧化①除FeCl3溶液中的溶液:2Fe2++Cl22Fe3++2Cl-①Br2:2Fe2++Br22Fe3++2Br-(2)能够被O2氧化①反应:12Fe2++O2+6H2O8Fe3++4Fe(OH)3↓①保存:密封保存,防止将Fe2+氧化;加少量将Fe3+还原成Fe2+(3)能够被酸性的H2O2氧化①反应:2Fe2++2H++H2O22Fe3++2H2O①应用:除去Fe3+中的最佳方法(4)与酸性条件下的等离子不能大量共存①酸性MnO4-:5Fe2++MnO4-+8H+5Fe3++Mn2++4H2O①酸性NO3-:3Fe2++NO3-+4H+3Fe3++NO↑+2H2O①酸性ClO-:2Fe2++2H++ClO-2Fe3++H2O+Cl-(5)还原性:I->Fe2+>Br-①向Fe Br2溶液通入Cl2,先氧化,后氧化①向Fe I2溶液通入Cl2,先氧化,后氧化3.与碱溶液反应①烧碱:Fe2++2OH-Fe(OH)2↓①氨水:二、铁盐的性质及应用含有Fe3+的溶液呈棕黄色,Fe3+处于铁的高价态,遇Fe、Cu、HI、H2S、SO2-3等均表现为氧化性。
铁盐与亚铁盐的性质ppt课件.ppt很抱歉,我无法创建PowerPoint课件在此平台上,但我可以提供一篇有关铁盐和亚铁盐性质的文章,希望对您有所帮助。
铁盐和亚铁盐是两种常见的金属离子化合物,在许多工业和化学应用中都有着广泛的应用。
下面是它们的一些主要性质:1. 氧化还原性铁的氧化还原性很强,可以形成不同价态的离子化合物。
在正常的化学反应中,铁通常存在于+2和+3价态。
亚铁通常存在于+2价态。
2. 溶解性铁盐的水溶性和有机溶解性较强,能够溶于水、醇、酸和氧化剂等溶液中。
但是,在碱性溶液中,它们会形成沉淀。
亚铁盐也有相似的溶解性。
3. 酸碱性铁盐能够与碱性物质反应,形成相应的盐和水。
在强酸性溶液中,它们可以形成稳定的阳离子,例如Fe2+或Fe3+。
亚铁盐的酸碱性与铁盐相似。
4. 颜色由于铁的不同价态,铁盐可以呈现不同的颜色。
Fe2+通常呈现白色,而Fe3+通常呈现黄色、橙色或红色。
这些颜色可以用于分析和识别这些化合物。
亚铁盐通常呈现无色或浅绿色。
5. 氧化性由于铁的氧化还原性,铁盐和亚铁盐具有一定的氧化性。
它们可以与其他物质反应,引起许多化学反应。
6. 应用铁盐和亚铁盐在很多领域都有广泛的应用。
例如,铁盐可以用于制备其他铁化合物,制备水处理剂、化妆品和染料。
亚铁盐也可以用于制备其他亚铁化合物,制备食品添加剂、电池和其他化学品。
总之,铁盐和亚铁盐都是重要的化学物质,具有广泛的应用和特性。
这些性质可以帮助我们更好地了解这些金属离子化合物,在学习和使用中发挥重要的作用。
高一化学铁盐和亚铁盐知识点总结一、铁盐和亚铁盐的基本概念在化学中,铁元素常以不同的价态形式存在,其中最常见的是二价的亚铁离子(Fe2+)和三价的铁离子(Fe3+)。
与这两种离子形式有关的化合物被称为铁盐和亚铁盐。
二、铁盐和亚铁盐的重要性铁盐和亚铁盐在生活中起着重要的作用,它们不仅被广泛应用于工业生产,还在医学和环境领域具有重要意义。
了解铁盐和亚铁盐的性质和应用,对于我们理解化学反应和环境保护等方面具有重要意义。
三、铁盐和亚铁盐的性质1. 溶解性:铁盐和亚铁盐的溶解性与其阴离子和阳离子的性质有关。
常见的铁盐和亚铁盐如氯化铁、硫酸亚铁等在水中溶解度较高。
2. 稳定性:铁盐和亚铁盐的稳定性与其氧化还原性质密切相关。
亚铁盐在氧气存在下容易被氧化成铁盐,而铁盐在还原剂的作用下可还原成亚铁盐。
3. 酸碱性:铁盐和亚铁盐在水溶液中会发生水解反应,生成铁离子和氢氧根离子。
由于铁离子的存在,所以铁盐和亚铁盐呈酸性。
4. 颜色:铁盐和亚铁盐溶液的颜色是由于其中Fe2+和Fe3+离子的吸收和反射光线的不同所致。
亚铁盐溶液呈绿色,铁盐溶液呈黄褐色。
四、铁盐和亚铁盐的应用1. 工业生产:铁盐和亚铁盐广泛用于制备其他化合物或作为催化剂。
例如,硫酸亚铁常被用于制备氢气,硫酸铁可用作催化剂促进化学反应。
2. 医学应用:铁盐和亚铁盐在医学领域中被用作治疗贫血等疾病的药物。
铁离子是人体合成血红蛋白的重要组成部分。
3. 环境保护:亚铁盐常被用作水处理剂,可以去除水中的氧气和其他杂质。
铁盐和亚铁盐在环境中起着重要的氧化还原作用,参与去除有害物质的过程。
五、常见的铁盐和亚铁盐1. 氯化铁:化学式为FeCl3,是一种常见的铁盐,可溶于水。
氯化铁可用作催化剂和染料等。
2. 硫酸亚铁:化学式为FeSO4,是一种常见的亚铁盐,常用于医学和水处理等领域。
3. 硫酸铁:化学式为Fe2(SO4)3,是一种常见的铁盐,常用于工业生产和实验室中。
六、铁盐和亚铁盐的反应1. 氧化反应:亚铁盐容易被氧气氧化成铁盐。
一、实验目的1. 探究铁盐在水溶液中的性质。
2. 观察铁盐与其他化学试剂反应的现象。
3. 分析铁盐的沉淀、溶解、氧化还原等性质。
二、实验原理铁盐是一类含有铁离子的盐类化合物,主要包括亚铁盐和铁盐。
在水溶液中,铁盐具有以下性质:1. 沉淀反应:铁盐与某些阴离子反应生成沉淀。
2. 氧化还原反应:铁盐在特定条件下发生氧化还原反应。
3. 酸碱反应:铁盐与酸、碱反应生成相应的盐和水。
三、实验材料与仪器1. 实验材料:- 硫酸亚铁(FeSO4)- 硫酸铁(Fe2(SO4)3)- 氢氧化钠(NaOH)- 硫氰酸钾(KSCN)- 氯化铁(FeCl3)- 稀硫酸(H2SO4)- 蒸馏水- 烧杯- 试管- 玻璃棒- 滴定管- 酸碱指示剂2. 实验仪器:- 电子天平- 移液管- 烧杯- 试管- 玻璃棒- 滴定管- 酸碱指示剂四、实验步骤1. 铁盐的沉淀反应:- 将0.5g硫酸亚铁溶解于10mL蒸馏水中,配制成硫酸亚铁溶液。
- 取1mL硫酸亚铁溶液于试管中,加入2mL氢氧化钠溶液,观察沉淀现象。
- 记录沉淀颜色和溶解情况。
2. 铁盐的氧化还原反应:- 将0.5g氯化铁溶解于10mL蒸馏水中,配制成氯化铁溶液。
- 取1mL氯化铁溶液于试管中,加入几滴稀硫酸,观察颜色变化。
- 记录颜色变化情况。
3. 铁盐的酸碱反应:- 将0.5g硫酸铁溶解于10mL蒸馏水中,配制成硫酸铁溶液。
- 取1mL硫酸铁溶液于试管中,加入几滴酸碱指示剂,观察颜色变化。
- 加入氢氧化钠溶液,观察沉淀现象和颜色变化。
4. 铁盐的鉴别:- 将0.5g硫酸亚铁溶解于10mL蒸馏水中,配制成硫酸亚铁溶液。
- 取1mL硫酸亚铁溶液于试管中,加入几滴硫氰酸钾溶液,观察颜色变化。
- 记录颜色变化情况。
五、实验结果与分析1. 铁盐的沉淀反应:- 硫酸亚铁溶液中加入氢氧化钠溶液后,生成白色沉淀,沉淀不溶解。
2. 铁盐的氧化还原反应:- 氯化铁溶液中加入稀硫酸后,溶液颜色由黄色变为橙黄色。
高三化学第一轮精讲与精练
(铁盐的性质)
班级姓名
1、Fe3+的性质(1)Fe3+通常是色,Fe3+主要表现。
(2)写出Fe3+与下列物质反应的现象及其离子方程式。
(3)Fe3+的性质
①水解性:A、做净水剂,B、配制时,加盐酸,C、除Fe3+时调PH值,PH=3时沉淀完全,如Mg2+中(酸性)有Fe3+(加去除)
Mg2+中(酸性)有Fe2+先,再加去除。
D、离子共存时,考虑水解
②强氧化性:
③络合性
2、Fe2+的性质
(1)Fe2+通常是色,Fe2+主要表现。
(2)写出Fe2+与下列物质反应的现象及其离子方程式。
(3)Fe2+的化学性质①强还原性:
②水解性:
3、Fe3+和Fe2+相关的离子共存
(1)Fe2+在酸性条件下不能与性离子共存,(填氧化或还原)例如。
不能与发生复分解反应和双水解反应的离子共存:如。
(2)Fe3+在酸性条件下不能与性离子共存,(填氧化或还原)例如。
不能与发生复分解反应和双水解反应的离子共存:如。
4、Fe3+和Fe2+的鉴别
【课后练习】
1、(07·江苏)下列反应的离子方程式正确的是( )
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O △
3↓+3H
+
B.用小苏打治疗胃酸过多:HCO3-+H+==CO2↑+H2O
C.实验室用浓盐酸与MnO2反应制C12:MnO2+2H++2C1-△
Cl2↑+Mn2++H2O
D用FeCl3溶液腐蚀印刷电路板:Fe3++Cu==Fe2++Cu2+
2、(07长郡中学).用高铁酸钠(Na2FeO4)对河湖水消毒是城市饮水处理的新技术。
已知反应
Fe2O3+3Na2O22Na2FeO4+Na2O,下列说法正确的是
A.Na2O2既是氧化剂又是还原剂B.Na2FeO4既是氧化产物又是还原产物
C.3 mol Na2O2发生反应,有12mol 电子转移
D.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀毒
3、(6分)已知:2Fe3++2I-=2Fe2++I22Fe2++Br2=2Fe3++2Br-
(1)含有 1 mol FeI2和 2 mol FeBr2的溶液中通入 2 mol Cl2,此时被氧化的离子是,被氧化的离子的物质的量分别是。
(2)如果向原溶液中通入3 mol C12,则被氧化的离子是,对应的氧化产物的物质的量分别是。
4、(07江苏联考)(1)请将5种物质:N2O、FeSO4、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个配平的化学方程式。
_________+__________→__________+__________+__________+H2O
(2)反应物中发生氧化反应的物质__________,被还原的元素是_________。
(3)反应中1 mol氧化剂_______(填“得到”或“失去”)___________ mol电子。
(4)人体中经常进行的转化,A中Fe2+做剂,B中Fe3+做剂。
(5)“服用维生素C,可使食物中的三价铁离子还原成二价铁离子。
”这句话指出维生素C在这一反应中做剂,具有性。
5.摩尔盐[(NH4)2SO4·FeSO4·6H2O]在空气中比一般亚铁盐稳定,是分析化学中常见的还原剂。
某研究性学习小组设计了下面的实验装置来制备摩尔盐。
实验步骤:
(1)把30%NaOH溶液和废铁屑混合、煮沸、冷却,将洗涤铁屑后的NaOH溶液装入F中。
(2)在E中用处理过的Fe屑和稀H2SO4反应制取FeSO4。
(3)将硫酸亚铁溶液与硫酸铵溶液混合,结晶得摩尔盐。
试回答下列问题:
(1)Fe屑和稀H2SO4反应产生的氢气可赶走装置中的氧气及(NH4)2SO4溶液中的溶解氧,操作时应
先关闭活塞,并同时打开活塞。
请写出Fe屑和稀H2SO4反应产生的氢气的另外一个作用
(2)使摩尔盐结晶可采取两种方法:①蒸发溶液、再自然冷却结晶;②不蒸发溶液、直接自然冷却结晶。
你认为较好的方法是。
(填序号)
(3)原料利用率高,副产品少,产生的有害废物少,保护环境是“绿色化学”的主要内涵。
请写出此实验中能体现“绿色化学”的具体做法(至少写出两点):
、。
6、(07海淀)某校同学为探究Br
2、I
2
和Fe+3的氧化性强弱,进行了如下实验。
实验①取少量KI溶液于试管中,先加入溴水,振荡,再加入CCl
4
, 振荡后静置,观察到下层液体呈紫红色;
②取少量FeSO
4
溶液于试管中,先加入溴水,振荡,再继续滴加两滴KSCN溶液,振荡,观察到溶液呈血红色。
(1)写出实验②中发生氧化还原反应的离子方程式__________________________;
(2)由上述两个实验,对物质的氧化性可以得出的正确结论是(填序号)_________;
A.Br
2>I
2
B.Fe+3>Br
2
C.Br
2
>Fe+3D.I->Br-
(3)已知Fe+3的氧化性强于I
2
,请你从所给试剂中选择所需试剂,设计一个实验加以证明。
①FeCl
3溶液②碘水③KI溶液④稀H
2
SO
4
⑤淀粉液
(友情提示:请写出实验步骤、现象及结论)_________________________________
____________________________________________________________________________。
7、将铁粉、铜粉、FeCl3溶液和CuCl2溶液混合于某容器中充分反应(假定容器不参与反应)。
试判断下列情况下,溶液中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器中不可能有;
(2)若氯化铜有剩余,则容器中可能有;
(3)若氯化铁和氯化铜都有剩余,则容器中不可能有,可能有;
(4)若氯化铁有剩余,则容器中不可能有。