DNA电泳常见问题分析
- 格式:docx
- 大小:39.82 KB
- 文档页数:9

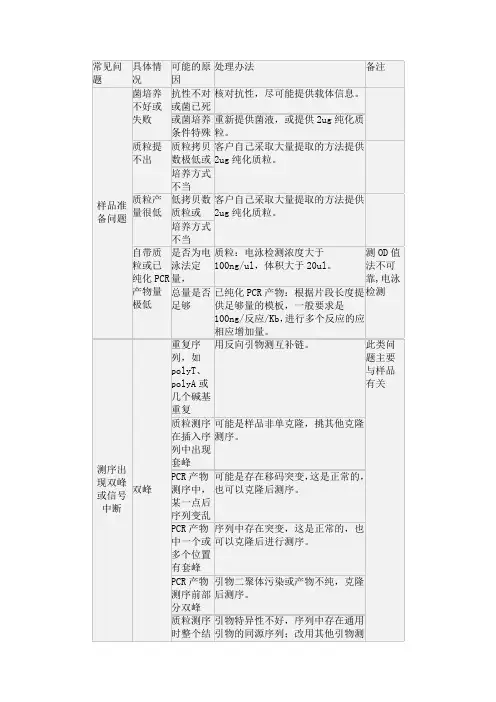

DNA电泳常见问题凝胶电泳操作注意事项1、琼脂糖:不同厂家、不同批号的琼脂糖,其杂质含量不同,影响DNA的迁移及荧光背景的强度,应有选择地使用。
2、凝胶的制备:凝胶中所加缓冲液应与电泳槽中的相一致,溶化的凝胶应及时倒入板中,避免倒入前凝固结块。
倒入板中的凝胶应避免出现气泡,以免影响电泳结果。
3、电泳缓冲液:为保持电泳所需的离子强度和pH,应经常更新电泳缓冲液。
4、样品加入量:一般情况下,0.5cm宽的梳子可加0.5μg的DNA量,加样量的多少依据加样孔的大小及DNA 中片段的数量和大小而定.当加样孔大时,样品上样量应相应加大,否则会造成条带浅甚至辨认不清;反之则应适当减少加样量,但是上样量过多会造成加样孔超载,从而导致拖尾或弥散,对于较大的DNA此现象更明显。
5、 DNA样品中盐浓度会影响DNA的迁移率,平行对照样品应使用同样的缓冲条件以消除这种影响。
6、 DNA迁移率取决于琼脂糖凝胶的浓度,迁移分子的形状及大小。
采用不同浓度的凝胶有可能分辩范围广泛的DNA分子,制备琼脂糖凝胶可根据DNA分子的范围来决定凝胶的浓度。
小片段DNA的检测应采用聚丙烯酰胺凝胶电泳,以提高分辨率。
7.选择的实验材料要新鲜,处理时间不易过长。
8.在加入细胞裂解缓冲液前,细胞必须均匀分散,以减少DNA团块形成。
9. 提取的DNA不易溶解:不纯,含杂质较多;加溶解液太少使浓度过大。
沉淀物太干燥,也将使溶解变得很困难。
10. 电泳检测时DNA成涂布状:操作不慎;污染核酸酶等。
11.分光光度分析DNA的A280/A260小于1.8;不纯,含有蛋白质等杂质。
在这种情况下,应加入SDS至终浓度为0.5%,并重复步骤2~8。
12.酚/氯仿/异戊醇抽提后,其上清液太黏不易吸取:含高浓度的DNA,可加大抽提前缓冲液的量或减少所取组织的量DNA电泳常见问题分析之一1 请问配制聚丙烯酰胺凝胶电泳胶时,促凝的是TEMED还是过硫酸铵?胶聚时间很长如何解决?过硫酸铵提供驱动丙烯酰胺和双丙烯酰胺聚合所需的自由基,而TEMED通过催化过硫酸铵形成自由基而加速它俩的聚合。
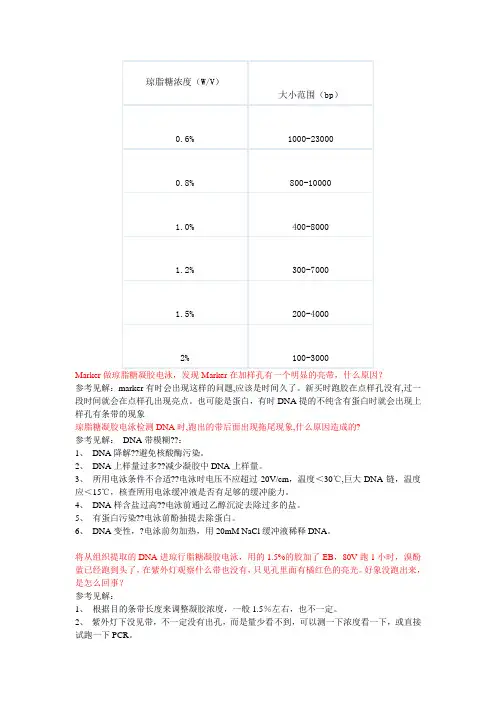
Marker参考见解:marker有时会出现这样的问题,应该是时间久了。
新买时跑胶在点样孔没有,过一段时间就会在点样孔出现亮点。
也可能是蛋白,有时DNA提的不纯含有蛋白时就会出现上样孔有条带的现象琼脂糖凝胶电泳检测DNA时,跑出的带后面出现拖尾现象,什么原因造成的?参考见解:DNA带模糊??:1、DNA降解??避免核酸酶污染。
2、DNA上样量过多??减少凝胶中DNA上样量。
3、所用电泳条件不合适??电泳时电压不应超过20V/cm,温度<30℃,巨大DNA链,温度应<15℃,核查所用电泳缓冲液是否有足够的缓冲能力。
4、DNA样含盐过高??电泳前通过乙醇沉淀去除过多的盐。
5、有蛋白污染??电泳前酚抽提去除蛋白。
6、DNA变性,?电泳前勿加热,用20mM NaCl缓冲液稀释DNA。
将从组织提取的DNA进琼行脂糖凝胶电泳,用的1.5%的胶加了EB,80V跑1小时,溴酚蓝已经跑到头了,在紫外灯观察什么带也没有,只见孔里面有橘红色的亮光。
好象没跑出来,是怎么回事?参考见解:1、根据目的条带长度来调整凝胶浓度,一般1.5%左右,也不一定。
2、紫外灯下没见带,不一定没有出孔,而是量少看不到,可以测一下浓度看一下,或直接试跑一下PCR。
3、最好加一个marker孔,尤其你第一次跑胶时。
4、电泳时间可能过长,一般75v×30min左右,但是具体看溴酚蓝的离孔距离和目的条带离孔距离。
怎样根据目测条带亮度来判断DNA浓度?参考见解:1、跑胶时候marker 可以加成定量marker,如1kb、100bp等marker,按说明书的量上样电泳,如加500ng量的DNA marker,电泳完毕后,就可将目的DNA条带和MARKER 条带的亮度做个大致的比较,找出两者最接近亮度的条带。
因为marker的各条带都已知所含的DNA浓度(说明书中详细注明),因此根据条带的亮度、大小大致就可推测目的DNA的浓度。
2、在通过目测DNA浓度的时候,最好要把加样量设一个梯度,比如从0。

1 、为什么开始一段序列的信号很杂乱,几乎难以辨别这主要是因为残存的染料单体造成的干扰峰所致,该干扰峰和正常序列峰重叠在一起;另外,测序电泳开始阶段电压有一个稳定期,所以经常有20-50 bp 的紧接着引物的片段读不清楚,有时甚至更长。
2 、为什么在序列的末端容易产生 N 值,峰图较杂由于测序反应的信号是逐渐减弱的,所以序列末端的信号会很弱,峰图自然就会杂乱,加上测序胶的分辨率问题,如果碱基分不开,就会产生 N 值,正常情况下ABI377测序仪能正确读出500个碱基的有效序列。
3 、测序结果怎么找不到我的引物序列如果找不到测序所用的引物序列。
这是正常的,因为引物本身是不被标记的,所以在测序报告中是找不到的;如果找不到克隆片段中的扩增引物,可能是您克隆的酶切位点距离您的测序引物太近,开始一段序列很杂,几乎难以辨别,有可能看不清或看不到扩增引物;另外插入片段的插入方向如果是反的,此时需找引物的互补序列。
4 、测序结果怎么看不到我克隆的酶切位点可能的原因同上,您克隆的酶切位点距离您的测序引物太近,开始一段序列很杂,几乎难以辨别,有可能看不清或看不到酶切位点。
通常我们会尽量选择距离酶切位点远点的引物,当然,若是样品出现意外原因,如空载、载体自连等,克隆的酶切位点也是看不到的。
5 、你测出的结果与我预想的不一致,给我的结果与我需要的序列有差距,这是怎么回事首先,我们会核实给您的测序结果是否对应您的样品编号,如果对应的是您的样品,由于不知您的实验背景,测得的序列是否与您预想的结果一致我们无法判断,我们能做到的是检查发送给您的测序结果和您提供来的样品是否一致。
6 、序列图为什么会有背景噪音(杂带)是否会影响测序结果序列图的背景杂带是由荧光染料引起,如果太强会影响测序结果,要看信噪比,我们给的结果信噪比大都在98%以上。
7 、测序结果为什么与标准序列有差别原因可能有:样品个体之间的差别、测序准确率的问题,自动测序仪分析序列的准确并非100%,建议至少测一次双向,通过双向测序可以最大限度减少测序的错误。

琼脂糖凝胶电泳条带不清晰的原因琼脂糖凝胶电泳是一种常用的分析和分离生物大分子的方法。
然而,有时候在进行琼脂糖凝胶电泳实验时,我们可能会遇到条带不清晰的问题,这给结果的解读和分析带来了困扰。
下面我将介绍一些可能导致琼脂糖凝胶电泳条带不清晰的原因。
1. DNA样品质量不佳琼脂糖凝胶电泳的前提是获得高质量的DNA样品。
如果DNA样品质量不佳,比如存在脏带、降解或者污染,都会导致条带不清晰。
因此,在进行实验之前,我们需要对DNA样品进行质控,确保其质量符合要求。
2. 样品预处理不当在进行琼脂糖凝胶电泳之前,我们通常需要对DNA样品进行一些预处理,比如酶切、PCR扩增或者纯化等。
如果预处理过程中存在问题,比如酶切反应时间过长、PCR扩增过程中出现非特异性扩增等,都会导致条带不清晰。
3. 聚丙烯酰胺凝胶浓度选择不当琼脂糖凝胶电泳中,聚丙烯酰胺凝胶的浓度是影响条带清晰度的重要因素之一。
一般来说,较低浓度的凝胶适用于较大的DNA片段分离,而较高浓度的凝胶适用于较小的DNA片段分离。
如果选择的凝胶浓度不合适,就会导致条带模糊不清。
4. 电泳条件设置不当电泳条件的设置也是影响琼脂糖凝胶电泳结果的重要因素。
比如,电泳电压、电泳时间和电泳缓冲液的配制等都会影响条带的清晰度。
如果电压过高或者电泳时间过长,都会导致条带模糊不清。
此外,如果电泳缓冲液的配制不正确,比如pH值不稳定或者离子浓度不合适,也会影响条带的清晰度。
5. 负载样品量过多或过少在进行琼脂糖凝胶电泳时,负载样品量的选择也是非常关键的。
如果负载样品量过多,会导致条带扩散,模糊不清;如果负载样品量过少,条带可能会变得非常弱或者根本看不到。
因此,在进行负载样品时,需要根据实验的需要选择适当的样品量。
琼脂糖凝胶电泳条带不清晰的原因可能是多方面的,包括DNA样品质量不佳、样品预处理不当、聚丙烯酰胺凝胶浓度选择不当、电泳条件设置不当以及负载样品量过多或过少等。
在进行琼脂糖凝胶电泳实验时,我们需要仔细检查每一个步骤,确保实验条件的准确性和合理性,从而获得清晰可靠的结果。

DNA琼脂糖凝胶电泳一,实验原理琼脂糖凝胶电泳是分离和纯化DNA 片段的常用技术.把DNA样品加入到一块包含电解质的多孔支持介质(琼脂糖凝胶)的样品孔中,并置于静电场上.由于DNA分子的双螺旋骨架两侧带有含负电荷的磷酸根残基,因此在电场中向正极移动.在一定的电场强度下,DNA分子的迁移速度取决于分子筛效应.具有不同的相对分子质量的DNA片段泳动速度不一样,因而可依据DNA分子的大小来使其分离.凝胶电泳不仅可分离不同分子质量的DNA, 也可以分离相对分子质量相同,而构型不同的DNA分子.在电泳过程中可以通过示踪染料或相对分子质量标准参照物和样品一起进行电泳而得到检测.相对分子质量标准参照物相对可以提供一个用于确定DNA片段大小的标准.在凝胶中加入少量溴化乙锭(ethidium bromide, EB),其分子可插入DNA的碱基之间,形成一种络合物,在254~365nm波长紫外光照射下,呈桔红色荧光,因此也可对分离的DNA进行检测.一般琼脂糖凝胶电泳适用于大小在0.2kb~50kb范围内的DNA 片段.本实验介绍琼脂糖凝胶的制备以及琼脂糖凝胶电泳在DNA片段分离中的应用方法.琼脂糖凝胶浓度(%)线状DNA分子分离范围(kb)0.3 5--600.6 1--200.9 0.5--71.2 0.4--61.5 0.2--32.0 0.1--2琼脂糖凝胶电泳是用于分离纯化和鉴定核酸的方法,根据琼脂糖的溶解温度,把琼脂糖分为一般琼脂糖和低熔点琼脂糖。
低熔点琼脂糖的熔点为62--65,溶解后在37下维持液体状态约数小时,主要用于DNA片断的回收、质粒与外源性DNA的快速连接等。
DNA在琼脂糖凝胶中的迁移速度与琼脂糖浓度、DNA分子量及其构象、电泳缓冲液、电场强度等因素有关,一般说来,DNA片断越大或者琼脂糖浓度越大,其迁移速率越大;而电场强度越高,其迁移速率越大。
不同浓度琼脂糖凝胶DNA分离范围见上图表。
二,仪器及试剂1.仪器及耗材:水平电泳槽,电泳仪,凝胶成像分析系统,微波炉,微量移液器,透明胶带,点样或parafilm,100 ml或250 ml锥形瓶,量筒,吸头等.2.试剂及配制:50×TAE缓冲液的配制:2 mol/L Tris-乙酸,0.05 mol/L EDTA(pH 8.0)配制1000 mlTris 242 g冰乙酸 57.1 ml0.5 mol/L EDTA 100 ml加入600 ml去离子水后搅拌溶解,将溶液定容至1 L后.高温高压灭菌,室温保存.1×TAE缓冲液的配制:称量20 ml的50×TAE缓冲液,再加入980 ml的去离子水.溴化乙啶贮存液:10 mg/ml 溴化乙啶配制:100 ml称取1 g溴化乙啶,置于100 ml烧杯中,加入80 ml去离子水后搅拌溶解.将溶液定容至100 ml后,转移到棕色瓶中.室温保存.6×上样缓冲液:0.25%溴酚蓝,0.25%二甲苯青FF,30%甘油.配制:10 ml溴酚蓝 25 mg二甲苯青FF 25 mg甘油 3 ml用6×TAE缓冲液定溶至10 ml,分装成1 ml/管.-20℃保存.其它试剂:DNA样品,DNA Ladder ,琼脂糖三,操作步骤1. 制备1%琼脂糖凝胶(大胶用70ml,小胶用50ml):称取0.7 g(0.5g)琼脂糖置于锥形瓶中,加入70 ml(50ml)1×TAE,瓶口倒扣小烧杯.微波炉加热煮沸3次至琼脂糖全部融化,摇匀,即成1.0%琼脂糖凝胶液.2. 胶板制备:取电泳槽内的有机玻璃内槽(制胶槽)洗干净,晾干,放入制胶玻璃板.取透明胶带将玻璃板与内槽两端边缘封好,形成模子.将内槽置于水平位置,并在固定位置放好梳子.将冷却到65℃左右的琼脂糖凝胶液混匀小心地倒入内槽玻璃板上,使胶液缓慢展开,直到整个玻璃板表面形成均匀胶层.室温下静置直至凝胶完全凝固,垂直轻拔梳子,取下胶带,将凝胶及内槽放入电泳槽中.添加1×TAE电泳缓冲液至没过胶板为止.3. 加样:在点样板或parafilm上混合DNA样品和上样缓冲液,上样缓冲液的最终稀释倍数应不小于1X.用10 ul微量移液器分别将样品加入胶板的样品小槽内,每加完一个样品,应更换一个加样头,以防污染,加样时勿碰坏样品孔周围的凝胶面.(注意:加样前要先记下加样的顺序).4. 电泳:加样后的凝胶板立即通电进行电泳,电压60-100V,样品由负极(黑色)向正极(红色)方向移动.电压升高,琼脂糖凝胶的有效分离范围降低.当溴酚蓝移动到距离胶板下沿约1cm处时,停止电泳. (5)电泳完毕后,取出凝胶,用含有0.5 ug/ml的溴化乙锭1×TAE溶液染色约20 min,再用清水漂洗10 min.(6)观察照相:在紫外灯下观察,DNA存在则显示出红色荧光条带,采用凝胶成像系统拍照保存.四,常见问题及注意事项1.配琼脂糖时应使其完全熔化后方可制胶.2.琼脂糖凝胶易于破碎,操作时要轻缓.3.电泳时应注意电源线路,预防触电.4.溴化乙淀具有致癌作用,配制及使用时应带乳胶或一次性塑料手套.并在专门的实验室内使用.5.紫外线对人体有损伤作用,开灯时间不宜太长,注意防护.6.DNA带形状模糊:DNA加样过多;电压太高;凝胶中有气泡.7.质粒DNA的存在形式有3种,①共价闭环DNA(cccDNA),常以超螺旋形式存在;②开环DNA(ocDNA),此种质粒DNA的两条链中有一条发生一处或多处断裂,因此可以自由旋转从而消除张力,形成松弛的环状分子;③线状DNA,因质粒DNA的两条链在同一处断裂而造成.因此质粒DNA电泳的结果中有可能出现三条泳带,它们的泳动速度为: cccDNA > 线状DNA > ocDNA.添加来自TIANGEN的资料:1,琼脂糖:不同厂家\不同批号的琼脂糖,其杂质含量不同,影响DNA的迁移及其荧光背景的强度,应有选择的使用.2,凝胶的制备:凝胶中所加的缓冲液应该与电泳槽中的相一致,溶化的凝胶应该及时倒入板中,避免倒入之前凝固结块,倒入板中的凝胶应该避免出现气泡,以免影响电泳结果.3,电泳缓冲液:为保持电泳所需的离子强度和PH,应经常更新电泳缓冲液.4,样品加入量:一般情况下,0.5CM宽的梳子可加0.5微克的DNA量,加样量的多少依据加样孔的大小及DNA中片断的数量和大小而定.当加样孔大时,样品上样量应相应加大,否则会造成条带浅甚至辨认不清楚;反之,则应该适当减少加样量,但是上样量过多会造成加样孔超载,从而导致拖尾或扩散,对于较大的DNA此现象更明显.5,DNA样品中盐浓度会影响DNA的迁移率,平行对照样品中应该使用同样的缓冲条件以消除这种影响.6,DNA迁移率取决于琼脂糖的浓度,迁移分子的形状及其大小.采用不同浓度的凝胶有可能分辨范围广泛的DNA分子,制备琼脂糖凝胶可根据DNA分子的范围来决定凝胶的浓度.小片断DNA的检测应采用聚丙烯酰胺凝胶电泳,以提高分辨率.。


分子生物学试验的常见问题与解决方案范文一、Southern 杂交问题 1:电泳后觉察凝胶中DNA 集中,导致结果难以确定,如何解决这一问题?解决方案:〔1〕在操作上:电泳时隔孔上样,电泳后要对凝胶准时处理使凝胶枯燥;〔2〕琼脂糖的质量应当较好,尤其是不应含有内切酶,否则有时将使低拷贝数基因的杂交结果难以解释。
问题 2:传统方法中转膜不完全的问题如何抑制?解决方案:经典的向上转移法会使凝胶短时间内变薄,此时即使延长转移时间至 24 小时以上,也不能使大分子DNA 良好地转移出去,因此,转膜不完全。
向下转膜法由于不需在吸水纸上增加重量,凝胶根本不变形;加之吸水纸的吸力与水受到的重力方向全都,故可以良好地完成 DNA 的转移, 它不需要特别的仪器,转移速度较快,转移效率高。
利用地高辛标记探针进展Southern 杂交时,对于大于 15kb 的DNA 片断,转膜之前用盐酸进展脱嘌呤可以促进转膜效率,但脱嘌呤过度可导致分子量相对较小的DNA 被打断成过小的片段而难以和尼龙膜结合。
假照试验转膜过程中同时含有大于 15kb 的DNA(通常为基因组)和小片段DNA(通常是基因组酶切产物),那么在转移的过程中倾斜容器,仅使凝胶上半局部浸泡于盐酸,这样既可以提高大片断DNA 的转移效率,又不会打碎小片段DNA。
另外,等承受琼指糖凝胶直接杂交的方法,来解决这一难题:以转基因鼠的检测为例,试验步骤如下:1.转基因鼠的建立:以鼠乳清酸蛋白(WAP)基因5’调控区指导人G-CSF 基由于构件,建立转基因小鼠。
转基因小鼠的检测承受剪取鼠尾DNA 做Southern 进展鉴定。
2.琼脂糖凝胶直接杂交:(l)用BanHI(150U)对由假孕鼠产生的仔鼠剪尾提取基因组DNA10μg酶切过液,取少量电泳检查酶切完全后,上样电泳 8 小时,(2)将电泳槽板连同凝胶置50℃放置 3 小时,用镊子轻轻揭起凝胶,放于变性液(0.5MNaOH,0.5MNaCl)20 分钟,转置中和液(0.5MTriHCl,0.15MNaCl)20 分钟,将胶放于玻璃板上沥干液体,室温放置 30 分钟。

琼脂糖凝胶电泳分离纯化DNA步骤和问题分析琼脂糖凝胶电泳是用琼脂或琼脂糖作支持介质的一种电泳方法。
其分析原理与其他支持物电泳最主要区别是:它兼有“分子筛”和“电泳”的双重作用。
对于分子量较大的样品,如大分子核酸、病毒等,一般可采用孔径较大的琼脂糖凝胶进行电泳分离。
琼脂糖凝胶具有网络结构,物质分子通过时会受到阻力,大分子物质在涌动时受到的阻力大,因此在凝胶电泳中,带电颗粒的分离不仅取决于净电荷的性质和数量,而且还取决于分子大小,这就大大提高了分辨能力。
但由于其孔径相比于蛋白质太大,对大多数蛋白质来说其分子筛效应微不足道,现广泛应用于核酸的研究中。
DNA分子在琼脂糖凝胶中泳动时有电荷效应和分子筛效应。
DNA分子在高于等电点的pH 溶液中带负电荷,在电场中向正极移动。
由于糖-磷酸骨架在结构上的重复性质,相同数量的双链DNA几乎具有等量的净电荷,因此它们能以同样的速率向正极方向移动,一般琼脂糖凝胶电泳适用于大小在0.2kb~50kb范围内的DNA片段,三种不同构型分子进行电泳时的迁移速度大小顺序为:超螺旋DNA>线型DNA>开环DNA.琼脂糖预制胶一、选择适合的电泳缓冲液:1、较高浓度的胶有利于提高小分子量核酸的分辨率,常规一般使用TBE缓冲液。
(即Tris 硼酸盐溶液)2、电泳时使用新制的缓冲液可以明显提高电泳效果。
注意电泳缓冲液多次使用后,离子强度降低,PH值上升,缓冲性能下降,可能使DNA电泳产生条带模糊和不规则的DNA带迁移的现象。
二、选择适合的Marker:DNA电泳一定要使用DNA marker或已知大小的正对照DNA来估计DNA片段大小。
Marker的选择要适中,Marker应该选择在目标片段大小附近ladder较密的,这样对目标片段大小的估计才比较准确。
如果marker太大就可能跑不开,挤到一起,起不到marker的作用。
三、设备和耗材:移液器、电泳仪电源、水平式凝胶电泳槽、凝胶成像系统、样品、枪头。

琼脂糖核酸电泳中的疑难问题及其解决方案一、分辨率问题问题描述:琼脂糖核酸电泳中,条带分辨不清,无法准确区分不同的DNA 片段。
解决方案:1.调整琼脂糖浓度:增加琼脂糖浓度可以提高分辨率。
2.调整缓冲液浓度:降低缓冲液浓度可以提高分辨率。
3.增加电压:适当增加电压可以提高迁移速率,从而提高分辨率。
二、迁移速率不均一问题描述:琼脂糖核酸电泳中,不同DNA片段的迁移速率不一致,导致条带不整齐。
解决方案:1.调整缓冲液浓度:适当增加缓冲液浓度可以提高迁移速率的一致性。
2.控制温度:保持恒温可以减少温度对迁移速率的影响。
3.更换电泳槽:电泳槽老化或污染可能导致迁移速率不均一,需要更换新的电泳槽。
三、拖尾现象问题描述:琼脂糖核酸电泳中,某些DNA片段出现拖尾现象,影响条带分析。
解决方案:1.调整琼脂糖浓度:适当增加琼脂糖浓度可以减少拖尾现象。
2.控制温度:保持恒温可以减少温度对DNA片段的影响,从而减少拖尾现象。
3.检查缓冲液:缓冲液不纯或被污染可能导致拖尾现象,需要更换新的缓冲液。
四、条带弥散问题描述:琼脂糖核酸电泳中,某些条带出现弥散现象,影响分辨率。
解决方案:1.调整琼脂糖浓度:适当增加琼脂糖浓度可以减少弥散现象。
2.控制温度:保持恒温可以减少温度对DNA片段的影响,从而减少弥散现象。
3.检查缓冲液:缓冲液不纯或被污染可能导致弥散现象,需要更换新的缓冲液。
五、背景问题问题描述:琼脂糖核酸电泳中,背景较深,影响条带分析。
解决方案:1.调整缓冲液浓度:适当降低缓冲液浓度可以减少背景问题。
2.控制温度:保持恒温可以减少温度对背景的影响。
3.检查电泳槽:电泳槽老化或污染可能导致背景问题,需要更换新的电泳槽。
六、染色不均一问题描述:琼脂糖核酸电泳后,某些条带染色不均一,影响分析结果。
解决方案:1.调整染色时间:适当延长染色时间可以提高染色效果。
2.更换染色剂:染色剂不纯或被污染可能导致染色不均一,需要更换新的染色剂。
D N A电泳常见问题分析 Company number:【0089WT-8898YT-W8CCB-BUUT-202108】DNA电泳常见问题凝胶电泳操作注意事项1、琼脂糖:不同厂家、不同批号的琼脂糖,其杂质含量不同,影响DNA的迁移及荧光背景的强度,应有选择地使用。
2、?凝胶的制备:凝胶中所加缓冲液应与电泳槽中的相一致,溶化的凝胶应及时倒入板中,避免倒入前凝固结块。
倒入板中的凝胶应避免出现气泡,以免影响电泳结果。
3、?电泳缓冲液:为保持电泳所需的离子强度和pH,应经常更新电泳缓冲液。
4、?样品加入量:一般情况下,宽的梳子可加μg的DNA量,加样量的多少依据加样孔的大小及DNA中片段的数量和大小而定.当加样孔大时,样品上样量应相应加大,否则会造成条带浅甚至辨认不清;反之则应适当减少加样量,但是上样量过多会造成加样孔超载,从而导致拖尾或弥散,对于较大的DNA此现象更明显。
5、?DNA样品中盐浓度会影响DNA的迁移率,平行对照样品应使用同样的缓冲条件以消除这种影响。
6、?DNA迁移率取决于琼脂糖凝胶的浓度,迁移分子的形状及大小。
采用不同浓度的凝胶有可能分辩范围广泛的DNA分子,制备琼脂糖凝胶可根据DNA分子的范围来决定凝胶的浓度。
小片段DNA的检测应采用聚丙烯酰胺凝胶电泳,以提高分辨率。
7.选择的实验材料要新鲜,处理时间不易过长。
8.在加入细胞裂解缓冲液前,细胞必须均匀分散,以减少DNA团块形成。
9. 提取的DNA不易溶解:不纯,含杂质较多;加溶解液太少使浓度过大。
沉淀物太干燥,也将使溶解变得很困难。
10. 电泳检测时DNA成涂布状:操作不慎;污染核酸酶等。
11.分光光度分析DNA的A280/A260小于;不纯,含有蛋白质等杂质。
在这种情况下,应加入SDS至终浓度为%,并重复步骤2~8。
12.酚/氯仿/异戊醇抽提后,其上清液太黏不易吸取:含高浓度的DNA,可加大抽提前缓冲液的量或减少所取组织的量DNA电泳常见问题分析之一1? 请问配制聚丙烯酰胺凝胶电泳胶时,促凝的是TEMED还是过硫酸铵胶聚时间很长如何解决过硫酸铵提供驱动丙烯酰胺和双丙烯酰胺聚合所需的自由基,而TEMED通过催化过硫酸铵形成自由基而加速它俩的聚合。
DNA电泳结果分析
(供参考)
首先看第二泳道,能够看见两条带,一般的质粒跑完电泳都是这种情况,因为质粒容易开链,变成线性的,或者是半线性半环状,而环状的比线性的跑的快,所以上面那条浅的应该是开链的质粒,下面的是环状的质粒,不过不要紧,一般都是这样。
看第三条泳带,说明你的目的条带大约在750bp。
再看第四个泳带,靠近点样孔的是你切掉了目的基因的质粒,此时为线性的质粒,能够看见它比第二条泳道那条亮带跑的要慢一些,这是对的结果。
还是因为环状的比线性的跑的快。
而第四条泳带下面那个浅带,是你的目的基因,它与你PCR产物大小一样。
因此说明了你的重组质粒构建成功,目的基因已经连入质粒了。
精选。
dna电泳分子量大的
DNA电泳分子量大的现象可以通过以下几点解释:
1. 分子大小:DNA分子的迁移速率与其分子量对数成反比。
分子量越大,DNA分子在凝胶孔隙中蠕行的阻力越大,因此迁移速度越慢。
在电泳过程中,分子量较大的DNA片段跑得较远。
2. 电泳电压和缓冲液:电泳电压过高或缓冲液放置时间过长可能导致D NA分子移动速度加快,从而使分子量大的DNA片段在电泳图中表现为拖尾现象。
3. 凝胶浓度:琼脂糖凝胶浓度偏高时,分子量大的DNA分子在胶中的阻力增加,导致其迁移速度减慢,可能出现拖尾现象。
4. 实验操作:实验过程中,如操作不当,如消化时间过长或过短,细胞膜易造成损伤,也可能影响DNA分子在电泳中的迁移速度。
为了避免上述现象,可以尝试以下改进措施:
1. 调整电泳电压:适当降低电压,以免电压过高导致分子量大的DNA 分子迁移过快。
2. 更换缓冲液:定期更换缓冲液,以保持其性能稳定。
3. 调整凝胶浓度:根据实验需求,选用适当浓度的琼脂糖凝胶。
一般情况下,凝胶浓度越低,DNA分子迁移速度越快。
4. 优化实验操作:严格控制消化时间,避免细胞膜损伤,确保实验过程中DNA分子的完整性。
综上所述,DNA电泳分子量大的现象可以通过调整实验条件和操作方法得到改善。
在实际操作中,还需根据具体情况和实验需求进行优化。
DNA电泳条带indel百分比分析
一、微笑形区带(两边翘起,中间凹下):
形成原因:主要是由凝胶中间部分凝固不均匀引起的,多出现于较厚的凝胶中。
处理办法:待其充分凝固再做实验。
二、皱眉形区带(两边向下,中间鼓起):
形成原因:主要出现在蛋白质垂直电泳槽中,一般是由两板之间的底部间隙气泡未排除干净引起的。
处理办法:可在两板之间加入适量缓冲液,以排除气泡。
三、区带拖尾:
形成原因:主要是由样品溶解效果不佳或分离胶浓度过大引起的。
处理办法:加样前离心;选择适当的样品缓冲液,加适量样品促溶剂;电泳缓冲液放置时间过长,重新配制;降低凝胶浓度。
四、区带出现纹理:
形成原因:主要是由样品不溶性颗粒引起的。
处理办法:加样前离心,加适量样品促溶剂。
五、鬼带:
形成原因:主要是由于还原剂在加热的过程中被氧化而失去活性,
致使原来被解离的蛋白质分子重新折叠结合和亚基重新缔合,聚合成大分子,其分子量比目标区带大,有时不能进入分离胶。
但它与目标区带有相同的免疫学活性,在免疫印迹反应中可见,能与目标区带对应的抗体作用。
处理办法:加热煮沸后再添加适量的DTT或Beta巯基乙醇,以补充不足的还原剂;加适量EDTA来阻止还原剂的氧化。
dna提取的电泳呈弥散状的原因DNA电泳是一种常用的生物分析技术,通过电场作用下的DNA分子的迁移速度差异来分离和检测DNA片段。
在电泳过程中,有时我们会观察到DNA在凝胶中呈现出弥散状的现象,本文将探讨这种现象的原因。
我们需要了解DNA电泳的基本原理。
DNA是双螺旋结构的大分子,由两条互补的链组成。
在电场作用下,DNA分子会迁移到电场的正极或负极方向,取决于DNA分子的电荷性质。
一般来说,DNA分子带有负电荷,所以会向电场的正极方向迁移。
然而,DNA电泳呈弥散状的现象并不常见,通常DNA在电泳过程中会形成清晰的条带。
那么,为什么有时候DNA会呈现出弥散状呢?一种可能的原因是DNA样本中存在着高分子杂质。
DNA提取过程中,我们通常使用各种试剂和方法来纯化DNA样本,以去除杂质。
然而,完全去除杂质是非常困难的,即使是微量的高分子杂质也足以影响DNA的电泳结果。
这些杂质可能会与DNA分子发生相互作用,导致DNA分子的迁移速度减慢或受阻,进而导致电泳呈弥散状。
另一个可能的原因是DNA分子本身的特性。
DNA分子具有一定的长度和结构,这些特性会影响DNA的迁移速度。
一般来说,较短的DNA片段会迁移得更快,而较长的DNA片段会迁移得更慢。
当DNA样本中存在不同长度的DNA片段时,较长的片段会被较短的片段“拖累”,导致电泳呈现出弥散状。
凝胶浓度也会影响DNA电泳的结果。
凝胶是DNA电泳中的重要载体,它能够形成一个网状结构,限制DNA分子的迁移。
当凝胶浓度较高时,DNA分子受到的阻力也较大,迁移速度会减慢,从而导致电泳呈弥散状。
除了上述原因,实验操作中的一些因素也可能导致DNA电泳呈弥散状。
例如,电泳过程中的电场强度、电泳时间和电解质浓度等参数的选择都会对电泳结果产生影响。
不同的实验条件可能导致DNA 分子的迁移速度差异,进而影响电泳结果。
在实际实验中,我们可以采取一些措施来解决DNA电泳呈弥散状的问题。
一种方法是优化DNA提取和纯化的步骤,尽量去除高分子杂质。
微专题:遗传系谱图与DNA电泳图谱问题分析电泳的原理:电泳是利用带电分子或离子所带电荷或分子量不同,在电场中移动距离(或速度)不同的原理分离分子或离子的方法,如等位基因A与a,经限制酶切开后,由于相关片段分子量等差异,在电场中移动距离不同,从而使两种基因得以分离。
【例题1】:对图1中1-4号个体进行基因检测,将含有该遗传病基因或正常基因的相关DNA片段各自用电泳法分离。
正常基因显示一个条带,患病基因显示为另一个不同的条带,结果如图2。
下列有关分析判断不正确是()A.图2中的编号c对应系谱图中的4号个体B.条带2的DNA片段含有该遗传病致病基因C.8号个体的基因型与3号个体的基因型相同的概率为2/3D.9号个体与该遗传病携带者结婚,孩子患病的概率为1/4【例题2】:(2010年·全国卷Ⅱ)人类白化病是常染色体隐性遗传病。
某患者家系的系谱图如图甲。
已知某种方法能够使正常基因A显示一个条带,白化基因a则显示为位置不同的另一个条带。
用该方法对上述家系中的每个个体进行分析,条带的有无及其位置表示为图乙。
根据上述实验结果,回答下列问题:(1)条带1代表_____基因。
个体2~5的基因型分别为_____、________、________和________。
(2)已知系谱图和图乙的实验结果都是正确的,根据遗传定律分析图甲和图乙,发现该家系中有一个体的条带表现与其父母的不符,该个体与其父母的编号分别是____________、________和________,产生这种结果的原因是__________________________________。
(3)仅根据图乙给出的个体基因型的信息,若不考虑突变因素,则个体9与一个家系外的白化病患者结婚,生出一个白化病子女的概率为________,其原因是____________。
【参考答案】:(1)A Aa AA AA aa(2)1034基因发生了突变(3)0个体9的基因型是AA,不可能生出aa个体【例题3】:(2015年·江苏盐城调研)神经性耳聋、腓骨肌萎缩症是两种单基因遗传病,分别由B、b 和D、d基因控制。
D N A电泳常见问题分析The final revision was on November 23, 2020
DNA电泳常见问题
凝胶电泳操作注意事项
1、琼脂糖:不同厂家、不同批号的琼脂糖,其杂质含量不同,影响DNA的迁移及荧光背景的强度,应有选择地使用。
2、凝胶的制备:凝胶中所加缓冲液应与电泳槽中的相一致,溶化的凝胶应及时倒入板中,避免倒入前凝固结块。
倒入板中的凝胶应避免出现气泡,以免影响电泳结果。
3、电泳缓冲液:为保持电泳所需的离子强度和pH,应经常更新电泳缓冲液。
4、
样品加入量:一般情况下,宽的梳子可加μg的DNA量,加样量的多少依据加样孔的大小及DNA中片段的数量和大小而定.当加样孔大时,样品上样量应相应加大,否则会造成条带浅甚至辨认不清;反之则应适当减少加样量,但是上样量过多会造成加样孔超载,从而导致拖尾或弥散,对于较大的DNA此现象更明显。
5、DNA样品中盐浓度会影响DNA的迁移率,平行对照样品应使用同样的缓冲条件以消除这种影响。
6、DNA迁移率取决于琼脂糖凝胶的浓度,迁移分子的形状及大小。
采用不同浓度的凝胶有可能分辩范围广泛的DNA分子,制备琼脂糖凝胶可根据DNA分子的范围来决定凝胶的浓度。
小片段DNA的检测应采用聚丙烯酰胺凝胶电泳,以提高分辨率。
7.选择的实验材料要新鲜,处理时间不易过长。
8.在加入细胞裂解缓冲液前,细胞必须均匀分散,以减少DNA团块形成。
9. 提取的DNA不易溶解:不纯,含杂质较多;加溶解液太少使浓度过大。
沉淀物太干燥,也将使溶解变得很困难。
10. 电泳检测时DNA成涂布状:操作不慎;污染核酸酶等。
11.分光光度分析DNA的A280/A260小于;不纯,含有蛋白质等杂质。
在这种情况下,应加入SDS至终浓度为%,并重复步骤2~8。
12.酚/氯仿/异戊醇抽提后,其上清液太黏不易吸取:含高浓度的DNA,可加大抽提前缓冲液的量或减少所取组织的量
DNA电泳常见问题分析之一
1 请问配制聚丙烯酰胺凝胶电泳胶时,促凝的是TEMED还是过硫酸铵胶聚时间很长如何解决
过硫酸铵提供驱动丙烯酰胺和双丙烯酰胺聚合所需的自由基,而TEMED通过催化过硫酸铵形成自由基而加速它俩的聚合。
胶聚合时间长可能是TEMED失效了,过硫酸铵固体时间过久也会失效的。
一个让PAGE胶很快聚合的方法:
不要先配AP(过硫酸铵)溶液,因为AP很容易变质。
在保证TEMED和AP质量的情况下,每次配胶时,直接称一定量的AP粉剂溶入液体状态的PAGE中,这样可以保证AP的催化能力,而且可以多加一点。
配25ml的PAGE胶,加克AP粉剂,最后加入25ulTEMED,20分钟左右就可以凝固(当然这个时候拔梳子,会有少量未凝固的PAGE在孔里形成丝状干扰,使加的样品看起来不太漂亮,但一般不影响跑胶效果和条带的形状和位置)。
2
DNA电泳的MARKER怎么是扭曲的
1、配制胶时的缓冲液需要和电泳缓冲液不是同时配制的.最好是同时配制.电泳时缓冲液高过液面1-2mm即可。
2、电泳时电压过高,可以在电泳前15分钟用较低电压(3V/cm),等条带出孔后比较漂亮了.然后再调电压。
3、上样时尽量慢慢加样,等样品自然沉降后再加电压。
3
跑出的DNA带模糊
1、 DNA降解:避免核酸酶污染。
2、电泳缓冲液陈旧:电泳缓冲液多次使用后,离子强度降低,pH值上升,缓冲能力减弱,从而影响电泳效果。
建议经常更换电泳缓冲液。
3、所用电泳条件不合适:电泳时电压不应超过20V/cm,温度<30℃;巨大DNA链电泳,温度应<15℃;核查所用电泳缓冲液是否有足够的缓冲能力。
4、 DNA上样量过多:减少凝胶中DNA上样量。
5、 DNA样含盐过高:电泳前通过乙醇沉淀去除过多的盐。
6、有蛋白污染:电泳前酚抽提去除蛋白。
7、 DNA变性:电泳前勿加热,用
20mM NaCl缓冲液稀释DNA。
4 有不规则DNA带迁移
1、对于λ/Hind III片段cos位点复性:电泳前于65℃加热DNA 5分钟,然后在冰上冷却5分钟。
2、电泳条件不合适:电泳电压不超过20V/cm;温度<30℃;经常更换电泳缓冲液。
3、 DNA变性:以20mM NaCl Buffer稀释DNA,电泳前勿加热。
5 跑出的DNA条带带弱或无DNA带
1、 DNA的上样量不够:增加DNA的上样量;聚丙烯酰胺凝胶电泳比琼脂糖电泳灵敏度稍高,上样量可适当降低。
2、 DNA降解:避免DNA的核酸酶污染。
3、 DNA走出凝胶:缩短电泳时间,降低电压,增强凝胶浓度。
4、对于EB染色的DNA,所用光源不合适应用短波长(254nm)的紫外光源。
6 跑出的DNA带缺失不完整是怎么回事
1、如果是小DNA带走出凝胶,可以缩短电泳时间或降低电压或增强凝胶浓度。
2、分子大小相近的DNA带不易分辨增加电泳时间,核准正确的凝胶浓度。
3、DNA 变性:电泳前请勿高温加热DNA链,以20mM NaCl Buffer稀释DNA。
DNA链巨大,常规凝胶电泳不合适在脉冲凝胶电泳上分析。
7 做PCR电泳后跑电泳,目的基因是489BP的,结果每次切胶回收后再跑电泳就变成500多了,快到600了为什么
有时只靠电泳结果判断是不准确的,同样的片段每次跑的远近会有不同。
有经验显示目的片段是1300多,结果就跑到1000的marker下面去了,后来证实片段没有问题。
也有做的一个片段也是这样,是490BP.理论上两个条带一样,可是PCR结果显示就是大小不一致。
然后回收以后的检测结果又全部都一样了,后来又拿去做了下一个测序,才知道根本没有问题。
8:为什么marker条带非常模糊,无法辨别具体条带
A:出现上述情况,可能有以下几个原因:
1. marker条带出现了降解。
请确保在使用过程中避免核酸酶污染;
2. 电泳缓冲液陈旧。
电泳缓冲液多次使用后,离子浓度降低,pH值上升,缓冲能力减弱,从而影响电泳效果,建议经常更换电泳缓冲液;
3. 电泳条件不合适。
电泳时电压应不超过
20V/cm,温度应低于30℃;4. marker上样量过多。
请根据说明书选用合适上样量;5. 凝胶质量不好。
建议使用质量较好的琼脂糖;此外,凝胶凝固不均匀也会导致条带模糊。
9:为什么marker条带出现不规则的条带(如哑铃状等)
A:出现上述情况,多与以下几个原因有关:1. 电泳缓冲液陈旧。
老化的电泳缓
冲液离子浓度降低,pH值上升,缓冲能力减弱,从而影响电泳效果,建议经常更换电泳
缓冲液;2. 电泳条件不合适。
电泳时电压应不超过20V/cm,电压太高可能也会导致marker条带出现不规则现象。
此外,凝胶质量差以及凝胶冷却时凝固不均匀也会导致该现象出现。
10为什么marker条带非常弱或者根本没有条带
A:出现上述情况可能是:1. marker上样量较低,可适当增加上样量;2. 凝胶质量较差或凝胶凝固不均匀也会导致电泳条带弱或根本没有条带;3. 电泳时间过长导致marker条带跑出凝胶,可缩短电泳时间,降低电压,增加凝胶浓度。
11:为什么marker缺带
A:对于含有较小片段的marker,如果出现缺带现象,可能是因为:
1. 小条带跑出凝胶或分子量大小非常相近的条带不易辨认所致,可适当缩短电泳时间,降低电压,同时增加凝胶浓度;
2. 凝胶中EB含量过低,导致大片段结合EB量太少或没有,在紫外光下亮度太低,可适当增加EB用量。