[理学]化学反应工程第五版课后答案
- 格式:doc
- 大小:4.32 MB
- 文档页数:120


第五章 化学平衡5-1.在某恒定的温度和压力下,取n 0﹦1mol 的A (g )进行如下化学反应:A (g )B (g )若0B μ﹦0A μ,试证明,当反应进度﹦0.5mol 时,系统的吉布斯函数G 值为最小,这时A ,B 间达到化学平衡。
解: 设反应进度为变量A (g )B (g )t ﹦0 n A , 0﹦n 0 0 0﹦0t ﹦t 平 n A n B﹦BBn ν n B ﹦B,n A ﹦n 0-n B ﹦n 0-B,n ﹦n A +n B ﹦n 0气体的组成为:y A ﹦A n n ﹦00B n n νξ-﹦01n ξ-,y B ﹦B nn﹦0n ξ各气体的分压为:p A ﹦py A ﹦0(1)p n ξ-,p B ﹦py B ﹦p n ξ各气体的化学势与的关系为:0000ln ln (1)A A AA p p RT RT p p n ξμμμ=+=+- 0000lnln B B B B p p RT RT p p n ξμμμ=+=+⋅ 由 G =n AA+n BB=(n A 0A μ+n B 0B μ)+00ln(1)A p n RT p n ξ-+00ln B p n RT p n ξ⋅ =[n 0-A μ+0B μ]+n 00lnpRT p +00()ln(1)n RT n ξξ--+0ln RT n ξξ 因为 0B μ﹦0A μ,则G =n 0(0A μ+0lnpRT p)+00()ln(1)n RT n ξξ--+0ln RT n ξξ ,0()ln T p G RT n ξξξ∂=∂- 20,20()()T p n RT Gn ξξξ∂=-∂-<0 令 ,()0T p Gξ∂=∂011n ξξξξ==-- ﹦0.5 此时系统的G 值最小。
5-2.已知四氧化二氮的分解反应 N 2O 4 (g ) 2 NO 2(g )在298.15 K 时,0r m G ∆=4.75kJ ·mol -1。
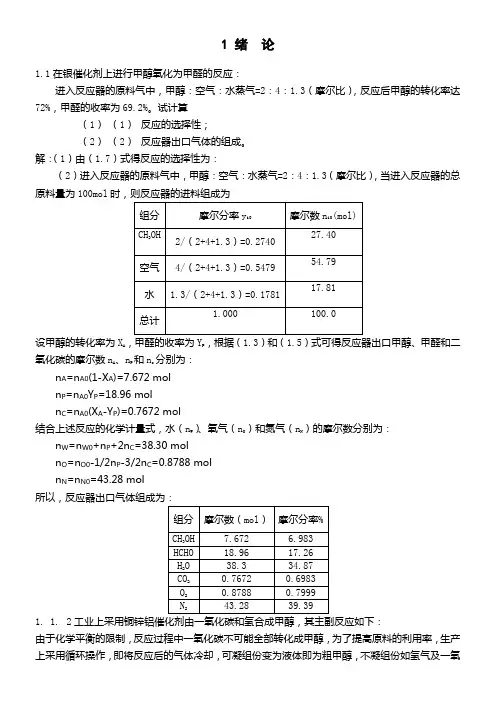
1 绪论1.1在银催化剂上进行甲醇氧化为甲醛的反应:进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1)(1)反应的选择性;(2)(2)反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),当进入反应器的总原料量为100mol设甲醇的转化率为X A,甲醛的收率为Y P,根据(1.3)和(1.5)式可得反应器出口甲醇、甲醛和二氧化碳的摩尔数n A、n P和n c分别为:n A=n A0(1-X A)=7.672 moln P=n A0Y P=18.96 moln C=n A0(X A-Y P)=0.7672 mol结合上述反应的化学计量式,水(n W)、氧气(n O)和氮气(n N)的摩尔数分别为:n W=n W0+n P+2n C=38.30 moln O=n O0-1/2n P-3/2n C=0.8788 moln N=n N0=43.28 mol所以,反应器出口气体组成为:1. 1.2工业上采用铜锌铝催化剂由一氧化碳和氢合成甲醇,其主副反应如下:由于化学平衡的限制,反应过程中一氧化碳不可能全部转化成甲醇,为了提高原料的利用率,生产上采用循环操作,即将反应后的气体冷却,可凝组份变为液体即为粗甲醇,不凝组份如氢气及一氧化碳等部分放空,大部分经循环压缩机后与原料气混合返回合成塔中。
下图是生产流程示意图原料气Bkg/h 粗甲醇Akmol/h100kmol 放空气体原料气和冷凝分离后的气体组成如下:(mol )组分 原料气 冷凝分离后的气体 CO 26.82 15.49 H 2 68.25 69.78 CO 2 1.46 0.82 CH 4 0.55 3.62 N 22.9210.29粗甲醇的组成为CH 3OH 89.15%,(CH 3)2O 3.55%,C 3H 9OH 1.10%,H 2O 6.20%,均为重量百分率。

![[理学]化学反应工程第五版课后答案](https://uimg.taocdn.com/5058eec2f7ec4afe05a1df2e.webp)
1 绪 论1.1在银催化剂上进行甲醇氧化为甲醛的反应:3222CH OH O 2HCHO 2H O +→+ 32222CH OH 3O 2CO 4H O +→+进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1) (1) 反应的选择性;(2) (2) 反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:0.629Y S 0.961196.11%X 0.720====(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),A P 出口甲醇、甲醛和二氧化碳的摩尔数n A 、n P 和n c 分别为:n A =n A0(1-X A )=7.672 mol n P =n A0Y P =18.96 moln C =n A0(X A -Y P )=0.7672 mol结合上述反应的化学计量式,水(n W )、氧气(n O )和氮气(n N )的摩尔数分别为:n W =n W0+n P +2n C =38.30 mol n O =n O0-1/2n P -3/2n C =0.8788 mol n N =n N0=43.28 mol1. 1. 2工业上采用铜锌铝催化剂由一氧化碳和氢合成甲醇,其主副反应如下:23CO 2H CH OH +⇔23222CO 4H (CH )O H O +⇔+ 242CO 3H CH H O +⇔+24924CO 8H C H OH 3H O +⇔+222CO H O CO H +⇔+由于化学平衡的限制,反应过程中一氧化碳不可能全部转化成甲醇,为了提高原料的利用率,生产上采用循环操作,即将反应后的气体冷却,可凝组份变为液体即为粗甲醇,不凝组份如氢气及一氧化碳等部分放空,大部分经循环压缩Bkg/h 粗甲醇100kmol 放空气体原料气和冷凝分离后的气体组成如下:(mol )组分 原料气 冷凝分离后的气体 CO 26.82 15.49 H 2 68.25 69.78 CO 2 1.46 0.82 CH 4 0.55 3.62 N 2 2.92 10.29粗甲醇的组成为CH 3OH 89.15%,(CH 3)2O 3.55%,C 3H 9OH 1.10%,H 2O 6.20%,均为重量百分率。

化学反应工程习题解答-第五版化学反应工程习题解答-第五版1.问题:对于以下反应方程式,请计算反应的平衡常数Kc值: 2A + 3B ⇌ C解答:反应的平衡常数Kc可以通过计算反应物和生成物的浓度之比得到。
根据方程式,反应物A和B的摩尔比为2:3,生成物C的摩尔比为1。
设反应物A和B的初始浓度分别为[A]0和[B]0,生成物C的初始浓度为[C]0。
在平衡状态下,反应物和生成物的浓度变化量为x,可以得到以下方程式: [A]0 - x = 2x [B]0 - 3x = 3x [C]0 + x = x解方程得到x = [A]0/5 = [B]0/10 = [C]0/11根据Kc定义,Kc = ([C]/[A]^2[B]^3) = (x/[A]0)^2 * (x/[B]0)^3 = ([A]0/5)^2 * ([A]0/10)^3 = [A]0^5/5000因此,反应的平衡常数Kc为[A]0^5/5000。
2.问题:对于以下反应方程式,请计算反应的平衡常数Kp值: 2A + B ⇌ 3C解答:反应的平衡常数Kp可以通过计算反应物和生成物的压力之比得到。
假设反应物A和B的初始压力分别为PA0和PB0,生成物C的初始压力为PC0。
在平衡状态下,反应物和生成物的压力变化量为x,可以得到以下方程式: PA0 - x = 2x PB0 - x = x PC0 + 3x = x解方程得到x = PA0/5 = PB0/3 = PC0/4根据Kp定义,Kp = (PC/PA^2PB) = (x/PA0)^3 * (x/PB0) = (PA0/5)^3 * (PA0/3) = PA0^4/375因此,反应的平衡常数Kp为PA0^4/375。
3.问题:在一定温度下,对于以下反应方程式,请计算反应的平衡常数Kc值: A + B ⇌ C + D已知在反应物和生成物的浓度分别为[A]0、[B]0、[C]0和[D]0的情况下,反应达到平衡时,反应物和生成物的浓度分别为[A]、[B]、[C]和[D]。

化学反应工程第五版答案【篇一:化学反应工程第一章习题参考答案】txt>1-1 在银催化剂上进行甲醇氧化为甲醛的反应:进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算:(1)反应的选择性;(2)反应器出口气体的组成解一:(1)由(1-17)式得反应的选择性为:s???0.9611?96.11%x0.720(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),当进入反应器的总原料量为设甲醇的转化率为ap醛和二氧化碳的摩尔数na、np和nc分别为: na=na0(1-xa)=7.672 molnp=na0yp=18.96 molnc=na0(xa-yp)=0.7672 mol结合上述反应的化学计量式,水(nw)、氧气(no)和氮气(nn)的摩尔数分别为:nw=nw0+np+2nc=38.30 molno=no0-1/2np-3/2nc=0.8788 molnn=nn0=43.28 mol解二:(1)根据定义:目的产物收率目的产物选择率y=消耗于主产物l上的关键组分a的量进入反应系统的a的初始量 s=消耗于主产物l上的关键组分a的量转化了的关键组分a的量反应物的转化率 xa=转化了的关键组分a的量进入反应系统的a的初始量转化率、收率和选择率的关系y=xas已知:xch3oh= 72%yhcho = 69.2%s?则yhchoxch3oh?69.2%72%?96.11%(2)为方便计算,设进入反应器的甲醇的物质的量为2mol,则即反应后混合气体中:nch3oh = 2*(1-72%) =0.56molnhcho = 2*69.2%=1.384molnh2o =1.3+2*69.2%+2*(72%-69.2%)*4/2=2.796molnco2 = 2*(72%-69.2%)=0.056moln空气 = 4-2*69.2%*1/2-2*(72%-69.2%)*3/2=3.224mol(其中no2 = 4*21%-2*69.2%*1/2-2*(72%-69.2%)*3/2=0.064molnn2 = 4*79%=3.16mol)总物质的量为:nt = 0.56+3.224+1.384+2.796+0.056=8.02mol各组分组成为:ych3oh=0.56/8.02*100%=6.98%y空气= 3.224/8.02*100%=40.20%(其中yo2=0.80%,yn2=39.4%) yhcho=1.384/8.02*100%=17.26%yh2o=2.796/8.02*100%=34.86%yco2 = 0.056/8.02*100%=0.70%解:(1)?dnadna?kvrfa;??kwfa; dvrdwvr??b??bdvr?dw??dnadna????bkwfa dwdvr?b或者vr?sissdndna?p?w?i?pdvr?dw??a???i?p?kwfa dwsvsvdvrsvsi?psv即kvrsgsi??b?kw??p?kw?kw或 svsivr?sisdnadnasi?w?idvr?dw??????kwfa dwsgsgdvrsgsisgkvrsgsi??b?kw??p?kw?kw svsi(2)?dna?kwfa?kffa dw?kdnap?kcca?kca?cpa?kppa dwrgtrgtdnapyap?kcca?kc?kcya?kyya dwrgtrgt?对于理想气体,f接近于p,所以有kc?rgt?kp?rgt?kf?rgt?kw?rgtp?ky?dna?kwfa?kffa?kf?apa dwrgtp?ky kc?rgt?kp?rgt?kf?rgt?a?kw?1-6 有如下平行反应,0p为目的产物,各反应均为一级不可逆放热反应,反应活化能依次为e2e1e3,kj为j反应的指前因子,证明最佳温度top?e3?e2 k30(e3?e1)rln0k2(e1?e2)k1?k10e证明:?e1rte2rtncancanca0k2?k2e?k3?k30e因n相同,所以p的选择率 e?3rts??rprp?rs?rt1 1?s?trprp10k2k30(e1?e3)/rt(e1?e2)/rt1?0e?0ek1k1?令ds?0 dt所以0k30(e1?e3)/rtk2(e1?e2)/rtd(1?0e?0e)0k1k1k2e1?e2(e1?e2)/rtk3 0e1?e3(e1?e3)/rt???0e?0e?022dtk1rtk1rt1d()ds??dtdt0k2e1?e2(e1?e2)/rtk30e3?e1(e1?e3)/rte?0e整理,得022k1rtk1rtk30e3?e1e(e1?e2)/rt?0 (e1?e3)/rtk2e1?e2et?即ope3?e2k30(e3?e1) rln0k2(e1?e2)【篇二:化学反应工程作业答案】解: a?b?c?dra?k?c设a的转化率为xa,b的转化率为xb a?cbxa?na0?na??nanb0?nb??nb??xb? na0na0nb0nb0∵na0?nb0 , ?na??nb ,∴ca?cb xaft=ca0?0dxa=ca0raxaf?011dxak=-=169.6 min2kc(1?x)ck?caa0afa0t与反应体积无关。


第五章 化学平衡5-1.在某恒定的温度和压力下,取n 0﹦1mol 的A (g )进行如下化学反应:A (g )垐?噲? B (g ) 若0B μ﹦0A μ,试证明,当反应进度﹦时,系统的吉布斯函数G 值为最小,这时A ,B 间达到化学平衡。
解: 设反应进度为变量A (g )垐?噲?B (g )t ﹦0 n A , 0﹦n 0 0 0﹦0 t ﹦t 平 n A n B ﹦BBn ν n B ﹦B ,n A ﹦n 0-n B ﹦n 0-B ,n ﹦n A +n B ﹦n 0气体的组成为:y A ﹦A n n ﹦00B n n νξ-﹦01n ξ-,y B ﹦B nn﹦0n ξ各气体的分压为:p A ﹦py A ﹦0(1)p n ξ-,p B ﹦py B ﹦p n ξ各气体的化学势与的关系为:0000ln ln (1)A A AA p p RT RT p p n ξμμμ=+=+- 0000lnln B B B B p p RT RT p p n ξμμμ=+=+⋅ 由 G =n AA +n BB =(n A 0A μ+n B 0B μ)+00ln(1)A p n RT p n ξ-+00ln B p n RT p n ξ⋅ =[n 0-0A μ+0B μ]+n 00lnpRT p +00()ln(1)n RT n ξξ--+0ln RT n ξξ 因为 0B μ﹦0A μ,则G =n 0(0A μ+0lnpRT p)+00()ln(1)n RT n ξξ--+0ln RT n ξξ ,0()ln T p G RT n ξξξ∂=∂- 20,20()()T p n RT Gn ξξξ∂=-∂-<0 令 ,()0T p Gξ∂=∂011n ξξξξ==-- ﹦ 此时系统的G 值最小。
5-2.已知四氧化二氮的分解反应 N 2O 4 (g )垐?噲? 2 NO 2(g )在 K 时,0r m G ∆=·mol -1。


化学反应工程习题(第五章)5.1乙炔与氯化氢在HgCl 2-活性炭催化剂上合成氯乙烯的反应2223C H HCl C H Cl+↔ ()A ()B ()C 其动力学方程式可有如下种种形式:(1)2(/)/(1)A B C A A B B C C r p p p K K p K p K p κ=-+++ (2)/(1)(1)A B A B B B C C A A r K K p p K p K p K p κ=+++ (3)/(1)A AB A A B B r K p p K p K p κ=++ (4)/(1)B A B B BC C r K p p K p K p κ=++试说明各式所代表的反应机理和控制步骤。
解:(1)A A σσ+↔B B σσ+↔ (控制步骤)A B C σσσσ+↔+C C σσ↔+(2)11A A σσ+↔(控制步骤)22122111B B A BC C C σσσσσσσσ+↔+→+↔+(3)A A σσ+↔B B σσ+↔(控制步骤)A B C σσ+→+(4) B B σσ+↔ (控制步骤)A B C σσ+→ C C σσ↔+5.2 在Pd-Al 2O 3催化剂上用乙烯合成醋酸乙烯的反应为243222321C H CH COOH O CH COOC H H O2++↔+ 实验测得的初速率数据如下[功刀等,化工志,71,2007(1968).]115℃, ,。
AcOH 200p mmHg =292O p mmHg =24()C H p mmHg701001952473154655010(/)r mol hr g ⨯⋅催化剂 3.94.46.06.67.255.4注:1mmHg=133.322Pa如反应机理设想为2424242422423223232222O ()O O+AcOH AcOH C H C H AcOH C H HC H OAc O O HC H OAc O C H OAc H C H OAc C H OAc H H σσσσσσσσσσσσσσσσ+↔+↔+↔++↔+→+↔+↔控制步骤试写出反应速率并检验上述部分数据能与之符合否。
1 绪 论1.1在银催化剂上进行甲醇氧化为甲醛的反应:3222CH OH O 2HCHO 2H O +→+32222CH OH 3O 2CO 4H O +→+进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1) (1) 反应的选择性;(2) (2) 反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:0.629Y S 0.961196.11%X 0.720====(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),A P 出口甲醇、甲醛和二氧化碳的摩尔数n A 、n P 和n c 分别为:n A =n A0(1-X A )=7.672 mol n P =n A0Y P =18.96 moln C =n A0(X A -Y P )=0.7672 mol结合上述反应的化学计量式,水(n W )、氧气(n O )和氮气(n N )的摩尔数分别为:n W =n W0+n P +2n C =38.30 mol n O =n O0-1/2n P -3/2n C =0.8788 mol n N =n N0=43.28 mol1. 1. 2工业上采用铜锌铝催化剂由一氧化碳和氢合成甲醇,其主副反应如下:23CO 2H CH OH +⇔23222CO 4H (CH )O H O +⇔+ 242CO 3H CH H O +⇔+24924CO 8H C H OH 3H O +⇔+222CO H O CO H +⇔+由于化学平衡的限制,反应过程中一氧化碳不可能全部转化成甲醇,为了提高原料的利用率,生产上采用循环操作,即将反应后的气体冷却,可凝组份变为液体即为粗甲醇,不凝组份如氢气及一氧化碳等部分放空,大部分经循环压缩Bkg/h 粗甲醇100kmol 放空气体原料气和冷凝分离后的气体组成如下:(mol )组分 原料气 冷凝分离后的气体 CO 26.82 15.49 H 2 68.25 69.78 CO 2 1.46 0.82 CH 4 0.55 3.62 N 2 2.92 10.29粗甲醇的组成为CH 3OH 89.15%,(CH 3)2O 3.55%,C 3H 9OH 1.10%,H 2O 6.20%,均为重量百分率。
化学反应⼯程习题解答第五版习题1-1:银催化剂上进⾏甲醇氧化为甲醛的反应:2CH3OH+O2→2HCHO+2H2O2CH3OH+3O2→2CO2+4H2O进⼊反应器的原料中,甲醇:空⽓:⽔蒸⽓=2:4:1.3。
反应后甲醇转化率为72%,甲醛的收率为69.2%。
试计算:(1)选择率;(2)出⼝组成。
解:(1)69.2%96.1%72%YSx===(2)设原料中甲醇、空⽓、⽔蒸⽓的物质的量分别是2mol、4mol和1.3mol. 则⽣成甲醛所耗的甲醇的物质的量为2×0.692=1.384mol副反应消耗的甲醇为:2×0.72-1.384=0.056mol由反应计量⽅程式可知:n(H2O)=1.3+1.384+2×0.056=2.796(mol)n(CO2)=0.056mol ;n(HCHO)=1.384moln(CH3OH)=2×(1-0.72)=0.56(mol)n(O2)=4×0.21-1.384×0.5-0.056×1.5=0.064(mol)n(N2等)=4×0.79=3.16(mol)则总的物质量为n= 0.56+0.064+1.384+2.796+0.056+3.16=8.02(mol)y(CH3OH) =0.56/8.02=6.98%y(O2) =0.064/8.02=0.80%y(HCHO) =1.384/8.02=17.26%y(H2O) =2.796/8.02=34.86%y(CO2) =0.056/8.02=0.70%y(N2) = 3.16/8.02=39.40%习题1—6:丁烯制丁⼆烯48462C H C H H +,已知反应的步骤为4848484624646()()()()()()()()()A C H C HC H C H H C C H C H +++ (1)请分别导出(A )(C )为控制步骤的均匀吸附动⼒学⽅程。
1 绪 论1.1在银催化剂上进行甲醇氧化为甲醛的反应:3222CH OH O 2HCHO 2H O +→+ 32222CH OH 3O 2CO 4H O +→+进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),反应后甲醇的转化率达72%,甲醛的收率为69.2%。
试计算(1) (1) 反应的选择性;(2) (2) 反应器出口气体的组成。
解:(1)由(1.7)式得反应的选择性为:0.629Y S 0.961196.11%X 0.720====(2)进入反应器的原料气中,甲醇:空气:水蒸气=2:4:1.3(摩尔比),A P 出口甲醇、甲醛和二氧化碳的摩尔数n A 、n P 和n c 分别为:n A =n A0(1-X A )=7.672 mol n P =n A0Y P =18.96 moln C =n A0(X A -Y P )=0.7672 mol结合上述反应的化学计量式,水(n W )、氧气(n O )和氮气(n N )的摩尔数分别为:n W =n W0+n P +2n C =38.30 mol n O =n O0-1/2n P -3/2n C =0.8788 mol n N =n N0=43.28 mol1. 1. 2工业上采用铜锌铝催化剂由一氧化碳和氢合成甲醇,其主副反应如下:23CO 2H CH OH +⇔23222CO 4H (CH )O H O +⇔+ 242CO 3H CH H O +⇔+24924CO 8H C H OH 3H O +⇔+222CO H O CO H +⇔+由于化学平衡的限制,反应过程中一氧化碳不可能全部转化成甲醇,为了提高原料的利用率,生产上采用循环操作,即将反应后的气体冷却,可凝组份变为液体即为粗甲醇,不凝组份如氢气及一氧化碳等部分放空,大部分经循环压缩Bkg/h 粗甲醇100kmol 放空气体原料气和冷凝分离后的气体组成如下:(mol )组分 原料气 冷凝分离后的气体 CO 26.82 15.49 H 2 68.25 69.78 CO 2 1.46 0.82 CH 4 0.55 3.62 N 2 2.92 10.29粗甲醇的组成为CH 3OH 89.15%,(CH 3)2O 3.55%,C 3H 9OH 1.10%,H 2O 6.20%,均为重量百分率。
在操作压力及温度下,其余组分均为不凝组分,但在冷凝冷却过程中可部分溶解于粗甲醇中,对1kg 粗甲醇而言,其溶解量为CO 2 9.82g,CO 9.38g,H 2 1.76g,CH 4 2.14g,N 25.38g 。
若循环气与原料气之比为7.2(摩尔比),试计算:(1) (1) 一氧化碳的单程转换率和全程转化率; (2) (2) 甲醇的单程收率和全程收率。
解:(1)设新鲜原料气进料流量为100kmol/h ,则根据已知条件,计算进料原料其中x i =y i i i i m i iM ’m =∑y i M i =9.554又设放空气体流量为Akmol/h ,粗甲醇的流量为Bkg/h 。
对整个系统的N 2作衡算得:5.38B/28×1000+0.1029A=2.92 (A) 对整个系统就所有物料作衡算得:100×10.42=B+9.554A (B) 联立(A )、(B )两个方程,解之得A=26.91kmol/h B=785.2kg/h 反应后产物中CO 摩尔流量为F CO =0.1549A+9.38B/(28×1000) 将求得的A 、B 值代入得F CO =4.431 kmol/h 故CO 的全程转化率为CO,0CO COCO,0F F 26.82 4.435X 83.48%F 26.82--===由已知循环气与新鲜气之摩尔比,可得反应器出口处的CO 摩尔流量为F ’CO,0=100×0.2682+7.2×100×0.1549=138.4 kmol/h 所以CO 的单程转化率为CO,0CO 'COCO,0F F 26.82 4.435X 16.18%F 138.4--===产物粗甲醇所溶解的CO 2、CO 、H 2、CH 4和N 2总量D 为(9.829.38 1.76 2.14 5.38)BD 0.02848Bkmol /h1000++++==粗甲醇中甲醇的量为(B-D)X 甲/M m =(785.2-0.02848B) ×0.8915/32=21.25 kmol/h 所以,甲醇的全程收率为Y 总=21.25/26.82=79.24% 甲醇的单程收率为Y 单=21.25/138.4=15.36%2 反应动力学基础2.1在一体积为4L 的恒容反应器中进行A 的水解反应,反应前 A 的含量为12.23%(重量),混合物的密度为1g/mL ,反应物A 的分子量为88。
在等温常压解:利用反应时间与组分A 的浓度变化数据,作出C A ~t 的关系曲线,用镜面法求得t=3.5h 时该点的切线,即为水解速率。
切线的斜率为0.760.125/.6.1α-==-mol l h由(2.6)式可知反应物的水解速率为0.125/.-==dC A r mol l hAdt2.2在一管式反应器中常压300℃等温下进行甲烷化反应:2423+→+CO H CH H O催化剂体积为10ml ,原料气中CO 的含量为3%,其余为N 2,H 2气体,改变进口原料气流量Q 0解:是一个流动反应器,其反应速率式可用(2.7)式来表示00000(1)(1)-==-=-=-A A RA A A A A A A AdF r dV F F X Q C X dF Q C dX故反应速率可表示为:000(/)==A AA A A R R dX dX r Q C C dV d V Q用X A ~V R /Q 0作图,过V R /Q 0=0.20min 的点作切线,即得该条件下的dX A /d(V R /Q 0)值α。
0.650.04 1.790.34α-==故CO 的转化速率为40030.10130.03 6.3810/8.31410573--⨯===⨯⨯⨯A A P C mol l RT4300 6.3810 1.79 1.1410/.min(/)--==⨯⨯=⨯AA A R dX r C mol l d V Q2.3已知在Fe-Mg 催化剂上水煤气变换反应的正反应动力学方程为: 20.850.4/-=⋅w CO CO r k y y kmol kg h式中y CO 和y CO2为一氧化碳及二氧化碳的瞬间摩尔分率,0.1MPa 压力及700K 时反应速率常数k W 等于0.0535kmol/kg.h 。
如催化剂的比表面积为30m 2/g ,堆密度为1.13g/cm 3,试计算:(1) (1) 以反应体积为基准的速率常数k V 。
(2) (2) 以反应相界面积为基准的速率常数k g 。
(3) (3) 以分压表示反应物系组成时的速率常数k g 。
(4) (4) 以摩尔浓度表示反应物系组成时的速率常数k C 。
解:利用(2.10)式及(2.28)式可求得问题的解。
注意题中所给比表面的单位换算成m 2/m 3。
33230.450.45330.45(1) 1.13100.053560.46/.6(2) 1.7810/.301011(3)()()0.05350.15080.1013..()8.3110700(4)()(0.05350.333(0.1)ρρρρ-==⨯⨯=-===⨯⨯⨯==⨯=⨯⨯==⨯=v b w bbg w wvb n p w nc w k k kmol m h k k k kmol m h a kmol k k P kg h MPa m RT k k P km 0.45)().kmol ol kg h2.4在等温下进行液相反应A+B →C+D ,在该条件下的反应速率方程为:1.50.50.8/min =⋅A A B r C C mol l若将A 和B 的初始浓度均为3mol/l 的原料混合进行反应,求反应4min 时A 的转化率。
解:由题中条件知是个等容反应过程,且A 和B 的初始浓度均相等,即为1.5mol/l ,故可把反应速率式简化,得1.50.522200.80.80.8(1)===-A A B A A A r C C C C X由(2.6)式可知00(1)⎡⎤⎢⎥⎣⎦--==-=A A A A A A d C X dC dX r C dt dt dt代入速率方程式2200.8(1)=-A A A A dX C C X dt化简整理得00.8(1)=-AA A dX C dtX积分得00.81=-AA A X C t X解得X A =82.76%。
2.5氨合成塔入口的气体组成为3.5%NH 3,20.8%N 2,62.6%H 2,7.08%Ar 及5.89CH 4。
该塔是在30MPa 压力下操作。
已知催化剂床层中某处的温度为490℃,反应气体中氨含量为10%(mol ),试计算该处的反应速率。
在Fe 催化剂上氨合成反应速率式为:322321.531.512/=-⋅NH H N NH H pp r k p k kmol m h p p 逆反应的活化能417.5810/=⨯su E J mol 。
450℃时30.5322277()/=⋅k m MPa m h ,且212/=Pk k K ,490℃时,Kp 可按下式计算:472log 2047.8/ 2.4943log 1.25610 1.856410 3.206--=--⨯+⨯+p K T T T T 注:m 3为标准立方米。
解:题中给出450℃时的k 2值,而反应是在490℃下,故首先要求出490℃时的k 2值。
利用(2.27)试,求出频率因子A:44217.5810/8.314723162'1617.5810/8.314723430.532exp()exp()2277/ 1.14510exp() 1.14510 1.05510()/.-⨯⨯-⨯⨯-=-===⨯-==⨯=⨯sususuE k A RT E A k e RT E k A e m MPa m hRT490℃的Kp 值由题给公式计算出4722log 2047.8/763 2.4943log763 1.25610763 1.8564107633.206 1.25245.59210 ---=--⨯⨯+⨯⨯+=-=⨯p p K K 求k 1值:22'112'22243 1.531(5.59210) 1.0551033()/.--===⨯⨯⨯=p p k K k K k k k m MPa m h求各组分的分压值:2233122+↔N H NH5716.0.14160*(-2)*2087.01.14160*2087.0*3-626.0 1y 13y y 1904.0 .14160*(-2)*2087.01)1416.0-(12087.0 1y y y 1416.05.6914.45*(-2)*2087.01*2087.0*211035.010.01y y y 22123211 %87.20Py , 1y y y 1000H H 000A A 00R 0R R 0000000==-)+-(=,+=δ+-==+=δ+-===+--=δ+νν-=δ==δ+νν-=δ+νν-=AA A AA AA A AA A A AA AA A AA AA A i i AA A A A Aii i AA A A A Aii i X y X X y X X X X X X y X y p X y X X y X p p p P y i i p =反应速率为:3 22321.5 1.541.512 1.5333317.15333.0 5.718 1.05510317.154.02310/.(179.6/.)=-=⨯⨯-⨯⨯=⨯NHHNNH Hppr k p kp pm m cat h kmol m cat h2.6下面是两个反应的T-X图,图中AB是平衡曲线,NP是最佳温度曲线,AM是等温线,HB是等转化率线。