高中化学奥林匹克竞赛辅导讲座 第9讲 络合物(配位化合物)化学基础-典型例题与知能训练
- 格式:doc
- 大小:234.00 KB
- 文档页数:10

高中化学奥林匹克竞赛辅导配合物(配位化合物)化学基础【竞赛要求】配位键。
常见的配合物的中心离子(原子)和常见的配体(水、羟离子、卤离子、拟卤离子、氨分子、酸根离子、不饱和烃等)。
螯合物及螯合效应。
常见的络合剂及常见的配合反应。
定性说明配合反应与酸碱反应、沉淀反应、氧化还原反应的联系。
配合物几何构型和异构现象的基本概念。
配合物的杂化轨道理论。
八面体配合物的晶体场理论。
Ti(H2O)6的颜色。
路易斯酸碱的概念。
1.配合物:由中心离子(或原子)和几个配体分子(或离子)以配位键相结合而形成的复杂分子络合物。
如[Co(NH3)6]3+、[Cr(CN)6]3–、Ni(CO)4都是配位单元,分别称作配阳离子、配阴离子、配分子。
判断物质是配合物的关键在于物质是否含有配位单元。
配合物和复盐的区别:前者一定含有配位键,后者没有配位键,如KCl·MgCl2·6H2O是复盐,不是配合物。
2.配合物的组成:为外界,内外界(1)配合物的内界和外界:以[Cu(NH3)4]SO4为例,[Cu(NH3)4]2+为内界,SO-24之间是完全电离的。
内界是配位单元,外界是简单离子。
又如K3[Cr(CN)6]之中,内界是[Cr(CN)6]3–,外界是K+。
配合物可以无外界,但不能没有内界,如Ni(CO)4。
(2)中心离子(原子)和配位体:a.中心离子(原子):又称配合物的形成体或中心体,多为过渡金属离子,如Fe3+、Fe2+、Co2+、Ni2+、Cu2+,也有电中性的原子为配合物的中心原子,如Ni(CO)4、Fe(CO)5中的Ni和Fe都是电中性的原子。
只要能提供接纳孤对电子的空轨道的离子或原子均可作中心体。
b.配位体:含有孤对电子的阴离子或分子。
如NH3、Cl—、CN—等。
配位体中直接同中心原子配合的原子,叫做配位原子。
如[Cu(NH3)4]2+配阳离子中,NH3是配位体,其中N原于是配位原子。
配位原子经常是含有孤对电子的原子。

高中化学竞赛专题辅导(四)配位化学(含解析)一.(12分)配位化合物A是单核配合物分子,由11个原子组成;微热后失重11.35%得到B;B进一步加热又失重26.66%(相对B)得到金属C;B极难溶于水,不溶于乙醇、乙醚,能溶于盐酸。
A有2种异构体A1、A2,其中A2能与草酸盐反应得到一种式量比A略大的配合物分子D(A1无相似反应)1.写出A、B、C的化学式;2.写出B溶于盐酸后产物的名称;3.试画出A1、A2、D的结构,并比较A1、A2在水中溶解性的大小。
4.A还有若干种实验式相同的离子化合物。
它们每个还满足如下条件:是由分立的、单核的离子配合物实体构成的;仅含1种阳离子和1种阴离子。
(1)符合上述条件的离子化合物的精确的分子式有多少种。
(2)其中1种与AgNO3反应(摩尔比1︰2)得到两种组成不同的配合物,写出反应的化学方程式。
二.(7分)某Ⅷ族不活泼金属A溶于足量的王水生成B的溶液(A的含量为47.60%);将SO2通入B的溶液中,得到C的溶液(A的含量为57.56%)。
已知B、C的组成元素完全相同,且阴离子所带电荷也相同。
1.通过计算推理,确定A的元素符号;2.写出所涉及反应的化学方程式。
3.画出B、C阴离子的空间构型。
三.(11分)太阳能发电和阳光分解水制氮,是清洁能源研究的主攻方向,研究工作之一集中在n-型半导体光电化学电池方面。
下图是n-型半导体光电化学电池光解水制氢的基本原理示意图,图中的半导体导带(未充填电子的分子轨道构成的能级最低的能带)与价带(已充填价电子的分子轨道构成的能级最高的能带)之间的能量差ΔE(=E c-E v)称为带隙,图中的e-为电子、h+为空穴。
瑞士科学家最近发明了一种基于上图所示原理的廉价光电化学电池装置,其半导体电极由2个光系统串联而成。
系统一由吸收蓝色光的WO3纳米晶薄膜构成;系统二吸收绿色和红色光,由染料敏化的TiO2纳米晶薄膜构成。
在光照下,系统一的电子(e-)由价带跃迁到导带后,转移到系统二的价带,再跃迁到系统二的导带,然后流向对电极。


促敦市安顿阳光实验学校配位化合物1. 熟悉配位化合物的基本概念、组成和命名;2. 熟悉配位化合物的价键理论,会进行一般配离子结构判断和磁性计算;理解晶体场理论的要点,弄清八面体场、四面体场面四边形场中 d轨道的分裂;理解分裂能和晶体场稳化能概念;4. 了解配位化合物顺反异构和旋光异构概念,初步上述两种异构体的判断;5. 熟悉配位实体热力学稳性中的有关概念。
7.1维尔纳学说的要点:●大多数化学元素表现出两种类的化合价,即主价和副价;●元素形成配合物时倾向于主价和副价都能得到满足;●元素的副价指向空间确的方向。
一.配位实体和络合物需要强调配位实体所带的电荷时,也可将其叫作络离子(Complex ion)。
这就是说,“络合物”和“络离子”都是“配位实体”的同义。
二.配位化合物配位化合物(Coordination compound) 指包含配位实体在内的整个化合物。
中心离子或原子:正离子(多)金属元素(多)中性原子(少)非金属元素(少)三.配位体和配位原子与中心原子结合的分子或离子(如例中的NH3分子、CO分子和CN-离子)叫做配位体(Ligand), 配位体中与中心原子直接键合的原子叫配位原子(如配位体NH3中的N原子,配位体CN-和CO中C原子)。
配位体又因含有的配位原子数目不同分为单齿配位体 (Monodentate ligand) 和多齿配位体 (Polydentate ligand) 。
四.配位数与中心离子(或原子)成键的配位原子的总数五.螯合物和金属大环配合物螯合物(Chelate)是多齿配位体以2个或2个以上配位原子配位于金属原子而形成的一种环状络合物 (环中包含了金属原子)。
能用作多齿配体的试剂叫螯合剂(Chelating agent)。
六.化学式的书写和配合物的命名命名原则:按照无机专业会制的规则命名;●含络离子的配合物:阴离子名称在前,阳离子名称在后,阴、阳离子名称之间加“化”字或“酸”字。

⾼中化学奥林匹克竞赛专题九络合物(配位化合物)化学基础练习专题九络合物(配位化合物)化学基础学号姓名得分1、填写下表空⽩处。
235235为_______________________________ 和 _______________________________________。
3、CuCl2溶液有时呈黄⾊,有时呈黄绿⾊或蓝⾊,这是因为在CuCl2的⽔溶液中存在如下平衡:[Cu(H 2O)4]2+(蓝⾊)+ 4Cl- [CuCl4]2-(黄⾊)+ 4H2O现欲使溶液由黄⾊变成黄绿⾊或蓝⾊,请写出两种可采⽤的⽅法:①,②。
4、已知铁的原⼦序数为26,则Fe2+在⼋⾯体场中的晶体场稳定化能(以△0 =10 Dq表⽰)在弱场中是_____________ Dq,在强场中是______________ Dq。
5、已知:配位化合物 [Co(NH3)4Cl2] 有两种异构体。
试判断其空间体构型是⼋⾯体型还是三棱柱型?6、今有化学式为Co(NH3)4BrCO3的配合物。
(1)画出全部异构体的⽴体结构。
(2)指出区分它们的实验⽅法。
7、下列结构中哪些是①⼏何异构体②光学异构体③完全相同的结构①②③④⑤⑥⑦⑧8、A、B、C为三种不同的配合物,它们的化学式都是CrCl3·6H2O,但颜⾊不同:A呈亮绿⾊,跟AgNO3溶液反应,有2/3的氯元素沉淀析出;B呈暗绿⾊,能沉淀1/3的氯;⽽C呈紫⾊,可沉淀出全部氯元素。
则它们的结构简式分别为:A ,B ,C 。
这三种配离⼦的空间构型为⾯体,其中某配离⼦中的2个Cl可能有两种排列⽅式,称为顺式和反式。
它们的结构图分别为:______ _和。
9、根据下列配离⼦的磁矩推断中⼼离⼦的杂化轨道类型和配离⼦的空间构型。
[Co(H2O)6]2+ [Mn(CN)6]4- [Ni (NH3)6]2+/B.M. 4.3 1.8 3.110、画出 [CoCl2(NH3)2(H2O)2]+配离⼦的⼏何异构体。
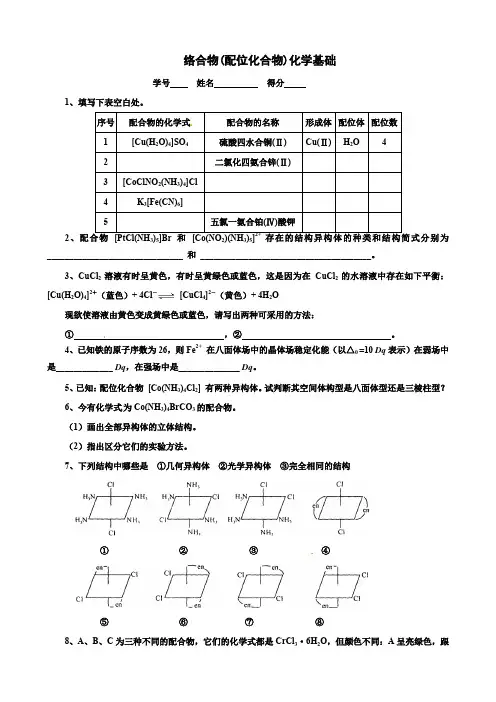
络合物(配位化合物)化学基础学号姓名得分1、填写下表空白处。
235235_______________________________ 和_______________________________________。
3、CuCl2溶液有时呈黄色,有时呈黄绿色或蓝色,这是因为在CuCl2的水溶液中存在如下平衡:[Cu(H 2O)4]2+(蓝色)+ 4Cl-[CuCl4]2-(黄色)+ 4H2O现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法:①,②。
4、已知铁的原子序数为26,则Fe2+在八面体场中的晶体场稳定化能(以△0 =10 Dq表示)在弱场中是_____________ Dq,在强场中是______________ Dq。
5、已知:配位化合物[Co(NH3)4Cl2] 有两种异构体。
试判断其空间体构型是八面体型还是三棱柱型?6、今有化学式为Co(NH3)4BrCO3的配合物。
(1)画出全部异构体的立体结构。
(2)指出区分它们的实验方法。
7、下列结构中哪些是①几何异构体②光学异构体③完全相同的结构①②③④⑤⑥⑦⑧8、A、B、C为三种不同的配合物,它们的化学式都是CrCl3·6H2O,但颜色不同:A呈亮绿色,跟AgNO3溶液反应,有2/3的氯元素沉淀析出;B呈暗绿色,能沉淀1/3的氯;而C呈紫色,可沉淀出全部氯元素。
则它们的结构简式分别为:A ,B ,C 。
这三种配离子的空间构型为面体,其中某配离子中的2个Cl可能有两种排列方式,称为顺式和反式。
它们的结构图分别为:______ _和。
9、根据下列配离子的磁矩推断中心离子的杂化轨道类型和配离子的空间构型。
[Co(H2O)6]2+[Mn(CN)6]4-[Ni (NH3)6]2+/B.M. 4.3 1.8 3.110、画出[CoCl2(NH3)2(H2O)2]+配离子的几何异构体。
11、把(NH4)2CO3浓溶液逐滴滴AgNO3稀溶液中,开始时出现浑浊,其后逐渐成为无色透明溶液。

⾼中化学奥林匹克竞赛辅导讲座第9讲络合物(配位化合物)化学基础-知识梳理⾼中化学奥林匹克竞赛辅导讲座第9讲络合物(配位化合物)化学基础【竞赛要求】配位键。
重要⽽常见的配合物的中⼼离⼦(原⼦)和重要⽽常见的配位(⽔、羟离⼦、卤离⼦、拟卤离⼦、氨分⼦、酸根离⼦、不饱和烃等)。
螯合物及螯合效应。
重要⽽常见的络合剂及其重要⽽常见的配合反应。
配合反应与酸碱反应、沉淀反应、氧化还原反应的联系(定性说明)。
配合物⼏何构型和异构现象基本概念。
配合物的杂化轨道理论。
⼋⾯体配合物的晶体场理论。
Ti(H2O)+36的颜⾊。
路易斯酸碱的概念。
【知识梳理】⼀、配合物基本知识1、配合物的定义由中⼼离⼦(或原⼦)和⼏个配体分⼦(或离⼦)以配位键相结合⽽形成的复杂分⼦或离⼦,通常称为配位单元。
凡是含有配位单元的化合物都称作配位化合物,简称配合物,也叫络合物。
[Co(NH3)6]3+,[Cr(CN)6]3–,Ni(CO)4都是配位单元,分别称作配阳离⼦、配阴离⼦、配分⼦。
[Co(NH3)6]Cl3、K3[Cr(CN)6]、Ni(CO)4都是配位化合物。
[Co(NH3)6]、[Cr(CN)6] 也是配位化合物。
判断的关键在于是否含有配位单元。
思考:下列化合物中哪个是配合物①CuSO4·5H2O②K2P t Cl6 ③KCl·CuCl2④Cu(NH2CH2COO)2 ⑤KCl·MgCl2·6H2O ⑥Cu(CH3COO)2注意:①配合物和配离⼦的区别②配合物和复盐的区别2、配合物的组成中⼼离⼦内界单齿配体配位体多齿配体配合物螯合配体外界(1)配合物的内界和外界以[Cu(NH3)4]SO4为例:[Cu(NH3)4]2+ SO-24内界外界内界是配位单元,外界是简单离⼦。
⼜如K3[Cr(CN)6] 之中,内界是[Cr(CN)6]3–,外界是K+。
可以⽆外界,如Ni(CO)4。
但不能没有内界,内外界之间是完全电离的。



第9讲络合物(配位化合物)化学基础【竞赛要求】配位键。
重要而常见的配合物的中心离子(原子)和重要而常见的配位(水、羟离子、卤离子、拟卤离子、氨分子、酸根离子、不饱和烃等)。
螯合物及螯合效应。
重要而常见的络合剂及其重要而常见的配合反应。
配合反应与酸碱反应、沉淀反应、氧化还原反应的联系(定性说明)。
配合物几何构型和异构现象基本概念。
配合物的杂化轨道理论。
八面体配合物的晶体场理论。
Ti(H2O)+36的颜色。
路易斯酸碱的概念。
【知识梳理】一、配合物基本知识1、配合物的定义由中心离子(或原子)和几个配体分子(或离子)以配位键相结合而形成的复杂分子或离子,通常称为配位单元。
凡是含有配位单元的化合物都称作配位化合物,简称配合物,也叫络合物。
[Co(NH3)6]3+,[Cr(CN)6]3–,Ni(CO)4都是配位单元,分别称作配阳离子、配阴离子、配分子。
[Co(NH3)6]Cl3、K3[Cr(CN)6]、Ni(CO)4都是配位化合物。
[Co(NH3)6]、[Cr(CN)6] 也是配位化合物。
判断的关键在于是否含有配位单元。
思考:下列化合物中哪个是配合物①CuSO4·5H2O②K2P t Cl6 ③KCl·CuCl2④Cu(NH2CH2COO)2 ⑤KCl·MgCl2·6H2O ⑥Cu(CH3COO)2注意:①配合物和配离子的区别②配合物和复盐的区别2、配合物的组成中心离子内界单齿配体配位体多齿配体配合物螯合配体外界(1)配合物的内界和外界以[Cu(NH3)4]SO4为例:[Cu(NH3)4]2+ SO-24内界外界内界是配位单元,外界是简单离子。
又如K3[Cr(CN)6] 之中,内界是[Cr(CN)6]3–,外界是K+。
可以无外界,如Ni(CO)4。
但不能没有内界,内外界之间是完全电离的。
(2)中心离子和配位体中心离子:又称配合物的形成体,多为金属(过渡金属)离子,也可以是原子。

高中化学奥林匹克竞赛辅导讲座第9讲络合物(配位化合物)化学基础【竞赛要求】配位键。
重要而常见的配合物的中心离子(原子)和重要而常见的配位(水、羟离子、卤离子、拟卤离子、氨分子、酸根离子、不饱和烃等)。
螯合物及螯合效应。
重要而常见的络合剂及其重要而常见的配合反应。
配合反应与酸碱反应、沉淀反应、氧化还原反应的联系(定性说明)。
配合物几何构型和异构现象基本概念。
配合物的杂化轨道理论。
八面体配合物的晶体场理论。
Ti(H2O)+36的颜色。
路易斯酸碱的概念。
【知识梳理】一、配合物基本知识1、配合物的定义由中心离子(或原子)和几个配体分子(或离子)以配位键相结合而形成的复杂分子或离子,通常称为配位单元。
凡是含有配位单元的化合物都称作配位化合物,简称配合物,也叫络合物。
[Co(NH3)6]3+,[Cr(CN)6]3–,Ni(CO)4都是配位单元,分别称作配阳离子、配阴离子、配分子。
[Co(NH3)6]Cl3、K3[Cr(CN)6]、Ni(CO)4都是配位化合物。
[Co(NH3)6]、[Cr(CN)6] 也是配位化合物。
判断的关键在于是否含有配位单元。
思考:下列化合物中哪个是配合物①CuSO4·5H2O②K2P t Cl6 ③KCl·CuCl2④Cu(NH2CH2COO)2 ⑤KCl·MgCl2·6H2O ⑥Cu(CH3COO)2注意:①配合物和配离子的区别②配合物和复盐的区别2、配合物的组成中心离子内界单齿配体配位体多齿配体配合物螯合配体外界(1)配合物的内界和外界以[Cu(NH3)4]SO4为例:[Cu(NH3)4]2+ SO-24内界外界内界是配位单元,外界是简单离子。
又如K3[Cr(CN)6] 之中,内界是[Cr(CN)6]3–,外界是K+。
可以无外界,如Ni(CO)4。
但不能没有内界,内外界之间是完全电离的。
(2)中心离子和配位体中心离子:又称配合物的形成体,多为金属(过渡金属)离子,也可以是原子。
高中化学奥林匹克竞赛辅导讲座 第9讲 络合物(配位化合物)化学基础【竞赛要求】配位键。
重要而常见的配合物的中心离子(原子)和重要而常见的配位(水、羟离子、卤离子、拟卤离子、氨分子、酸根离子、不饱和烃等)。
螯合物及螯合效应。
重要而常见的络合剂及其重要而常见的配合反应。
配合反应与酸碱反应、沉淀反应、氧化还原反应的联系(定性说明)。
配合物几何构型和异构现象基本概念。
配合物的杂化轨道理论。
八面体配合物的晶体场理论。
Ti(H 2O)+36的颜色。
路易斯酸碱的概念。
【典型例题】例1、某配合物的摩尔质量为260.6 g ·mol -1,按质量百分比计,其中Cr 占20.0%,NH 3占39.2%,Cl 占40.8%;取25.0 mL 浓度为0.052 mol ·L-1的该配合物的水溶液用0.121 mol ·L-1的AgNO 3滴定,达到终点时,耗去AgNO 332.5 mL ,用NaOH 使该化合物的溶液呈强碱性,未检出NH 3的逸出。
问:该配合物的结构。
分析:由Cr 、NH 3、Cl 的百分比之和为100知该物不含其他元素;由Cr 、NH 3、Cl 的百分比,可得它们的物质的量比为Cr ︰NH 3︰Cl = 1︰6︰3。
由滴定消耗的Ag +的量可算出可被Ag +沉淀的Cl -是全部所含的Cl -。
由使该化合物溶液呈强碱性不能释放出氨可见NH 3被Co 3+牢牢结合住。
综合以上信息,得出结论:结构为[Cr(NH 3)6]Cl 3;该配合物含有[Cr(NH 3)6]3+配离子。
解:Cr ︰NH 3︰Cl =526.26020.0⨯︰176.260392.0⨯︰5.356.260408.0⨯ = 1︰6 ︰3每摩尔配合物里所含的氯 =052.00.25121.05.32⨯⨯≈3 mol所以该配合物为[Cr(NH 3)6]Cl 3例2、用氨水处理K 2[PtCl 4]得到二氯二氨合铂 Pt(NH 3)2Cl 2,该化合物易溶于极性溶剂,其水溶液加碱后转化为Pt(NH 3)2(OH)2,后者跟草酸根离子反应生成草酸二氨合铂Pt(NH 3)2C 2O 4,问Pt (NH 3)2Cl 2的结构。
分析:Pt(NH 3)2Cl 2是平面四边形配合物,有顺式和反式之分:反式异构体有对称中心,无极性,顺式异构体有极性。
顺式的两个氯原子(Cl -)处于邻位,被羟基(OH -)取代后为顺式Pt(NH 3)2 (OH)2,后者两个羟基处于邻位,可被双齿配体C 2O -24取代得到Pt(NH 3)2C 2O 4,反式则不可能发生此反应,因为C 2O -24的C —C 键长有限,不可能跨过中心离子与双齿配体形成配价键。
解:K 2[PtCl 4]−−→−3NH Pt (NH 3)2Cl 2−−→−-OH Pt (NH 3)2 (OH)2−−→−-242O C Pt (NH 3)2C 2O 4由水溶液证实产物Pt (NH 3)2Cl 2有极性;加之可将Pt (NH 3)2 (OH)2转化为Pt (NH 3)2C 2O 4,证实Pt (NH 3)2Cl 2为顺式异构体。
例3、写出Pt (NH 3)2(OH)2Cl 2的异构体。
分析:八面体的6个顶点被3对不同的配体占据,只可能有三种模式(见下图)(I )式a 、b 、c 三对配体均取对位,(II )式a 、b 、c 三对配体均取邻位,(III )式为“一反二顺”式。
对于I 、II 式,a ,b ,c 的空间关系是无区别的,而III 式中a 与b ,c 空间有区别,当a 分别为OH -,NH 3和Cl -时,便出现三种异构体。
再则,II 、III 式分子内均有对称面,不可能出现对映异构体,而I 式无对称面,存在一对对映异构体。
解:该化合物有6种异构体,结构如下:(VI )是(I )的对映体例4、试给出Cr(NH 3)+36的杂化轨道类型,并判断中心离子Cr 3+是高自旋型还是低自旋型?分析:该配离子配位数为6,其空间构型应是正八面体,中心离子杂化轨道类型可能是内轨型d 2sp 3或外轨型sp 3d 3。
因Cr 3+电子构型是3d 3,内层有空的3d 轨道,因而形成内轨型的杂化轨道。
对于八面体场(C.N.=6),只有当络离子中中心离子(或原子)的d 电子数为4~7时,才可能有高自旋与低自旋之分。
因Cr 3+只有3个d 电子,故无高自旋与低自旋之分。
解:Cr 3+的基态电子构型为3d 3,因而3个未成对电子以自旋平行的方式填入3个3d 轨道,尚有2个空3d 轨道,因而可以容纳NH 3分子的电子对,故Cr(NH 3)+36的杂化轨道类型是d 2sp 3。
因Cr 3+只有3个d电子,故无高自旋与低自旋之分。
例5、已知[Cu(NH 3)4]2+ 的不稳K = 4.79×10-14若在1.0 L 6.0 mol ·L-1氨水溶液中溶解0.10 mol CuSO 4求溶液中各组分的浓度(假设溶解CuSO 4后溶液的体积不变)。
解:①先假设全部Cu 2+ 被结合,然后解离Cu 2+(0.10 mol ·L -1)−→−[Cu(NH 3)4]2+(0.10 mol ·L -1) [Cu(NH 3)4]2+ Cu 2+ + 4NH 3平衡关系 0.10—x x 6.0-(0.1×4)+4x不稳K =])([]][[24323+++NH Cu NH Cu =xx x -+10.0)46.5(= 4.79×10-14解得 x = 4.90×10-18x 很小可略②计算各组分浓度c c (Cu 2+ )= 4.9×10-18mol ·L -1c (NH 3 )= 6.0+0.10×4 = 5.6 mol ·L -1c (SO -24)= 0.10 mol ·L -1(原始CuSO 4浓度)c [Cu(NH 3)+24] = 0.10-[Cu 2+ ] = 0.10 mol ·L -1例6、在上述溶液中 ①加入1.0 mol ·L -1 NaOH 10 mL 有无Cu(OH)2沉淀生成?②加入0.10 mol ·L-1 Na2S 1.0 mol有无CuS 沉淀生成?(已知2)(,OH Cu sp K = 2.2×10-20CuS sp K , = 6.3×10-36)解:先求[Cu 2+],然后用sp K 关系式比较 ①浓度换算(原题为1L 溶液)加入NaOH 后NaOH 浓度 1.0 mol ·L -1×10mL = c (NaOH )·(1000+10)mLc (NaOH )=1010100.1⨯= 0.01 mol ·L -1 Cu 2+浓度换算变化很小,忽略。
离子积 [Cu 2+][OH -]2 = 4.9×10-18×(0.01)2 = 4.9×10-22<sp K 无沉淀。
②加Na 2S 后Na 2S 浓度 0.10×1.0 = (1000+1) c (S 2-)c (S 2-)=10010.40.1⨯=10-4 mol ·L -1 [Cu 2+][S 2-] = 4.9×10-18×10-4= 4.90×10-22>sp K 故CuS 沉淀。
例7、如果溶液中同时有NH 3、S 2O -23、CN -存在,则Ag + 将发生怎样的反应?(已知配离子的不稳K :NH 3 5.89×10-8 S 2O -23 7.08×10-15 CN - 2.5×10-21)分析:不稳K 越小,稳K 越大,配合物易形成。
故Ag 首先生成[Ag(CN)2]-,若有足够量Ag + 时,最后能生成[Ag(NH 3)2]+。
该题同时表明CN -的配位场很强。
配位场顺序,由弱到强,参见光谱化学序列I -<Br -(0.76)<Cl -(0.80)<-SCN -<F -(0.90)~ 尿素(0.91)<OH -~ –O –N=0-(亚硝酸根) <C 2O -24(0.98)<H 2O (1.00)<-NCS -(1.02)<EDTA -4<吡啶(1.25)~NH 3(1.25)<en (1.28)<SO -23<联吡啶(1.33)~ 1,10–邻二氮菲<–NO -2(硝基)<CN -(1.5~3.0)解:先生成Ag(CN)-2Ag + + 2 CN -= Ag(CN)-2本题也可用多重平衡规则通过计算来判断Ag(NH 3)2++2CN-Ag(CN)-2+2NH 3①Ag(CN)-2 Ag ++2CN - 不稳1K = 2.51×10-21②Ag(NH 3)+2Ag ++2NH 3 不稳2K = 5.89×10-8②-①得: Ag(NH 3)+2+2CN -Ag(CN)-2 +2NH 3K = 不稳2K /不稳1K =21--8102.51105.89⨯⨯= 2.34×1013 1Ag(CN)-2+2S 2O -23Ag(S 2O 3)-32+2CN -① Ag(CN)-2Ag ++2CN -不稳1K = 2.51×10-21② Ag(S 2O 3)-32Ag ++2S 2O -23 不稳2K = 7.08×10-15①-②得: Ag(CN)-2 + 2S 2O -23Ag(S 2O 3)-32 + 2CN -K = 不稳1K /不稳2K =2.51×10-21/ 7.08×10-151不可进行结论:先生成Ag(CN)-2例8、结合平衡与酸碱反应分析AgCl 被NH 3溶解后,滴入HAc 有何现象发生?若换成[Ag(CN)2]-中滴入Hac 又怎样?(已知:HAc a K ,= 1.75×10-5 O H NH b K 23,⋅ = 1.75×10-5 HCN a K ,= 4.93×10-10+23)(,NHAg K 不稳 = 5.89×10-8-2)(,CN Ag K 不稳 = 2.51×10-21)解:① [Ag(NH 3)2]+ Ag ++2NH 3 不稳K = 5.89×10-8②×2 2HAc2H ++2Ac -2a K = (1.75×10-5)2③×2 2NH 3+2H 2O 2OH -+2NH 4+ 2b K= (1.75×10-5)2④×2 2H 2O2H ++2OH -K w 2 = (1×10-14)2① + ② + ③-④ 得: ⑤ [Ag(NH 3)2]+ + 2HAcAg + +2Ac -+ 2NH 4+5K =不稳K ·2aK ·2b K / K w 2 =21425258)101()1075.1()1075.1(1089.5----⨯⨯⨯⨯⨯⨯= 3.2×10 61 转化可实现⑥ AgClAg ++Cl -sp K =1.56×10-10⑤-⑥得:[Ag(NH 3)2]++Cl -+2HAc AgCl+2Ac -+2NH 4+K = sp K K 5= 1061056.1102.3-⨯⨯= 2.0×10161 转化可实现,即有AgCl ↓析出。