2003年华南理工大学 《物理化学》考研试题及参考答案(理工)
- 格式:doc
- 大小:122.50 KB
- 文档页数:9



华南理工大学2004年攻读硕士学位研究生入学考试试卷(329)参考答案科目名称:物理化学(化)适用专业:无机化学、分析化学、物理化学、环境科学说明:本答案由葛华才老师完成,试题做了规范化和少量处理,若有不恰当之处特别是错误之处,欢迎用电子邮件方式告知葛老师本人(邮箱:**************)。
一. 2 mol 乙醇在正常沸点(78.4℃)下,变为蒸汽,其摩尔汽化焓为41.50kJ . mol-1,乙醇蒸汽可视为理想气体。
(1)试求该相变过程的Q,W,△U,△S,△A,△G。
(2)若乙醇摩尔汽化焓可认为与温度无关时,那么50℃时乙醇的饱和蒸汽压应为多少?(3)当2mol乙醇蒸汽在101325Pa下,从78.4℃升温至100℃时,△H,△S各为多少?(已知C p,m(C2H5OH,g)=65.44 J . mol-1 . K-1)。
(本题15分)解:(1) Q p=∆H=n ∆vap H m= 2mol×41.50kJ . mol-1= 83.00 kJW= -p∆V= -pV g= -nRT= -[2×8.315×(273.15+78.4)] J =5846J∆U=Q+W= 83.00kJ+5.846kJ=88.85kJ∆S=Q/T= 83000J/(273.15+78.4)K=236.1J . K-1∆G=0 (可逆相变)∆A=∆U-T∆S=W= 5846J(2) 已知T=351.55K,p=101.325kPa,蒸发焓∆vap H m= 41.50kJ . mol-1,利用克-克方程可求T’=323.15K时的蒸气压p’:ln(p’/101.325kPa)=-(41500/8.315)[(1/323.15)-(1/351.55)]p’=28.10kPa(3) 乙醇蒸汽C p,m与温度无关,△H=nC p,m△T=(2×65.44×21.6)J = 2827J△S = nC p,m ln(T2/T1)=[2×65.44×ln(373.15/351.55)]J . K-1 = 7.804J . K-1二. 已知在298K,100 kPa下,反应:C2H4 (g)+H2O (l)==C2H5OH (l)数据如下:(C2H4(g)视为理想气体)C2H4 (g) H2O (l) C2H5OH (l) △f H mθ/kJ . mol-152.26 -285.83 -277.7S m θ/J . mol -1 . K -1219.6 69.91 161 C p ,m /J . mol -1 . K -1 43.56 75.291 111.5(1) 试求在298K 下,反应的标准平衡常数K θ。
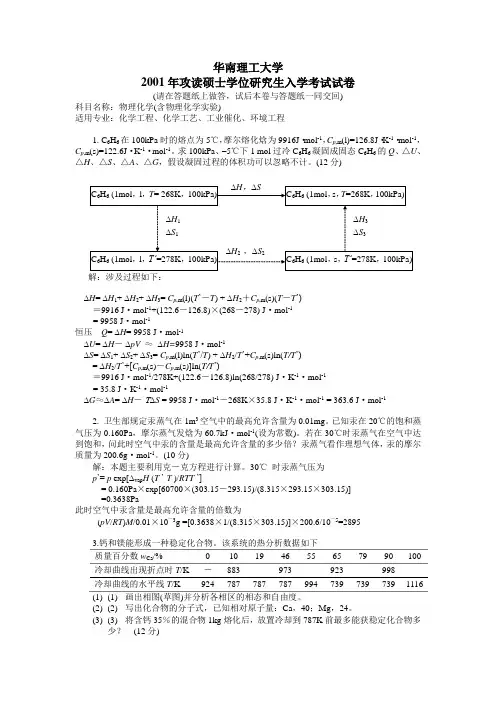
华南理工大学2001年攻读硕士学位研究生入学考试试卷(请在答题纸上做答,试后本卷与答题纸一同交回)科目名称:物理化学(含物理化学实验)适用专业:化学工程、化学工艺、工业催化、环境工程1. C6H6在100kPa时的熔点为5℃,摩尔熔化焓为9916J²mol-1,C p,m(l)=126.8J²K-1²mol-1,C p,m(s)=122.6J²K-1²mol-1。
求100kPa、–5℃下1 mol过冷C6H6凝固成固态C6H6的Q、△U、△H、△S、△A、△G,假设凝固过程的体积功可以忽略不计。
(12分)解:涉及过程如下:∆H= ∆H1+ ∆H2+ ∆H3= C p,m(l)(T’-T) +∆H2+C p,m(s)(T-T’)=9916 J²mol-1+(122.6-126.8)³(268-278) J²mol-1= 9958 J²mol-1恒压Q= ∆H= 9958 J²mol-1∆U= ∆H- ∆pV ≈∆H=9958 J²mol-1∆S= ∆S1+ ∆S2+ ∆S3= C p,m(l)ln(T’/T) +∆H2/T’+C p,m(s)ln(T/T’)= ∆H2/T’+[C p,m(s)-C p,m(s)]ln(T/T’)=9916 J²mol-1/278K+(122.6-126.8)ln(268/278) J²K-1²mol-1= 35.8 J²K-1²mol-1∆G≈∆A= ∆H- T∆S = 9958 J²mol-1-268K³35.8 J²K-1²mol-1 = 363.6 J²mol-12. 卫生部规定汞蒸气在1m3空气中的最高允许含量为0.01mg。
已知汞在20℃的饱和蒸气压为0.160Pa,摩尔蒸气发焓为60.7kJ²mol-1(设为常数)。



华南理工大学2002年攻读硕士学位研究生入学考试试卷(请在答题纸上做答,试后本卷与答题纸一同交回)科目名称:物理化学(含物理化学实验)适用专业:化学工程、化学工艺、工业催化、环境工程1. 在绝热的条件下,将0.4mol某理想气体从200kPa压缩到1000kPa时,温度从300K 上升到900K,求该过程的W、△H、△S、△U、△G,判断过程的性质并指出判据,已知:该理想气体在300K和200kPa时的摩尔熵为S m=205J·K-1·mol-1,定压摩尔热容为C p,m =3.5R(12分)解:分析过程:(p1=200kPa,V1,T1=300K) →(p2=1000kPa,, V2, T2=900K)绝热Q=0理想气体△U = nC V,m△T = n(C p,m-R)△T△H = nC p,m△T故W =△U -Q过程熵△S = nC p,m ln(T2/ T1)+nR ln(p1/ p2)△G =△(H-TS) =△H-(T2S2-T1S1) =△H-(T2△S-S1△T)过程绝热,所以只能用△S判断过程的方向。
注意:本题非恒外压,功一般由热力学第一定律式计算W =△U -Q。
2. 298K时,反应N2O4(g)=2NO2(g) 的平衡常数Kθ=0.155,标准摩尔焓为57.24kJ·mol-1(假定温度对反应焓的影响可以忽略不计)。
(共10分)求(1) 373K时反应的平衡常数Kθ。
(2) 298K,总压为pθ时N2O4的离解度。
(3) 298K,总压为pθ,离解前N2O4和N2(惰性气体)物质的量为1:1时N2O4的离解度。
解:本题主要利用等压方程求不同温度下的平衡常数,以及与组成关系。
(1) 等压方程:ln(K2θ/ K1θ)= (T2-T1)∆r H mθ/R(T2T1)(2)N2O4(g) =2NO2(g)t=0 1mol 0 molt=∞时n 1-x2x n总=1+x分压(1-x) pθ/( 1+x) 2x pθ/( 1+x)K1θ=[2x/( 1+x)]2/[(1-x)/( 1+x)] =4x2/(1-x2)可求出x=(3)N2O4(g) =2NO2(g) N2t=0 1mol 1molt=∞时n1-x2x1mol n总=2+x分压(1-x) pθ/( 2+x) 2x pθ/( 2+x)K1θ=[2x/( 2+x)]2/[(1-x)/( 2+x)] =4x2/(2-x-x2)可求出x=3. 水的蒸汽压与温度之间可用如下关系式表示: lg (p /Pa) =-A /T +B若已知水在77℃时的饱和蒸汽压为41.847kPa ,求:(1) 常数A ,B 的值以及水的摩尔蒸发焓;(2) 在多大外压下水的沸点可以改变为101℃;(共8分)解:(1) 给出的关系式实际上为克-克方程的不定积分式。

华南理工大学2003年攻读硕士学位研究生入学考试试卷(试卷上做答无效,请在答题纸上做答,试后本卷必须与答题纸一同交回)科目名称:高分子化学与物理适用专业:高分子化学与物理、材料学、材料加工工程高分子化学部分一、选择题(每题2分,工10分)1、烯类单体自由基聚合中,存在自动加速效应时,将导致----。
A、聚合速度和分子量同时下降B、聚合速度增加但分子量下降C、聚合速度下降但分子量增加D、聚合速度和分子量同时增加而分子量分布变宽。
2、在无终止的阴离子聚合中,阴离子无终止的主要原因是----。
A、阴离子本身比较稳定B、阴离子无双基终止而是单基终止C、从活性链上脱除负氢原子困难D、活化能底,在底温下聚合3、在自由基共聚中,e值相差较大的单体,易发生---。
A、交替共聚B、理想共聚C、非理想共聚D“嵌段”共聚4、所有缩聚反映所共的是----。
A、逐步特性B、通过活性中心实现链增长C、引发速率很快D、快终止5、开发一聚合物时,单体能否聚合需要从热力学和动力学两方面进行考察。
热力学上判断聚合倾向的主要参数是----。
A、聚合物玻璃化转变温度B、聚合焓△GC、聚合物的分解温度D、聚合反应速率二、填空题(每题4分,共16分)1、阻聚剂、缓聚剂和链转移剂(分子量调节剂)共同作用原理是----,主要区别是---。
2、能进行自由基聚合的单体有----、----、----。
能进行阳离子聚合的单体有----、----、----。
能进行阴离子聚合的单体有----、----、----。
3、已知M1和M2的Q1=2.39,e1=-1.05,Q2=0.60,e2=1.20.比较两单体的共轭稳定性是--大于--,两单体的活性是--大于--,两自由基的稳定性是--大于--,如两单体分别均聚合,--的KP大于--的KP。
4、合成高聚物的几种聚合方法中,能获得最窄分子量分布的是--聚合。
三、完成下列各题(33分)1、在尼龙6和尼龙66生产中为什么要加入醋酸或已二酸作为分子量控制剂?在涤纶生产中为什么不加分子量控制剂?在涤纶生产中是采用什么措施控制分子量的?(8分)2、用图示的方法,比较在自由基聚合和逐步聚合中(6分)(1)单体转化率反应时间的关系;(2)聚合物分子量与反应时间的关系;3、从聚合物结构出发,分析天然橡胶和丁基橡胶的耐氧化性(5分)4、以乙二醇二甲醚为溶剂,分别以RLi、RNa、RK为引发剂,在相同条件下,使苯乙烯聚合.判断采用上述不同引发剂时聚合速率大小顺序。

华南理工大学2004年攻读硕士学位研究生入学考试试卷(329)参考答案科目名称:物理化学(化)适用专业:无机化学、分析化学、物理化学、环境科学说明:本答案由葛华才老师完成,试题做了规范化和少量处理,若有不恰当之处特别是错误之处,欢迎用电子邮件方式告知葛老师本人(邮箱:ge1963@)。
一. 2 mol 乙醇在正常沸点(78.4℃)下,变为蒸汽,其摩尔汽化焓为41.50kJ²mol-1,乙醇蒸汽可视为理想气体。
(1)试求该相变过程的Q,W,△U,△S,△A,△G。
(2)若乙醇摩尔汽化焓可认为与温度无关时,那么50℃时乙醇的饱和蒸汽压应为多少?(3)当2mol乙醇蒸汽在101325Pa下,从78.4℃升温至100℃时,△H,△S各为多少?(已知C p,m(C2H5OH,g)=65.44 J²mol-1²K-1)。
(本题15分)解:(1) Q p=∆H=n ∆vap H m= 2mol³41.50kJ²mol-1= 83.00 kJW= -p∆V= -pV g= -nRT= -[2³8.315³(273.15+78.4)] J =5846J∆U=Q+W= 83.00kJ+5.846kJ=88.85kJ∆S=Q/T= 83000J/(273.15+78.4)K=236.1J²K-1∆G=0 (可逆相变)∆A=∆U-T∆S=W= 5846J(2) 已知T=351.55K,p=101.325kPa,蒸发焓∆vap H m= 41.50kJ²mol-1,利用克-克方程可求T’=323.15K时的蒸气压p’:ln(p’/101.325kPa)=-(41500/8.315)[(1/323.15)-(1/351.55)]p’=28.10kPa(3) 乙醇蒸汽C p,m与温度无关,△H=nC p,m△T=(2³65.44³21.6)J = 2827J△S = nC p,m ln(T2/T1)=[2³65.44³ln(373.15/351.55)]J²K-1 = 7.804J²K-1二. 已知在298K,100 kPa下,反应:C2H4 (g)+H2O (l)==C2H5OH (l)数据如下:(C2H4(g)视为理想气体)C2H4 (g) H2O (l) C2H5OH (l) △f H mθ/kJ²mol-152.26 -285.83 -277.7S mθ/J²mol-1²K-1219.6 69.91 161C p,m/J²mol-1²K-143.56 75.291 111.5(1)试求在298K下,反应的标准平衡常数Kθ。

历年华南理工大学629物理化学(一)考研真题试卷与真题答案历年华南理工大学629物理化学(一)考研真题试卷与真题答案一、考试解读:part 1 学院专业考试概况:①学院专业分析:含学院基本概况、考研专业课科目:629物理化学(一)的考试情况;②科目对应专业历年录取统计表:含华工相关专业的历年录取人数与分数线情况;③历年考研真题特点:含华南理工大学考研专业课629物理化学(一)各部分的命题规律及出题风格。
part 2 历年题型分析及对应解题技巧:根据华工629物理化学(一)考试科目的考试题型(计算题、简答题等),分析对应各类型题目的具体解题技巧,帮助考生提高针对性,提升答题效率,充分把握关键得分点。
part 3 近年真题分析:最新真题是华工考研中最为珍贵的参考资料,针对最新一年的华南理工大学考研真题试卷展开深入剖析,帮助考生有的放矢,把握真题所考察的最新动向与考试侧重点,以便做好更具针对性的复习准备工作。
part 4 2020考试展望:根据上述相关知识点及真题试卷的针对性分析,提高2020考生的备考与应试前瞻性,令考生心中有数,直抵华工考研的核心要旨。
part 5 华南理工大学考试大纲:①复习教材罗列(官方指定或重点推荐+拓展书目):不放过任何一个课内、课外知识点。
②官方指定或重点教材的大纲解读:官方没有考试大纲,高分学长学姐为你详细梳理。
③拓展书目说明及复习策略:专业课高分,需要的不仅是参透指定教材的基本功,还应加强课外延展与提升。
part 6 专业课高分备考策略:①考研前期的准备;②复习备考期间的准备与注意事项;③考场注意事项。
part 7 章节考点分布表:罗列华工考研专业课试卷中,近年试卷考点分布的具体情况,方便考生知晓华工考研专业课试卷的侧重点与知识点分布,有助于考生更具针对性地复习、强化,快准狠地把握高分阵地。
二、华南理工历年考研真题与部分答案:2000年华南理工大学物理化学考研真题试卷2001年华南理工大学物理化学考研真题试卷2002年华南理工大学物理化学考研真题试卷2003年华南理工大学329物理化学(一)考研真题试卷2004年华南理工大学329物理化学(一)考研真题试卷2005年华南理工大学329物理化学(一)考研真题试卷2006年华南理工大学329物理化学(一)考研真题试卷2007年华南理工大学329物理化学(一)考研真题试卷2008年华南理工大学629物理化学(一)考研真题试卷2009年华南理工大学629物理化学(一)考研真题试卷2010年华南理工大学629物理化学(一)考研真题试卷2011年华南理工大学629物理化学(一)考研真题试卷2012年华南理工大学629物理化学(一)考研真题试卷2013年华南理工大学629物理化学(一)考研真题试卷2014年华南理工大学629物理化学(一)考研真题试卷2015年华南理工大学629物理化学(一)考研真题试卷2016年华南理工大学629物理化学(一)考研真题试卷2017年华南理工大学629物理化学(一)考研真题试卷2018年华南理工大学629物理化学(一)考研真题试卷2000年华南理工大学物理化学考研真题答案解析2001年华南理工大学物理化学考研真题答案解析2002年华南理工大学329物理化学(一)考研真题答案解析2003年华南理工大学329物理化学(一)考研真题答案解析2004年华南理工大学329物理化学(一)考研真题答案解析2005年华南理工大学329物理化学(一)考研真题答案解析2006年华南理工大学329物理化学(一)考研真题答案解析2007年华南理工大学329物理化学(一)考研真题答案解析2008年华南理工大学629物理化学(一)考研真题答案解析2009年华南理工大学629物理化学(一)考研真题答案解析2010年华南理工大学629物理化学(一)考研真题答案解析2011年华南理工大学629物理化学(一)考研真题答案解析2012年华南理工大学629物理化学(一)考研真题答案解析2013年华南理工大学629物理化学(一)考研真题答案解析2014年华南理工大学629物理化学(一)考研真题答案解析2015年华南理工大学629物理化学(一)考研真题答案解析2016年华南理工大学629物理化学(一)考研真题答案解析2017年华南理工大学629物理化学(一)考研真题答案解析此真题试卷与真题答案摘自致远华工考研网。

华南理工大学2001年攻读硕士学位研究生入学考试试卷(请在答题纸上做答,试后本卷与答题纸一同交回)科目名称:物理化学(含物理化学实验)适用专业:化学工程、化学工艺、工业催化、环境工程1. C6H6在100kPa时的熔点为5℃,摩尔熔化焓为9916J·mol-1,C p,m(l)=126.8J·K-1·mol-1,C p,m(s)=122.6J·K-1·mol-1。
求100kPa、–5℃下1 mol过冷C6H6凝固成固态C6H6的Q、△U、△H、△S、△A、△G,假设凝固过程的体积功可以忽略不计。
(12分)解:涉及过程如下:∆H= ∆H1+ ∆H2+ ∆H3= C p,m(l)(T’-T) +∆H2+C p,m(s)(T-T’)=9916 J·mol-1+(122.6-126.8)×(268-278) J·mol-1= 9958 J·mol-1恒压Q= ∆H= 9958 J·mol-1∆U= ∆H- ∆pV ≈∆H=9958 J·mol-1∆S= ∆S1+ ∆S2+ ∆S3= C p,m(l)ln(T’/T) +∆H2/T’+C p,m(s)ln(T/T’)= ∆H2/T’+[C p,m(s)-C p,m(s)]ln(T/T’)=9916 J·mol-1/278K+(122.6-126.8)ln(268/278) J·K-1·mol-1= 35.8 J·K-1·mol-1∆G≈∆A= ∆H- T∆S = 9958 J·mol-1-268K×35.8 J·K-1·mol-1 = 363.6 J·mol-12. 卫生部规定汞蒸气在1m3空气中的最高允许含量为0.01mg。
已知汞在20℃的饱和蒸气压为0.160Pa,摩尔蒸气发焓为60.7kJ·mol-1(设为常数)。
华南理工大学2001年攻读硕士学位研究生入学考试试卷(请在答题纸上做答,试后本卷与答题纸一同交回)科目名称:物理化学(含物理化学实验)适用专业:化学工程、化学工艺、工业催化、环境工程1. C6H6在100kPa时的熔点为5℃,摩尔熔化焓为9916J·mol-1,C p,m(l)=126.8J·K-1·mol-1,C p,m(s)=122.6J·K-1·mol-1。
求100kPa、–5℃下1 mol过冷C6H6凝固成固态C6H6的Q、△U、△H、△S、△A、△G,假设凝固过程的体积功可以忽略不计。
(12分)解:涉及过程如下:∆H= ∆H1+ ∆H2+ ∆H3= C p,m(l)(T’-T) +∆H2+C p,m(s)(T-T’)=9916 J·mol-1+(122.6-126.8)×(268-278) J·mol-1= 9958 J·mol-1恒压Q= ∆H= 9958 J·mol-1∆U= ∆H- ∆pV ≈∆H=9958 J·mol-1∆S= ∆S1+ ∆S2+ ∆S3= C p,m(l)ln(T’/T) +∆H2/T’+C p,m(s)ln(T/T’)= ∆H2/T’+[C p,m(s)-C p,m(s)]ln(T/T’)=9916 J·mol-1/278K+(122.6-126.8)ln(268/278) J·K-1·mol-1= 35.8 J·K-1·mol-1∆G≈∆A= ∆H- T∆S = 9958 J·mol-1-268K×35.8 J·K-1·mol-1 = 363.6 J·mol-12. 卫生部规定汞蒸气在1m3空气中的最高允许含量为0.01mg。
已知汞在20℃的饱和蒸气压为0.160Pa,摩尔蒸气发焓为60.7kJ·mol-1(设为常数)。
物理化学复习要览(48学时)试题结构:一选择题(10题20分)二计算题(6题60分)三简答题(5题20分)第二章热力学第一定律一、重要概念系统与环境,隔离系统,封闭系统,(敞开系统),广延量(加和性:V,U,H,S,A,G),强度量(摩尔量,T,p),功,热,内能,焓,热容,状态与状态函数,平衡态,过程函数(Q,W),可逆过程,节流过程,真空膨胀过程,标准态,标准反应焓,标准生成焓,标准燃烧焓二、重要公式与定义式1. 体积功:δW= -p外dV2. 热力学第一定律:∆U = Q+W,d U =δQ +δW3.焓的定义:H=U + pV4.热容:定容摩尔热容C V,m = δQ V /dT = (∂U m/∂T )V定压摩尔热容C p,m = δQ p /dT = (∂H m/∂T )P理想气体:C p,m- C V,m=R5. 标准摩尔反应焓:由标准生成焓∆f H Bθ (T)或标准燃烧焓∆c H Bθ(T)计算∆r H mθ = ∑v B∆f H Bθ (T) = -∑v B∆c H Bθ (T)6. 基希霍夫公式(适用于相变和化学反应过程)∆r H mθ(T2)= ∆r H mθ(T1)+⎰21TT∆r C p,m d T7. 恒压摩尔反应热与恒容摩尔反应热的关系式Q p-Q V = ∆r H m(T) -∆r U m(T) =∑v B(g)RT8. 理想气体的可逆绝热过程方程:p1V1γ= p2V2γ,p1V1/T1 = p2V2/T2,γ=C p,m/C V,m三、各种过程Q 、W 、∆ U 、∆ H 的计算1.解题时可能要用到的内容(1) 对于气体,题目没有特别声明,一般可认为是理想气体,如N 2,O 2,H 2等。
恒温过程d T =0, ∆ U =∆ H =0, Q =W非恒温过程,∆ U = n C V ,m ∆ T , ∆ H = n C p ,m ∆ T(2) 对于凝聚相,状态函数通常近似认为只与温度有关,而与压力或体积无关,即∆ U ≈∆ H = n C p ,m ∆ T2. 恒压过程:p 外=p =常数,无其他功W '=0(1) W = -p 外(V 2-V 1), ∆ H = Q p =⎰21T T n C p ,m d T , ∆ U =∆ H -∆(pV ),Q =∆ U -W(2) 真空膨胀过程p 外=0,W =0,Q =∆ U理想气体(Joule 实验结果):d T =0,W =0,Q =∆ U =0,∆ H =0(3) 恒外压过程:例1: 1mol 理想气体于27℃ 、101325Pa 状态下受某恒定外压恒温压缩到平衡,再由该状态恒容升温到97 ℃ ,则压力升到1013.25kPa 。
华南理工大学2003年攻读硕士学位研究生入学考试试卷(请在答题纸上做答,试后本卷与答题纸一同交回)科目名称:物理化学适用专业:材料物理化学、材料加工工程、环境工程、生物医学工程点评:本套题题量偏多,至少多了3题,部分题难度偏大,且其中一道题所给的条件有误,使学生根本无法计算。
1. 一绝热容器中装有10mol、80 ℃的纯水。
已知液态水的恒压摩尔热容C p,m(H2O,l) 为75.3J·mol-1·K-1;水的摩尔气化焓和冰的摩尔焓分别为40 kJ·mol-1、46.004 kJ·mol-1。
在101325Pa下,为了使容器中的水温降至50 ℃。
试问:(1)(1)需加入0℃的冰为多少?(2)(2)水和冰混合过程的总熵变。
(10分)解:本题求解需冰的溶化焓,但题目没有给出,题目给的冰的摩尔焓没有任何意义,所以是一个无法求解的题。
也许,题目给的应该是冰的摩尔升华焓,这时冰的溶化焓可近似计算如下:∆fus H= ∆sub H- ∆vap H= 46.004 kJ·mol-1-40kJ·mol-1=6.004 kJ·mol-1(1)(1)设加入的冰量为x mol,根据绝热条件有Q p=∆H = n(H2O) C p,m(H2O,l)(50-80)K+ x [∆fus H +C p,m(H2O,l)(50-0)K] = 0于是:x =n(H2O) C p,m(H2O,l)×30K/[∆fus H +C p,m(H2O,l)×50K]=10mol×75.3J·mol-1·K-1×30K/[6004 J·mol-1+75.3J·mol-1·K-1×50K]= 2.31 mol(2) ∆S = n(H2O) C p,m(H2O,l)×ln(333.15K/353.15K)+x [∆fus H /273.15K+C p,m(H2O,l)×ln(333.15K/273.15K)]=10mol×75.3J·mol-1·K-1×ln(333.15K/353.15K)+2.31mol×[6004 J·mol-1 /273.15K+75.3J·mol-1·K-1×ln(333.15K/273.15K)]= 41.42 J·K-12. 2mol 理想气体在101325Pa下由300K加热到500K,该过程的热为18kJ。
华南理工大学2003攻读硕士学位研究生入学考试试卷物理化学部分(与化工原理合一门课程)(试题已由葛华才老师整理求解,有错请告知!)1. 1mol 水在100℃、101.325kPa下正常气化, 已知水的正常蒸发焓为40.64 kJ . mol-1,求此过程的Q、W、∆U、∆H、∆S、∆G。
(15分)解:Q=∆H=n∆Vap H m= 1mol×40.64 kJ . mol-1= 40.64kJ (注:若题目未给出蒸发焓,可以不算出数值)∆S= ∆H/T= 40.64kJ/373.15K= 108.9J . K-1(可逆相变过程)∆G=0W= -p[V(g)-V(l)]≈-pV(g) = -nRT= -1mol×8.3145J . K-1 . mol-1×373.15K=-3103J∆U=Q+W= 40.64kJ-3103J = 37.54kJ2. 已知反应2NaHCO3(s) = Na2CO3(s) + H2O(g) + CO2(g)温度为50℃、100℃时系统的平衡总压分别为3950Pa、96300Pa。
设反应的∆r H m与温度无关,试求:(1) 计算50℃时该反应的K、∆r G m。
(2) 计算该反应的∆r H m。
(3) 计算NaHCO3(s)的分解温度。
(15分)解:(1) 设平衡总压为p,则2NaHCO3(s)= Na2CO3(s) + H2O(g) + CO2(g)平衡p/2 p/2K=p[H2O(g)] p [CO2(g)]/ p2 = (p / p)2/4 =(3950Pa/100000Pa)2/4=0.0003901∆r G m= -RT ln K= -8.3145J . K-1 . mol-1×323.15K×ln(0.0003901)= 21089 J . mol-1(2) T’=373.15K时,K= (p’ / p)2/4 =(96300Pa/100000Pa)2/4=0.2318∆r H m= [RT’T/(T’-T)]ln(K’/ K)=[8.3145J . K-1 . mol-1×373.15K×323.15K/(373.15K-323.15K)]×ln(0.2318/0.0003901)=128075J . mol-1=128.1 kJ . mol-1(3) 若分解温度即为平衡总压p=101325Pa时对应的温度T”,此时K= (p”/ p)2/4 =(101325Pa/100000Pa)2/4=0.2567利用等压方程ln (K”/ K ) = (∆r H m / R )(1/T -1/T”)即 ln(0.2567/0.0003901)=(128100kJ . mol -1/8.3145J . K -1 . mol -1)(1/323.15K -1/T ”) T ”= 374.06K3.硫酸在常压下与水可形成3种水合物,其相图如右。
(1) 指出三个水合物的组成。
已知硫酸和水分子的相对质量分别为 98、18。
(2) 指出各区和三相线的相态和自由度。
(3) 生产过程中用管道输送液态硫酸,若是98%的浓硫酸,会不会出现问题?若是93%的浓硫酸,又会如何? (15分)答:(1) 组成分别为H 2SO 4 .4H 2O(C)、H 2SO 4 . 2H 2O(D)、H 2SO 4 . H 2O(E)。
(2) 在常压下,硫酸与水的相图看起来似乎复杂,实际上很简单,是H 2O —H 2SO 4 . 4H 2O 、H 2SO 4 . 4H 2O —H 2SO 4 . 2H 2O 、H 2SO 4 . 2H 2O —H 2SO 4 . H 2O 、H 2SO 4 . H 2O —H 2SO 4固相完全不互溶的相图的组合,因此各区和三相线的相态很容易确定,自由度为F =C -P +1=3-P ,具体相态(L 为液体,S 为固体)和自由度数值见下表: 相区 I II III IV V VI VII 相态 L 冰+L L +C (s ) 冰+ C (s ) C (s )+L L+ D (s ) C(s )+ D (s )自由度 2111111相区 VIII IX X XI XII XIII 相态 D (s ) + E (s )E (s )+L D (s )+L E (s )+L L + B (s ) E (s )+ B (s )自由度111111三相线的相态(F =0)三相线 FGH JKL MNO PQR 相态冰+L+ C (s )L+ C (s )+ D (s )L + D (s )+ E (s )L + E (s )+ B (s )(3) 从相图上可知道,98%的浓硫酸在温度降至0℃左右时会产生固体硫酸,影响管道输送,所以冬天时将无法输送。
对于93%的浓硫酸,其凝固点约-35℃,一般的室温都高于此温度,故用管道输送时将不会因产生固体而堵塞管道的问题。
EDC H 2SO 4 (B)H 2O(A)t / ℃%(质量)H 2O -H 2SO 4系统的相图4. 298K时,已知反应2Hg(l) + 2AgCl(s) → Hg2Cl2(s)+2Ag(s)的∆r G m= -201.88kJ. mol-1, E(Ag+/Ag)=0.799V,K sp(AgCl)=1.76×10-10。
(1)将反应设计成电池并计算出该电池的标准电动势。
(2)计算E[AgCl(s)/Ag,Cl-]。
(3)若该电池电动势的温度系数(∂E/∂T)p=1×10-4V . K-1,计算该电池反应的∆r S m、∆r H m、Q r。
(15分)解:(1) 正极:2AgCl(s) +2e-→ 2Ag(s)+2Cl-负极:2Hg(l) +2Cl-→ Hg2Cl2(s) +2e-电池: Hg(l) | Hg2Cl2(s) | Cl-(a) | AgCl(s) | Ag电动势E= -∆r G m/zF= -(-201880J . mol-1)/(2×96500C . mol-1)=1.046V(2) 将反应AgCl(s) → Ag++Cl-设计成电池:正极:AgCl(s) +e-→ Ag(s)+Cl-负极:Ag(s) → Ag+ + e-电池:Ag(s) | Ag+ | Cl-| AgCl(s) | Ag(s)E= RT ln K/zF= RT ln K sp/zF = E[AgCl(s)/Ag,Cl-]- E[Ag+/Ag]E[AgCl(s)/Ag,Cl-]= E[Ag+/Ag]+RT ln K sp/zF= {0.799+0.05916×ln(1.75×10-10)}V = 0.222V∆r S m=zF(∂E/∂T) p =2×96500C . mol-1×1×10-4V . K-1=19.3 J . K-1 . mol-1Q r =T∆r S m= 298.15K×19.3 J . K-1 . mol-1=5754J . mol-1∆r H m=∆r G m+T∆r S m=∆r G m+Q r = -201.88kJ . mol-1+5754J . mol-1=-196.1kJ . mol-15. 某溶液含有NaOH 和CH3CO2C2H5,浓度均为0.0100mol . dm-3。
298.2K 时,反应经600s 有39.0% 的CH3CO2C2H5分解;而在308.2K 时,反应经600s 有55.0% 的分解。
已知该皂化反应为二级反应。
(1)求反应在两种温度下的速率常数。
(2)求反应的活化能。
(3)计算288.2K时的速率常数(4)计算288.2K时600s能分解多少? (15分)解:(1) 反应为NaOH +CH3CO2C2H5→CH3CO2Na+ C2H5OH该反应为二级且初浓度相同,故有-d c A/d t=kc A2 , c A=c A0(1-x),积分后得k= (1/t)(1/c A-1/c A0) = x/tc A0(1-x)298.2K 时,k=0.390/[600s×0.0100mol . dm-3×(1-0.390)]=0.107 mol-1 . dm3 . s-1308.2K 时,k’=0.550/[600s×0.0100mol . dm-3×(1-0.550)]=0.204 mol-1 . dm3 . s-1(2)E a = RTT’ln(k’/k)/(T’-T)= 8.3145J . K-1 . mol-1×298.2K×308.2K×ln(0.204/0.107)/(308.2K-298.2K)= 49.3 kJ . mol-1(3)288.2K时的速率常数k”:ln(k”/k)=E a (T”-T)/ RTT”ln(k”/0.107 mol-1 . dm3 . s-1)=49300J . mol-1×(288.2K-298.2K)/(8.3145J . K-1 . mol-1×298.2K×288.2K)k”= 0.0537 mol-1 . dm3 . s-1(4)x =1/(1+1/ktc A0) = 1/[1+1/( 0.0537 mol-1 . dm3 . s-1×600s×0.0100mol . dm-3)]= 0.244 =24.4%6. 某液体的表面张力与温度的关系如下:γ /(10-3N . m-1) =21.50 -0.086( t /℃)今将该液体在80℃及101325Pa 下等温可逆分散成球形小液滴,计算:(1)小液滴半径为1.00×10-7m 时的附加压力。
(2)该小液滴的饱和蒸气压。
(3)若将半径为1.00×10-7m 的毛细管插入该液体中,已知润湿角θ为20°,则管中液面将上升多少?已知80℃及101325Pa时该液体的密度为882kg . m-3,摩尔质量为74×10-3kg . mol-1,不考虑分散度对表面张力的影响。
(15分)解:(1) 80℃时的表面张力γ / (10-3N . m-1) =21.50 -0.086×80 =14.62∆p = 2γ/r = 2×14.62×10-3N . m-1/ 1.00×10-7m = 2.924×105Pa(2) 由开尔文公式RT ln(p r/p) = 2γM/ρr8.3145J . K-1 . mol-1×353.15K×ln(p r/101325Pa)=2×14.62×10-3N . m-1×74×10-3 kg . mol-1/(882kg . m-3×1.00×10-7m) p r = 102175Pa(3) ∆p = 2γ /r =2γ cos θ /r ’ = ρghh =2γ cos θ / ρgr ’ = 2×14.62×10-3N . m -1×cos20°/(882kg . m -3×9.80m . s -2×1.00×10-7m) = 31.8m7 (1) 10cm 3、0.02mol . dm -3 AgNO 3 溶液,缓慢地滴加到60cm 3、0.003 mol . dm -3 的KBr 溶液中,可制得AgBr 溶胶,写出其胶团结构的表示式,并指出该溶胶的电泳方向。