仪器分析第十二章习题解答PPT
- 格式:ppt
- 大小:60.00 KB
- 文档页数:7





仪器分析课后习题答案讲课稿仪器分析课后习题答案第一章绪论第二章光学分析法导论第三章紫外-可见吸收光谱法第四章红外吸收光谱法第五章分子发光分析法第六章原子发射光谱法第七章原子吸收与原子荧光光谱法第八章电化学分析导论第九章电位分析法第十章极谱分析法第十一章电解及库仑分析法第十二章色谱分析法第一章绪论1.解释下列名词:(1)仪器分析和化学分析;(2)标准曲线与线性范围;(3)灵敏度、精密度、准确度和检出限。
答:(1)仪器分析和化学分析:以物质的物理性质和物理化学性质(光、电、热、磁等)为基础的分析方法,这类方法一般需要特殊的仪器,又称为仪器分析法;化学分析是以物质化学反应为基础的分析方法。
(2)标准曲线与线性范围:标准曲线是被测物质的浓度或含量与仪器响应信号的关系曲线;标准曲线的直线部分所对应的被测物质浓度(或含量)的范围称为该方法的线性范围。
(3)灵敏度、精密度、准确度和检出限:物质单位浓度或单位质量的变化引起响应信号值变化的程度,称为方法的灵敏度;精密度是指使用同一方法,对同一试样进行多次测定所得测定结果的一致程度;试样含量的测定值与试样含量的真实值(或标准值)相符合的程度称为准确度;某一方法在给定的置信水平上可以检出被测物质的最小浓度或最小质量,称为这种方法对该物质的检出限。
2.对试样中某一成分进行5次测定,所得测定结果(单位μg ?mL -1)分别为 0.36,0.38,0.35,0.37,0.39。
(1)计算测定结果的相对标准偏差;(2)如果试样中该成分的真实含量是0.38μg ?mL -1,试计算测定结果的相对误差。
解:(1)测定结果的平均值37.0539.037.035.038.036.0=++++=x μg ?mL -1 标准偏差122222120158.015)37.039.0()37.037.0()37.035.0()37.038.0()37.036.0(1)(-=?=--+-+-+-+-=--=∑mL g n x x s n i i μ相对标准偏差 %27.4%10037.00158.0%100=?=?=x s sr (2)相对误差 %63.2%10038.038.037.0%100-=?-=?-=μμx Er 。

现代仪器分析习题解答2009年春第12章电位分析及离子选择性电极分析法P2161.什么是电位分析法?什么是离子选择性电极分析法?答:利用电极电位和溶液中某种离了的活度或浓度Z间的关系來测定待测物质活度或浓度的电化学分析法称为电位分析法。
以离子选择性电极做指示电极的电位分析,称为离子选择性电极分析法。
2.何谓电位分析中的指示电极和参比屯极?金属基电极和膜电极冇何区别?答:电化学中把电位随溶液中待测离了活度或浓度变化而变化,并能反映出待测离了活度或浓度的电极称为指示电极。
电极电位恒定,不受溶液组成或电流流动方向变化影响的电极称为参比电极。
金属基电极的敏感膜是由离子交换型的刚性基质玻璃熔融烧制而成的。
膜电极的敏感膜一般是由在水中溶解度很小,11能导屯的金属难溶盐经加压或拉制而成的单晶、多晶或混晶活性膜。
4.何谓TISAB溶液?它有哪些作用?答:在测定溶液屮加入大量的、对测定离子不干扰的惰性电解质及适量的pH缓冲剂和一定的掩蔽剂,构成总离子强度调节缓冲液(TISAB)。
其作用有:恒定离了强度、控制溶液pH、消除干扰离了影响、稳定液接电位。
5.25°C时,用pH=4.00的标准缓冲溶液测得电池:“玻璃电极I H+ (a=X mol.L1) |饱和甘汞电极”的电动势为0.814V,那么在6?(HA C)=1.00X103 mol.L-1的醋酸溶液中,此电池的电动势为多少?(K H Ac=1.8X10t设a H+=[H+])解:•产(p 叶申孑(p(+)- (K-0. 0592pHi)E2= (p(+>-</)(-)=(p(+)- (K-0. 0592pH2)/.E2- Ei= E2-0. 814=0. 0592 (pH2- pH】)AE2=0. 814+0. 0592(-lg VKc^4. 00) =0. 806 (V)6.25°C时,用pH二5. 21的标准缓冲溶液测得电池:“玻璃电极I H~ (a=X mol.If1) |饱和甘汞电极”的电动势为0. 209V,若用四种试液分别代替标准缓冲溶液,测得电动势分别为①0.064V;②0. 329V;③0. 510V;④0. 677V,试求各试液的pH和K活度解:(1) A E F O. 064-0. 209=0. 0592 (pH-pH s)VpH s=5. 21・・・pHf2. 76 a H=l. 74X10-3 mol.L-1(2) A E2=0. 329-0. 209=0. 0592 (pH2-pH s)VpH s=5.21(3) A E3=0. 510-0. 209=0. 0592 (pH:厂pH JVpH s=5. 21・・・pll3 二10.29 a H-=5. 10X10-11 mol.L-1(4) A E F O. 677-0. 209=0. 0592 (pH 厂pH JVpH =5. 21・・・pH尸13. 12 a lf=7. 60X10-14 mol .If17.25°C时,电池:“镁离子电极I Mg2+ (a=1.8X10-3mol.L_1) |饱和甘汞电极”的电动势为0.411V,用含\1尹试液代替已知溶液,测得电动势为0.439V,试求试液屮的pMg值。
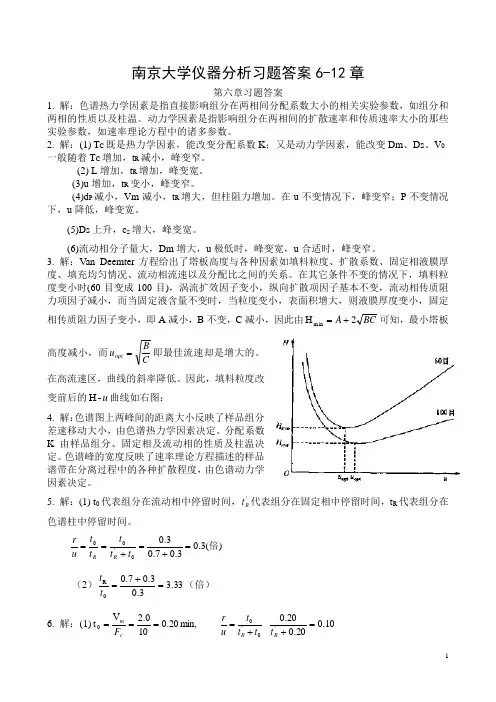
南京大学仪器分析习题答案6-12章第六章习题答案1. 解:色谱热力学因素是指直接影响组分在两相间分配系数大小的相关实验参数,如组分和两相的性质以及柱温。
动力学因素是指影响组分在两相间的扩散速率和传质速率大小的那些实验参数,如速率理论方程中的诸多参数。
2. 解:(1) T C 既是热力学因素,能改变分配系数K ;又是动力学因素,能改变Dm 、Ds 、V 0。
一般随着T C 增加,t R 减小,峰变窄。
(2) L 增加,t R 增加,峰变宽。
(3)u 增加,t R 变小,峰变窄。
(4)d P 减小,Vm 减小,t R 增大,但柱阻力增加。
在u 不变情况下,峰变窄;P 不变情况下,u 降低,峰变宽。
(5)Ds 上升,c s 增大,峰变宽。
(6)流动相分子量大,Dm 增大,u 极低时,峰变宽,u 合适时,峰变窄。
3. 解:Van Deemter 方程给出了塔板高度与各种因素如填料粒度、扩散系数、固定相液膜厚度、填充均匀情况、流动相流速以及分配比之间的关系。
在其它条件不变的情况下,填料粒度变小时(60目变成100目),涡流扩效因子变小,纵向扩散项因子基本不变,流动相传质阻力项因子减小,而当固定液含量不变时,当粒度变小,表面积增大,则液膜厚度变小,固定相传质阻力因子变小,即A 减小,B 不变,C 减小,因此由BC A 2H min +=可知,最小塔板高度减小,而CB u opt =即最佳流速却是增大的。
在高流速区,曲线的斜率降低。
因此,填料粒度改变前后的u -H 曲线如右图:4. 解:色谱图上两峰间的距离大小反映了样品组分差速移动大小,由色谱热力学因素决定。
分配系数K 由样品组分、固定相及流动相的性质及柱温决定。
色谱峰的宽度反映了速率理论方程描述的样品谱带在分离过程中的各种扩散程度,由色谱动力学因素决定。
5. 解:(1) t 0代表组分在流动相中停留时间,'R t 代表组分在固定相中停留时间,t R 代表组分在色谱柱中停留时间。

第一章绪论第二章光学分析法导论第三章紫外-可见吸收光谱法第四章红外吸收光谱法第五章分子发光分析法第六章原子发射光谱法第七章原子吸收与原子荧光光谱法第八章电化学分析导论第九章电位分析法第十章极谱分析法第十一章电解及库仑分析法第十二章色谱分析法第一章绪论1.解释下列名词:(1)仪器分析与化学分析;(2)标准曲线与线性范围;(3)灵敏度、精密度、准确度与检出限。
答:(1)仪器分析与化学分析:以物质的物理性质与物理化学性质(光、电、热、磁等)为基础的分析方法,这类方法一般需要特殊的仪器,又称为仪器分析法;化学分析就是以物质化学反应为基础的分析方法。
(2)标准曲线与线性范围:标准曲线就是被测物质的浓度或含量与仪器响应信号的关系曲线;标准曲线的直线部分所对应的被测物质浓度(或含量)的范围称为该方法的线性范围。
(3)灵敏度、精密度、准确度与检出限:物质单位浓度或单位质量的变化引起响应信号值变化的程度,称为方法的灵敏度;精密度就是指使用同一方法,对同一试样进行多次测定所得测定结果的一致程度;试样含量的测定值与试样含量的真实值(或标准值)相符合的程度称为准确度;某一方法在给定的置信水平上可以检出被测物质的最小浓度或最小质量,称为这种方法对该物质的检出限。
2. 对试样中某一成分进行5次测定,所得测定结果(单位μg ⋅mL -1)分别为 0、36,0、38,0、35,0、37,0、39。
(1) 计算测定结果的相对标准偏差;(2) 如果试样中该成分的真实含量就是0.38μg ⋅mL -1,试计算测定结果的相对误差。
解:(1)测定结果的平均值37.0539.037.035.038.036.0=++++=x μg ⋅mL -1 标准偏差122222120158.015)37.039.0()37.037.0()37.035.0()37.038.0()37.036.0(1)(-=⋅=--+-+-+-+-=--=∑mL g n x x s n i iμ相对标准偏差%27.4%10037.00158.0%100=⨯=⨯=x s s r (2)相对误差%63.2%10038.038.037.0%100-=⨯-=⨯-=μμx E r 。


第八章 电化学分析导论1. 答:液接电位产生于具有不同电解质或浓度不同的同种电解质溶液界面之间,由于离子扩散通过界面的速率不同有微小的电位差产生,这种电位差称为液接电位。
2. 答:负极:电子流出的极 正极:电子流入的极 阴极:接电源负极 阳极:接电源正极3. 答:指示电极:在电化学测试过程中,溶液主体浓度不发生变化的电极 参比电极:在测量过程中,具有恒定电位的电极 4:解:左: 2Zn ++ 2e = Znϕ左=2,Zn Znφϕ++0.05922lg 2Zn +⎡⎤⎣⎦ =-0.764+0.05922lg0.1=-0.793V右: Ag e Ag ++=,0.0592lg AgAgAg φϕϕ++⎡⎤=+⎣⎦右 0.7990.0592lg0.01=+=0.681VE ϕϕ=-右左()0.6810.793=--=1.474V0E >,所以是原电池。
5.解:左边: 2222HA eH A -++20.0592lg H H H φϕϕ++⎡⎤=+⎣⎦左,20.0592lg H HH φϕϕ++⎡⎤=+⎣⎦左,=0.0592lg H +⎡⎤⎣⎦E ϕϕ=-右左0.4130.2440.0592l gH +⎡⎤=-⎣⎦ 0.0592lg 0.169H +⎡⎤=-⎣⎦31.410/H mol l +-⎡⎤=⨯⎣⎦[]HA H A H A K HA +-+-=+⎡⎤⎡⎤⎣⎦⎣⎦==31.4100.1160.215-⨯⨯=47.610-⨯ 6.解:E ϕϕ=-右左0.9210.2443ϕ=-左0.6767V ϕ=-左左边:2424CdX eCd X --++22,0.0592lg 2CdCdCd φϕϕ++⎡⎤=+⎣⎦左 2244Cd XCdX +-+2442CdX K Cd X -+-⎡⎤⎣⎦=⎡⎤⎡⎤⎣⎦⎣⎦稳2424CdX Cd K X -+-⎡⎤⎣⎦⎡⎤=⎣⎦⎡⎤⎣⎦稳2244,0.0592lg2CdCdCdX K X φϕϕ+--⎡⎤⎣⎦=+⎡⎤⎣⎦左稳[]40.05920.20.67670.403lg 20.150K -=-+稳 117.010K =⨯稳7.解:E ϕϕ=-右左 0.8930.2443ϕ=-左0.6487V ϕ=-左222CdX eCd X -++22,0.0592lg 2CdCdCd φϕϕ++⎡⎤=+⎣⎦左 22Cd X CdX -+22sp K Cd X +-⎡⎤⎡⎤=⎣⎦⎣⎦ 22sp K Cd X +-⎡⎤=⎣⎦⎡⎤⎣⎦22,0.0592lg 2sp CdCdK X φϕϕ+-=+⎡⎤⎣⎦左 []20.05920.64870.403lg 20.02sp K -=-+122.010sp K -=⨯第九章 电位分析法1.答:玻璃膜的化学组成对电极的性能影响很大,纯2SiO 制成的石英玻璃就不具有响应氢离子的功能。