石灰软化处理的石灰加量如何估算
- 格式:docx
- 大小:13.31 KB
- 文档页数:2

石灰软化除硬计算公式石灰软化除硬是一种常见的水处理方法,用于去除水中的硬度物质,如钙和镁。
这种方法通过与水中的硬度物质发生化学反应,将其转化为不溶性的沉淀物,从而达到软化水的目的。
在实际应用中,需要根据水的硬度和处理量来确定所需的石灰用量,因此需要使用相应的计算公式来进行计算。
石灰软化除硬的计算公式主要涉及到两个方面,一是确定所需的石灰用量,二是计算反应后生成的沉淀物量。
下面将分别介绍这两个方面的计算公式。
1. 确定石灰用量的计算公式。
石灰软化除硬的关键是要确定适当的石灰用量,以确保水中的硬度物质能够完全被沉淀。
一般来说,石灰的用量取决于水的硬度和处理量。
下面是确定石灰用量的计算公式:石灰用量(kg)= (水的硬度×处理量)/ (100 ×反应效率)。
其中,水的硬度以CaCO3计算,单位为mg/L;处理量为软化水的总体积,单位为L;反应效率是指石灰与水中的硬度物质发生反应后,生成的沉淀物的质量占石灰用量的百分比,一般取值为80%。
举个例子,如果要处理一批硬度为300mg/L的水,总体积为1000L,那么石灰用量的计算公式为:石灰用量(kg)= (300mg/L × 1000L)/ (100 × 80%)= 3.75kg。
因此,需要使用3.75kg的石灰来处理这批水。
2. 计算沉淀物量的计算公式。
石灰软化除硬后,水中的硬度物质会与石灰发生反应生成沉淀物。
为了确定生成的沉淀物量,可以使用下面的计算公式:沉淀物量(kg)= 石灰用量×反应效率。
继续以上面的例子,如果使用了3.75kg的石灰来处理水,那么生成的沉淀物量为:沉淀物量(kg)= 3.75kg × 80% = 3kg。
因此,处理这批水后会生成3kg的沉淀物。
总结。
石灰软化除硬的计算公式涉及到石灰用量和生成的沉淀物量两个方面。
通过使用这些计算公式,可以确定在处理不同硬度和量的水时所需的石灰用量,以及生成的沉淀物量。


石灰软化水的用量计算公式水是生活中不可或缺的重要物质,但有时候水中的硬度会对我们的生活造成一定的影响。
硬水中含有大量的钙和镁离子,这些离子会与肥皂和洗涤剂发生化学反应,导致肥皂不易起泡,同时还会在管道和设备上形成水垢,影响设备的正常运行。
因此,软化水是一种常见的水处理方式,而石灰软化水是其中的一种方法。
石灰软化水是通过向水中添加石灰来沉淀出水中的钙和镁离子,从而达到软化水的目的。
在进行石灰软化水处理时,需要根据水的硬度和处理量来计算石灰的用量,以确保软化水的效果。
下面我们将介绍石灰软化水的用量计算公式及其具体应用。
石灰软化水的用量计算公式如下:石灰用量 = (水的硬度×处理量)/ (石灰的纯度× 1000)。
其中,石灰用量的单位为克(g),水的硬度的单位为mg/L,处理量的单位为L,石灰的纯度为百分数。
首先,我们需要了解水的硬度。
水的硬度通常是以钙碳酸盐和镁碳酸盐的形式存在,硬度的单位通常为mg/L。
在进行石灰软化水处理前,需要对水进行化验,得到水的硬度值。
其次,我们需要确定处理量。
处理量是指需要进行软化水处理的水的总量,通常以升(L)为单位。
最后,我们需要知道石灰的纯度。
石灰的纯度是指石灰中有效成分的含量,通常以百分数表示。
在进行石灰软化水处理时,需要选择纯度较高的石灰,以确保软化水的效果。
通过以上三个参数,我们就可以根据石灰软化水的用量计算公式计算出所需的石灰用量。
以确保软化水的效果。
举个例子来说明石灰软化水的用量计算公式的具体应用。
假设我们需要软化一批水,其硬度为200mg/L,处理量为1000L,而我们选择的石灰纯度为90%。
那么我们可以按照以下步骤计算出所需的石灰用量:石灰用量 = (200mg/L × 1000L)/ (90% × 1000) = 222.22g。
通过以上计算,我们可以得出所需的石灰用量为222.22克。
这样,我们就可以根据计算出的石灰用量进行软化水处理,以达到软化水的效果。

石灰软化法使用石灰软化硬水的方法称为石灰软化法,又称石灰纯碱软化法,在硬水中加入消石灰,使水中的镁生成氢氧化镁沉淀,这样,加入碳酸钠使水中的钙生成碳酸钙而沉淀,硬水即变为软水,利用这种方法可使水中钙浓度降低到10~35ppm。
其化学反应式如下:CaSO4+Na2CO3→CaCO3↓+Na2SO4CaCl2+Na2CO3→CaCO3↓+2NaClMgSO4+Na2CO3→MgCO3+Na2CO3MgCO3+Ca(OH)2→CaCO3↓+Mg(OH)2↓采用石灰软化法处理高硬度含氟地下水,考察了药剂投量、反应时间对处理效果的影响。
结果表明,在CaO和Na2CO3的投量分别为187和106mg/L并反应25min的条件下,再投加10mg/L的聚合氯化铝铁和0.25mg/L的PAM可将出水浊度降至1NUT以下;若要将出水总硬度分别降至400、300、200mg/L,在略高于理论投药量的条件下,需控制搅拌反应时间分别为25、35、50min;水中氟化物可通过与软化过程中生成的Mg(OH)2形成共沉淀而得到有效去除,但由于出水pH值过高,需进行调节。
华东地区某市因地表水污染严重,计划适度开采高储量的地下水作为饮用水水源(开采量约为5.0×10 m /d)。
取样分析结果表明,该市地下水清澈透明,但水中硬度和氟化物含量不达标,为保证居民饮水安全,需对该地下水进行软化及除氟处理。
降低水中硬度的常用方法有离子交换法、电渗析法及药剂软化法等。
其中离子交换法和电渗析法均存在造价高、运行费用高等缺点;石灰是药剂软化法中最常用的药剂,其价格较低,但如果用量不当,则会造成出水水质稳定性欠佳,给实际操作管理带来麻烦,因此有必要进行试验确定药剂用量。
去除氟离子的常用方法有电化学法(电凝聚、电渗析)、·49·第23卷第13期中国给水排水www.watergasheat.corn 混凝沉淀法和离子交换法等。

水的软化几种方法通常对硬度高、碱度高的水采用石灰软化法;对硬度高、碱度低的水采用石灰-纯碱软化法;而对硬度低、碱度高的负硬水则采用石灰-石膏处理法。
1. 石灰软化法为避免投加生石灰(CaO)产生的灰尘污染,通常先将生石灰制成消石灰Ca(OH)2(即熟石灰)使用,其反应如下CaO+H2O====Ca(OH)2消石灰投入高硬水中,会产生下列反应Ca(OH)2+CO2====CaCO3+H2OCa(OH) 2+Ca(HCO3) 2====2CaCO3+2H2O2Ca(OH) 2+Mg(HCO3) 2====2CaCO3+Mg(OH) 2+2H2O形成的CaCO3和Mg(OH)2都是难溶化合物,可从水中沉淀析出。
但水中的永硬和负硬却不能用石灰处理的方法除去,因为镁的永硬与负硬和消石灰会产生下列反应MgSO4+Ca(OH) 2====Mg(OH) 2+CaSO4MgCl2+Ca(OH) 2====Mg(OH) 2+CaCl2NaHCO3+Ca(OH) 2====CaCO3+NaOH+H2O由反应式可看出,镁的永硬全部转化为等量的溶解度很大的钙的永硬,而负硬则转化为等量的氢氧化钠、碱度,所以水中的碱度没有除去。
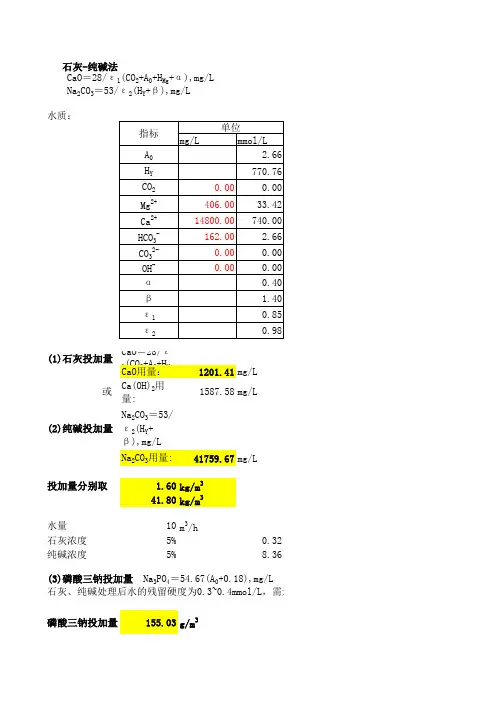
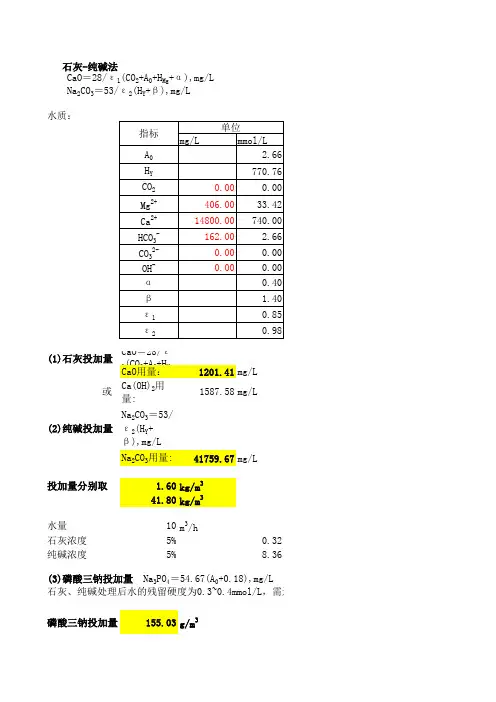
石灰加入量可按下式估算[CaO]=28/Z1{[CO2]+[Ca(HCO3) 2]+2[Mg(HCO3)2+B]}式中[CaO]——需投加的工业石灰量,mg/L;[CO2]——原水中CO2的浓度(1/2CO2计),mmol/L;[Ca(HCO3) 2]——原水中Ca(HCO3) 2的浓度[1/2Ca(HCO3) 2计],mmol/L[Mg(HCO3) 2]——原水中Mg(HCO3) 2的浓度[1/2 Mg(HCO3) 2计]mmol/L;Z1——工业石灰纯度,%;28——1/2CaO的摩尔质量,g/mol;B——石灰过剩量(1/2CaO计),mmol/L(一般为0.2—0.4mmol/L)。
2.石灰-纯碱软化法石灰软化法只适用于暂硬高、永硬低的水质处理。

石灰软化法使用石灰软化硬水的方法称为石灰软化法,又称石灰纯碱软化法,在硬水中加入消石灰,使水中的镁生成氢氧化镁沉淀,这样,加入碳酸钠使水中的钙生成碳酸钙而沉淀,硬水即变为软水,利用这种方法可使水中钙浓度降低到10~35ppm。
其化学反应式如下:CaSO4+Na2CO3→CaCO3↓+Na2SO4CaCl2+Na2CO3→CaCO3↓+2NaClMgSO4+Na2CO3→MgCO3+Na2CO3MgCO3+Ca(OH)2→CaCO3↓+Mg(OH)2↓采用石灰软化法处理高硬度含氟地下水,考察了药剂投量、反应时间对处理效果的影响。
结果表明,在CaO和Na2CO3的投量分别为187和106mg/L并反应25min的条件下,再投加10mg/L的聚合氯化铝铁和0.25mg/L的PAM可将出水浊度降至1NUT以下;若要将出水总硬度分别降至400、300、200mg/L,在略高于理论投药量的条件下,需控制搅拌反应时间分别为25、35、50min;水中氟化物可通过与软化过程中生成的Mg(OH)2形成共沉淀而得到有效去除,但由于出水pH值过高,需进行调节。
华东地区某市因地表水污染严重,计划适度开采高储量的地下水作为饮用水水源(开采量约为5.0×10 m /d)。
取样分析结果表明,该市地下水清澈透明,但水中硬度和氟化物含量不达标,为保证居民饮水安全,需对该地下水进行软化及除氟处理。
降低水中硬度的常用方法有离子交换法、电渗析法及药剂软化法等。
其中离子交换法和电渗析法均存在造价高、运行费用高等缺点;石灰是药剂软化法中最常用的药剂,其价格较低,但如果用量不当,则会造成出水水质稳定性欠佳,给实际操作管理带来麻烦,因此有必要进行试验确定药剂用量。
去除氟离子的常用方法有电化学法(电凝聚、电渗析)、·49·第23卷第13期中国给水排水www.watergasheat.corn 混凝沉淀法和离子交换法等。

石灰用量计算4%、6%、8%、12%灰土石灰用量计算一、材料费计算通过击实试验,得出以下数据:4%灰土最大干密度cm3 最佳含水量%6%灰土最大干密度cm3 最佳含水量%8%灰土最大干密度cm3 最佳含水量%6%灰土最大干密度cm3 最佳含水量%4%灰土石灰用量计算:每一方4%灰土最大总质量为:M灰土=ρ灰土*v=1689Kg*1m3=1689 Kg干混合料质量为:M干混合料=M灰土/(1+w最佳)=1689Kg/(1+%)=干土质量:M干土= M干混合料/(1+4%)= Kg/(1+4%)=干灰质量:M干灰质量=M干混合料- M干土= Kg=通过石灰含水量试验得出:石灰天然含水量为w灰=%所以石灰的质量为:M干灰质量*(1+%)=*(1+%)=6%灰土石灰用量计算:每一方6%灰土最大总质量为:M灰土=ρ灰土*v=1672Kg*1m3=1672 Kg干混合料质量为:M干混合料=M灰土/(1+w最佳)=1672Kg/(1+%)= Kg干土质量:M干土= M干混合料/(1+6%)= Kg/(1+6%)= Kg干灰质量:M干灰质量=M干混合料- M干土= Kg= Kg通过石灰含水量试验得出:石灰天然含水量为w灰=%所以石灰的质量为:M干灰质量*(1+%)=*(1+%)= Kg 8%灰土石灰用量计算:每一方8%灰土最大总质量为:M灰土=ρ灰土*v=1659Kg*1m3=1659Kg干混合料质量为:M干混合料=M灰土/(1+w最佳)=1659Kg/(1+%)= Kg干土质量:M干土= M干混合料/(1+6%)= Kg/(1+8%)=干灰质量:M干灰质量=M干混合料- M干土= =通过石灰含水量试验得出:石灰天然含水量为w灰=%所以石灰的质量为:M干灰质量*(1+%)=*(1+%)= Kg 12%灰土石灰用量计算:每一方12%灰土最大总质量为:M灰土=ρ灰土*v=1642Kg*1m3=1642Kg干混合料质量为:M干混合料=M灰土/(1+w最佳)=1642Kg/(1+%)=干土质量:M干土= M干混合料/(1+6%)= Kg/(1+12%)=干灰质量:M干灰质量=M干混合料- M干土=通过石灰含水量试验得出:石灰天然含水量为w灰=%所以石灰的质量为:M干灰质量*(1+%)=*(1+%)=。

软化的几种方法:当硬度高、碱度也高的水直接作补充水进入循环冷却水系统后,会使循环水水质处理的难度增大,同时浓缩倍数的提高也受到限制。
另外高硬水也不宜直接作锅炉水的给水。
立式水管锅炉、立式火管锅炉及卧式内燃锅炉的给水总硬度要求在4.0mmol/L以下。
总硬度过高的水不能直接采用离子交换方法达到软化水的要求,经济效果也不好。
碱度过高的水,也不能直接作为锅炉的补给水。
所以上述这类水质均需在进入冷却水系统、锅炉和离子交换软化系统前,首先采用化学药剂方法进行预处理。
(一)软化方法通常对硬度高、碱度高的水采用石灰软化法;对硬度高、碱度低的水采用石灰-纯碱软化法;而对硬度低、碱度高的负硬水则采用石灰-石膏处理法。
1.石灰软化法为避免投加生石灰(CaO)产生的灰尘污染,通常先将生石灰制成消石灰Ca(OH)2(即熟石灰)使用,其反应如下CaO+H2O====Ca(OH)2消石灰投入高硬水中,会产生下列反应Ca(OH)2+CO2====CaCO3 +H2OCa(OH) 2+Ca(HCO3) 2====2CaCO3 +2H2O2Ca(OH) 2+Mg(HCO3) 2====2CaCO3 +Mg(OH) 2+2H2O形成的CaCO3和Mg(OH)2都是难溶化合物,可从水中沉淀析出。
但水中的永硬和负硬却不能用石灰处理的方法除去,因为镁的永硬与负硬和消石灰会产生下列反应MgSO4+Ca(OH) 2====Mg(OH) 2 +CaSO4MgCl2+Ca(OH) 2====Mg(OH) 2 +CaCl2NaHCO3+Ca(OH) 2====CaCO3 +NaOH+H2O由反应式可看出,镁的永硬全部转化为等量的溶解度很大的钙的永硬,而负硬则转化为等量的氢氧化钠、碱度,所以水中的碱度没有除去。
石灰加入量可按下式估算[CaO]=28/☪1{[CO2]+[Ca(HCO3) 2]+2[Mg(HCO3)2+ ]}式中 [CaO]——需投加的工业石灰量,mg/L;[CO2]——原水中CO2的浓度(1/2CO2计),mmol/L;[Ca(HCO3) 2]——原水中Ca(HCO3) 2的浓度[1/2Ca(HCO3) 2计],mmol/L[Mg(HCO3) 2]——原水中Mg(HCO3) 2的浓度[1/2 Mg(HCO3) 2计]mmol/L;☪1——工业石灰纯度,%;28——1/2CaO的摩尔质量,g/mol;——石灰过剩量(1/2CaO计),mmol/L(一般为0.2—0.4mmol/L)。

水质:CaO 用量:198.08mg/L Ca(OH)2用量:261.75mg/L 实际用量:373.92mg/L 利用率取70%水质:CaO 用量:227.94mg/L Ca(OH)2用量:301.20mg/L 实际用量:430.29mg/L 利用率取70%(2)当H Ca <H Z 时,按下式计算CaO =28(2Hz-H Ca +CO 2+Fe+K+α),mg/L(1)当H Ca ≥H Z 时,按下式计算CaO =28(Hz+CO 2+Fe+K+α),mg/LCa(OH)2=CaO*74/56,mg/L实际用量=Ca(OH)2用量/(0.5-0.8),石灰有效利用率50%-80%Ca(OH)2=CaO*74/56,mg/L实际用量=Ca(OH)2用量/(0.5-0.8),石灰有效利用率50%-80%石灰处理后的水质水质:Hc=2.93mmol/L 式中:g c---石灰处理后水中残留的溶解固体(mg/L)g Y ---原水中的溶解固体(mg/L)50---1/2CaCO 3的摩尔质量(mg/mmol)37---1/2Ca(OH)2的摩尔质量(mg/mmol)42---1/2MgCO 3的摩尔质量(mg/mmol)8----1/2CaCO 3与1/2MgCO 3的摩尔质量差值(mg/mmol)H Mg ---原水中的镁硬度(mmol/L)M gc---石灰处理后水中残留的镁硬度(mmol/L)(O r )----水中耗氧量的降低值(mg/L)水质:(1)当H Ca ≥Hz时,g c =g Y -50(Hz-Hzc)+8(H Mg -Mgc)+37α+48K-3.5(O r )H ZC ---软化后水中残留的碳酸盐硬度(mmol/L),一般为0.5-1.0mmol/L石灰处理后,由于碳酸盐硬度降低,去除了碳酸钙和氢氧化镁,相应减少了原水中的溶解固体,因此水中剩余的溶解固体近似值可用下式计算:经石灰处理后,水中OH-剩余量保持在0.1-0.2mmol/L的范围内,水中碳酸盐硬度大部分被除掉,根据加药量及水温的不同,残留碳酸盐硬度可降低到0.5-1.0mmol/L,残余碱度达0.8-1.2mmol/L,有机物去除25%左右,硅化物去除30%-35%,铁的残留量<0.1mg/L,出水悬浮物<20mg/L,一般可达10mg/L以下,pH=10-10.3。
发酵料中石灰用量计算公式一、引言。
发酵料是一种常见的有机肥料,它可以提高土壤的肥力和改善土壤结构,是农业生产中不可或缺的重要物质。
而石灰是发酵料中常用的一种添加剂,它可以调节发酵料的酸碱度,促进有机物质的分解和转化,提高发酵效果。
因此,合理计算发酵料中石灰的用量是十分重要的。
二、石灰用量计算公式。
在发酵料的制作过程中,石灰的用量计算是根据原料的酸碱度和发酵料的体积来确定的。
一般来说,可以使用以下的计算公式来确定石灰的用量:石灰用量(kg)=(原料总重量(kg)×原料酸碱度)÷发酵料体积(m³)。
其中,原料总重量是指发酵料中所有原料的总重量,原料酸碱度是指原料的PH值,发酵料体积是指发酵料的总体积。
三、石灰用量计算公式的应用。
1. 确定原料总重量。
在进行发酵料的制作前,首先需要确定所有原料的总重量。
这些原料可以包括秸秆、畜禽粪便、菜渣等有机物质。
通过称重的方式可以得到原料的总重量。
2. 测定原料酸碱度。
原料的酸碱度是指原料的PH值,它可以通过PH试纸或PH计来测定。
一般来说,发酵料的理想酸碱度在6-8之间,如果原料的酸碱度偏低,可以适量添加石灰来提高酸碱度。
3. 确定发酵料体积。
发酵料的体积可以通过测量发酵堆的长、宽、高来计算得到。
一般来说,发酵料的体积越大,需要的石灰用量也会相应增加。
通过以上三个步骤,就可以得到石灰的用量。
在实际操作中,需要根据具体情况进行调整,以确保发酵料的酸碱度和发酵效果达到最佳状态。
四、石灰用量计算公式的意义。
合理计算石灰的用量可以帮助农民和生产者在发酵料的制作过程中节约成本,提高发酵效果。
一方面,过少的石灰用量可能导致发酵料酸碱度过低,影响发酵效果;另一方面,过多的石灰用量则会增加生产成本,降低经济效益。
因此,通过石灰用量计算公式的应用,可以更好地控制石灰的用量,提高发酵料的质量和产量。
五、结论。
发酵料中石灰用量的计算是发酵料制作过程中的重要环节,它可以帮助生产者合理控制石灰的用量,提高发酵效果,降低生产成本。
石灰软化处理的石灰加量如何估算石灰软化处理的石灰加量如何估算石灰软化处理中所发生的全部反应很复杂,除主要沉淀反应外还有共沉淀及吸附反应。
所以石灰加量难以计算得十分精确。
但可以根据主要反应估算,能基本满足生产需要。
在实际处理时可以根据估算量通过调整试验确定最佳加量。
处理的目的与要求不同,加量也不同。
当不加混凝剂时,估算如下:(1)只要求消除Ca(HCO3)2,不要求除Mg(HCO3)2。
石灰主要与CO2及Ca(HCO3)2起反应,则石灰加量D1为:D1=[CO2]+[Ca(HCO3)2mmol/L或mol/m3式中[CO2]、[Ca (HCO3)2]分别为各自在原水中的物质的量浓度,mmol/L或mol/m3。
石灰软化处理中所发生的全部反应很复杂,除主要沉淀反应外还有共沉淀及吸附反应。
所以石灰加量难以计算得十分精确。
但可以根据主要反应估算,能基本满足生产需要。
在实际处理时可以根据估算量通过调整试验确定最佳加量。
处理的目的与要求不同,加量也不同。
当不加混凝剂时,估算如下:(1)只要求消除Ca(HCO3)2,不要求除Mg(HCO3)2。
石灰主要与CO2及Ca(HCO3)2起反应,则石灰加量D1为:D1=[CO2]+[Ca(HCO3)2mmol/L或mol/m3式中[CO2]、[Ca (HCO3)2]分别为各自在原水中的物质的量浓度,mmol/L或mol/m3。
因此,加混凝剂时估算的石灰总加量D为:D=(D1、D2或D3)+D A+0.1 mmol/L或mol/m3以上的D1、D2、D3、D A及D的石灰加量均按100%CaO计,实际加量需按石灰产品的纯度进行折合。
总硬度是指水中Ca2+、Mg2+的总量,它包括暂时硬度和永久硬度。
总硬度mg/L=V*c*100.09*1000/V0V--滴定消耗EDTA的体积c--EDTA的浓度V0--水样的体积100.09--1mL1mol/LEDTA相当于CaCO3的质量总碱度mg/L=V*c*50.04*1000/V0V--滴定消耗HCl的体积c--HCl的浓度V0--水样的体积50.04--1mL1mol/LHCl相当于CaCO3的质量总硬度总碱度均以CaCO3计。
石灰软化处理的石灰加量如何估算石灰软化处理中所发生的全部反应很复杂,除主要沉淀反应外还有共沉淀及吸附反应。
所以石灰加量难以计算得十分精确。
但可以根据主要反应估算,能基本满足生产需要。
在实际处理时可以根据估算量通过调整试验确定最佳加量。
处理的目的与要求不同,加量也不同。
当不加混凝剂时,估算如下:
(1)只要求消除Ca(HCO3)2,不要求除Mg(HCO3)2。
石灰主要与CO2及Ca(HCO3)2起反应,则石灰加量D1为:
D1=[CO2]+[Ca(HCO3)2mmol/L或mol/m3式中[CO2]、[Ca(HCO3)2]分别为各自在原水中的物质的量浓度,mmol/L或mol/m3。
石灰软化处理中所发生的全部反应很复杂,除主要沉淀反应外还有共沉淀及吸附反应。
所以石灰加量难以计算得十分精确。
但可以根据主要反应估算,能基本满足生产需要。
在实际处理时可以根据估算量通过调整试验确定最佳加量。
处理的目的与要求不同,加量也不同。
当不加混凝剂时,估算如下:
(1)只要求消除Ca(HCO3)2,不要求除Mg(HCO3)2。
石灰主要与CO2及Ca(HCO3)2起反应,则石灰加量D1为:
D1=[CO2]+[Ca(HCO3)2mmol/L或mol/m3式中[CO2]、[Ca(HCO3)2]分别为各自在原水中的物质的量浓度,mmol/L或mol/m3。
因此,加混凝剂时估算的石灰总加量D为:
D=(D1、D2或D3)+D A+0.1 mmol/L或mol/m3
以上的D1、D2、D3、D A及D的石灰加量均按100%CaO计,实际加量需按石灰产品的纯度进行折合。
总硬度是指水中Ca2+、Mg2+的总量,它包括暂时硬度和永久硬度。
总硬度mg/L=V*c*100.09*1000/V0
V--滴定消耗EDTA的体积
c--EDTA的浓度
V0--水样的体积
100.09--1mL1mol/LEDTA相当于CaCO3的质量总碱度mg/L=V*c*50.04*1000/V0
V--滴定消耗HCl的体积
c--HCl的浓度
V0--水样的体积
50.04--1mL1mol/LHCl相当于CaCO3的质量总硬度总碱度均以CaCO3计。