分析化学-中国海洋大学
- 格式:doc
- 大小:71.50 KB
- 文档页数:6


中国海洋大学本科生课程大纲课程属性:公共基础/通识教育/学科基础/专业知识/工作技能,课程性质:必修、选修一、课程介绍1.课程描述:生物化学是生命科学中重要的领域,尤其与临床医学和药学的关系密切,是一门理论性与验证性很强的学科。
生物化学实验教学应用化学的方法和手段来研究生物有机体的物质组成及变化。
其作用是使学生在生化实验技术、仪器的使用、分析和解决问题能力等方面有所提高;同时使学生掌握一般生物化学实验中的实验原理和操作方法。
2.设计思路:本课程内容设置包括糖、蛋白质、核酸、酶方面的基本实验,以及为培养学生应用能力和创新能力的综合实验。
除了涵盖生物化学研究中常用的方法和技术外,还包括了药学科研中常用的高通量与微量分析的新技术和新方法。
3. 本课程与其他课程的关系:先修课程:《无机化学》、《分析化学》、《有机化学》;并行课程:《生物化学》、《微生物学实验》等;后置课程:《分子生物学》、《药物化学》等。
二、课程目标生物化学实验课程的教学目标是使学生熟悉并掌握生物化学和分子生物学技术中- 1 -的基本实验操作,了解本门技术在药学领域中的应用前景,培养学生的基本研究技能及综合实践能力。
通过本课程使学生对现代生物化学实验方法与实验原理有一定的了解,增强学生解决实际问题的能力。
三、学习要求生物化学实验教学以学生在实验室实践为主,发挥学生的主体作用,教师只作必要的实验原理和注意事项的讲解,并注意引导学生拓展所学的内容,通过实验内容的学习了解生物化学技术的原理和操作要点,提高学生的实践能力和创新能力。
1.遵守实验室规则,爱护实验仪器设备。
2.实验前要充分预习实验指导,做好实验记录,认真完成实验报告。
3.实验操作要细心谨慎,严格遵守操作规则,注意安全。
4.实验完毕,注意关闭灯、电、火、窗。
四、参考教材与主要参考书《生物化学实验》,陈钧辉、李俊,科学出版社,第五版五、进度安排- 2 -六、成绩评定(一)考核方式 E :A.闭卷考试 B.开卷考试 C.论文 D.考查 E.其他(二)成绩综合评分体系:附:实验报告和平时表现评分标准1)实验报告的评分标准2)平时表现评分标准- 3 -七、学术诚信学习成果不能造假,如考试作弊、盗取他人学习成果、一份报告用于不同的课程等,均属造假行为。


化学 专业人才培养方案学科门类 理学 专业代码 070301 授予学位理学学士(从2013级本科生开始执行)一、培养目标培养具有良好人文和科学素质,具有社会责任感,创新意识和实践能力强,掌握化学和海洋化学基础知识、基本理论和基本技能,并受到良好基础研究和应用研究初步训练,能胜任化学、海洋化学及相关领域的科研、教学及其他工作的人才。
毕业生可到科研部门、高等或中等学校从事科学研究和教学工作;可到厂矿企事业、技术和行政部门从事应用研究、科研开发、生产技术和管理工作;可继续攻读化学、海洋化学及相关学科的硕士研究生。
本专业含应用化学和海洋化学两个方向。
二、培养规格本专业学生在学好数学、物理的基础上,主要学习化学和海洋化学方面的基础知识、基本理论与方法和基本技能,接受科学思维和科学实验的训练,具有一定的科学研究、应用研究及科技开发的能力。
毕业生应获得以下几方面的知识和能力:1.掌握数学、物理学的基本理论和基本知识;2.掌握无机化学、分析化学、有机化学、物理化学及化学工程的基础知识、基本原理和基本实验技能;3.了解化学、海洋化学某些领域的理论前沿、应用前景、最新发展动态以及化学、海洋化学相关产业发展状况;4.了解相近专业的一般原理和知识;了解国家关于科学研究、化学相关产业的政策,国内外知识产权等方面的法律法规;5.具有获取有关专业信息的能力,掌握中外文资料查询、文献检索及运用现代信息技术获取信息的基本方法;6.具有一定的研究能力, 能自主进行实验的设计和改进,能够正确处理实验数据,讨论、分析实验结果,撰写论文,具有一定的学术交流能力。
三、支撑学科应用化学方向:化学、化学工程与技术海洋化学方向:化学四、核心课程应用化学方向:无机化学I、分析化学I(含仪器分析I)、有机化学I、物理化学I(含结构化学)海洋化学方向:无机化学I、分析化学I(含仪器分析I)、有机化学I、物理化学I、化学海洋学五、特色课程应用化学方向:海洋资源化学、应用化学专业实验、专业实习海洋化学方向:化学海洋学、海水分析化学、海洋物理化学、专业实习六、实践环节必修实践环节应用化学方向:1. 无机化学实验 I 96课时/3学分 7. 应用化学专业实验(1和2) 80课时/2.5学分2. 分析化学实验 I 64课时/2学分 8. 化工原理实验 II 32课时/1学分3. 有机化学实验 I 128课时/4学分 9. 认识实习 1周/1学分4. 物理化学实验 I 128课时/4学分 10. 专业实习 4周/4学分5. 仪器分析实验 I 64课时/2学分 11. 毕业论文 16周/12学分6. 大学物理实验 III 96课时/3学分 12. 创新创业教育 /2学分海洋化学方向:1. 无机化学实验 I 96课时/3学分 7. 海水分析化学实验 54课时/1.5学分2. 分析化学实验 I 64课时/2学分 8. 化学海洋学实验 36课时/1学分3. 有机化学实验 I 128课时/4学分 9. 认识实习 1周/1学分4. 物理化学实验 I 128课时/4学分 10. 专业实习 4周/4学分5. 仪器分析实验 I 64课时/2学分 11. 毕业论文 16周/12学分6. 大学物理实验 III 96课时/3学分 12. 创新创业教育 /2学分选修实践环节应用化学方向:海水分析化学实验 48课时/1.5学分海洋化学方向:1. 海洋化学综合实验 32课时/1学分2. 化工原理实验II 32课时/1学分七、学分分配八、专业课程设置1.公共基础教育层面2.通识教育层面通识教育层面的课程设置参见学校的通识教育课程设置一览表。

附件2:中国海洋大学化学海洋学(海洋化学)课程大纲(Chemical Oceanography)【开课单位】化学化工学院【课程模块】专业知识【课程编号】【课程类别】必修【学时数】64 (理论64 实践)【学分数】 4一、课程描述本课程大纲根据2011年本科人才培养方案进行修订或制定。
(一)教学对象面向化学(海洋化学)国家理科基地3年级本科生开设。
也可作为化学(应用化学方向)、海洋科学、海洋技术等专业本科生选修课程。
(二)教学目标及修读要求1.教学目标通过课堂讲授和讨论,结合《化学海洋学实验》、《海洋学和海洋化学专业实习》等教学环节,使学生掌握海洋化学的基础知识、基本概念和基本理论,包括海洋中各种化学成分的含量、性质、特点、存在形式、分布、迁移变化规律以及相关研究方法等内容。
在此基础上,使学生了解海洋化学研究需综合考虑的因素以及与物理海洋学、生物海洋学和海洋地质学等其它海洋分支学科的联系,了解当前海洋化学研究的热点和发展方向,了解与资源、环境与可持续发展相关的问题,为学习其它海洋化学专业课程和将来从事海洋科学研究打下基础。
2.修读要求化学海洋学是化学与海洋学交叉的一门边缘学科,是研究海洋各部分的化学组成、物质分布、化学性质和化学过程的科学,是化学(海洋化学)方向的专业基础课程。
学生应掌握无机化学、分析化学、有机化学、物理化学(上)和海水分析化学、海洋学II的理论知识,掌握无机化学实验、分析化学实验、物理化学实验(上)和海水分析化学实验的基本技能。
(三)先修课程海洋学II。
二、教学内容第一章绪论1.主要内容1.1 化学海洋学的内容和特点1.2 化学海洋学的历史与发展1.3 化学海洋学的研究意义和作用2.教学要求理解化学海洋学的主要内容和特点,了解海洋化学的历史与发展,及其研究意义和作用。
第二章海洋的形成和海水的组成1.主要内容2.1 海洋的形成与海水化学组成的演化2.2 海洋中元素的平衡和元素逗留时间2.3 海洋中元素的分布2.教学要求了解地球起源、海洋形成与海水化学组成的演化,理解海洋中元素的地球化学平衡,掌握元素逗留时间的概念,掌握海洋中元素保守性与非保守性以及混合过程中元素的行为,掌握海洋中元素分布类型和描述方法。
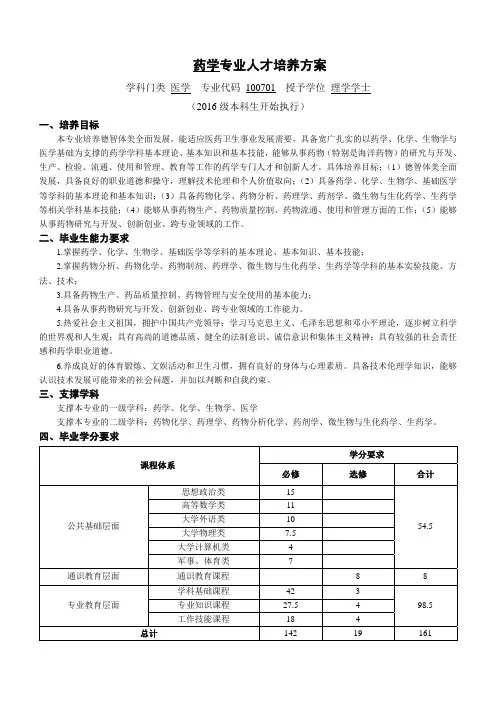

全国分析化学专业排名
排名学校名称等级
1 武汉大学A+
2 北京大学A+
3 吉林大学A+
4 浙江大学A+
5 南开大学A+
6 复旦大学 A
7 湖南大学 A
8 厦门大学 A
9 中国科学技术大学 A
10 南京大学 A
11 清华大学 A
12 兰州大学 A
13 华东师范大学 A
14 中山大学 A
15 西北大学 A
16 东北大学 A
17 四川大学 A
18 山东大学 A
19 西南大学 A
B+等(30个):陕西师范大学、西北师范大学、北京化工大学、河北大学、中南大学、北京理工大学、山西大学、华东理工大学、福州大学、湖南师范大学、郑州大学、苏州大学、上海交通大学、同济大学、华中科技大学、山东师范大学、北京师范大学、安徽师范大学、扬州大学、广西师范大学、江南大学、河南师范大学、云南大学、上海师范大学、中国地质大学、南昌大学、暨南大学、中国农业大学、河南大学、聊城大学
B等(29个):华中师范大学、上海大学、首都师范大学、东北师范大学、桂林工学院、华南理工大学、辽宁大学、浙江工业大学、湖北师范学院、青岛科技大学、东南大学、西南科技
大学、东华理工大学、西安交通大学、辽宁石油化工大学、漳州师范学院、重庆大学、安徽大学、广西大学、浙江师范大学、山东农业大学、中国海洋大学、湘潭大学、青岛大学、济南大学、沈阳药科大学、河北农业大学、贵州师范大学、沈阳师范大学。

中国海洋大学本科生课程大纲_、课程介绍1.课程描述:本课程是面向化学类专业学生的选修课程,通过本课程学习,使学生比较系统地掌握复杂物质分析中各种常用分离与富集方法的理论和实践知识,了解分离技术领域的最新发展动向及其趋势,培养学生独立思考和解决问题的能力,激发学生的创新精神。
2.设计思路:本课程引导化学专业学生通过掌握各种常用分离与富集方法基本原理与方法来探讨和理解山实际问题所驱动的复杂物料的处理过程。
课程内容主要包括:沉淀与共沉淀、液一液萃取、离子交换分离、物质的挥发、气浮分离、色谱法、膜分离、固相萃取、高效毛细管电泳以及分离方法的选择。
3.课程与其他课程的关系:先修课程:分析化学I、分析化学实验I;后置课程:仪器分析I、仪器分析实验I、海水分析化学。
二、课程目标本课程LI标是引导化学专业学生掌握車要分离方法的原理、特点、适用性,拓展学生的科学视野,培养学生分析、解决问题的能力,全面提高学生的科学素养和应用创新能力。
到课程结束时,学生应能:(1)系统地掌握分离科学中常用分离富集方法的基本理论与适用性,熟悉常用分离富集方法的特点,了解分离技术领域的最新发展动向及其趋势;(2)运用所学的基本原理和方法设计复杂物料的分离富集实验方案,初步具有分析问题、解决问题的能力;三、学习要求要完成所有的课程任务,学主必须:(1)按时上课,上课认真听讲,积极参与课堂讨论、随堂练习和测试。
本课程将包含较多的随堂练习、讨论等课堂活动,课堂表现和出勤率是成绩考核的组成部分。
(2)完成教师布置的一定量的阅读文献和背景资料等作业,其中大部分内容要求以小组合作形式完成。
这些作业能加深对课程内容的理解、促进同学间的相互学习、并能引导对某些问题和理论的更深入探讨。
四、教学进度附:各章教学目标及重点、难点:第一章概论教学目标:1.掌握分离富集的分类和评价指标;2.了解分离科学的任务、作用和意义;3.了解分离科学的发展概况。
第二章沉淀与共沉淀教学目标:1.掌握常量组分沉淀分离法的分离原理和应用特点;2.掌握痕量组分共沉淀分离富集法的分类和特点,共沉淀剂的性质和特点。

2021年硕士研究生招生考试大纲003化学化工学院目录初试考试大纲 (2)619 分析化学 (2)815 物理化学A (10)971 化工原理 (14)复试考试大纲 (17)F0301综合化学 (17)F0302物理化学 (25)初试考试大纲619 分析化学一、考试性质全国硕士研究生入学考试是为高等学校招收硕士研究生而设置的。
其中,分析化学是化学专业、分析专业与海洋化学专业的专业基础课程,属我校命题的考试。
它的评价标准是高等学校优秀毕业生能达到及格或及格以上水平,以保证录取者具有较扎实的分析化学的基础知识。
考试对象为报考中国海洋大学硕士研究生入学考试的准考考生。
二、考查目标分析化学可分为定量分析化学和仪器分析两部分。
要求考生了解分析化学在科研及生产实际中的重要意义;能系统理解分析化学的基本概念和基本原理,提高定量处理水溶液中离子平衡关系的能力,准确树立“量”的概念;掌握常用仪器分析方法的基本原理、仪器构造和分析应用;能够根据具体问题选择合适的仪器分析方法。
正确掌握分析化学的基本操作,并初步具有解决某些实际分析化学问题的能力。
三、考试形式本考试为闭卷考试,满分为150分,考试时间为180分钟。
试卷结构:选择20-30%,填空20-30%,简答20-30%,计算20-30%。
四、考试内容《分析化学》部分:(40%)第一章概论1.分析化学的定义、任务、作用和分析方法的分类;分析化学发展简史和现代分析化学学科发展趋势及特点;2.定量分析过程和分析方法;3.滴定分析的方法;滴定分析对化学反应的要求和滴定方式及分类;基准物质和标准溶液;4.掌握滴定分析的基本计算,浓度换算。
第二章分析试样的采集与制备1.定量分析的基本过程及各步操作的主要目标;2.试样采集、制备、分解及预处理的基本操作。
第三章分析化学中的误差与数据处理1.总体和样本的统计学计算;2.随机误差的正态分布的特点及区间概率的概念;3.t分布曲线,置信度和平均值的置信区间;显著性检验:t检验和F检验;异常值的取舍方法;4.系统误差和随机误差的传递计算;5.提高分析结果准确度的方法。
008 医药学院目录一、初试考试大纲 (1)614专业基础综合A (1)615专业基础综合B (11)616专业基础综合C (19)837 药物化学 (27)二、复试考试大纲 (31)药物化学 (31)药学分子生物学 (35)细胞生物学 (37)药理学 (38)一、初试考试大纲614专业基础综合A《有机化学》部分一、考试性质有机化学是药学专业硕士研究生入学初试考试的专业基础课程之一。
二、考察目标要求考生掌握各类有机化合物的命名、物理性质和制备方法;掌握各类有机化合物的结构特征、典型反应和反应性质;掌握典型有机反应历程和取代基效应;掌握各种异构现象,重要反应中的立体化学;熟练运用有机化学基本理论知识进行有机化合物的反合成分析及设计合理合成路线;初步掌握有机化学的光谱波谱学理论,能够通过多种光谱波谱学技术鉴定简单有机化合物的结构,熟悉各类有机化合物的鉴别和一般分离纯化方法。
三、考试形式本考试为闭卷考试,满分为100分,考试时间为60分钟。
答题方式为闭卷、笔试。
试卷由试题和答题纸组成,所有题目的答案必须写在答题纸相应的位置上。
考生不得携带具有存储功能的计算器。
四、考试内容1、掌握有机化学的基本概念(有机化合物命名、有机化合物分类、结构式、离子键和共价键、共价键理论、有机酸碱理论等);掌握立体化学的基本概念(构象、相对构型、绝对构型、对映异构现象、对映异构体和非对映异构体、手性碳、手性分子、旋光性和有机化合物的比旋光、手性碳原子及其构型、外消旋体和内消旋体、立体结构的表达法等)。
2、掌握各类有机化合物(烷烃、卤代烃、有机金属化合物、烯烃、炔烃、共轭双烯烃、芳烃、醇和醚、酚和醌、羰基化合物、羧酸和取代羧酸、羧酸衍生物、杂环化合物、糖类等)的化学结构和基本化学反应性和类型(马氏/反马氏加成、Diels-Alder反应、Wittig反应、Darzen反应、Michael加成、Robinson 关环、周环反应等)。
中国海洋大学本科生课程大纲课程属性:公共基础/通识教育/学科基础/专业知识/工作技能,课程性质:必修、选修一、课程介绍1.课程描述:无机及分析化学实验是我校的公共基础课,计划学时为48学时。
本课程是本科生进入大学后的第一门化学实验课,它不仅对无机及分析化学理论教学有着重要作用,而且是后续化学课及其它与之相关的交叉学科的科学实验基础。
无机及分析化学实验大致可分为:制备、测试、性质、分析化学及综合设计性实验五大部分,各个部分既各有侧重,又相互联系,相互渗透。
2.设计思路:(1)学时安排:本课程选取11个实验,其中5个无机化学实验,5个分析化学实验,每个实验4学时;1个综合设计性实验8学时,共计48学时。
(2)实验内容:为了提高学生分析问题、解决问题的能力,安排实验内容时适当减少验证性实验,增加适合大一学生的综合设计性实验。
如:三草酸合铁(Ⅲ)酸钾的制备及组分分析这一实验,除了让学生制备出产品,还让他们自己设计实验方案,在老师的指导下,分析自己制备的三草酸合铁(Ⅲ)酸钾产品中草酸根和铁的含量。
通过进行综合设计性实验,可提高学生的综合素质和创新能力。
(3)学生安排:实验1人1组,学生在老师的指导下,在规定的时间内独立完成每- 4 -个实验。
3. 课程与其他课程的关系:本课程在大学一年级开设。
并行课程:无机及分析化学;后置课程:有机化学实验,物理化学实验。
本课程学习效果对并行课程及后续化学课程的学习起着重要作用。
二、课程目标1.通过无机及分析化学实验使学生获得大量的感性知识,巩固和加深对无机及分析化学基本理论和基本知识的理解。
2.学生经过严格的实验训练, 能够规范地掌握实验的基本操作、基本技术和基本技能。
3.通过实验训练,使学生能够正确地使用各类相关化学仪器,掌握无机物的一般制备、分离、提纯及定性和定量分析方法。
4.通过实验训练,使学生学会获得可靠而必要的实验数据,正确处理数据和表达实验结果的方法,提高对实验现象及实验结果进行分析判断、逻辑推理,并做出正确结论的能力。
003 化学化工学院
初试考试大纲:
619分析化学
一、考试性质
全国硕士研究生入学考试是为高等学校招收硕士研究生而设置的。
其中,分析化学是化学专业、分析专业与海洋化学专业的专业基础课程,属我校命题的考试。
它的评价标准是高等学校优秀毕业生能达到及格或及格以上水平,以保证录取者具有较扎实的分析化学的基础知识。
考试对象为报考中国海洋大学硕士研究生入学考试的准考考生。
二、考试的基本要求
分析化学可分为定量分析化学和仪器分析两部分。
要求考生了解分析化学在科研及生产实际中的重要意义;能系统理解分析化学的基本概念和基本原理,提高定量处理水溶液中离子平衡关系的能力,准确树立“量”的概念;掌握常用仪器分析方法的基本原理、仪器构造和分析应用;能够根据具体问题选择合适的仪器分析方法。
正确掌握分析化学的基本操作,并初步具有解决某些实际分析化学问题的能力。
三、适用专业
分析化学、海洋化学、海洋化学工程与技术
四、考试内容
《分析化学》部分:(50%)
第一章概论
1.分析化学的任务、作用和分析方法的分类;分析化学发展简史和现代分析化学学科发展趋势及特点;
2.定量分析的基本概念、定量分析过程,分析化学中的误差概念;
3.有效数字的概念及运算规则,滴定分析常用的几种滴定方式;
4.掌握滴定分析的基本计算,浓度换算。
第二章分析试样的采集与制备
1.定量分析的基本过程及各步操作的主要目标;
2.试样采集、制备、分解及预处理的基本操作。
第三章分析化学中的数据处理
1.总体和样本的统计学计算;
2.随机误差的正态分布的特点及区间概率的概念;
3.t分布曲线,平均值的置信区间;显著性检验:t检验和F检验;异常值的取舍方法;
4.系统误差的传递计算和随机误差的传递计算;
5.一元线性回归分析法及线性相关性的评价;
6.提高分析结果准确度的方法。
第五章酸碱平衡及酸碱滴定法
1.活度的概念及计算,酸碱质子理论;
2.酸碱的离解平衡,酸碱水溶液酸度、质子平衡方程;
3.酸碱平衡体系中各型体的分布分数的计算和用质子理论即PBE方程式处理酸碱平衡的基本方法;
4.酸碱平衡中溶液酸碱度的计算方法,包括强酸(碱)溶液、一元和多元弱酸(碱);酸混合溶液;两性物质溶液;酸碱缓冲溶液的pH计算;
5.缓冲溶液的作用原理,缓冲容量的计算;几种常用的缓冲溶液的配制和应用;
6.指示剂的变色原理及选择原则;常用指示剂的变色范围及终点变化情况;
7.酸碱滴定过程中氢离子浓度的变化规律,化学计量点、滴定突跃、滴定终点的含义、指示剂的选择。
酸碱直接准确滴定、多元酸分步滴定的判别式。
酸碱滴定的终点误差;
8.酸碱滴定分析结果的计算及酸碱滴定法的应用。
第六章络合滴定法
1.分析化学中的络合物:简单络合物与螯合物;EDTA及其络合物;络合物溶液中的离解平衡。
络合物的稳定常数:络合物的逐级平衡常数和积累稳定常数;溶液中各级络合物的分布;平均配位数;
2.络合平衡中的副反应系数和条件稳定常数的计算;
3.络合滴定基本原理:滴定曲线讨论;化学计量点pM计算;影响滴定突跃大小的因素;终点误差;准确滴定与分步滴定判别式;金属离子指示剂的作用原理及选择原则;常用的指示剂;指示剂的封闭与僵化;
4.络合滴定中的酸度控制:单一离子滴定的适宜酸度范围;分别滴定的酸度控制;
5.提高络合滴定的选择性的方法;选择滴定的可能性;酸度控制;掩蔽与解蔽;络合滴定终点误差的计算;
6.掌握络合滴定的方式及其应用和结果的计算。
第七章氧化还原滴定
1. 氧化还原平衡:能斯特方程;氧化还原反应的平衡常数;条件电位;氧化还原反应的方向、次序和程度;氧化还原反应的速度及其影响因素;催化反应和诱导反应;
2. 氧化还原滴定法的基本原理:可逆对称氧化还原滴定曲线;不可逆体系的滴定曲线;等当点电位的计算;氧化还原滴定指示剂;氧化还原滴定结果的计算:用物质的量的关系处理比较复杂的氧化还原测定的计算问题,包括多组分体系和有机物的测定计算;终点误差;
3. 氧化还原常用的预处理方法
4. 氧化还原滴定法的应用:高锰酸钾法、重铬酸钾法、碘量法、溴酸钾法和铈量法的原理和应用;不同氧化还原滴定法标准溶液在配制、标定及滴定过程中应注意的问题。
第八/九章重量分析法与沉淀滴定法
1.重量分析的基本概念;沉淀的溶解度的计算及影响沉淀溶解度的因素;
2.沉淀滴定法:莫尔法,佛尔哈德法和法扬司法;各种方法的基本原理、滴定条件、指示剂及其应用;
3.沉淀的类型、形成过程及影响沉淀纯度的因素;沉淀条件的选择;
4.掌握重量分析结果计算;掌握沉淀滴定法。
第十章吸光光度法
1. 光吸收的基本定律:光的基本性质;吸收光谱的产生;朗伯-比耳定律及其偏离的原因;吸光度的加和性;比色法和吸光光度法及其仪器;
2. 光度分析法的设计:对显色反应的要求;显色条件的选择;测量波长和吸光度范围的选择;参比溶液的选择;
3. 光度分析法的误差:吸光度测量的误差;仪器测量误差,测量条件的选择;
4. 其它吸光光度法和光度分析法的应用:示差光度法;双波长分光光度法;多组分分析;弱酸弱碱条件常数的测定;络合物的组成测定;稳定常数的测定;光度滴定法;
第十一章分析化学中常用的分离方法
1.分析化学中常用的富集分离方法:沉淀分离与共沉淀分离、溶剂萃取分离、离子交换分离、液相色谱分离的基本原理;
2.萃取条件的选择及主要的萃取体系,掌握液液萃取分离的基本参数及有关计算。
《仪器分析》部分(50%)
第一章绪论
1. 仪器分析与化学分析
2. 仪器分析方法概述及分类
3. 仪器分析的特点
4. 仪器分析的发展趋势
第二章光分析法导论
1. 光的波动性
2. 光的粒子性
3. 光谱仪器的构造:光源、波长选择器(类型、棱镜和光栅的分光原理和光学特性)、检测器
第三章原子光谱法导论
1. 原子光谱:产生和分类
2. 试样原子化和导入方法
第四章原子吸收光谱法(AAS)
1. AAS基本原理:谱线轮廓和谱线变宽、原子吸收测量方法
2. AAS仪器:基本结构、各部分的作用。
空心阴极灯;原子化器:火焰、无火
焰原子化器的原理、特点、比较;分光系统:光谱通带
3. AAS干扰及消除:光谱干扰:谱线干扰、背景干扰;非光谱干扰:物理干扰、
化学干扰、电离干扰
4. AAS定量分析:分析方法、灵敏度、检测限;应用
5. 原子荧光(AFS):AFS产生、仪器基本结构及特点;应用
第五章原子发射光谱法(AES)
1. AES的产生
2. AES仪器:基本结构、各部分的作用;常用的激发光源的原理和特点
3. 光谱定性分析:基本原理、常用方法
4. 光谱定量分析:赛伯•罗马金公式、内标法的原理、常用光谱定量分析方法
第六章紫外-可见分光光谱法
1. 分子吸收光谱概述:分子光谱的产生、有机分子中的电子跃迁类型、常见有机化合物的紫外-可见吸收光谱
2. 紫外-可见分光光度计:基本结构及各部分作用
3. 紫外-可见分光光度法的分析应用:定量分析、溶剂效应
第七章分子发光光谱法
1. 荧光及磷光光谱法:荧光及磷光的产生过程、能量传递方式;影响If、Ip的因素;仪器构造及其特点;分析应用
2. 化学发光光谱法:化学发光产生的原理;仪器:流动注射式、流动注射分析
法(FIA)
第八章电位分析法
1. 电分析化学基本概念
2. 离子选择电极的作用原理:离子选择性电极膜电位的产生、电位表达式
3. 离子选择电极的类型、结构、原理和特点:晶体膜电极、pH玻璃电极、气敏电极
4. 离子选择电极的性能参数
5. 电位分析法的分析应用:电位选择性系数及其应用;pA的测定原理、测定方法;电位法误差的计算;应用
第九章电解和库仑分析法
1. 基本原理:分解电压、析出电位;极化现象、过电位;电解时离子的析出次序及完全程度;法拉第定律
2. 电解分析:控制电位电解、恒电流电解、汞阴极电解分离法的特点及应用
3. 库仑分析法:恒电位库仑分析法、库仑滴定法的特点及应用
第十章极谱和伏安分析法
1. 普通极谱法基本原理
2. 极谱定量分析及应用:扩散电流方程式;干扰电流及其消除:充电电流、迁移电流、极谱极大电流、氧波
3. 极谱波方程式:简单金属离子、络合物的极谱波方程式
4. 极谱分析新技术的原理、特点及应用:单扫描极谱法、循环伏安法、脉冲极谱法、溶出伏安法、催化极谱波
第十一章色谱法导论
1.色谱法概述:色谱法常用术语
2.色谱法基本理论:塔板理论、速率理论
3.色谱分离度
4.定性、定量方法:校正因子;常用定量方法:归一化法、内标法、外标法
第十二章气相色谱法
1. 气相色谱仪:基本构造、各部分作用;常用检测器的原理、应用范围、性能参数、特点
2. 色谱分离条件的选择
3. 气相色谱法固定相及其选择
4. 气相色谱定性、定量分析:利用保留值、保留指数、经验规律定性;应用
5. 毛细管色谱法
第十三章高效液相色谱法(HPLC)
1. 概述:HPLC特点、分类、原理及应用
2. 高效液相色谱仪:基本结构、各部分作用
3. 分配色谱法:原理;特点;应用;正相色谱和反相色谱;化学键合固定相;溶剂极性参数
4. 吸附色谱法:原理;特点;应用
5. 离子交换色谱法和离子色谱法:原理;特点;应用
6. 尺寸排阻色谱法:原理;特点;应用
仪器分析实验:各种仪器的基本操作;定性、定量分析方法及其应用
五、考试形式及总分
本考试为闭卷考试,满分为150分,考试时间为180分钟。