燃烧学(各种燃料的比较)
- 格式:doc
- 大小:31.00 KB
- 文档页数:2


《燃料的燃烧》讲义一、引言燃料的燃烧是我们日常生活和工业生产中不可或缺的一部分。
从家庭取暖、烹饪到汽车驱动、发电,燃料的燃烧为我们提供了能源和动力。
然而,燃烧过程并非简单的化学反应,它涉及到众多的物理和化学原理,以及对环境和能源利用的重要影响。
二、燃料的种类1、固体燃料常见的固体燃料包括煤炭、木材和生物质等。
煤炭是一种重要的化石燃料,其种类繁多,如无烟煤、烟煤和褐煤等。
不同种类的煤炭在热值、含碳量和杂质含量等方面存在差异。
木材作为一种传统的燃料,在一些地区仍然被广泛使用,但燃烧效率相对较低,且会产生较多的烟尘。
生物质燃料如秸秆、木屑等,具有可再生的特点,但也需要合适的燃烧技术来提高效率和减少污染。
2、液体燃料液体燃料主要有石油及其衍生品,如汽油、柴油和煤油等。
石油是一种复杂的混合物,通过精炼可以得到不同用途的液体燃料。
汽油通常用于轻型车辆,柴油则适用于重型车辆和工业设备。
此外,还有一些生物液体燃料,如生物柴油和乙醇,它们来自可再生资源,对环境相对友好。
3、气体燃料气体燃料包括天然气、液化石油气(LPG)和煤气等。
天然气是一种清洁高效的燃料,主要成分是甲烷。
LPG 通常由丙烷和丁烷组成,易于储存和运输。
煤气则是通过煤炭的气化过程产生的,但其使用范围相对较窄。
三、燃烧的基本原理1、燃烧的化学方程式燃烧是燃料与氧气发生的剧烈氧化反应。
以甲烷(CH₄)的燃烧为例,其化学方程式为:CH₄+ 2O₂ → CO₂+ 2H₂O +热量。
在这个过程中,燃料中的碳和氢与氧气结合,生成二氧化碳和水,并释放出大量的热能。
2、燃烧的条件燃烧需要同时满足三个条件:可燃物、助燃物(通常是氧气)和达到着火点的温度。
只有当这三个条件都具备时,燃烧才能发生。
例如,纸张是可燃物,在空气中(含有氧气),当受到足够高的温度(着火点)时,就会燃烧起来。
3、完全燃烧与不完全燃烧完全燃烧是指燃料中的碳和氢完全与氧气反应,生成二氧化碳和水,此时释放的热量最多,对环境的污染也相对较小。

化学燃料及其利用是九年级化学内容中的一个重要知识点,下面是九年级化学燃料及其利用的知识点总结,包括什么是燃料、常见的燃料种类、燃烧反应及其特点、燃料的效能、燃料和环境的关系以及节约能源和绿色能源等方面。
一、什么是燃料燃料是指直接或间接用于产生热能或动力的物质。
燃料主要为化学物质,它们能够在适当的条件下与氧气反应产生热能。
常见的燃料有化石燃料、木炭、天然气等。
二、常见的燃料种类2.木炭:木炭是由木材等植物有机物经过热分解得到的固体燃料。
木炭燃烧时释放的热量高,但燃烧产物中会有很多固体颗粒物。
3.液体燃料:液体燃料主要指石油和汽油,它们被广泛用于交通运输和工业生产等领域,但燃烧产生的尾气对环境有污染。
4.天然气:天然气是一种主要由甲烷组成的气态燃料,它燃烧时产生的污染物相对较少,因此被认为是较为清洁的燃料。
三、燃烧反应及其特点燃烧是指物质与氧气发生化学反应,放出焓变为负的化学反应。
燃烧反应一般包括燃料和氧气的反应,产物主要有二氧化碳、水和能量(热能和光能)。
燃烧反应具有自燃性、连续性、放热性和产物不稳定性等特点。
四、燃料的效能燃料的效能指用于产生能量的燃料利用效果的好坏。
常用的衡量燃料效能的指标包括燃烧的热效率和排放的污染物。
炉具和发动机等的效能主要取决于其热损失的多少,减少热损失可以提高燃料的效能。
五、燃料和环境的关系燃料的燃烧过程中会产生大量的污染物,包括二氧化碳、二氧化硫、氮氧化物和颗粒物等。
这些污染物对环境和人类健康都有一定的危害。
因此,燃料和环境的关系十分密切,我们应该选择清洁和高效的燃料,减少污染物的排放。
六、节约能源和绿色能源近年来,随着全球能源危机的日益突出和环境保护意识的提高,节约能源和绿色能源成为了研究的热点。
节约能源主要包括提高能源利用效率、合理使用能源和开发新能源等。
绿色能源是指对环境友好、可持续利用的能源,如太阳能、风能和生物能等。
总的来说,九年级化学燃料及其利用的知识点包括了什么是燃料、常见的燃料种类、燃烧反应及其特点、燃料的效能、燃料和环境的关系以及节约能源和绿色能源等方面。


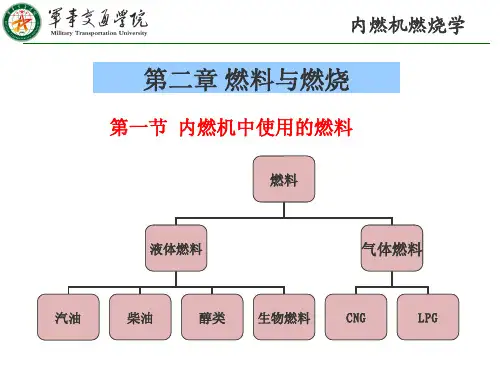
一、燃料
一、固体燃料
* 煤是由植物残骸在适宜的地质环境下通过漫长岁月的天然煤化作用形成的一种棕色至黑色的可燃烧的固体矿物质燃料
*天然煤化作用:植物的积存时期、菌解作历时期、炭化作历时期
*按炭化程度:泥煤——最年轻的煤、保留着植物尸体的痕迹、质地酥松、吸水性强(40%)、
堆积密度300-400kg/m3(露天风干)、含氧量高(28-38%)、含氢量
高(20-30%)、含碳量少——挥发分高、可燃性好,反映活性好,含
硫量低,机械性能很差、灰分熔点低——要紧用于产区周围的锅炉
燃烧、气化原料、不适于远途运输工业应用价值不大
褐煤——外表呈褐色或暗褐色,无光泽、真密度较大()、堆积密度700-800
kg/m3、含碳量较高、含氢氧量较少、挥发分产率较低——粘结性
弱、极易氧化和自燃、吸水性较强、机械强度较大(新开采)、在
空气中极易风化和破碎,致使其机械性能很差
——要紧用于产区周围的锅炉燃烧、气化原料、不适于远途运输工
业应用价值不大
烟煤——褐煤通过变质作用后形成——煤化程度较高、挥发份较少、密度较
大、吸水性较小、含碳量继续增加、含氢、氧量继续减少、具有粘
结性
无烟煤——煤化程度最高,年龄最老、灰黑色、具有金属光泽、无明显条带、
密度大、含碳量高、挥发份极少、组织致密,坚硬、吸水性小
——发烧量大(29260kJ/kg)。

九年级化学燃料知识点总结燃料在我们的日常生活中扮演着重要的角色,它不仅用于加热、照明和运输,还是许多工业过程的基础。
在化学课程中,我们学习了许多关于燃料的知识,本文将对九年级化学燃料知识点进行总结和归纳。
一、什么是燃料?燃料是一种能够发生燃烧的物质。
它可以提供能量,通过化学反应释放出热能,从而进行加热、照明等常见应用。
燃料可以分为化石燃料和可再生能源两类。
二、化石燃料1.石油:石油是一种常见的化石燃料,它是由古代生物的化石经过地质作用形成的。
石油是一种复杂的混合物,主要由烷烃、脂肪烃和环烷烃组成。
石油燃烧时会产生二氧化碳和水蒸气,释放出大量热能。
2.天然气:天然气主要由甲烷组成,属于无色、无味、无毒的气体。
它是一种清洁的燃料,燃烧时几乎不会产生固体废物,只释放出二氧化碳和水蒸气。
3.煤炭:煤炭是一种含碳的矿物质,是一种传统的化石燃料,广泛用于发电、加热和工业生产中。
煤炭可以分为无烟煤、烟煤和褐煤等不同品种,根据含碳量的不同,其能量释放也有所差异。
三、可再生能源可再生能源是指自然界中能够以可持续方式再生的能源。
它们不会因为使用而消耗殆尽,并且对环境友好。
以下是几种常见的可再生能源。
1.太阳能:太阳能是由太阳辐射产生的能量,可转化为电能和热能。
太阳能电池板可以通过光伏效应将太阳能转化为电能,而太阳能热水器则用于加热水。
2.风能:风能是指利用风的动力来产生能量。
风力发电机通过转动叶片,将风能转化为电能。
风能具有广泛分布、无污染等优点,是一种环保的可再生能源。
3.水力能:水力能是指利用水流的能量来产生能量。
水电站通过水轮机将水流的动能转化为机械能,然后通过发电机转化为电能。
水力能是一种成熟的可再生能源,具有高效、可控和环保的特点。
四、燃料的利用和环境问题燃料的利用是一个关键问题。
燃料的高效利用可以减少能源浪费,降低碳排放。
我们可以采取一些措施来提高燃料利用效率,如优化燃烧技术、开发清洁能源替代传统能源等。



《燃料的燃烧》讲义一、引言燃料的燃烧是一个我们日常生活和工业生产中常见且至关重要的现象。
从家庭取暖的炉火到驱动汽车的汽油,从发电站的煤炭燃烧到航天飞机的燃料喷射,燃烧现象无处不在。
深入了解燃料的燃烧过程、原理以及影响因素,对于提高能源利用效率、减少环境污染、保障能源安全都具有极其重要的意义。
二、燃料的种类(一)固体燃料常见的固体燃料有煤炭、木材等。
煤炭是一种重要的能源资源,根据其品质和成分的不同,可以分为无烟煤、烟煤和褐煤等。
木材在一些地区仍然被用作取暖和烹饪的燃料,但相对来说其能量密度较低,燃烧效率不高。
(二)液体燃料液体燃料包括石油制品如汽油、柴油、煤油等。
汽油通常用于汽车的内燃机,柴油则多用于卡车和船舶的发动机。
石油作为液体燃料的主要来源,其储量和开采情况对全球能源格局有着重大影响。
(三)气体燃料天然气是最为常见的气体燃料之一,它主要由甲烷组成,具有清洁、高效的特点。
此外,还有煤气、液化气等气体燃料,在不同的应用场景中发挥着作用。
三、燃烧的基本原理(一)燃烧的化学过程燃烧本质上是一种剧烈的氧化反应。
燃料中的可燃成分(如碳、氢等元素)与氧气发生化学反应,释放出热能。
以碳的燃烧为例,碳与氧气反应生成二氧化碳:C + O₂= CO₂,同时放出大量的热。
(二)燃烧所需的条件燃烧需要同时具备三个条件:可燃物、助燃物(通常是氧气)以及达到可燃物的着火点。
只有这三个条件同时满足,燃烧才能发生。
(三)燃烧反应的热力学燃烧过程中的能量变化可以通过热力学原理来描述。
燃料燃烧释放的能量等于反应物与生成物之间的能量差。
这一能量差决定了燃烧的热效率和可利用程度。
四、燃烧的过程(一)预热阶段在燃烧开始前,燃料需要吸收一定的热量,温度逐渐升高,达到其着火点。
(二)燃烧阶段一旦达到着火点,燃料与氧气迅速反应,产生火焰和热能。
燃烧过程中,燃料分子不断分解、氧化,释放出大量的热量和气体产物。
(三)燃尽阶段随着燃烧的进行,燃料中的可燃成分逐渐减少,直至完全燃烧。

燃料及燃烧知识点总结燃料是生产生活中常用的燃烧物质,包括固体、液体和气体。
在现代社会中,燃料在各个行业都扮演着至关重要的角色,包括发电、交通运输和工业生产等领域。
因此,燃料及其燃烧相关知识是非常重要的。
本文将从燃料的分类、性质、燃烧过程以及燃烧产物等方面对燃料及燃烧知识进行总结。
一、燃料的分类根据物理状态的不同,燃料可以分为固体燃料、液体燃料和气体燃料。
1.固体燃料常见的固体燃料包括木材、煤炭、木炭等。
固体燃料具有密度大、体积小、便于储存和运输等特点,但燃烧时产生的灰烬多,排放的烟气中含有大量的固体颗粒物,对环境和健康造成影响。
2.液体燃料主要包括汽油、柴油、天然气液化气等。
液体燃料的能量密度高,易于储存和运输,但在使用过程中会产生大量的尾气排放,其中包含对环境有害的化学物质。
3.气体燃料包括天然气、煤气和氢气等。
气体燃料具有清洁、高效的特点,燃烧后产生的废气较少,对环境影响较小。
因此,在一些特定领域得到广泛应用。
二、燃料的性质1.热值燃料的热值是指单位质量或单位体积燃料在完全燃烧时所释放的热量。
热值越高的燃料,其能量利用率越高,燃烧效率也越高。
2.易燃性燃料的易燃性是指燃料在受到外界能量激发后燃烧的速度和顺利程度。
易燃性越好的燃料,燃烧所需的能量越少,燃烧速度也越快。
3.灰分和挥发份含量燃料中的灰分和挥发份含量对燃烧过程中的热值和污染物排放都有一定影响。
灰分越高,燃烧后产生的灰烬和污染物也越多。
而挥发份含量越高,燃烧时产生的尾气排放也越多。
4.氧化性氧化性是燃料在空气中燃烧的倾向,氧化性越好的燃料,燃烧所需的能量越少,燃烧速度也越快。
5.稳定性燃料的稳定性是指在存储和运输过程中,燃料是否能够保持其性质不发生变化。
若燃料稳定性较差,容易发生氧化、挥发和分解等现象,对储存和管理都造成不利影响。
三、燃烧过程燃烧是指燃料与氧气在一定条件下发生化学反应,释放出热量和灭菌气体的过程。
下面将从燃料的燃烧条件、燃烧反应和燃烧机理三个方面对燃烧过程进行分析。
初中化学知识点归纳燃烧与燃料的选择初中化学知识点归纳——燃烧与燃料的选择燃烧是指物质与氧气发生剧烈反应并产生火焰、光热以及废气等现象。
燃烧是化学学科中非常重要的内容之一,它与我们的日常生活息息相关。
了解燃烧的原理以及燃料的选择对我们理解能源利用、环境保护等方面具有重要意义。
本文将对初中化学中有关燃烧与燃料选择的知识进行归纳总结。
一、燃料的分类燃料是指能够进行燃烧的物质。
它们主要可分为化石燃料和生物质燃料两大类。
1. 化石燃料化石燃料是指由生物体经过长时间埋藏、分解和变质而形成的燃料。
常见的化石燃料有煤、石油和天然气等。
化石燃料是人类社会主要能源来源,广泛应用于发电、加热、交通等领域。
2. 生物质燃料生物质燃料是指由生物体或其代谢物质作为能源来源的燃料。
例如,木材、秸秆、柴火等都是常见的生物质燃料。
生物质燃料属于可再生能源,对环境影响较小,因此在一些地区被广泛使用。
二、燃烧的要素与条件燃烧是一种化学反应,它通常有三个要素:燃料、氧气和点火源。
只有当这三个要素同时满足一定条件时,燃烧才能发生。
1. 燃料燃料是发生燃烧的物质,它能与氧气反应产生热量、光热等现象。
燃料可以是固体(如木材、煤)、液体(如汽油、柴油)或气体(如天然气)。
不同的燃料在燃烧时会产生不同的火焰颜色、光亮度等特征。
2. 氧气氧气是燃烧的最重要的条件之一,它能与燃料发生反应,产生大量的能量。
空气中含有约21%的氧气,因此在日常生活中,空气中的氧气是主要提供燃烧所需的。
在实验室或一些特殊环境中,也可以采用纯氧气进行燃烧。
3. 点火源点火源是引发燃烧的初始能源,它能提供足够的能量将燃料与氧气反应起来。
常见的点火源有明火、电火花、摩擦火花等。
通常情况下,燃料的挥发性越高,点燃所需的能量越低。
三、燃烧与能量转化燃烧是一种能量的转化过程,燃料与氧气反应时,化学能转化为热能、光能等形式的能量,并释放出来。
这种能量转化是通过氧化还原反应来实现的。
燃烧反应可以用通式进行表示,例如:燃料 + 氧气→ 二氧化碳 + 水 + 能量烷烃 + 氧气→ 二氧化碳 + 水 + 能量其中,燃料是碳氢化合物,燃烧过程中产生的二氧化碳和水是废气,而能量则可以利用于发电、供暖等方面。
种类
特点
优点缺点能量来源热值污染物排放
液化石油气(LPG):主要成分是甲烷①比汽油便
宜;②国际国
内丰富的储
量;③丁烷和
丙烷混合可以
形成一定量的
辛烷,使液化
气有较好的抗
爆性。
④易于
运输。
⑤辛烷
值高。
①相对较高的
更换费用;②
若用一些低质
的液化气,系
统需要定期调
试以维持恰当
的混合状态,
并易发生气阻
现象;③极度
寒冷天气下启
动受到液化气
混合中所需
丁烷含量的
限制
是炼油厂在进
行原油催化裂
解与热裂解时
所得到的副产
品。
标态:
25600kcal/m3
液态:
10847kcal/kg
完全燃烧后
产物是二氧
化碳和水。
无
粉尘,污染物
极少。
液化天然气(LNG):主要成分是丙烷和丁烷
1.辛烷值
高,燃烧速度
快,自燃温度
高,是一种抗
爆性能好的优
质燃料。
2.在
大气中爆炸下
限高于汽油。
3.与空气混合
是气-气混合,
较易混合均
匀,有利于完
全燃烧,降低
排放污染物。
4.液化石油气
可降低CO2排
放,减少温室
效应。
1.改装后的天
然气汽车动力
有所不足;2.
改装成本较
高;3.不易储
存;4.低负荷
下发动机的性
能和排放较差
混合气难以着
火,且燃烧缓
慢。
是天然气经压
缩、冷却至其
沸点(-161.5
摄氏度)温度
后变成液体
标态:
8500kcal/m3
液态:
11305kcal/kg
主要成分是
甲烷,燃烧后
对空气污染
非常小,而且
放出的热量
大
醇类燃料:主要有甲醇、乙醇两种
1.辛烷值比
汽油高,可采
用高压缩比,
提高热效率
2.携带方便
3.可燃界限
宽,燃烧速度
快 4.价格低
廉 5.其优点
是这些原料能
够再生
1.热值低。
2.
沸点低,蒸气
压高,容易产
生气阻 3.甲
醇有毒,腐蚀
性大 4.醇混
合燃料易分层
1.甲醇汽油是
由10%-2
5%的甲醇与
其他化工原
料、添加剂合
成的
2.乙醇主要采
用农林业产品
或者副产物等
发酵制取
热值较低,甲
醇的热值只有
汽油的48%,
乙醇的热值只
有汽油的
64%。
排气中相应
的含有
未燃甲醇
和甲醛等
非法规排
放,有毒
汽柴油 1.能量密度高
2.价格低
3.不
易变质4.便于
运输通过石油炼制
获得的汽油和
柴油
汽油:
7591.1kcal/l
柴油:
8534.5kcal/l
污染物有固
体悬浮微粒、
一氧化碳、二
氧化碳、碳氢
化合物、氮氧
化合物、铅及
硫氧化合物
等,污染较大。