催化作用原理课程教学大纲
- 格式:doc
- 大小:32.50 KB
- 文档页数:5

《催化原理》课程简介课程编号:03024917课程名称:催化原理/Principles of catalysis学分:2学时:32(实验:0上机:0课外实践:0)适用专业:应用化学建议修读学期:6开课单位:化学与化工学院应用化学系先修课程:无机化学、分析化学、有机化学、物理化学、结构化学考核方式与成绩评定标准:结合平时成绩以专题论文方式综合考查教材与主要参考书目:甄开吉, 等编著,《催化作用基础(第三版)》, 北京:科学出版社,2005年2月。
吴越,《催化化学(上下册)》,北京:科学出版社,2000年。
阎子峰,《催化原理导论(双语教材)》, 化学工业出版社, 2006年1月。
内容概述:中文:本课程系统讲授了化学反应过程中催化作用和原理、基本概念和基本研究方法,主要内容包括:基本概念,吸附作用,气固多相催化反应动力学基础以及不同催化剂(主要是金属催化剂和过渡金属氧化物催化剂)的催化机理及其在实际生产过程中的应用。
通过本课程的学习,让学生全面掌握催化作用的基础知识和基本规律,了解催化过程的化学本质及工业催化技术的基本要求和特性,为今后从事催化领域的科学研究工作打下良好基础。
英文:This course instructs the catalytic principle, basic concepts and research methods in chemical reaction processes. The main contents include:basic concept, adsorption,reaction kinetics foundation of gas-solid heterogeneous catalysis, catalytic mechanism and application in the actual production process of different catalysts (metal catalysts and transition metal oxide catalysts). This course enables students to master the basicknowledge and basic law of catalytic principle, know the chemical nature of catalytic process and the basic requirements and characteristics ofindustrial catalytic processes. Also, through this course, students can lay a good foundation for future research work in the field of catalysis.《催化原理》教学大纲课程编号:03024917课程名称:催化原理/Principles of catalysis学分:2学时:32(实验:0上机:0课外实践:0)适用专业:应用化学建议修读学期:6开课单位:化学与化工学院应用化学系先修课程:无机化学、分析化学、有机化学、物理化学、结构化学一、课程性质、目的与任务使学生了解有关催化剂与催化作用的基础知识,掌握金属及过渡金属氧化物催化剂等重要工业催化剂的催化反应原理,了解环境催化等本学科及交叉学科的发展动态。

催化原理教学大纲催化原理教学大纲引言:催化原理是化学领域中的重要学科,涉及到许多实际应用,如工业催化、环境保护和能源转换等。
本文旨在探讨催化原理教学的重要性,介绍催化原理的基本概念和原理,并提出一份催化原理教学大纲,以帮助教师和学生更好地理解和应用这一学科。
催化原理的重要性:催化原理在现代化学中扮演着重要的角色。
催化剂可以加速化学反应的速率,降低反应所需的能量,提高反应的选择性和效率。
催化剂广泛应用于工业生产中,如石油加工、化学合成和环境净化等领域。
了解催化原理有助于我们理解和改进这些实际应用,推动科学技术的发展。
催化原理的基本概念:催化是指在化学反应中,通过引入催化剂来改变反应的速率和机理,而催化剂本身在反应结束后不发生永久性变化。
催化剂可以通过多种方式影响反应,如提供反应表面、调整反应中间体的能量和稳定性,以及改变反应的活化能等。
在催化过程中,催化剂与反应物发生相互作用,形成中间体,然后再与中间体发生解离或反应,最终生成产物。
催化原理的基本原理:催化原理涉及到许多基本原理,包括催化剂的选择性、活性和稳定性等。
选择性是指催化剂对特定反应的偏好程度,即在多个可能的反应路径中选择最有利的路径。
活性是指催化剂对反应物的吸附能力和反应能力,高活性的催化剂可以有效地与反应物发生相互作用。
稳定性是指催化剂在反应条件下的稳定性,即催化剂在反应中不发生永久性变化。
催化原理的实际应用:催化原理在许多实际应用中起着重要的作用。
例如,在石油加工中,催化剂可以降低石油分子的裂解温度,提高燃料的产率和质量。
在化学合成中,催化剂可以加速有机合成反应,提高产物的选择性和收率。
在环境保护中,催化剂可以将有害气体转化为无害物质,净化废气和废水。
在能源转换中,催化剂可以促进能源的转化和存储,如光催化水分解和电池催化等。
催化原理教学大纲:为了更好地教授催化原理,以下是一份催化原理教学大纲的建议:1. 催化原理的基本概念和定义- 催化的概念和应用范围- 催化剂的定义和分类2. 催化原理的基本原理和机理- 催化剂的活性和选择性- 催化剂与反应物的相互作用- 催化剂的表面结构和反应机理3. 催化原理在实际应用中的案例分析- 工业催化的典型例子和应用- 环境保护中的催化应用- 能源转换中的催化应用4. 催化原理的实验技术和方法- 催化剂的制备和表征方法- 催化反应的动力学和热力学测量- 催化反应的机理研究和模拟5. 催化原理的前沿研究和发展趋势- 新型催化剂的设计和开发- 催化反应机理的深入研究- 催化原理在可持续发展中的应用结论:催化原理教学是化学教育中的重要内容,它不仅帮助学生理解化学反应的基本原理和机理,还培养了学生的实验技能和科学思维。

课程名称:催化作用原理一、课程编码:1000010课内学时:48学分:3二、适用学科专业:工业催化,应用化学,生物化工,化学工程,化学工艺以及其他相关专业。
三、先修课程:物理化学。
四、教学目标通过本课程的学习,使研究生:1、掌握各类催化剂的催化作用;2、掌握工业催化剂的制备方法;3、掌握各类催化剂结构表征与性能评价方法;4、能够分析催化反应体系中催化剂各组分与催化性能关系;5、能够利用催化知识,分析催化反应体系中催化剂影响目的产物的因素,深入了解催化反应过程;6、能够利用催化知识,进行催化剂的设计。
五、教学方式课堂讲授,学生查阅相关文献,材料自学与课堂讨论。
六、主要内容及学时分配1.概论4学时1.1催化、工业与环境1.2催化剂和催化反应1.3催化的基本特征和本质1.4催化反应发生的条件和方式1.5催化相关概念与术语2.催化作用的物理化学基础4学时2.1化学反应的电子概念(催化反应)2.2基元化学反应机理(催化反应)2.3晶体场和配位场理论(催化作用的基本理论)2.4均相、多相和酶催化反应机理的同一性2.5催化剂结构对其催化性能的影响2.6催化反应热力学和动力学2.7固体表面吸附与表面反应3.催化剂制备、结构表征及其性能评价10学时3.1催化剂的制备原理3.2催化剂的结构和性能3.3催化剂的表征方法3.4热分析技术在催化研究中的应用3.5电子显微技术在催化研究中的应用3.6电子能谱技术在催化研究中的应用3.7其它分析技术在催化研究中的应用3.8催化剂性能评价及其动力学分析4.酸碱催化剂及其催化作用机理6学时4.1酸碱催化剂及其性质4.2均相酸碱催化反应及其作用机理4.3多相酸碱催化反应及其作用机理4.4典型酸碱催化反应过程及其催化剂5.金属配合物催化剂及其催化作用原理6学时5.1金属配合物理论5.2金属配合物的催化特性5.3配位催化过程反应物分子活化、反应以及配位催化反应循环5.5典型配位催化反应过程及其催化剂6.金属催化剂及其催化作用原理6学时6.1金属的电子论6.2金属的几何论6.3金属催化的几何论和能量匹配论6.4金属催化反应机理6.5合金催化剂与负载型催化剂6.6重要的金属催化反应过程及其催化剂7.金属氧化物催化剂及其催化作用原理6学时7.1半导体的形成与能带理论7.2金属氧化物催化剂的电子催化理论7.3金属氧化物催化剂表面与催化性能7.4烃类的催化氧化理论7.5典型金属氧化物催化反应过程及催化剂7.6光催化及其复合催化作用机理8.生物催化剂及其催化作用原理4学时8.1酶的结构与性能8.2酶催化作用机理8.3典型生物催化反应过程及其催化剂9.催化与催化材料新进展2学时9.1工业催化剂的开发9.2工业催化剂的制备设计9.3催化与生态工业七、考核与成绩评定成绩以百分制衡量。

催化基础教学大纲催化基础教学大纲催化是一门重要的科学领域,它在化学、材料科学、能源等众多领域中发挥着重要作用。
为了培养学生对催化的深入理解和掌握,制定一份催化基础教学大纲是非常必要的。
本文将就催化基础教学大纲的制定进行探讨。
首先,催化基础教学大纲的制定需要明确教学目标。
催化基础教学的目标是培养学生对催化的基本概念、原理和应用的理解和掌握。
学生应该能够理解催化反应的基本概念,包括催化剂、反应速率、活性位点等;掌握催化反应的原理,包括催化剂的作用机理、反应动力学等;了解催化在化学、材料科学、能源等领域中的应用,包括催化剂的设计和合成、催化反应的工艺优化等。
其次,催化基础教学大纲的内容应该全面而系统。
催化基础教学大纲应该包括以下几个方面的内容:催化反应的基本概念,包括催化剂、反应速率、活性位点等;催化剂的作用机理,包括催化剂的吸附、解离、表面扩散等过程;催化反应的动力学,包括反应速率方程、反应速率常数等;催化剂的设计和合成,包括催化剂的选择、制备和表征等;催化反应的工艺优化,包括反应条件的选择、催化剂的再生等。
此外,催化基础教学大纲的教学方法应该多样化。
催化基础教学大纲的制定不仅要考虑到教学内容的全面性和系统性,还要考虑到教学方法的多样性。
催化基础教学应该采用多种教学方法,包括讲授、实验、讨论等。
讲授可以帮助学生了解催化反应的基本概念和原理;实验可以帮助学生掌握催化反应的操作技能和实验方法;讨论可以帮助学生深入理解和应用催化反应的知识。
最后,催化基础教学大纲的评估方式应该合理。
催化基础教学大纲的制定不仅要考虑到教学内容和教学方法,还要考虑到教学评估的方式。
催化基础教学的评估方式应该合理,既要考察学生对催化反应的理解和掌握,又要考察学生对催化反应的应用能力。
评估方式可以包括课堂测验、实验报告、项目设计等。
通过合理的评估方式,可以更好地了解学生的学习情况,及时调整教学内容和教学方法。
总之,催化基础教学大纲的制定是培养学生对催化的深入理解和掌握的重要途径。

《催化原理》课程教学大纲课程代码:080151003课程英文名称:Principle of catalysis课程总学时:40 讲课:40 实验:0 上机:0适用专业:化学工程与工艺大纲编写(修订)时间:2010.7一、大纲使用说明(一)课程的地位及教学目标本门课程为化学工程与工艺专业B方向的专业主干课,是选择催化专业方向学生必修的一门课程。
通过本门课程的教学,学生应系统地掌握工业催化的基本概念、基本原理、基本方法及技巧,为今后进一步深入学习和研究打下良好的理论基础。
(二)知识、能力及技能方面的基本要求通过本门课程的学习,学生应对催化科学的特点及重要性有所了解,认识催化作用的基本规律,掌握几种常用的工业催化剂及其相关的催化过程。
培养学生综合运用所学的基本知识的能力和工程实践能力。
(三)实施说明根据教学需要以及选用教材不同,教学内容可适当增减,各部分学时数可作适当的增删。
(四)对先修课的要求该课程在完成教学计划规定的公共基础课、大部分专业基础必修课和专业基础选修课教学之后开设。
先修课包括高等数学、无机化学、有机化学、物理化学、化工原理A1和化学反应工程。
(五)对习题课、实践环节的要求习题的设置应突出各部分重点,多联系工程实践。
(六)课程考核方式本课程的考核方式为考试,考试方法采用笔试,闭卷,课程总成绩为最终理论考试、平时考核(包括测验、作业等)的总和。
(七)参考书目《催化作用基础》,甄开吉编,科学出版社,2005《催化化学》,吴越编,科学出版社,1995二、中文摘要本课程是化学工程与工艺专业工业催化方向学生必修的一门主干课程。
方向学生在学习本课程之前必须掌握高等数学、物理化学、化工原理等课程。
本课程的授课对象是专业高年级学生。
本课程系统地介绍工业催化的基本原理、方法和技术。
通过本课程的学习,使学生掌握催化科学的基本原理,为工业催化应用打下基础。
三、课程学时分配表四、教学内容及基本要求第1部分绪论总学时(单位:学时):2 讲课:2 实验:0 上机:0 具体内容:1、催化科学的重要性;2、催化科学的形成;3、催化科学的特点;4、基本概念。

催化原理教学大纲课程名称:催化原理英文名称:The principle of catalysis总学时:32学时理论学时:32 实验学时:0 总学分:2.0一、课程的性质、目的及任务本课程主要介绍工业催化技术的应用以及催化剂设计、制备、表征的一般知识和规律。
研究催化剂结构与性质之间的关系,从微观的角度探讨催化剂组成、比例及表面层原子、分子及离子的位置、运动以及构型与催化剂性能的关系。
通过本课程的学习使同学们系统地掌握工业催化的基本概念、基本原理、基本方法及技巧,为今后的科研和开发打下良好的基础。
二、课程教学基本要求本课程要求学生掌握催化作用的基本原理,了解各类催化剂及其催化作用,包括固体酸碱催体、分子筛催化、金属催化、络合催化、金属氧化物和金属硫化物催化等,并跟踪工业催化的最新进展;初步了解工业催化剂的基本要求,催化剂的组成、制备原理和方法;初步了解催化实验用的反应器和检测仪器、手段等。
三、课程教学基本内容第一章催化作用与催化剂(含绪论)第一节绪论第二节催化作用与催化剂第二章均相催化第一节配位催化的主要原理及应用第二节酸碱催化的主要原理及应用第三章多相催化第一节多相催化的反应步骤第二节..吸附等温线第三节.金属表面上的化学吸附第四节.氧化物表面上的化学吸附第五节.固体酸碱催化剂及其催化作用第六节.分子筛催化剂及其催化作用第七节.金属催化剂及其催化作用第八节.金属氧化物和硫化物催化剂及其催化作用第四章酶催化第一节.酶的结构及命名第二节.酶催化的特征第三节.酶催化动力学第五章工业催化剂的制备与表征第一节工业催化剂的制备第二节..催化剂的使用、失活与再生第三节催化剂的表面积及其测定第四节催化剂的孔结构及其测定第五节催化剂微观结构的表征第六章工业催化剂的设计主要介绍国外几个主要的催化剂设计专家系统.学时分配表教学内容讲课时实验时实践时上]机时自学时习题课讨论时第一章催化作用与催化剂(含绪论) 4第二章均相催化 4第三章多相催化10第四章酶催化 4第五章工业催化剂的制备与表征8第六章工业催化剂的设计 2合计32总计32.主要参考书目[1]《工业催化剂设计与开发》,黄仲传等编著,华南理工大学出版社;[2]《工业催化原理》,李玉敏,天津大学出版社;[3]《液相化学反应动力学原理》,金家骏,上海科学技术出版社;[4]《催化剂成型》,朱洪法,中国石油化工出版社;1987;[5]《实用催化》,高正中,化学工业出版社,1996。

催化原理课程教学大纲催化原理课程教学大纲催化原理是化学工程与材料科学领域中的一门重要课程,它涉及到催化剂的性质、催化反应机理以及催化反应的工程应用等方面。
本文将围绕催化原理课程的教学大纲展开讨论,探讨如何有效地传授这门课程。
一、课程简介催化原理课程是化学工程与材料科学专业的核心课程之一,旨在培养学生对催化原理的基本理论和实践应用的理解。
通过本课程的学习,学生将掌握催化剂的基本概念、催化反应的动力学和热力学原理以及催化反应的工程应用等知识。
二、课程目标1. 培养学生对催化原理的基本概念和基本原理的理解;2. 培养学生对催化剂的性质和催化反应机理的掌握;3. 培养学生对催化反应的动力学和热力学原理的理解;4. 培养学生对催化反应的工程应用和催化剂的设计的认识。
三、教学内容1. 催化剂的基本概念和分类:介绍催化剂的定义、特点和分类方法,包括酸碱催化剂、金属催化剂、酶催化剂等;2. 催化反应的动力学和热力学原理:介绍催化反应的速率方程、反应机理和催化反应的热力学条件;3. 催化反应的工程应用:讨论催化反应在化学工程、石油化工、环境工程等领域的应用,包括催化裂化、催化加氢等;4. 催化剂的设计和改性:介绍催化剂的设计原则和改性方法,包括载体选择、活性组分的选择和催化剂的表面改性等。
四、教学方法1. 理论授课:通过讲授催化原理的基本概念和原理,引导学生建立催化反应的基本认识;2. 实验教学:组织学生进行催化反应实验,让学生亲自操作和观察催化反应过程,加深对催化原理的理解;3. 讨论与案例分析:组织学生进行小组讨论,分析和解决催化反应中的实际问题,培养学生的分析和解决问题的能力;4. 研究文献阅读:引导学生阅读相关的研究文献,了解最新的催化原理研究进展,培养学生的科研能力。
五、教学评估1. 平时成绩:包括课堂表现、作业完成情况等;2. 实验报告:评估学生在实验中的操作技能和实验结果的分析能力;3. 期末考试:考核学生对催化原理的理解和应用能力;4. 课程设计:要求学生根据所学知识设计一个催化反应的工程方案,评估学生的综合能力。

《工业催化》课程教学大纲工业催化第一章催化作用与催化剂基础第一节催化作用的定义与特征一、定义二、特征1、只能加速热力学上可行的反应2、只加速反应趋于平衡,而不改变平衡的位置3、通过改变反应历程改变反应速度4、降低反应活化能5、催化剂对反应具有选择性6、催化剂的寿命三、其他基本概念第二节对工业催化剂的要求一、估量一个催化剂价值的四个重要因素二、催化剂的工业性能第三节催化剂的组成与功能一、催化剂成分(固体Cat)二、活性组分1、主剂成分2、按活性组分作用分类3、按导电性分三、载体1、定义2、分类3、载体催化剂命名4、催化剂载体功能四、助催化剂1、帮助载体2、帮助活性组分3、一些主要过程常用助Cat和其功能4、存在的最适宜含量第四节催化体系分类一、相的均一性分类二、作用机理分类三、按反应类别分类第二章催化剂中的吸附作用第一节多相催化的反应过程一、多相催化反应步骤二、外扩散与外扩散系数 DE1、外扩散2、外扩散速率影响因数三、内扩散与内扩散系数 DI1、内扩散2、内扩散的三种类型第二节固体表面结构一、几个概念二、晶体表面的晶面1、晶体2、金属晶体的三种典型结构3、晶格、晶面4、暴露晶面的影响因数三、晶体的不完整性1、固体中缺陷分类2、点缺陷3、线缺陷4、结晶剪切5、堆垛层错与颗粒边界四、晶体表面与体相比较1、合金表面组成2、晶体表面结构3、氧化物表面组成五、晶体表面能量的不均匀性1、原子水平的团体不均匀2、表面力的差别六、晶体的不完整性与催化作用1、不完整性关联到表面催化活性中心2、表面结构与所处气氛有关3、表面组成与反应混合物组成有关第三节分子在固体表面的吸附一、物理吸附与化学吸附1、定义2、物理吸附与化学吸附的区别3、化学吸附与催化二、吸附质的可动性1、吸附质点的两种平均寿命2、定位吸附与非定位吸附3、固体Xe上吸附惰性气体的表面势能三、吸附的位能曲线1、气体分子撞击晶面情况2、吸附位能曲线3、过渡态4、物理吸附价值5、双原子分子另一种吸附情况四、化学吸附的类型1、离解吸附和不离解化学吸附2、均裂离解吸附和非均裂离解吸附3、离解化学吸附的氧化与还原4、非离解化学吸附下氧化与还原5、三种化学吸附键第四节晶体的电子结构一、分子轨道理论和固体能带模型1、原子轨道近似,相对能量和形状2、分子轨道理论3、能带的形成(固体)4、能带结构5、能级的密度6、能带结构理论说明7、物质按能带结构分类8、固体按导电性分类二、配位场模型1、配位场效应2、 d 轨道取向性3、3、实例三、价键理论—金属键的d%1、电子配对理论2、金属价键理论3、d 特性%第三章各类催化剂及催化作用第一节金属催化剂及催化作用一、金属催化剂1、种类2、用途3、特征二、金属催化剂的化学吸附1、气体在不同金属上化学吸附热变化2、气体在金属上化学吸附强度顺序3、金属按其对气体分子化学吸附的能力分类三、金属催化剂化学吸附的状态1、金属催化剂的电子逸出功φ2、反应物粒子的电势 I3、吸附状态四、化学吸附中的几何因素1、几何因素对活性影响2、理论五、吸附与催化——火山型原理1、火山型原理2、火山曲线3、实例六、一些气体的化学吸附态1、氢的吸附2、氧的吸附态2、氮的吸附态3、CO的吸附态5、烃类的吸附态6、乙炔7、苯8、饱和烃第二节固体酸碱催化剂一、定义、分类1、定义Brφnsted 和Lewis 定义2、分类二、机理1、金属氧化物2、混合金属氧化物3、影响酸位和碱位的因数三、固体表面酸、碱性测定1、酸位的类型及鉴定2、固体酸强度和酸量3、固体碱强度与碱量4、酸—碱对协同位5、固体超强酸、超强碱四、固体酸、碱催化作用1、酸位的性质与催化作用关系2、酸强度与催化活性和选择性关系3、酸量与催化剂活性关系4、正碳离子的形成及反应规律5、固体碱催化剂第三节分子筛催化剂一、概述1、沸石:2、沸石特点:3、沸石存在形式4、分类5、分子筛二、发展史1、五十年代——沸石2、六十年代——人工合成工业催化剂3、七十年代——工艺路线、产品质量改进4、八十年代——AlPO4磷酸铝分子筛5、九十年代以来三、分子筛沸石的结构特点1、基本结构单元2、环结构3、笼结构4、分子筛结构四、沸石分子筛的酸、碱催化性能及其调变1、酸中心的形成与本征催化性能2、沸石分子筛酸性调变五、分子筛择型催化性质1、反应物择型催化2、产物择型催化3、过渡状态限制择形催化剂4、分子交通控制的择型催化六、沸石分子筛催化剂碱催化和酸、碱协同催化作用七、新型磷酸铝分子筛 AlPO4第四章催化剂设计与制备第一节催化剂的分子设计基础一、催化剂分子设计的理论与实验1、理论2、实验二、催化剂分子设计的特点第二节催化剂分子设计方法一、催化剂设计方法分类1、传统经验法2、定性催化剂设计方法3、数学模型模拟辅助催化剂设计4、电子计算机辅助催化剂设计二、催化剂分子设计方法1.程序框图2.组分筛选3.热力学可行性分析4.催化剂原料的确定三、催化剂类别第三节工业催化剂的制备原理一、沉淀法1、沉淀过程和沉淀剂的选择2、影响沉淀的因素3、沉淀法类型4、典型沉淀法生产工艺二、浸渍法1、载体的选择和浸渍液的配制2、活性组分在载体上的分布与控制3、浸渍法分类4、工艺三、离子交换法1、无机离子交换剂制备(分子筛)2、有机离子交换剂制备(离子交换树脂)四、共混法五、固体催化剂的成型1、形状及使用性能六、干燥与焙烧1、干燥2、焙烧第三节常用催化剂的制备工艺一、活性氧化铝的制备(沉淀法)1、酸法沉淀工艺2、影响因素二、新型甲醇酮系催化剂制备(分步沉淀)1、目前使用工业催化剂(生产甲醇)2、新型合成甲醇铜素催化剂三、负载型镍催化剂的制备(浸渍沉淀法)1、浸渍沉淀的制备流程2、影响因素四、分子筛的合成(导晶沉淀法)1、高硅钠型分子筛原粉2、最佳原料配比第五节催化剂制备技术的新进展一、微乳化技术与催化剂二、稀土元素与催化剂三、纳米技术与催化剂四、超临界技术五、膜技术与催化剂六、绿色化学化工及环境友好催化剂。
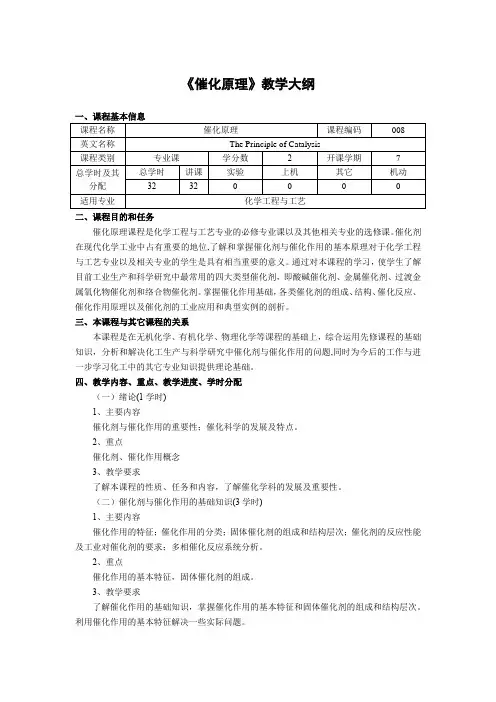
《催化原理》教学大纲二、课程目的和任务催化原理课程是化学工程与工艺专业的必修专业课以及其他相关专业的选修课。
催化剂在现代化学工业中占有重要的地位,了解和掌握催化剂与催化作用的基本原理对于化学工程与工艺专业以及相关专业的学生是具有相当重要的意义。
通过对本课程的学习,使学生了解目前工业生产和科学研究中最常用的四大类型催化剂,即酸碱催化剂、金属催化剂、过渡金属氧化物催化剂和络合物催化剂。
掌握催化作用基础,各类催化剂的组成、结构、催化反应、催化作用原理以及催化剂的工业应用和典型实例的剖析。
三、本课程与其它课程的关系本课程是在无机化学、有机化学、物理化学等课程的基础上,综合运用先修课程的基础知识,分析和解决化工生产与科学研究中催化剂与催化作用的问题,同时为今后的工作与进一步学习化工中的其它专业知识提供理论基础。
四、教学内容、重点、教学进度、学时分配(一)绪论(1学时)1、主要内容催化剂与催化作用的重要性;催化科学的发展及特点。
2、重点催化剂、催化作用概念3、教学要求了解本课程的性质、任务和内容,了解催化学科的发展及重要性。
(二)催化剂与催化作用的基础知识(3学时)1、主要内容催化作用的特征;催化作用的分类;固体催化剂的组成和结构层次;催化剂的反应性能及工业对催化剂的要求;多相催化反应系统分析。
2、重点催化作用的基本特征,固体催化剂的组成。
3、教学要求了解催化作用的基础知识,掌握催化作用的基本特征和固体催化剂的组成和结构层次。
利用催化作用的基本特征解决一些实际问题。
(三)催化剂的吸附、表面积、孔结构(2学时)1、主要内容催化剂的物理吸附和化学吸附;化学吸附类型和化学吸附态;吸附平衡与吸附等温方程;催化剂的表面积及孔结构。
2、重点物理吸附和化学吸附鉴别,吸附平衡,化学吸附态。
3、教学要求了解催化剂的物性及主要表征方法,催化剂的吸附。
(四)金属催化剂及其催化作用(8学时)1、主要内容金属催化剂的应用及催化作用;金属催化剂的化学吸附;金属催化剂电子因素与催化作用的关系;金属催化剂晶格结构与催化作用的关系;负载型金属催化剂及其催化作用;合金催化剂及其催化作用;金属催化剂催化作用的典型反应分析。

《催化原理》教学大纲、课程基本信息、课程教学目标1. 掌握有关催化的基本概念(如选择性,活性,稳定性,外扩散,内扩散,催化循环等等)和基本理论(如催化剂的酸中心、多位理论和配位催化理论等)。
2. 掌握如何将理论知识和应用研究有机结合,培养学生新的思维方法和创新能力。
三、理论教学内容与要求四、考核方式采用期末考试和平时考核相结合的考核方式。
总成绩为100分,其中期末考试成绩占总成绩的70%, 平时成绩(包括作业、出勤、课堂小测验等)占总成绩的30%。
五、习题1. 为什么说催化过程本质上是一个动力学过程?2. 加氢功能催化剂往往对脱氢反应也有活性,水合功能催化剂往往对脱水反应也有活性。
试给出解释。
3. 试比较各种表示催化剂活性方法的特点和要求。
4. 催化剂依照功能大致可以分为几类?5. 在为某原料寻找加氢催化剂时,利用简单的反应器试验过许多样品,催化剂均是粉末或仔细研磨过的材料。
每次试验均加0.1g催化剂到50ml原料内,良好搅拌,过一定时间测定H2的吸收速率。
在某些情况下,如果加入两倍量的催化剂,反应速率却提高至4—6倍。
这可能是什么原因。
6. 设反应C2H5 + H 2 T CH3其反应历程可能是:(1) C2H b <--> 2CH3 K i(2) CH 3 + H 2 t CH4 + H K 2(3) H + C 2H6 t CH4 + CH 3 K 3设反应(1)为平衡状态,对H作稳态处理,试证明1/2 2d[CH4]/dt=2k 2k1/2[C2H6]2[H2]7. 光气分解的总反应为COC2= CO + Cl 2,该反应历程为(1) Cl 2 <--> 2Cl •(2) Cl + COCl 2 t CO + Cl 3(3) Cl 3 <--> Cl 2 + Cl其中( 2)为控制步骤,( 1) , (3)为平衡状态,试证明反应速率方程为dx/dt = K [COCl 2 ][Cl 2]28. 为什么结构助剂不改变反应的活化能,而调变性助剂却有此功能?9. 硅藻土在使用前要用酸处理的作用。
催化作用原理课程教学大纲
英文名称:Catalysis Principles 课程编码:
学时:32 学分:2
课程性质:专业限选课课程类别:理论课
先修课程:无机化学、分析化学、有机化学、物理化学
开课学期:第五学期
适用专业:化学工程与工艺
一、课程的性质与任务
本课程是化学工程与工艺专业的专业限选课。
本课程的教学任务是:使学生理解催化剂与催化作用的基础知识,掌握酸碱催化剂、金属及过渡金属氧化物催化剂、络合催化剂等几种典型催化剂的催化作用原理,了解环境催化的特点及研究内容,使学生具备有关催化剂合成、表征与测试的基础知识及基本技能,使学生了解本学科的最新发展动态。
二、教学目标与要求
使学生了解有关催化剂与催化作用的基础知识,掌握酸碱催化剂、金属及过渡金属氧化物催化剂、络合催化剂等重要工业催化剂的催化反应原理,了解环境催化等本学科及交叉学科的发展动态。
使学生具备有关催化剂的合成、表征与测试等基本理论知识,了解相关的研究方法,培养学生分析和解决催化剂制备技术中各种实际问题的能力,以适应社会对于化工专业人才的需求。
三、课程的基本内容与教学要求
第一章催化剂与催化作用的基础知识
[教学目的与要求]:
了解催化剂与催化作用的基本特征、催化反应的分类等基础知识,明确固体催化剂的组成与结构,催化剂的反应性能及对工业催化剂的要求等。
[本章主要内容]:
1.1 催化剂与催化作用的特征
1.2 催化反应和催化剂的分类
1.3 固体催化剂的组成与结构
1.4 催化剂的反应性能
1.5 多相催化反应体系分析
[本章重点]:
1.催化剂与催化作用的基本特征
2.多相催化反应体系中的物理过程与化学过程分析
[本章难点]:
缔合活化催化循环和非缔合活化催化循环
第二章催化剂的表面吸附与孔内扩散
[教学目的与要求]:
了解有关固体表面吸附的基本概念,掌握物理吸附与化学吸附的特性、化学吸附的类型、化学吸附态和吸附平衡的两种表示方法,了解催化剂的表面积及其测定方法,了解催化剂重要孔结构参数的类型及测定方法,了解孔内扩散的类型及影相因素等。
[本章主要内容]:
2.1 催化剂的物理吸附与化学吸附
2.2 化学吸附类型和化学吸附态
2.3 吸附平衡与等温方程
2.4 催化剂的表面积及其测定
2.5 催化剂的孔结构与孔内扩散
[本章重点]:
1.催化剂的物理吸附与化学吸附
2.催化剂的表面积、孔结构及其测定方法
[本章难点]:
吸附等温方程的意义及其应用
第三章酸碱催化剂及其催化应用
[教学目的与要求]:
理解酸和碱定义、酸碱催化剂的应用及其类型,掌握固体酸碱的性质及其测量方法,重点掌握酸碱催化剂的催化机理,了解沸石分子筛催化剂的结构、特点、分类及其催化作用。
[本章主要内容]:
3.1 酸碱催化剂的应用及其类型
3.2 酸碱定义及酸碱中心形成
3.3 固体酸的性质及其测量
3.4 酸碱催化反应机理
3.5 沸石分子筛催化剂及其催化作用
[本章重点]:
1.均相和多相酸催化反应机理
2.沸石分子筛催化剂的结构、特点及其催化作用
[本章难点]:
1.固体酸性质的测量原理及方法
2.沸石分子筛催化剂的孔道结构及其酸性质调变
第四章金属催化剂及其催化作用
[教学目的与要求]:
熟悉金属催化剂的应用及其特征,重点掌握金属催化剂电子因素、晶体结构与催化作用的关系,掌握金属及负载型金属催化剂及其催化作用。
[本章主要内容]:
4.1 金属催化剂的应用及其特征
4.2 金属催化剂的电子因素与催化作用的关系
4.3 金属催化剂的晶体结构与催化作用的关系
4.4 负载型金属催化剂及其催化作用
4.5 合金催化剂及其催化作用
[本章重点]:
1.金属催化剂的电子因素对其催化性能的影响
2.金属催化剂的晶体结构对其催化性能的影响
[本章难点]:
负载型金属催化剂的分散度概念及其与催化性能的关系
第五章过渡金属氧化物催化剂及其催化作用
[教学目的与要求]:
了解过渡金属氧化物催化剂的应用及氧化物的类型,掌握半导体催化剂的化学吸附与半导体电子催化理论,理解过渡金属氧化物催化剂的氧化还原机理。
[本章主要内容]:
5.1 过渡金属氧化物催化剂的应用及类型
5.2 金属氧化物中的缺陷和半导体性质
5.3 半导体催化剂化学吸附与半导体电子催化理论
5.4 过渡金属氧化物催化剂的氧化还原机理
5.5 过渡金属氧化物中晶体场的影响
[本章重点]:
1.半导体催化剂的电子催化理论及其应用
2.过渡金属氧化物催化剂的氧化还原机理及其反应实例
[本章难点]:
1.过渡金属氧化物中晶体场理论
2.晶体场稳定化能的概念
第六章络合催化剂及其催化作用
[教学目的与要求]:
了解络合催化剂的应用,对络合催化剂的形成与络合物的反应有进一步的认识,掌握络合空位的形成、反应物的活化和络合催化剂的调变,理解络合催化反应机理及其典型催化反应实例等内容。
[本章主要内容]:
6.1 络合催化剂的应用及化学成键作用
6.2 络合催化剂的形成与络合物的反应
6.3 络合空位的形成、反应物的活化和络合催化剂的调变
6.4 络合催化机理
[本章重点]:
1.络合催化剂的配位体类型与络合物的反应
2.络合空位的形成、反应物的活化和络合催化剂的调变
3.络合催化机理
[本章难点]:
1.络合催化剂对反应物的活化
2.络合催化剂的调变
第七章催化剂的制备、使用、表征与测试
[教学目的与要求]:
详细了解沉淀、浸渍、还原、热分解、离子交换等传统催化剂制备方法,掌握有关催化剂的积碳、中毒、烧结等失活原因及催化剂的再生方法。
了解采用X射线衍射、红外光谱、紫外-可见光谱分析等技术进行催化剂物理性能测试的原理,了解催化剂的催化反应性能评价装置与过程。
[本章主要内容]:
7.1 催化剂的制备方法
7.2 催化剂的失活与再生
7.3 催化剂的表征与测试
[本章重点]:
1.催化剂的几种重要制备方法
2.催化剂的失活类型及其再生方法
[本章难点]:
几种催化剂表征与测试方法的原理与方法
第八章环境催化
[教学目的与要求]:
了解环境催化的特点和研究内容,重点掌握机动车尾气净化催化技术、脱硫、脱氮技术及CO2的催化治理技术,了解氯氟烃的催化治理和水污染治理方法,了解清洁燃料的生产和绿色催化技术的开发等。
[本章主要内容]:
8.1 环境催化的特点和研究内容
8.2 机动车尾气净化催化技术
8.3 脱硫、脱氮技术
8.4 CO2和氯氟烃的催化治理
8.5 水污染治理
8.6 清洁燃料的生产和绿色催化技术的开发
[本章重点]:
1.机动车尾气净化催化剂-三效催化剂的组成和发生的反应
2.对烟道气进行脱硫和脱氮的反应及所使用的催化剂
[本章难点]:
光催化氧化法治理水污染的原理及设备
四、课程学时分配
五、课程习题课(讨论课)的要求
无。
六、实验内容与要求
无。
七、教学方法及手段(含现代化教学手段)
本课程教学活动所运用的主要教学手段和方法是理论教学和运用多媒体课件相结合。
八、课程考核方式
本课程是考试课,考试的形式采用开卷。
本课程成绩评定按考试成绩确定。
九、课程教材及主要参考书
[课程教材]:
《催化剂与催化作用》第三版,王桂茹主编,大连理工大学出版社;2007年。
[课程主要参考书]:
1.《催化剂工程》,储伟主编,四川大学出版社,2006年。
2.《绿色催化过程与工艺》,王延吉,赵新强编著,化学工业出版社,2002年。
3.《催化剂工程导论》,王尚弟,孙俊权著,化学工业出版社,2001年。
4.《实用催化》,高正中编著,化学工业出版社,1996年。
5.《工业催化》,黄仲涛主编,化学工业出版社,1994年(2001年再版)。
6.《催化剂表征与测试》,J. R. 安德森,K. C. 普拉特著,庞礼,李琬,李国英,王建国译,烃加工出版社,1989年。
制定人:王丽琴
审定人:王丽琴
批准人:邵光杰。