高一化学硫酸、硝酸和氨
- 格式:ppt
- 大小:415.50 KB
- 文档页数:17


第四节氨硝酸硫酸课时1 氨气知识分层讲解学知识基础知识讲解敲黑板知识点 1 氨气【重点】1.氮的固定(1)氮元素的存在游离态:N2,占空气总体积的78%或总质量的75%。
氮元素化合态:硝酸盐等无机盐,蛋白质等有机物。
(2)氮的固定:将游离态的氮转变为氮的化合物叫做氮的固定。
【易错1】目前工业制取氨气的反应原理即人工固氮的反应。
2. 氨气的物理性质及喷泉实验(1)氨的物理性质①氨气是无色、有刺激性气味的气体。
②氨气的密度为0.771 g/L,比空气小;氨气极易溶于水,常温下,1体积水大约能溶解700体积NH3。
因此一般用向下排空气法收集氨气。
③氨气的沸点为-33.5℃,易液化,常用作制冷剂。
(2)氨气溶于水的喷泉实验示例1实验装置实验准备实验操作实验现象在干燥的圆底烧瓶中充满氨气,用带有玻璃管和滴管(滴管里预先吸入水)的塞子塞紧瓶口,倒置烧瓶,使玻璃管插入盛有水(含酚酞)的烧杯中打开橡胶管上的夹子,轻轻挤压滴管的胶头使少量水进入烧瓶。
烧杯中的溶液由玻璃管进入烧瓶,形成美丽的喷泉,烧瓶内液体颜色呈红色。
氮的循环【易错1】在判断氮的固定时,学生往往把由气态的含氮化合物转化为固态的含氮化合物的过程认为是氮的固定。
如:由氨气合成碳酸氢铵的过程。
喷泉划重点:氨气喷泉实验的解释①能形成喷泉说明氨气极易溶于水,使烧瓶内的压强迅速减小,烧杯内的水在大气压的作用下进入烧瓶;烧瓶内液体呈红色,说明氨气溶于水得到的溶液呈碱性。
②氨气喷泉实验成功的关键是:①装置气密性良好;②圆底烧瓶要干燥;③装置内气体的纯度要高。
3. 氨气的化学性质(1)氨与水的反应氨气溶于水时,大部分NH3与H2O反应生成一水合氨(NH3·H2O);常温下,一水合氨中有一小部分(约1%)电离成NH4+和OH-,所以氨水显弱碱性,发生反应的化学方程式为:NH3+H2O NH3·H2O、NH3·H2O NH4++OH-,或表示为:NH3+H2O NH3·H2O NH4++OH-。

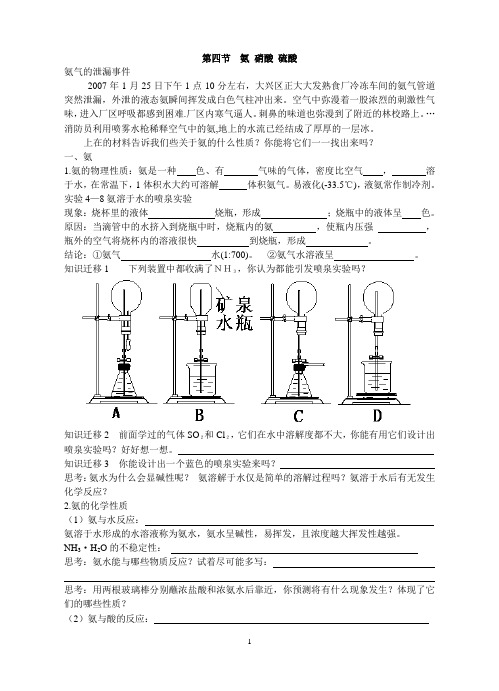
第四节氨硝酸硫酸氨气的泄漏事件2007年1月25日下午1点10分左右,大兴区正大大发熟食厂冷冻车间的氨气管道突然泄漏,外泄的液态氨瞬间挥发成白色气柱冲出来。
空气中弥漫着一股浓烈的刺激性气味,进入厂区呼吸都感到困难.厂区内寒气逼人。
刺鼻的味道也弥漫到了附近的林校路上。
…消防员利用喷雾水枪稀释空气中的氨,地上的水流已经结成了厚厚的一层冰。
上在的材料告诉我们些关于氨的什么性质?你能将它们一一找出来吗?一、氨1.氨的物理性质:氨是一种色、有气味的气体,密度比空气,溶于水,在常温下,1体积水大约可溶解体积氨气。
易液化(-33.5℃),液氨常作制冷剂。
实验4—8氨溶于水的喷泉实验现象:烧杯里的液体烧瓶,形成;烧瓶中的液体呈色。
原因:当滴管中的水挤入到烧瓶中时,烧瓶内的氨,使瓶内压强,瓶外的空气将烧杯内的溶液很快到烧瓶,形成。
结论:①氨气水(1:700)。
②氨气水溶液呈。
知识迁移1 下列装置中都收满了NH3,你认为都能引发喷泉实验吗?知识迁移2 前面学过的气体SO2和Cl2,它们在水中溶解度都不大,你能有用它们设计出喷泉实验吗?好好想一想。
知识迁移3 你能设计出一个蓝色的喷泉实验来吗?思考:氨水为什么会显碱性呢?氨溶解于水仅是简单的溶解过程吗?氨溶于水后有无发生化学反应?2.氨的化学性质(1)氨与水反应:氨溶于水形成的水溶液称为氨水,氨水呈碱性,易挥发,且浓度越大挥发性越强。
NH3·H2O的不稳定性:思考:氨水能与哪些物质反应?试着尽可能多写:思考:用两根玻璃棒分别蘸浓盐酸和浓氨水后靠近,你预测将有什么现象发生?体现了它们的哪些性质?(2)氨与酸的反应:氨与酸反应生成铵盐。
铵盐又叫铵态氮肥。
思考:有一位农民看到自己买的一袋碳酸氢铵化肥受了潮,就在太阳底下晒,等他下午去取时,发现少了许多,是谁偷了他的氮肥?铵盐可以做氮肥体现了铵盐的什么物理性质?铵盐的性质①铵盐都易溶于水②铵盐受热易分解NH4HCO3受热:NH4Cl受热:③铵盐与碱反应(NH4)2SO4 + NaOH:实质:(离子方程式)NH4HCO3 + NaOH:实质:(离子方程式)一切铵盐的共同性质,实验室可利用这个性质来检验NH4+的存在。


高一化学每日一练——第四章第四节氨、硝酸、硫酸(1)班级姓名1.下列气体不能用H2SO4干燥的是()A.CO2B.NH3C.SO2D.HC12.关于氨的下列叙述中,错误的是()A.氨易液化,因此可用来作制冷剂B.氨易溶解于水,因此可用来作喷泉实验C.氨极易溶解于水,因此氨水比较稳定(不容易分解)D.氨溶解于水显弱碱性,因此可使酚酞试剂变为红色3.下列物质不能用于检验NH3的是A.湿润的红色石蕊试纸B.无色的酚酞溶液C.蘸有浓盐酸的玻璃棒D.湿润的蓝色石蕊试纸4.下列反应属于氮的固定的是()A.空气在雷电作用下所产生NO B.NO和O2生成NO2C.铜与浓硝酸反应产生NO2D.NH4Cl与Ca(OH)2反应生成NH35.关于反应的说法中正确的是()A.NH3做还原剂,体现氧化性B.O2做氧化剂,体现氧化性C.参加反应的O2中只有一部分做氧化剂,其中做氧化剂的和不做氧化剂的物质的量之比是4:6D.该反应中氧化剂和还原剂的质量之比是5:46.下列实验现象与氧化还原反应有关的是A.NH3使湿润的红色石蕊试纸变蓝B.向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成C.NO2通入水中,气体由红棕色逐渐转变为无色D.向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀7.在下列变化①N2和H2合成氨,②NO与O2化合,③NH4Cl受热分解中,按氮元素被氧化、被还原、既不被氧化又不被还原的顺序排列,正确的是A.①②③B.②①③C.③②①D.③①②8.有关氨气的实验较多,下面对这些实验的实验原理的分析中,正确的是 ( )A .氨气极易溶解于水的性质可以解释氨气的喷泉实验B .氨气的还原性可以解释氨气与氯化氢的反应实验C .铵盐的水溶性大是实验室中用NH 4Cl 和Ca(OH)2的混合物制取氨气的原因D .NH 3·H 2O 的热不稳定性可以解释实验室中用加热氨水的方法制取氨气9.将湿润的红色石蕊试纸放在进行下列实验的试管口,试纸变蓝色的有 ( )A .加热浓氨水B .加热NH 4Cl 固体C .加热NH 4Cl 和Ca(OH)2的混合物D .加热饱和NH 4Cl 溶液 10.如图所示,室温下A 、B 两个容积相等的烧瓶中分别集满了两种气体(同温、同压),( )A .①②③B .②③①C .③①②D .③②①11.右图是实验室制取氨气的装置图。
高一化学人教版,第一章第一节第五讲酸碱盐的性质酸:电离时产生的阳离子全部都是氢离子。
例如:H₂SO₄(硫酸),HCl(盐酸),HNO₃(硝酸),H₂CO₃(碳酸)碱:电离时产生的阴离子全部都是氢氧根离子。
例如:NaOH(氢氧化钠),KOH(氢氧化钾),Ca(OH)₂(氢氧化钙),NH₃·H₂O,NH₄OH(氨水)盐:电离时生成含有金属阳离子(或NH₄铵根)和酸根离子的化合物。
例如:Na₂CO₃(碳酸钠),CuSO₄(硫酸铜),NH₄NO₃(硝酸铵)仅由氢离子和酸根离子、非金属单质结合生成的化合物为酸。
由金属离子和氢氧根离子结合生成的化合物为碱。
由金属离子和酸根离子结合生成的化合物为盐,不一定都是如此。
例子如Cu₂(OH)₂CO₃碱式碳酸铜,有氢氧根酸碱盐类化合物一定含有非金属元素。
1、酸的化学性质(1)酸+金属——盐+氢气(2)酸+金属氧化物——盐+水氧化铁和稀盐酸反应:Fe2O3+6HCl==2FeCl3+3H2O氧化铁和稀硫酸反应:Fe2O3+3H2SO4==Fe2(SO4)3+3H2O氧化铜和稀盐酸反应:CuO+2HCl==CuCl2+H2O氧化铜和稀硫酸反应:CuO+H2SO4==CuSO4+H2O(3)酸+碱——盐+水(中和反应)盐酸和烧碱起反应:HCl+NaOH==NaCl+H2O盐酸和氢氧化钙反应:2HCl+Ca(OH)2==CaCl2+2H2O氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3==AlCl3+3H2O 硫酸和烧碱反应:H2SO4+2NaOH==Na2SO4+2H2O(4)酸+盐——另一种酸+另一种盐大理石与稀盐酸反应:CaCO3+2HCl==CaCl2+H2O+CO2↑碳酸钠与稀盐酸反应:Na2CO3+2HCl==2NaCl+H2O+CO2↑碳酸氢钠与稀盐酸反应:NaHCO3+HCl==NaCl+H2O+CO2↑硫酸和氯化钡溶液反应:H2SO4+BaCl2==BaSO4↓+2HCl2、碱的化学性质(1)碱+非金属氧化物——盐+水苛性钠暴露在空气中变质:2NaOH+CO2==Na2CO3+H2O苛性钠吸收二氧化硫气体:2NaOH+SO2==Na2SO3+H2O苛性钠吸收三氧化硫气体:2NaOH+SO3==Na2SO4+H2O消石灰放在空气中变质:Ca(OH)2+CO2==CaCO3↓+H2O消石灰吸收二氧化硫:Ca(OH)2+SO2==CaSO3↓+H2O(2)碱+酸——盐+水(中和反应,方程式见上)(3)碱+盐——另一种碱+另一种氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH3、盐的化学性质(1)盐(溶液)+金属单质——另一种金属+另一种盐铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu(2)盐+酸——另一种酸+另一种盐碳酸钠与稀盐酸反应:Na2CO3+2HCl==2NaCl+H2O+CO2↑碳酸氢钠与稀盐酸反应:NaHCO3+HCl==NaCl+H2O+CO2↑(3)盐+碱——另一种碱+另一种盐氢氧化钙与碳酸钠:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH (4)盐+盐——两种新盐氯化钠溶液和硝酸银溶液:NaCl+AgNO3==AgCl↓+NaNO3硫酸钠和氯化钡:Na2SO4+B aCl2==BaSO4↓+2NaCl。
硫酸、硝酸和氨(3)一、教学目标【知识目标】浓硫酸和硝酸的氧化性、氨的化学性质。
【水平目标】观察水平及实验动手水平、形成规律性理解和总结归纳的水平。
【道德情感目标】1、重视对学生知识的建构水平的培养,让同学们理解知识结构由主干知识和基本知识构成,主干知识作支撑。
2、重视环境教育,提倡环境保护的思想。
二、重点与难点【重点】浓硫酸、硝酸的强氧化性,氨的化学性质。
【难点】浓硫酸、硝酸的强氧化性,氨的化学性质。
三、教学器材投影仪四、教学方法与过程:探究式教学,实验总结法[知识补充]:介绍氨分子结构,呈三角锥形。
氨易液化,液化的同时放出大量的热。
液态氨汽化时要吸收大量的热,所以常用作致冷剂,举例说明液氨的用途。
如:首都体育馆的制冷设备。
[迁移试问]:NH3和H2O互溶解的情况如何?[实验演示]:演示【实验4-8】观察实验现象并根据实验现象分析以下问题:(1)烧瓶内为什么会形成喷泉?(2)溶液为什么变成红色?[强调指出]:只要能够引起烧瓶内气压迅速下降的情况,都能够产生喷泉。
[深化知识]:氨溶于水使酚酞溶液变红,说明产生了一种新物质即一水合氨,是弱碱,氨水具有碱性。
它能够局部电离出铵根离子和氢氧根离子。
NH3+H2O⇌NH3·H2O⇌NH4++OH-NH3·H2O⇌NH3+H2O氨与酸反应,演示“魔棒生烟或者空杯生烟”,并加以解释。
NH3+HCl=NH4Cl补充NH3与O2的反应:4NH3+5O2=4NO+6H2O从氧化还原的角度分析氨的催化氧化。
铵盐的不稳定性:参照课本内容铵盐的检验:增强碱共热,有刺激性气味的气体产生,能够使红色石蕊试纸变蓝。
方程式训练。
NH3的实验室制法:展示装置,2H4Cl+Ca(OH)2= CaCl2+ 2H3+22O补充实验室快速制取NH3的方法:(1)加热浓氨水制氨气。
在烧瓶中加入2~4 mL浓氨水,加热即可得到氨气。
此法也可用于做喷泉实验。
(2)在常温下,用浓氨水与固体烧碱混合制氨气。