蛋白激酶小分子抑制剂
- 格式:docx
- 大小:912.56 KB
- 文档页数:4


生物医学中的小分子抑制剂研究在生物医学研究中,小分子抑制剂具有广泛的应用前景。
它可以通过特定的结构与生物分子结合,从而影响生物分子的功能,达到治疗疾病或预防病变的目的。
近年来,小分子抑制剂研究取得了很大的进展,成为药物研发领域的重要一环。
一、小分子抑制剂研究的意义小分子抑制剂是目前常见的药物类型之一。
相对于生物大分子,如蛋白质、核酸等,小分子具有分子结构简单、制备容易、易于运输和渗透生物膜等优势。
它可以准确地作用于特定的靶标分子,从而实现药物的精准治疗。
除此之外,小分子抑制剂还可以在药代动力学方面表现出更好的特点。
它可以通过口服、静脉注射等多种途径快速达到治疗浓度,在疾病的快速发展和急救等方面具有重要的意义。
二、抑制剂的分类以前,研究者常常将抑制剂分为远程控制型和邻近控制型两类。
但随着研究的深入,发现这种划分方式并不准确,无法真正体现小分子抑制剂的作用方式。
根据抑制剂与靶标分子的结合方式,现在一般将抑制剂分为竞争性抑制剂、非竞争性抑制剂、可逆性抑制剂和不可逆性抑制剂等四种。
竞争性抑制剂是指抑制剂与靶标分子竞争同一位点的结合,从而影响靶标分子的功能。
竞争性抑制剂的缺点在于,药物作用时必须与靶标分子相互竞争,容易出现受体饱和现象。
因此,竞争性抑制剂的用途受到了一定限制。
非竞争性抑制剂与靶标分子的结合位点不同,不会与其竞争。
它可以通过改变靶标分子的构象或使其失活来实现抑制目的。
相比竞争性抑制剂,非竞争性抑制剂的效果更加稳定,但也更难制备。
可逆性抑制剂与靶标分子的结合是可逆的,药物在体内的作用只能持续一段时间。
不可逆性抑制剂与靶标分子的结合则是永久性的,药物在体内作用的时间较长。
不可逆性抑制剂一般用于治疗慢性疾病。
三、小分子抑制剂的研究方法小分子抑制剂的研究方法主要有结构基础研究和药物发现研究两种。
结构基础研究是指通过对靶标分子的结构研究,设计出合适的药物分子,以实现药物抑制的目的。
这种方法需要先对靶标分子进行晶体结构分析或NMR等实验技术的研究,从而确定结合位点的位置和空间构型。

银屑病生物制剂及小分子抑制药物科普常常被人们称作“牛皮癣”的银屑病是一种在生活中常见的慢性炎症性的、不具传染性、具有复发特点的传染性皮肤病。
在医学领域,这种病的病因尚未彻底的查明,也没有研究出具体的治疗方法。
一旦患病,就有可能伴随一生,因此常常被称作“不死的癌症”。
据相关的数据统计,全球有超过1.25亿的银屑病患者,银屑病成为了一个全球性的难题。
在我国,几乎有超过700多万的患者在遭受银屑病的困扰,银屑病患者数量也在呈现逐年剧增的趋势。
目前在医学界对银屑病的治疗只能达到近期的治疗效果,无法防治其复发,在目前看来,生物制剂和相关的小分子抑制药物治疗银屑病起到了可观的治疗效果,那么,治疗银屑病具体的生物制剂和小分子抑制药物有哪些呢?生物制剂:1.斯库奇尤抗单:这种生物制剂的别名是苏金单抗,是专门针对白介素的单克隆抗体抑制剂,通过特异性结合使得致病因子无法发挥其治病作用,此外,苏金单抗也会选择性识别致病因子,防止其与人体的受体细胞相结合,此两种作用,有效的抑制了致病因子在人体内的活动及引发银屑病的能力。
从宏观上来讲,这种药物在银屑病的治疗中,减少了患者发红、肿痒的症状,还能快速的增生新的细胞。
据目前的治疗经验,这种生物制剂对于已知的几种类型的银屑病具有显著的疗效。
2.英夫利昔单抗:英夫利昔单抗是19世纪90年代被美国政府批准投放到医疗市场上的一种药物,目前也已经获得中国食品药物监督总局的批准并已投放在中国的医疗界。
英夫利昔单抗对于可溶性的、跨膜性的致病因子具有特异的亲和力,致使诱导免疫反应的模式有一定的偏移,以便于清除人体内活化的T细胞,随之减少银屑病多余血管的生成和细胞的浸润,此外,还可以相对的抑制角质形成细胞的不正常过度增殖。
需要注意的是,英夫利昔单抗是通过人体的静脉输入药物,需要患者按时、定期住院,以便于在出现任何不良反应时能得到及时的解决;但需要引起高度重视的是,对于英夫利昔单抗有关成分过敏的患者、患有结核病及其他感染者、重度心力衰竭患者不得使用英夫利昔单抗。
化学抗肿瘤药物经过半个多世纪的发展,已经进入靶向治疗药物时代。
小分子靶向药物在临床上的应用日益增多,在一些肿瘤类别中已经进入一线用药地位,比如肾癌、慢粒白、多发性骨髓瘤等。
本文对小分子靶向治疗药物做一综述。
小分子靶向治疗药物简介一、受体酪氨酸激酶抑制剂作为抗肿瘤药物靶点的酪氨酸激酶有两类,一类是受体酪氨酸激酶(RTKs),另一类是非受体酪氨酸激酶(nrRTKs)。
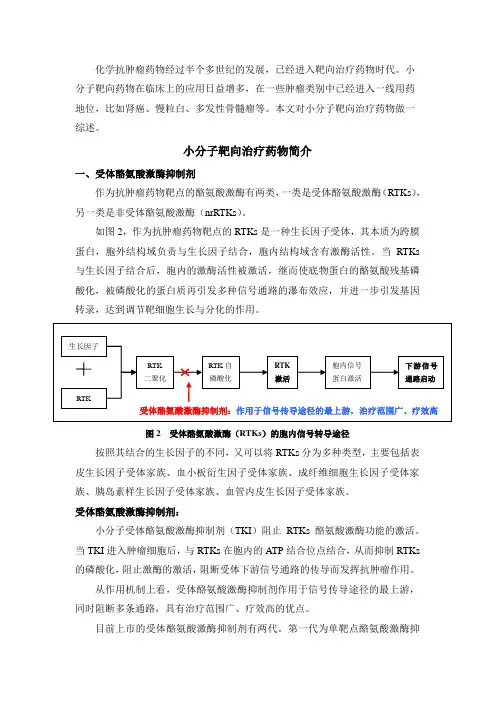
如图2,作为抗肿瘤药物靶点的RTKs是一种生长因子受体,其本质为跨膜蛋白,胞外结构域负责与生长因子结合,胞内结构域含有激酶活性。
当RTKs 与生长因子结合后,胞内的激酶活性被激活,继而使底物蛋白的酪氨酸残基磷酸化,被磷酸化的蛋白质再引发多种信号通路的瀑布效应,并进一步引发基因转录,达到调节靶细胞生长与分化的作用。
图2 受体酪氨酸激酶(RTKs)的胞内信号转导途径按照其结合的生长因子的不同,又可以将RTKs分为多种类型,主要包括表皮生长因子受体家族、血小板衍生因子受体家族、成纤维细胞生长因子受体家族、胰岛素样生长因子受体家族、血管内皮生长因子受体家族。
受体酪氨酸激酶抑制剂:小分子受体酪氨酸激酶抑制剂(TKI)阻止RTKs酪氨酸激酶功能的激活。
当TKI进入肿瘤细胞后,与RTKs在胞内的ATP结合位点结合,从而抑制RTKs 的磷酸化,阻止激酶的激活,阻断受体下游信号通路的传导而发挥抗肿瘤作用。
从作用机制上看,受体酪氨酸激酶抑制剂作用于信号传导途径的最上游,同时阻断多条通路,具有治疗范围广、疗效高的优点。
目前上市的受体酪氨酸激酶抑制剂有两代。
第一代为单靶点酪氨酸激酶抑制剂,如吉非替尼、厄洛替尼。
表已上市的酪氨酸激酶抑制剂注:EGFR:表皮生长因子受体,属HER家族;VEGFR:血管内皮生长因子;PDGFR:血小板衍生因子;HER2:HER家族的一种受体;Abl-Bcr:一种非受体酪氨酸激酶;Raf:酪氨酸激酶的下游信号通路中的一种蛋白;Flt-3:Src:一种非受体酪氨酸激酶;c-kit:Ret:胶质细胞源性神经营养因子的受体吉非替尼为EGFR酪氨酸激酶抑制剂,主要用于非小细胞肺癌,对酪氨酸激酶基因编码区突变型肿瘤的有效率高达80%以上。

小分子抑制剂化学生物学
(实用版)
目录
一、什么是小分子抑制剂
二、小分子抑制剂的分类
三、小分子抑制剂的应用
四、小分子抑制剂的发展前景
正文
一、什么是小分子抑制剂
小分子抑制剂是一种化学物质,具有抑制生物体内某些特定分子的功能。
通常,这些分子是蛋白质,而小分子抑制剂可以阻止它们在生物体内的活性。
小分子抑制剂被广泛用于治疗各种疾病,包括癌症、糖尿病和炎症等。
二、小分子抑制剂的分类
小分子抑制剂可以分为不同的类别,其中最常见的是激酶类抑制剂。
已上市的小分子创新药物中,80% 以上属于激酶类抑制剂,包括受体酪氨酸激酶抑制剂、非受体酪氨酸激酶抑制剂和丝氨酸/色氨酸激酶抑制剂三个类别。
蛋白激酶是一种重要的信号传导分子,它们在细胞内调控许多生物学过程。
三、小分子抑制剂的应用
小分子抑制剂在医学领域具有广泛的应用。
例如,吉非替尼(gefitinib)是一种针对表皮生长因子受体(EGFR)的酪氨酸激酶抑制剂,已被用于治疗非小细胞肺癌。
另一个例子是利妥昔单抗(rituximab),它是一种针对 CD20 受体的单克隆抗体,已被用于治疗淋巴瘤和慢性淋巴细胞性白血病。
四、小分子抑制剂的发展前景
随着对生物学信号传导机制的深入了解,研究人员发现了越来越多的潜在药物靶点。
这为小分子抑制剂的研究和开发提供了广阔的空间。
此外,计算机辅助药物设计和高通量筛选技术等先进方法的应用,也大大加快了小分子抑制剂的研发速度。

表皮生长因子受体酪氨酸激酶抑制剂的研究进展一、本文概述表皮生长因子受体(EGFR)酪氨酸激酶抑制剂(TKIs)是一类针对EGFR信号通路的关键药物,广泛应用于非小细胞肺癌、结直肠癌、头颈癌等多种癌症的治疗。
本文旨在综述近年来EGFR TKIs的研究进展,包括其作用机制、药物研发、临床应用以及面临的挑战等方面。
通过深入了解EGFR TKIs的研究现状和发展趋势,有望为癌症治疗提供新的思路和方法,进一步改善患者的生活质量和预后。
本文将从EGFR TKIs的作用机制出发,阐述其如何通过抑制EGFR 的酪氨酸激酶活性来阻断癌细胞的增殖和转移。
接着,我们将回顾EGFR TKIs的药物研发历程,介绍目前市场上主流的EGFR TKIs药物及其特点。
在此基础上,我们将重点关注EGFR TKIs在临床试验中的应用情况,包括其疗效、安全性以及耐药性等问题。
我们将探讨EGFR TKIs面临的挑战和未来发展方向,包括如何克服耐药性、提高治疗效果以及拓展新的适应症等。
通过本文的综述,我们希望能够为相关领域的研究者和临床医生提供有价值的参考信息,推动EGFR TKIs在癌症治疗中的进一步应用和发展。
二、EGFR-TK抑制剂的分类与机制表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TK抑制剂)是近年来癌症治疗领域的重要突破,其通过抑制表皮生长因子受体(EGFR)的酪氨酸激酶活性,从而阻断细胞的生长、增殖和转移过程。
根据药物的作用机制和化学结构,EGFR-TK抑制剂主要分为两大类:可逆性抑制剂和不可逆性抑制剂。
可逆性抑制剂,如吉非替尼和厄洛替尼,能够与EGFR的ATP结合位点形成可逆性结合,从而竞争性地抑制酪氨酸激酶的活性。
这类药物对于EGFR敏感突变的非小细胞肺癌具有较好的疗效,但在长期治疗过程中,患者往往会出现耐药现象。
不可逆性抑制剂,如阿法替尼和奥希替尼,能够与EGFR的ATP 结合位点形成共价键,导致EGFR的永久性失活。

小分子抑制剂成为研究的前沿热点
以蛋白激酶为靶标的分子靶向抗肿瘤药物由于重点针对肿瘤发生发展机制中的关键酶或蛋白,具有选择性好、安全性较高等优点,基于蛋白激酶的分子靶向药物已成为目前抗肿瘤药物研究的前沿领域,至今已有二十余个蛋白激酶小分子抑制剂获批上市。
渐变性淋巴瘤激酶(anaplastic lymphoma kinase,ALK)是蛋白激酶家族重要成员,2007年在非小细胞肺癌中首次发现的ALK融合基因EML4-ALK,引发了靶向ALK 抑制剂的研发热潮。
针对ALK 融合基因的第一代药物—克唑替尼(Crizotinib)已于2011年上市,成为标志性的个性化治疗药物,在ALK阳性患者中获得良好的无进展生存和客观有效率。
不断的反复的实验才能得到需要的结果,陶素生化现可提供诸多不同信号通路的抑制剂、调节剂以及小分子化合物,并附客户评价、产品相关参考文献、技术支持等助力您的实验研究,且保证产品的高纯度和高活性,交货及时并附带完整的谱图信息。
陶素生化能够提供的118种酪氨酸激酶抑制剂的独特集合,可用于高通量筛选和高内涵筛选通过前期临床研究和临床实验,生物活性和安全性得到验证其中一些抑制剂已经得到FDA批准,优点如下:
作用于酪氨酸激酶,如EGFR,VEGFR,SRC,c-Met和JAK
结构多样,药效显著,可渗透细胞
具有充分详细的结构说明,IC50值,及客户反馈资料
NMR和HPLC技术保证产品高纯度。
PI3K/AKT/mTORPI3K/AKT/mTOR是调节细胞周期的重要细胞内信号通路。
PI3K/AKT/mTOR信号通路与细胞的生长、存活、增殖、凋亡、血管生成、自吞噬过程中发挥着重要的生物学功能。
该通路是由磷脂酰肌醇3- 激酶(PI3Ks)、丝氨酸/苏氨酸蛋白激酶(Akt)和哺乳动物雷帕霉素靶蛋白(mTOR)组成。
PI3K/Akt/mTOR通路过程PI3K激活后产生PIP3, PIP3促使PDK1(phosphoinositide dependent kinase-1)磷酸化含有PH结构域的信号AKT蛋白(Ser308),从而活化AKT。
AKT有很多下游效应,可通过磷酸化多种酶、激酶和转录因子等下游因子,进而调节细胞的功能。
mTOR,是PI3K/Akt 下游的一种重要的丝氨酸-苏氨酸蛋白激酶,调节肿瘤细胞的自噬的经典通路。
PI3K/Akt/mTOR信号通路图按靶点分类:*PI3KPI3K,是一种胞内磷脂酰肌醇激酶,也具有丝氨酸/苏氨酸(Ser/Thr)激酶的活性。
能够通过PI3K诱发PIP3生成的激活因子,则能够激活Akt 信号途径,包括受体酪氨酸激酶、整合素、B 细胞和T 细胞受体、细胞因子受体、G 蛋白偶联受体等等。
*Akt又称PKB或Rac,是一种丝氨酸/苏氨酸特异性蛋白激酶B,在细胞存活和凋亡中起重要作用,如葡萄糖代谢、凋亡、细胞增殖、转录和细胞迁移。
Akt的Thr308可以被PDK1磷酸化,而被部分激活。
或者473位点上的丝氨酸被mTORC2磷酸化,激发Akt的完全酶活性。
*mTORmTOR是细胞生长和增殖的重要调节因子。
mTOR与其它蛋白质结合,形成两种不同蛋白质复合物,mTORC1和mTORC2,参与调节不同的细胞过程。
*GSK-3。

学报Journal of China Pharmaceutical University2020,51(3):260-269小分子ERK抑制剂的研究进展梁停停1,2,王文杰1,郝思远1,何光超1,2,徐云根1,2*(1中国药科大学药物化学系,南京211198;2江苏省药物分子设计与成药性优化重点实验室,南京211198)摘要细胞外信号调节激酶(ERK)是一种丝/苏氨酸蛋白激酶。
作为RAS-RAF-MEK-ERK信号通路中关键的下游蛋白,其异常活化在肿瘤的发生发展中起着重要作用。
选择性ERK1/2抑制剂能够阻断ERK信号通路,同时克服上游靶点突变而导致的耐药性。
本文概述了MAPK信号通路的组成、ERK的结构与功能以及ERK信号通路在肿瘤发生发展中的作用,并重点介绍一些具有代表性的处于临床和临床前研究阶段的ERK抑制剂。
关键词细胞外信号调节激酶;细胞外信号调节激酶抑制剂;抗肿瘤;耐药性;进展中图分类号R914.5文献标志码A文章编号1000-5048(2020)03-0260-10doi:10.11665/j.issn.1000-5048.20200302引用本文梁停停,王文杰,郝思远,等.小分子ERK抑制剂的研究进展[J].中国药科大学学报,2020,51(3):260–269.Cite this article as:LIANG Tingting,WANG Wenjie,HAO Siyuan,et al.Research progress of ERK small molecule inhibitors[J].J China Pharm Univ,2020,51(3):260–269.Research progress of ERK small molecule inhibitorsLIANG Tingting1,2,WANG Wenjie1,HAO Siyuan1,HE Guangchao1,2,XU Yungen1,2*1Department of Medicinal Chemistry,China Pharmaceutical University,Nanjing211198;2Jiangsu Key Laboratory of Drug Molecular Design and Optimization,Nanjing211198,ChinaAbstract Extracellular signal-regulated kinase(ERK)is a kind of serine/threonine protein kinase.As a key downstream protein in RAS-RAF-MEK-ERK signaling pathway,its abnormal activation plays an important role in the development of tumors.Selective ERK1/2inhibitors can block ERK signaling pathway while overcoming drug resistance caused by upstream target mutation.In this paper,the components of MAPK signaling pathway, the structure and functions of ERK and the role of ERK signaling pathway in tumor development are summarized, and some representative ERK inhibitors in clinical or preclinical studies are emphasized.Key words extracellular signal-regulated kinase(ERK);ERK inhibitors;antitumor;drug resistance;progressThis study was supported by the Undergraduate Innovation and Entrepreneurship Training Program of China Pharmaceutical Univer⁃sity(No.201910316099)RAS-RAF-MEK-ERK信号通路是一条广泛存在于哺乳动物细胞中的信号级联通路,在细胞的分化、存活、衰老和凋亡等细胞活动中发挥着极其重要的作用[1-2]。
FDA批准的激酶小分子抑制剂类药物及分类一览蛋白激酶蛋白激酶(Kinase)是细胞生命活动重要的信号使者,可催化将ATP末端的γ-磷酸基团转移至底物上,从而将各种信号进行传递(图1)。
蛋白激酶参与了众多的生理过程,包括细胞增殖、存活、凋亡、代谢、转录以及分化等。
药理学及病理学研究表明,对于很多疾病,如肿瘤、炎症性疾病、中枢神经系统疾病、心血管疾病及糖尿病等,蛋白激酶都是一个理想的药物靶点。
图1 Mechanism of protein kinases and related publications对于蛋白激酶的研究始于20世纪50年代,并在90年代随着MAPK/ERK、JAK 及PI3K等信号通路的揭示而达到一个研究热潮。
迄今为止,在人体中发现了518种蛋白激酶,而编码具有激酶活性蛋白的基因则高达900多种。
与之相对应,有关激酶抑制剂的研究也逐步发展,并在激酶作用机制的阐明过程中扮演了重要角色,并成为重要的药物研究热点。
该领域研究的文献数量也是逐年上升,从侧面反映了其在基础研究和药物发现中的重要性。
蛋白激酶抑制剂及其分类过去的15年间,激酶抑制剂作为药物候选的研究取得了长足的进步,不论是基础研究还是在工业界。
在人体现有药物靶点里面,蛋白激酶家族成员占比高达10%(FDA批准药物分子靶点深度解读)。
2001年,第一个激酶抑制剂类药物Imatinib获得FDA批准,成为该领域发展的里程碑,此后十年该类药物以平均每年获批一种的速度稳步发展。
而在2012年1月至2015年2月期间,小分子激酶抑制剂类药物迎来爆发式发展,共有15种新药获得审批。
截至2016年12月底,共有31种小分子激酶抑制剂类药物获得审批,同时还有大量的化合物处于临床或临床前研究中。
除此之外,科研人员还解析了超过5000种的蛋白激酶或蛋白激酶-抑制剂复合体的晶体结构,且超过五分之一的人类蛋白激酶具有明确的小分子抑制剂。
因此,小分子激酶抑制剂已成为药物研发的一个热点领域。
MAPK丝裂原活化蛋白激酶(MAPK)信号通路介导信号从细胞表面向细胞核内转导,通过三级激酶级联的形式传导细胞外信号,调控着细胞的生长、分化、炎症、凋亡、癌化、肿瘤细胞的侵袭和转移等多种生理活动过程。
MAPK通路参与了许多疾病的发展,包括阿尔茨海默病(AD)、帕金森病(PD)、肌萎缩性侧索硬化(ALS),在癌症、免疫及神经退行性疾病的治疗中发挥了重大作用。
MAPK通路转导过程MAPK家族在哺乳动物细胞中3个经典转导通路:MAPK(ERK)、C-Jun N末端kinse/应激激活蛋白激酶(JNK/SAPK)和p38激酶。
每个与MAPK相关的级联反应由不少于三种酶串联激活:MAPK激酶激酶(MAPKK)、MAPK 激酶(MAPKK)和MAPK激酶(MAPK)。
MAPK通路被多种细胞外和细胞内刺激激活,包括肽生长因子、细胞因子、激素和各种细胞应激源。
在ERK信号通路中,ERK1/2被MEK1/2激活,而MEK1/2被Raf激活。
Raf被Ras-GTPase激活,其激活是由表皮生长因子受体等RTKs诱导的。
JNK和p38 MAPK信号通路被不同类型的细胞应激激活。
JNK路径由JNK(一种MAP2K(如MKK4(SEK1)或MKK7))和MAP3K(如ASK1、TAK1、MEKK1或MLK3)组成。
在p38通路中,p38被MKK3或MKK6激活,这些MAP2K被JNK通路中功能相同的MAP3K激活。
MAPK信号通路图Selumetinib (AZD6244) 606143-52-6 MEK1 14 nM *RafAZ 628 878739-06-1 无细胞BRAF,BRAFV600E105 nM *p38 MAPK*JNK。