《金属有机化学》作业参考答案分解
- 格式:doc
- 大小:835.01 KB
- 文档页数:8


初三化学金属的化学性质试题答案及解析1.废旧金属的回收利用不仅可以节约金属资源,而且可以减少对环境的污染。
硬铝是铝、铜、硅的合金,是火箭、飞机、轮船等制造业的主要原料。
下图是从废铝中回收镁、铝的生产流程(部分生成物省略)请回答下列问题:(1)写出步骤①中的任意一个化学方程式。
(2)步骤②中的分离操作为;需用到的玻璃仪器有玻璃棒、烧杯、(填仪器名称)(3)步骤③的化学方程式为:;(4)步骤④的基本反应类型;(5)铝具有很好抗腐蚀性的原因是。
【答案】(1)Mg + H2SO4="==" MgSO4+ H2↑或2Al + 3H2SO4="==" Al2(SO4)3+ 3H2↑;(2)过滤、漏斗;(3)Mg(OH)2+2HCl==MgCl2+2H2O;(4)分解反应;(5)铝在空气中与氧气反应,其表面形成一层致密的氧化物薄膜,从而阻止铝进一步氧化。
【解析】根据生产流程(1)步骤一中的反应方程式为:Mg + H2SO4="==" MgSO4+ H2↑或2Al+ 3H2SO4="==" Al2(SO4)3+ 3H2↑;(2)步骤二中的分离操作名称为过滤;因为是固液分离;需用到的玻璃仪器有玻璃棒、烧杯、漏斗等;(3)步骤三的化学方程式为Mg(OH)2+2HCl==MgCl2+2H2O;(4)步骤四的基本类型为分解反应;(5)铝具有很好的抗腐蚀性能的原因是:铝在空气中与氧气反应,其表面形成一层致密的氧化物薄膜,从而阻止铝进一步氧化。
【考点】金属资源的回收利用、化学方程式的书写、反应类型的判断2.同学们在帮助老师整理实验室时,从1、2号橱窗中发现了两瓶失去标签的黑色粉末药品,并确定了这两瓶黑色粉末是木炭粉、铁粉、氧化铜、高锰酸钾中的两种。
他们继续进行了分析、试验和反思:【查阅资料】 CuO、Fe2O3等金属氧化物与酸反应,生成盐和水(1)分析:小燕同学认为一定不是高锰酸钾,原因是__________________________________;(2)实验一:实验操作原因是:_______________________________________________________________;(4)实验二:他们又进行了如下实验:将两种黑色粉末混合加热(实验装置如下图),发现黑色粉末逐渐变_______,澄清石灰水变____________。

第四章 有机金属化合物【补充习题及答案】1.简述EAN 规则,指出其作用。
答案:有效原子序数(Effective Atomic Number )规则,简称EAN 规则。
该规则预言稳定存在的有机金属化合物应该是符合“金属原子的电子总数加上所有配体提供的电子数等于同周期的稀有气体的原子序数”要求的化合物。
对于过渡金属元素,每个金属原子的价电子数加上配体提供的电子数等于18的化合物是稳定的,因此该规则又称为“18电子规则”。
EAN 规则是一条经验规则,其将有机金属化合物的电子结构系统化,可用于定性解释或预言有机金属化合物的稳定性。
2.请给出含有下列有机配体的配合物实例:(1)共轭4电子配体;(2)共轭5电子配体;(3)单电子烷基配体。
答案:(1)含有共轭4电子配体CH 2=CHCH =CH 2的例子: FeOC CO CO HCH 2C CH CH 2(2)二茂铁;(3)Al (C 2H 6)33.试用价键(VB )法解释[PtCl 3(C 2H 4)]-配离子中的化学成键。
答案:Pt 2+为d 8电子构型,其5d 、6s 、6p 22y x −x 和6p y 轨道组成4个dsp 2杂化轨道。
3个杂化轨道接受3个Cl -配体的3对孤对电子,形成3个σ–键。
第4个杂化轨道接受C 2H 4配体的π–电子形成第4个σ–键,同时Pt 2+的d xz 电子向C =C 键的π*轨道反馈,形成1个反馈π–键。
4.完成下列反应式:C 5H 6Mg 500~600 ºC Co CO H 2Fe (CO )5NaMn (CO )5Br Mn (CO )5-Fe (CO )42-H 3O +(1)(2)(4)(5)(3) 答案: ℃ (1) 2C 5H 6 + Mg (C 2H 5)2Mg + H 2↑(2)2Co + 8CO + H 20~35MPa 2HCo (CO )4(3)Fe(CO)5 + 2Na Na 2[Fe(CO)4] + CO(4) Mn(CO)5Br + Mn(CO)5Mn 2(CO)10 + Br (5) Fe(CO)42 + H 3O HFe(CO)4 + H 2O -5.指出下列配体中哪些是π 配体,哪些是π 酸配体:CO C 5H 5− N 2 CN − PR 3 AsR 3 C 6H 6 C 2H 4 C 4H 6 bipy phen答案:π 配体:C 2H 4、C 4H 6、C 5H 5−、C 6H 6π 酸配体:CO 、N 2、CN −、PR 3、AsR 3、bipy 、phen6.双氮配合物中N 2配体的伸缩振动频率一般比自由N 2分子低100~300 cm -1,最多可降低600 cm -1 。

剑门中学2019年寒假化学假期作业人教版第八单元课题3《金属资源的利用和保护》第1课时解析及答案编写者:化学组执教者:学生:【学习目标】1、知道常见的用来提炼金属的矿石,记住可用来炼铁的矿石。
2、了解炼铁的基本原理。
3、会根据化学方程式对含有某些杂质的反应物或生成物进行有关计算。
【知识准备】分析“真金不怕火炼”的原因:。
解析:“真金不怕火炼”证明金在高温下也不会与氧气反应,说明金的化学性质比较稳定。
初学单【教材助读】画出本节课内容的相关知识点,思考下列问题自然界中金属存在的形式有哪些?什么叫矿山?任何冶炼金属铁?【预习自测】阅读课本第15—16页内容,勾画出本节课内容的相关知识点,思考下列问题1、地壳中居前五位的元素含量由大到小的排列顺序为,地壳中含量最多的元素与含量最多的金属元素所形成的化合物的化学式为解析:地壳中居前五位的元素含量“氧、硅、铝、铁、钙”;地壳中含量最多的元素“氧”和最多的金属元素“铝”,所形成的化合物的化学式为“氧化铝(Al2O3)”。
2、地球上的金属资源广泛的存在于和中,除少数很不活泼的金属如、等以形式存在外,其余都以形式存在。
解析:地球上的金属资源广泛的存在于“地壳和海洋”中,除少数很不活泼的金属如“金、银”等以“单质”形式存在外,其余都以“化合物”形式存在。
3、工业上把能叫作矿石,常见的铁、铜、铝的矿石是工业炼铁的主要设备是,原料是、、、等。
解析:工业上把能提炼金属的矿物叫作矿石,常见的铁、铜、铝的矿石是“赤铁矿、磁铁矿、黄铁矿菱铁矿、铝土矿、黄铜矿、辉铜矿”,工业炼铁的主要设备是高炉,原料是焦炭、铁矿石、石灰石、空气。
【我的疑问】深学单【活动与探究】探究一:根据课本第16页上面提炼金属的矿石图,比较哪种铁矿石最适宜炼铁。
(提示:可考虑铁元素的含量高低及在冶炼过程中对环境的影响大小)解析:常见的铁矿石有:磁铁矿(主要成分是四氧化三铁)、赤铁矿(主要成分是三氧化二铁)、褐铁矿(主要成分是Fe2O3、 3H2O)、菱铁矿(主要成分是FeCO3)、黄铁矿(主要成分是FeS2)理论上最适宜炼铁则选择含铁量最高的,所以,磁铁矿(72%)赤铁矿(70%)是最适宜的,理由是含铁量最高。

第八章--金属和金属材料(人教版)课题1---金属材料题号解析1 密度小,具有抗腐蚀性。
2 铁:可用于做菜刀、镰刀、锤子等;利用了硬度大的性质。
铜:可用于制电线、火锅等;利用了其导电性好,导热性好,熔点高的性质。
金:可用于制作项链、戒指等饰品;利用了其具有较好的金属光泽的性质。
点拨:物质的性质决定物质的用途。
3需要有光泽好,抗腐蚀,硬度大的性质。
提示:合金的强度和硬度一般比组成它们的纯金属更高,抗腐蚀性能等也更好。
4 (1)外科手术刀:不锈钢,因为其抗腐蚀性好。
(2)防盗门:锰钢,硬度大。
(3)门锁:黄铜,因为强度高,可塑性好、易加工、耐腐蚀。
(4)自行车支架:锰钢,因为其韧性好,硬度大。
5该金属可能的用途有:制作机器零件、火箭、飞机、轮船、电线、电榄、化工和通讯设备等。
6 解:1 000 kg铁红中铁的质量=1 000 kg××100%=1 000 kgX xl00%=700 kg答:1 000 kg铁红中最多含铁的质量为700 kg。
点拨:利用化学式中某元素的质量分数来求物质中某元素的质量。
课题2---金属的化学性质题号解析1 常温下铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步被氧化,因此铝具有良好的抗腐蚀性能。
如果刷洗铝制品时,用钢刷、沙等来摩擦,就会破坏铝制品表面的致密氧化膜,使铝被腐蚀的速度加快。
2 配制波尔多液的硫酸铜溶于水可制成硫酸铜溶液,铁与硫酸铜在溶液中反应,使铁制品被腐蚀,硫酸铜变质发生反应的化学方程式为Fe+CuS04=FeS04+Cu,所以不能用铁制容器配制波尔多液,也不能在配制时用铁棒搅拌。
3 ①C+O2CO2。
(化合反应)或C+2CuO2Cu+CO2 (置换反应)②CO2+C2CO (化合反应) ③3Fe+2O2Fe3O4 (化合反应)④Fe3O4+4CO3Fe+4CO2⑤Fe+H2SO4=FeSO4+H2↑(置换反应)或Fe+CuSO4=FeSO4+Cu(置换反应)⑥Fe+2HCl=FeCl2+H2↑(置换反应)Fe+CuCl2=FeCl2+Cu(置换反应)点拨:本题主要熟练掌握有关化学方程式的书写,并会判断反应类型。

化学与可持续发展第四章开发利用金属矿物和海水资源第一节•、金属矿物的开发利用、金属的存在:除了金、钳等少数金属外,绝大多数金属以化合态的形式存在于自然界。
1、金属冶炼的涵义:简单地说,金属的冶炼就是把金属从矿石中提炼出来。
金属冶炼的实质是把金属元素从化2+nO 。
M合态还原为游离态,即H (化合态)(游离态)得电子、被还原3、金属冶炼的•般步骤:(1)矿石的富集:除去杂质,提高矿石中有用成分的含量。
(2)冶炼:利用氧化还原反应原理,在-定条件下,用还原剂把金属从其矿石中还原出来,得到金属单质(粗)。
(3)精炼:采用淀的方法,捉炼纯金属。
4、金属冶炼的方法⑴电解法:适用于一些非常活泼的金属。
电解电解电W 4A12A1O (熔融)+30 f Mg+C12NaCl (熔慰〉t 2Na+Cl f MgCl (熔融)22222s(2)热还原法:适用于较活泼金属。
药温高温岛温Zn+C0f 3CO2Fe+f W0+3H ZnO+CFeO+3COW+3HO 212122常用的还原剂:焦炭、CO、H等。
•些活泼的金属也可作还原剂,如A1, 2鯛高温2Cr+A1O (铝热反应)OFe+2AlCrO+2Al (铝热反应)2Fe+AlO 33323222(3)热分解法:适用于一些不活泼的金属。
△△ 4Ag+ 2Ag2HgOOO t 2Hg+O f 2225、(1)回收金属的意义:节约矿物资源,节约能源,减少环境污染。
(2)废I口金属的最好处理方法是回收利用。
(3)回收金属的实例:废1口钢铁用于炼钢:废铁屑用于制铁盐;从电影业、照相业、科研单位和医院X 光室回收的定影液中,可以捉取金属银。
二、海水资源的开发利用1、海水是-个远未开发的巨大化学资源宝库海水中含有80多种元素,其中Cl、Na、K、Mg. Ca、S、C、F、B、Br、Sr 11种元素的含量较高,其余为微量元素。
常从海水中提取食盐,并在传统海水制盐工业基础上制取镁、钾、溟及其化合物。
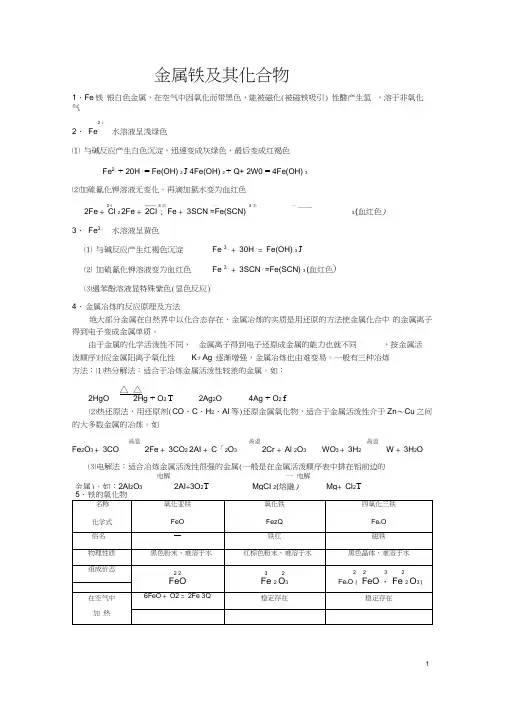
金属铁及其化合物1、Fe 铁 银白色金属,在空气中因氧化而带黑色,能被磁化(被磁铁吸引) 性酸产生氢气2 +2、 Fe 水溶液呈浅绿色⑴ 与碱反应产生白色沉淀,迅速变成灰绿色,最后变成红褐色Fe 2++ 20H 「= Fe(OH) 2 J 4Fe(OH) 2 + Q+ 2W0 = 4Fe(OH) 3⑵加硫氰化钾溶液无变化,再滴加氯水变为血红色2 I --------3 丰 一 3 丰 一 ______2Fe + Cl 2 2Fe + 2CI ; Fe + 3SCN =Fe(SCN) 3(血红色)3、 Fe 3+水溶液呈黄色⑴ 与碱反应产生红褐色沉淀 Fe 3 ++ 30H 「= Fe(OH) 3 J⑵ 加硫氰化钾溶液变为血红色Fe 3 ++ 3SCN 「=Fe(SCN) 3 (血红色)⑶遇苯酚溶液显特殊紫色(显色反应) 4、 金属冶炼的反应原理及方法绝大部分金属在自然界中以化合态存在,金属冶炼的实质是用还原的方法使金属化合中 的金属离子得到电子变成金属单质。
由于金属的化学活泼性不同, 金属离子得到电子还原成金属的能力也就不同 ,按金属活泼顺序对应金属阳离子氧化性K +T Ag +逐渐增强,金属冶炼也由难变易。
一般有三种冶炼方法:⑴热分解法:适合于冶炼金属活泼性较差的金属。
如:△ △2HgO2Hg + O 2 T2Ag 2O4Ag + O 2 f⑵热还原法,用还原剂(CO 、C 、H 2、Al 等)还原金属氧化物,适合于金属活泼性介于 Zn 〜Cu 之间的大多数金属的冶炼。
如咼温咼温Fe 2O 3 + 3CO 2Fe + 3CO 2 2AI + C 「2O 32Cr + Al 2O 3⑶电解法:适合冶炼金属活泼性很强的金属(一般是在金属活泼顺序表中排在铝前边的,溶于非氧化 咼温WO 3 + 3H 2 W + 3H 2O电解金属)。
如:2AI 2O 32AI +3O 2T一 电解MgCI 2(熔融)Mg + CI 2T、习题巩固1由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③ 加盐酸;④过滤;⑤浓缩结晶。
![金属有机化学课件和习题及答案]](https://uimg.taocdn.com/4f46a807f18583d049645982.webp)


一、错题重做1、用N A表示阿伏加德罗常数的值,下列叙述正确的是A.含有N A个原子的氢气在标准状况下的体积为22.4 LB.25 ℃,1.01×105 Pa下,64 g SO2中含有的原子数为3N AC.40 g NaOH溶解在1 L水中,则其100 mL溶液中含Na+数为0.1N AD.标准状况下,11.2 L CCl4含有的分子数为0.5N A二、教学过程金属的化学性质一、金属在自然界中的存在及通性金属在自然界中的存在1.自然界中绝大多数金属元素的存在形态是。
2.地壳中含量占据前两位的金属元素是。
金属的通性1.金属的物理通性2.金属的化学通性(1)金属化学性质特点(2)金属还原性的强弱取决于其失去电子的难易程度,而不是失去电子的个数。
典例1:下列推理正确的是A.铝粉在氧气中燃烧生成Al2O3,故铁丝在氧气中燃烧生成Fe2O3B.铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜C.活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中D.钠与氧气、水等反应时钠均作还原剂,故金属单质参与反应时金属均作还原剂同步训练:1.下列关于金属的叙述中正确的是A.常温下所有的金属都是固态B.金属具有导电、导热和延展性C.地壳中含量最多的金属铁元素D.金属元素大多数以游离态存在于自然界2.下列关于金属性质的叙述正确的是A.金属一般都容易导电导热,有延展性B.金属具有较高的硬度和熔点C.所有金属都是固态D.金属单质都能与稀H2SO4反应产生H23.下列有关金属元素性质的叙述正确的是A.金属元素的原子只有还原性,离子只有氧化性B.金属元素在化合物中一定显正化合价C.金属元素在不同化合物中化合价一定是不同的D.金属元素的单质在常温下均为固体4.下列关于金属的通性说明不正确的是A.金属的熔点差别较大B.在自然界中没有游离态的钠C.金属单质在化学反应中既可作氧化剂又可作还原剂D.与酸反应越剧烈的金属活泼性越强5.人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。

金属的化学性质(基础) 知识讲解含答案解析一、初中化学金属的化学性质选择题1.将a、b、c三种金属分别投入稀盐酸中,只有b溶解并产生气泡;把a和c分别放入硫酸铜溶液中,在a表面有铜析出,c没有变化。
则a、b、c的金属活动性顺序是()A.c>b>aB.b>a>cC.a>c>bD.b>c>a2.下列关于金属材料的说法不.正确的是A.硬铝(铝合金)的硬度大于纯铝B.铁在干燥的空气中容易生锈C.常温下,铝能与空气中的氧气反应,在其表面生成致密的氧化铝薄膜D.金属资源的回收利用既保护了环境,又节约了矿石资源3.X、Y、Z三种金属中,只有Z能和稀硫酸反应;将Y放人X的盐溶液中,Y表面有X析出。
则X、Y、Z三种金属的活动性顺序为A.X > Z > Y B.Y > X > Z C.Y > Z > X D.Z > Y > X4.等质量的稀硫酸分别与足量的镁、铁、锌三种金属反应,下列图象能正确生产氢气质量与反应时间之间关系的是()A.B.C.D.5.为探究铁、铜、银的金属活动性顺序,下列各组试剂不可以的是( )A.Fe、Ag、Cu(NO3)2B.Fe、Cu、AgNO3C.Fe、CuSO4、AgNO3D.Fe、Cu、Ag、HCl6.对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂不可行的是()A.Fe、Ag、CuSO4溶液B.Cu、Ag、FeSO4溶液C.Fe、Cu、稀盐酸、AgNO3溶液D.Cu、FeSO4溶液、AgNO3溶液7.新型材料纳米铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,工业上可以利用H2 和 FeCl2 在高温反应器中制备,同时得到 HCl。
下列有关说法错误的是( )A.制备纳米级铁粉的反应属于置换反应B.纳米级铁粉与氧气反应,生成物是 Fe3O4C.反应前需向反应器中通入氮气,目的是排除装置中的空气D.纳米级铁粉比普通铁粉更易与氧气反应是因为物质种类不同8.金属钴(Co)与铁的化学性质相似,都能与稀盐酸反应,在化合物中钻元素常显+2、+3价,下列说法正确的是( )A.CoCl3读作“氯化亚钴B.CoCl3中钴元素的化合价为+2价C.金属铜不能与CoCl2溶液发生反应D.CoCl2中钻元素的质量分数约为33.3%9.如图所示,在等臂杠杆两端各系一个等质量的铁球,调平后将分别浸没在稀H2SO4和CuSO4溶液中,一段时间后,杠杆将会()A.右端上翘B.左端上翘C.保持平衡D.无法判断10.现有甲、乙、丙三种金属,如果把甲和丙分别放入稀硫酸中,甲溶解并产生氢气,丙不反应.如果把乙和丙分别放入硝酸银溶液中,过一会儿,在丙表面有银析出,而乙没有变化.根据以上实验事实,甲、乙、丙的金属活动性顺序正确的是A.甲>乙>丙B.甲>丙>乙C.丙>甲>乙D.乙>丙>甲11.将过量的铁粉投入硫酸和硫酸铜的混合溶液中,充分反应后过滤,滤出剩余的铁和生成的铜,在滤液里含有的溶质是()A.FeSO4B.CuSO4C.Fe2(SO4)3D.H2SO412.某工厂废液中含有 Fe(NO3)2和 Cu(NO3)2两种溶质,取部分废液于烧杯中,加入一定量的锌粉,测定所得溶液中某溶质质量与时间的关系如图所示,同时得到以下结论:①图中纵坐标表示 Cu(NO3)2的质量②a 点时溶液中有三种溶质,b 点时溶液中有两种溶质③c 点时烧杯中有两种金属单质,d 点时烧杯中有三种金属单质④完全反应后烧杯中溶液呈浅绿色⑤完全反应后过滤,滤渣中加入少量稀盐酸,一定有气泡产生其中正确结论的个数是()A.4 个B.3 个C.2 个D.1 个13.印刷铜制电路板的“腐蚀液”是FeCl3溶液。
《金属有机化学》作业一选择题1.最早的哪个金属有机化合物是1827年由丹麦药剂师Zeise合成的。
()A. (CH3)4TiB. K[Pt(C2H4)Cl3]C. (CH3)2HgD. CH3MgCl2.二茂铁(C5H5)2Fe属于哪一类非经典键合的化合物?()A. M—C键中为缺电子型键B. M—C键中碳原子为π键电子给予体的多中心键化合物C. M—C键以夹心型键形成的π键化合物D. M—C键以σ—π配键形成的化合物3.烯烃和B—H键的加成遵循以下哪个规则?()A. Markovnikov规则B. 反Markovnikov规则C. Zaitsev规则D. 反Zaitsev规则4.下列有关烷基铝说法不正确的是()A.烷基铝化合物是缺电子化合物B.烷基铝化合物一般是强的Lewis酸C.当三烷基铝的烷基为烷氧基所取代后,烷基铝化合物的反应性即降低。
D.从烷基铝和烯烃的反应能得到有很长链的烷基的化合物5.Ni(CO)4的几何构型是()A.正四面体型 B. 正方锥型 C.八面体型 D. 三角锥型6.Si—C键的反应性一般比C—C键的反应性为()A. 大B. 小C. 相等D. 不确定7.下列采用sp3杂化轨道成键的是()A. Cr(CO)6B. Fe(CO)5C. Ni(CO)4D. [Ag(CN)2]-8.Fred属于下列哪类配合物?()A. 混合配体羰基金属配合物B. 单核全羰基金属配合物C. 双核羰基金属配合物D. 原子簇配合物9.炔烃配体配合物中炔配体提供给金属的电子数是()A.4B.3C.2D.110.下列不属于类环戊二烯基配体的是()A. B. C. D.11.IA族金属的烷基物和芳基物的活性正确的是()A. Li-R<Na-R<K-R<Rb-R<Cs-RB. Li-R<K-R<Na-R<Rb-R<Cs-RC. Cs-R<Rb-R<K-R<Na-R<Li-RD. Cs-R<Rb-R<Na-R<K-R<Li-R12.Ni(CO)4属于哪一类非经典键合的化合物?()A. M—C键中为缺电子型键B. M—C键中碳原子为π键电子给予体的多中心键化合物C. M—C键以夹心型键形成的π键化合物D. M—C键以σ—π配键形成的化合物13.铝氢化物中最重要的是氢化铝锂,LiAlH4是重要的()A.还原剂 B. 氧化剂C. 催化剂D.脱水剂14.Fe(CO)5的几何构型是( )A. 正四面体型B. 正方锥型C. 三角锥型D. 八面体型15.Si —C 键的反应性一般比C —C 键的反应性为( )。
《金属有机化学》作业参考答案一选择题1、B;2、C;3、B;4、D;5、A;6、A;7、C;8、A;9、C;10、D;11、A;12、D;13、A;14、C;15、A;16、A;17、C;18、B;19、A;20、A;21、B;22、C;23、D;24、B;25、D;26、A;27、A;28、A;29、D;30、A.31、A;32、B;33、A;34、B;35、B; 36、D;37、A;38、A;39、A;40、B;41、D;42、C 43、C 44、A 45、D 46、A 47、D二填空题1.金属;2.聚氯乙烯稳定剂;3.双键; 4.L=(12-n)/2; 5.四腿琴凳式; 6.非键电子;7.茂; 8.聚硅氧烷; 9.光照;10.环戊二烯基钠;11.配体取代法; 12.酰基;13.活性空位; 14.2电子配体; 15.金属一金属键.; 16.d—p一dπ键; 17.福州模型;18.Dewar-Chatt-Duncanson模型; 19.π给予体簇合物;20.金属羰基原子簇; 21.d—p一dπ键;22.歧化反应。
23、有机化学无机化学24、M—C 过渡金属有机化合物非过渡(主族)金属有机化合物25、离子型化合物σ键合的化合物非经典键合的化合物26、RM R2M27、过渡金属环戊二烯基28、Grignard29、离子键化合物、共价键化合物、缺电子化合物30、有机化学无机化学31、金属-碳( M-C )键32、过渡金属环戊二烯基33、σ-π配键34、Ziegler Natta35、MR2 RMX直线36、Grignard 试剂三简答题1.韦德规则的要点:(1)硼烷和碳硼烷呈三角面多面体构型;(2)由多面体顶点全占据是封闭型;空一个顶点的是巢穴型;空两个顶点是网兜型;(3)每一个骨架B有一个H(或其它单键配体)端基连结在它上面,一对电子定域在上面,剩余的b对电子是骨架成键电子;(4)每一个B提供三个原子轨道(AO)给骨架成键,多面体的对称性由这些AO产生的(M+1)个骨架成键分子轨道(MO)决定(M是多面体顶点),即:因此,算出任一硼烷的成键MO数就能知道它的对称性,而成键MO数=骨架成键电子对数b。
有机化学课后习题参考答案The following text is amended on 12 November 2020.《有机化学》习题参考答案引言这本参考答案是普通高等教育“十二五”规划教材《有机化学》(周莹、赖桂春主编,化学工业出版社出版)中的习题配套的。
我们认为做练习是训练学生各种能力的有效途径之一,是对自己所学内容是否掌握的一种测验。
因此,要求同学们在学习、消化和归纳总结所学相关知识的基础上完成练习,即使有些可能做错也没有关系,只要尽心去做就行,因为本参考答案可为读者完成相关练习后及时核对提供方便,尽管我们的有些参考答案(如合成题、鉴别题)不是唯一的。
北京大学邢其毅教授在他主编的《基础有机化学习题解答与解题示例》一书的前言中写道:“解题有点像解谜,重在思考、推理和分析,一旦揭开了谜底,就难以得到很好的训练。
”这句话很符合有机化学解题的特点,特摘录下来奉献给同学们。
我们以为,吃透并消化了本参考答案,将会受益匪浅,对于报考研究生的同学,也基本够用。
第一章绪论1-1解:(1)C1和C2的杂化类型由sp3杂化改变为sp2杂化;C3杂化类型不变。
(2)C1和C2的杂化类型由sp杂化改变为sp3杂化。
(3)C 1和C 2的杂化类型由sp 2杂化改变为sp 3杂化;C 3杂化类型不变。
1-2解:(1) Lewis 酸 H + , R + ,R -C +=O ,Br + , AlCl 3, BF 3, Li +这些物质都有空轨道,可以结合孤对电子,是Lewis 酸。
(2)Lewis 碱 x -, RO -, HS -, NH 2, RNH 2, ROH , RSH这些物质都有多于的孤对电子,是Lewis 碱。
1-3解:硫原子个数 n=5734 3.4%6.0832..07⨯=1-4解:甲胺、二甲胺和三甲胺都能与水形成氢键,都能溶于水。
综合考虑烷基的疏水作用,以及能形成氢键的数目(N 原子上H 越多,形成的氢键数目越多),以及空间位阻,三者的溶解性大小为:CH 3NH 2 >(CH 3)2NH >(CH 3)3N1-5解: 32751.4%1412.0C n ⨯==,327 4.3%141.0H n ⨯==,32712.8%314.0N n ⨯==,3279.8%132.0S n ⨯==, 32714.7%316.0O n ⨯==, 3277.0%123.0Na n ⨯==甲基橙的实验试:C14H14N3SO3Na1-6解: CO2: H2O:第二章有机化合物的分类和命名2-1解:(1) 碳链异构(2)位置异构(3)官能团异构(4)互变异构2-2解:(1) 2,2,5,5-四甲基己烷 (2 ) 2,4-二甲基己烷(3)1-丁烯-3-炔(4)2-甲基-3-氯丁烷(5)2-丁胺(6)1-丙胺(7)(E)-3,4-二甲基-3-己烯(8)(3E,5E)-3-甲基-4,5-二氯-3,5-辛二烯(9)2,5-二甲基-2,4-己二烯(10)甲苯(11)硝基苯(12)苯甲醛(13)1-硝基-3-溴甲苯(14)苯甲酰胺(15)2-氨基-4-溴甲苯(16)2,2,4-三甲基-1-戊醇(17)5-甲基-2-己醇(18)乙醚(19)苯甲醚 (20) 甲乙醚 (21) 3-戊酮 (22 ) 3-甲基-戊醛(23)2,4-戊二酮(24)邻苯二甲酸酐(25)苯乙酸甲酯(26)N,N-二甲基苯甲酰胺(27)3-甲基吡咯(28)2-乙基噻吩(29)α-呋喃甲酸(30)4-甲基-吡喃(31)4-乙基-吡喃(32)硬脂酸(33)反-1,3-二氯环己烷(34)顺-1-甲基-2-乙基环戊烷(35)顺-1,2-二甲基环丙烷2-3解:(1)CH3CHCH3CH3CH3CHCH3CH3C(2)CH3CHCH3CH2CH2CH2CH3C2H5(3)CH3CHCH3CHCH22CH3C2H525 (4)C2H5HCH3H(5)H 2252CH 2CH 3(6)(7)HCH 3H CH 3HH(8)3(9)52H 5(10)(11)CH 3NO 2NO 2(12)H 3(13)(14)OH COOHBr(15)BrCHOCH 3CH 3(16)CH 3CH 2OH(17)OH(18)OHBrBr(19)OH SO 3HNO 2(20)OO O(21)O(22)O(23)HCH 3H CHO(24)H 33(25)N HCH 3O(26)NH 2N H(27) N HO(28)S(29)NCH 2H 5OCH 2H 5(30)CH 3(CH 2)7CH=CH(CH 2)7COOH(31)NH 2ONH 2 (32)H 2N-C O NH-C-NH 2O(33)OOO(34)OCHO2-4解: (1)CH 3C H 2CH 3CH 3C HCH 3CH 3C 命名更正为:2,3,3-三甲基戊烷(2)CH 3C H 2C H CH CH 3CH 3CH 3(3)(4)(5)(6)(7)(8)2-5解:可能的结构式2-6解:(1)(2)CH3C2H5CH2CH2CH3CH2CH2CH2CH3(3)CH3CH32CH2CH3CH3C2H5C2H5C2H5CH2CH2CH3 2-7解:1,3-戊二烯 1,4-戊二烯H 2CH 2CH 32CH 3H 31-戊炔 2-戊炔H 2CH C 2H 5CH 3CH 31,2-戊二烯 2,3-戊二烯H 2333-甲基-1,2-丁二烯第三章 饱和烃3-1解:(1) 2,3,3,4-二甲基戊烷 (2) 3-甲基-4-异丙基庚烷(3) 3,3-二甲基戊烷 (4) 2,6-二甲基-3,6-二乙基辛烷 (5) 2,5-二甲基庚烷 (6) 2-甲基-3-乙基己烷 (7)2-甲基-4-环丙基自己烷 (8)1-甲基-3-乙基环戊烷(1)H3332CH3(2)(3) H333(4)(5) (6)3-3解:(1) 有误,更正为:3-甲基戊烷(2) 正确(3) 有误,更正为:3-甲基十二烷(4) 有误,更正为:4-异丙基辛烷(5) 4,4-二甲基辛烷(6) 有误,更正为:2,2,4-三甲基己烷(3) > (2) > (5) > (1) > (4)3-5解:BrHH HHBr BrHHHHBrBrHHBrHHBrHHB rHH(A)对位交叉式 (B)部分重叠式 (C)邻位交叉式 (D)全重叠式A>C>B>D3-6解:(1)相同 (2)构造异构(3)相同(4)相同(5)构造异构体 (6)相同3-7解:由于烷烃氯代是经历自由基历程,而乙基自由基的稳定性大于甲基自由基,故一氯甲烷的含量要比一氯乙烷的含量要少。
习题答案
第一章
1、判断下列化合物中那些是金属有机化合物?
(1)NaCN (2)Bu2SnCl2 (3)EtCO2K (4)Et3Al (5)Co2(CO)8 (2)、(4)、(5)
2、(1)Bu3GeLi 三丁锗基锂,三丁基锗锂
(2)Et2AlCl 一氯二乙基合铝,二乙基铝合(一)氯
(3)i PrMgCl 一氯一异丙基合镁,(一)异丙基镁合(一)氯
(4)(CO)4MnPPh3四羰基一三苯基膦合锰
(5)k[(CH2CH2)PtCl3]·H2O 一水合三氯一乙烯合铂酸钾
(6)η5-CpMn(CO)3三羰基-eita-5-环戊二烯基合锰
(7)η5-Cp2ZrCl2二氯二-eita-5-环戊二烯基合锆,二-eita-5-环戊二烯基锆合二氯(8)Co2(CO)8八羰基合二钴
(9)IrCl(CO)(PPh3)2一羰基一氯二三苯基膦合铱,一羰基二三苯基膦铱合氯(10)RhCl(PPh3)3一氯三三苯基膦合铑,三三苯基膦铑合氯
第二章
第四章 2、
第五章
1、羰基钴络合物催化烯烃氢甲酰化反应历程.
Co 2(CO)8 + H 2
HCo(CO)43RCH=CH 2
RCH 2CH 23
RCH 2CH 2RCH 2CH 2CCo(CO)3
O
RCH 2CH
O
H 2
HCo(CO)3
2
RCH 22CCo(CO)3H H (18e)(16e)(18e)
(18e)
(16e)(16e)
2、
第七章
1、Wacker 法合成乙醛反应机理
Wacker 法反应机理
2、以烷基过氧化氢为氧化剂,钼酸酯为催化剂的烯烃环氧化反应机理。
初三化学金属的化学性质(讲义及答案)含答案(2)一、选择题1.下列实验现象记录正确的是 ( )A.把铜丝放入硫酸铝溶液中,紫红色固体表面产生银白色固体,溶液变成蓝色B.向氢氧化钾溶液中滴入氯化铁溶液,有浅绿色沉淀生成C.将一氧化碳通过灼热的氧化铁,红棕色粉末逐渐变为黑色粉末D.硫在氧气中燃烧,发出淡蓝色火焰,生成无色无味的气体并放出热量答案:C解析:C【解析】A、金属的位置越靠前,金属的活动性越强。
位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。
铜的活动性比铝弱。
把铜丝放入硫酸铝溶液中,不发生反应,无明显现象,错误;B、向氢氧化钾溶液中滴入氯化铁溶液,有红褐色沉淀生成,错误;C、将一氧化碳通入灼热的氧化铁生成铁粉和二氧化碳,红棕色粉末逐渐变为黑色粉末,正确;D、硫在氧气中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体并放出热量,错误。
故选C。
2.向氧化铜和铁粉的混合物中加入一定量稀硫酸,充分反应后过滤,向滤渣中再滴入稀硫酸,有气泡产生,则下列判断正确的是A.滤渣中可能含 Cu B.滤渣中只含 FeC.滤液中不含 CuSO4D.滤液中不一定含 FeSO4答案:C解析:C【解析】反应时应是氧化铜先和酸反应,转化为铜离子,当铜离子与氢离子同时存在时,铁应该先和铜离子反应;当向滤渣中再滴入稀硫酸,有气泡产生,说明所加入的铁粉过量,说明原稀硫酸完全反应,且铜离子没有剩余,才会有氢气生成,也就说明,铜离子完全转化为铜单质而成为不溶物;A、氧化铜与硫酸反应生成硫酸铜,铁的活动性比铜强,铁能置换出硫酸铜溶液中的铜,所以不溶物中一定含有铜;故A错误;B、氧化铜与硫酸反应生成硫酸铜,铁的活动性比铜强,铁能置换出硫酸铜溶液中的铜,所以不溶物中一定含有铜,当向滤渣中再滴入稀硫酸,有气泡产生,说明所加入的铁粉过量,故B错误;C、铁的活动性比铜强,铁能置换出硫酸铜溶液中的铜,因此,所生成的硫酸铜可能会被铁粉完成反应,所得滤液中一定不含有硫酸铜,故C正确;D、铁与硫酸或硫酸铜反应都能生成可溶于水的硫酸亚铁,因此,滤液中一定含有硫酸亚铁;故D错误。
课时作业15金属材料[学业达标]1.下列说法不正确的是( )A.我国有丰富的稀土资源,要合理开采B.稀土金属在自然界中含量很少,只能用于生产合金C.稀土金属用途广泛,被称为“冶金工业的维生素”D.稀土元素的化学性质相似2.下列说法中不正确的是()A.人类历史上使用最早的合金是青铜B.钢属于铁合金C.目前世界上使用量最大的合金是铝合金D.目前世界上用途最广的是合金钢3.下列关于合金的叙述中正确的是( )A.合金是由两种或多种金属熔合而成的B.日常生活中用到的五角硬币属于铜合金C.合金在任何情况下都比单一金属性能优良D.钢不属于合金4.由于铝制品对大脑发育有不良影响,厨具中铝制品已逐步被不锈钢代替,不锈钢的组成是( ) A.含铁、锌、铜的合金B.含铁、镁、铝的合金C.含铁、铬、镍的合金D.普通钢表面镀镍5.纯铁的熔点为1 535 ℃,而高炉中炼铁时生铁(含碳量较高的铁合金)在1 200 ℃左右就熔化了,这是因为()A.铁的纯度越高,熔点越低B.合金的熔点比其成分物质的熔点高C.形成了铁碳合金,所以熔点变低D.在高炉中熔化的过程发生了化学反应6.用于制造飞机的材料应具备高比强度(断裂强度/密度),还应具备密度小、质地轻的特点。
你认为下列材料中可用于飞机制造业的是()A.Mg.Al合金B.黄铜(Cu.Zn合金)C.NaK合金D.生铁(FeC合金)7.除去镁粉中的少量铝粉,可选用()A.硫酸B.氨水C.盐酸D.氢氧化钠溶液8.足量下列物质与相同质量的铝反应,放出氢气且消耗溶质物质的量最少的是( )A.氢氧化钠溶液B.稀硫酸C.盐酸D.氢氧化钡溶液9.等量镁铝合金粉末分别与足量下列四种物质充分反应,放出氢气最多的是()A.NaOH溶液B.稀硫酸C.蔗糖溶液D.NaCl溶液10.在500 mL NaOH溶液中加入足量铝粉,反应完全后共收集到标准状况下的气体33.6 L,该NaOH溶液的浓度为()A.1.0 mol·L-1B.2。
《金属有机化学》作业参考答案一选择题1、B;2、C;3、B;4、D;5、A;6、A;7、C;8、A;9、C;10、D;11、A;12、D;13、A;14、C;15、A;16、A;17、C;18、B;19、A;20、A;21、B;22、C;23、D;24、B;25、D;26、A;27、A;28、A;29、D;30、A.31、A;32、B;33、A;34、B;35、B; 36、D;37、A;38、A;39、A;40、B;41、D;42、C 43、C 44、A 45、D 46、A 47、D二填空题1.金属;2.聚氯乙烯稳定剂;3.双键; 4.L=(12-n)/2; 5.四腿琴凳式; 6.非键电子;7.茂; 8.聚硅氧烷; 9.光照;10.环戊二烯基钠;11.配体取代法; 12.酰基;13.活性空位; 14.2电子配体; 15.金属一金属键.; 16.d—p一dπ键; 17.福州模型;18.Dewar-Chatt-Duncanson模型; 19.π给予体簇合物;20.金属羰基原子簇; 21.d—p一dπ键;22.歧化反应。
23、有机化学无机化学24、M—C 过渡金属有机化合物非过渡(主族)金属有机化合物25、离子型化合物σ键合的化合物非经典键合的化合物26、RM R2M27、过渡金属环戊二烯基28、Grignard29、离子键化合物、共价键化合物、缺电子化合物30、有机化学无机化学31、金属-碳( M-C )键32、过渡金属环戊二烯基33、σ-π配键34、Ziegler Natta35、MR2 RMX直线36、Grignard 试剂三简答题1.韦德规则的要点:(1)硼烷和碳硼烷呈三角面多面体构型;(2)由多面体顶点全占据是封闭型;空一个顶点的是巢穴型;空两个顶点是网兜型;(3)每一个骨架B有一个H(或其它单键配体)端基连结在它上面,一对电子定域在上面,剩余的b对电子是骨架成键电子;(4)每一个B提供三个原子轨道(AO)给骨架成键,多面体的对称性由这些AO产生的(M+1)个骨架成键分子轨道(MO)决定(M是多面体顶点),即:因此,算出任一硼烷的成键MO数就能知道它的对称性,而成键MO数=骨架成键电子对数b。
(5)若骨架原子数n,则b=n+1是封闭型;b=n+2是巢穴型;b=n+3是网兜型。
2.金属有机化合物的三大主要类别是:结合金属元素在周期表中的位置以及各金属与碳成键的类型,可把金属有机化合物分为:离子型化合物,金属碳键以σ键合的化合物和非经典键合的化合物等三大类型。
3.π―酸:既供σ电子又接受金属反馈的电子的π―受体,称为π―酸;例如CO。
属于这一类的有:CO, N2, bipy, PR3, AsR3, CN-π―配位体:没有孤对电子,键轨道上的π电子给予金属的空轨道,而金属的d电子又反馈到它的反键π*轨道中,这类配位体称为π -配位体,例如烯烃。
属于这一类的有:C5H5-,C6H6, C2H4, C4H6 4.影响形成M—M键的因素是:当金属原子具有较低的形式氧化态和适宜的价轨道构型,并存在有适宜的配位体时,就有可能形成含有M—M 键的,具有丰富多采的分子构型的原子簇化合物。
5.“18电子规则”:对于单核的反磁性过渡金属配合物(n为偶数,所有电子成对),指定给定的dn只有一个最高配位数CN,(coordination number)则有: n + 2 (CN)最高 =18这就是重要的“18电子规则”.既对于稳定的单核反磁性过渡金属配合物,金属d电子数与配位体给予的电子数和等于18。
大部分过渡金属配合物服从18电子规则,例如:Fe(CO)5 ; Ni(CO)4;Cr(CO)6;CH3Mn(CO)5;Mn2(CO)10;6.命名下列化合物(1)--cyclopentadienyl)titanium(2)(1,2,3-trihaptocycloheptatrienyl)pentahaptocyclopentadienylcarbonyliron7.金属原子簇化合物是一类以金属一金属键合或金属一桥基键合,而使相邻的金属原子或含配体的金属中心连接在一起的两个或两个以上金属原子的化合物。
8.金属茂可用于催化不对称环氧化反应、不对称Diels—Alder反应、不对称羰基加成以及不对称异构化等不对称合成反应。
9.Grignard试剂合成方程式为:Mg + R X RM gX硼氢化反应方程式为:1/2B2H6 +乙醚(6.6)3C C B(C C H)3或C =C+ H B H C C B(6.10)10.金属有机化合物的主要反应类型有:插入反应,取代反应,加成反应,氧化加成反应,消除反应,加合离解反应。
11.小结金属茂的结构:能生成金属茂的金属,遍及整个元素周期表,包括过渡金属和一般金属。
它们绝大多数是π配位,即形成夹心型结构,考虑到结构特点和化学键的本质,这些π配位的夹心型金属茂可分为四种类型:(1)夹心型,弯曲夹心,包括柄型夹心;(2)半夹心,又称钢琴椅式;(3)多层夹心;(4)开环夹心化合物,又叫开环金属茂;与金属茂比较,其配位体是戊二烯的负离子——戊二烯基,即开环茂。
12.命名下列化合物(1) (1,2,3-trihaptocycloheptatrienyl)pentahaptocyclopentadienylcarbonyliron(2)(1,2,3,4-tetrahapto-buta-1,3-dienyl)tricarbonyliron13.金属有机化学,一门常被称为“有机分子与无机分子一起跳舞”的学科,是当代化学的前沿领域之一,发展最为活跃、迅速和富有生命力,在这个广阔的领域内可能蕴藏着极为丰富的化学现象,有待人们去开发和探索,并且它在制药、工业生产等方面都有着广泛的应用。
金属有机化学是无机化学和有机化学之间的一门边缘学科,其研究对象是烃基或烃分子中的碳原子与金属原子直接键合的化合物(也包括非金属B、Si等)。
是研究具有键化合物的科学。
金属有机化合物的性质与有机化合物相似,但是又具有无机配合物的性质,如易形成晶体,不稳定,易分解,尊循无机配合物的化学键理论。
所以金属有机化学是在无机化学和有机化学基础之上的扩展和交叉。
14.15.晶体场理论是一种静电理论, 它把配合物中中心原子与配体之间的相互作用, 看作类似于离子晶体中正负离子间的相互作用。
但配体的加入, 使得中心原子五重简并的d 轨道(见图)失去了简并性。
在一定对称性的配体静电场作用下, 五重简并的d轨道将解除简并, 分裂为两组或更多的能级组, 这种分裂将对配合物的性质产生重要影响。
16. 4个BHB 8e1个BBB 2e2个BB 4e0 个BH20e5个BH 10e总电子: 24e17. 晶体场稳定化能的大小与下列因素有关:★配合物的几何构型;★中心原子的d电子的数目;★配体场的强弱;★电子成对能大小。
18.在CoF63-中, 杂化轨道的类型为sp3d2, 配离子有4个单电子, 显顺磁性, 为外轨型配合物(也叫电价配合物)。
在Co(CN)63-中, Co3+中心离子以d2sp3杂化轨道成键, 配离子没有成单电子, 显抗磁性, 为内轨型配合物(也叫共价型配合物)。
四综合应用题1.给出金属有机化学基元反应的各个名称,并分别举例说明。
⑴配位体的配位和解离例:⑵氧化加成和还原消除Pd(PPh3)4Pd(PPh3)3+PPh3PPhHPPh例:RLi2R-COO-Li+H3ORCOOHM—CCo(CN)63-d2sp3-⑶ 插入反应和反插入反应⑷ 成键配位反应2.Fischer 型卡宾和Schrock 型卡宾在结构特点和反应性能上的不同之处在于:CO Mn 314CO Mn CH 3+ 14CO R 3Sn-NR 2 + CO 2R 3SnOCONR 2Ti(NR 2)4 + 4CS 2Ti(S 2CNR 2)4R 3PbR' +SO 2R 3PbOSOR'+NaOM eM eOH_OOPd X OO(Z)HX两种类型金属卡宾的比较ⅥB-Ⅷ过渡金属低氧化态,卡宾呈sp2杂化3.锂试剂的主要用途有以下七个方面。
有机锂具有共价键化合物的典型特性,可以溶于烃溶剂或其它非极性溶剂中,易挥发,加热时可以升华或进行蒸馏,在熔融状态下或溶液中不显导电性。
锂的有机化合物通常为液体或低熔点固体,室温下,除CH 3Li 、C 2H 5Li 和C 6H 5Li 为固体外,其余都是液体。
在晶体或溶液中,烷基锂化合物的分子缔合作用是其重要特征。
例如甲基锂是以四聚体(CH 3Li )4形式存在。
Li 原子居于四面体的四个顶点 ,四个甲基分别处于四面的每个面之上,每一个甲基对称的与三个锂原子结合,形成两电子四中心键,属于烷基桥式缺电子多中心键。
具体作用① 新轨道形成使RLi 具有缔合作用,使烷基锂具有一定的稳定性并导致CH 3Li ,Et 2Li 等为固体;② 由于缔合分子中有空轨道,使其成为Lewis 酸而易于碱发生作 用,进而影响烷基锂的性质,甚至可发生解聚。
③ 烷基锂可与Mg ,Gd ,Zn 等烷基化合物作用形成配合物。
④ 烷基锂与CO 2反应(为什么在制备烷基锂的保护气中去CO 2 )⑤ 烷基锂与醛、酮反应。
⑥ 烷基锂与羧酸衍生物反应。
CH 3+ (n-BuLi)TMEDA THFCH 2Li+ n-BuLi)phLi+ph 2MgLi 2[Mgph 4]RLi2R-COO-Li+H 3O +RCOOHRLi+C R 'R"C OLi R "R R'C OH R "R⑦ 烷基和芳基锂化合物可以和Mg 、Cd 、Zn 的烷基化合物生成酸根型络合物(ate 型络合物)其中最重要的是铜络合物(cuprate):2RLi + CuX Li+CuR 2-+ LiX4.简述18电子规则的原理及应用,并举5个以上的典型例子加以说明。
对于单核的反磁性过渡金属配合物(n 为偶数,所有电子成对),指定给定的d n 只有一个最高配位数CN ,(coordination number)则有: n + 2 (CN)最高 =18这就是重要的“18电子规则”.既对于稳定的单核反磁性过渡金属配合物,金属d 电子数与配位体给予的电子数和等于18。
大部分过渡金属配合物服从18电子规则,例如:Fe(CO)5 ; Ni(CO)4;Cr(CO)6;CH 3Mn(CO)5;5.烯烃与过渡金属配位后,由于金属原子对烯烃 π* 反键轨道电子的反馈,使配体可接受外来亲核试剂的进攻。
进攻的立体化学是亲核试剂从烯烃与金属配位的反面进攻。
被配位的炔烃也可接受外来亲核试剂的反式进攻。
烯丙基丙炔酸酯中的叁键被钯配位后,即可接受卤素离子的进攻发生卤钯化反应。