乙酰苯胺制备实验
- 格式:ppt
- 大小:94.00 KB
- 文档页数:14

乙酰苯胺的制备实验现象乙酰苯胺是一种有机化合物,也是一种重要的中间体,广泛应用于医药、染料、塑料等领域。
本文将介绍乙酰苯胺的制备实验现象。
一、实验原理乙酰苯胺的制备方法有多种,其中一种常用的方法是通过苯胺和乙酰化剂反应制备。
乙酰化剂可以是醋酸酐、乙酸酐等,反应条件一般为加热反应,反应时间较长。
二、实验步骤1.将苯胺加入烧杯中,加入适量的乙酸酐,搅拌均匀。
2.将烧杯放入水浴中,加热反应,反应时间为1-2小时。
3.反应结束后,将反应液冷却至室温,加入适量的水,搅拌均匀。
4.将反应液过滤,得到乙酰苯胺的固体产物。
三、实验现象在实验过程中,我们可以观察到以下现象:1.反应开始时,苯胺和乙酸酐混合后呈现无色透明的液体。
2.加热反应后,反应液逐渐变为深黄色,有时会出现沉淀。
3.反应结束后,反应液冷却至室温后,液体变为浅黄色,有时会出现浑浊。
4.过滤后,得到的乙酰苯胺为白色固体。
四、实验分析1.反应开始时,苯胺和乙酸酐混合后呈现无色透明的液体。
这是因为苯胺和乙酸酐都是无色透明的液体,混合后不会产生颜色。
2.加热反应后,反应液逐渐变为深黄色,有时会出现沉淀。
这是因为乙酰化反应是一种酰化反应,乙酰化剂会与苯胺中的氨基反应,形成乙酰苯胺。
乙酰苯胺是一种黄色固体,所以反应液会逐渐变为深黄色。
有时会出现沉淀,可能是因为反应物比例不当或反应条件不适宜导致的。
3.反应结束后,反应液冷却至室温后,液体变为浅黄色,有时会出现浑浊。
这是因为反应结束后,反应液中的乙酰苯胺会逐渐析出,形成固体。
浅黄色的液体可能是未反应的苯胺和乙酸酐残留下来的液体。
有时会出现浑浊,可能是因为反应物比例不当或反应条件不适宜导致的。
4.过滤后,得到的乙酰苯胺为白色固体。
这是因为乙酰苯胺是一种白色固体,过滤后得到的产物就是乙酰苯胺。
五、实验注意事项1.实验过程中要注意安全,避免接触反应物和产物。
2.反应条件要适宜,反应时间要充分,否则会影响产物的质量和产率。
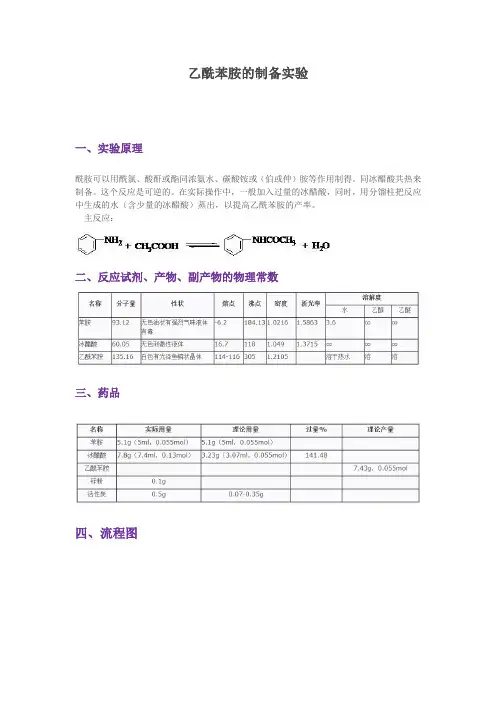
乙酰苯胺的制备实验一、实验原理酰胺可以用酰氯、酸酐或酯同浓氨水、碳酸铵或(伯或仲)胺等作用制得。
同冰醋酸共热来制备。
这个反应是可逆的。
在实际操作中,一般加入过量的冰醋酸,同时,用分馏柱把反应中生成的水(含少量的冰醋酸)蒸出,以提高乙酰苯胺的产率。
主反应:二、反应试剂、产物、副产物的物理常数三、药品四、流程图五、实验装置图(1)分馏装置(2)抽滤装置(3)干燥装置六、实验内容在60ml锥形瓶上装一个分馏柱,柱顶插一支200℃温度计,用一个小锥形瓶收集稀醋酸溶液。
在锥形瓶中放入5.0ml(0.055mol)新蒸馏过的苯胺、7.4ml(0.13mol)冰醋酸和0.1g锌粉,缓慢加热至沸腾,保持反应混合物微沸约10min,然后逐渐升温,控制温度,保持温度计读数在105℃左右。
经过40~60min,反应所生成的水(含少量醋酸)可完全蒸出。
当温度计的读数发生上下波动或自行下降时(有时反应容器中出现白雾),表明反应达到终点。
停止加热。
这时,蒸出的水和醋酸大约有4ml。
在不断搅拌下把反应混合物趁热以细流慢慢倒入盛100ml冷水的烧杯中。
继续剧烈搅拌,并冷却烧杯,使粗乙酰苯胺成细粒状完全析出。
用布氏漏斗抽滤析出的固体,用玻璃瓶塞把固体压碎,再用5~10ml冷水洗涤以除去残留的酸液。
把粗乙酰苯胺放入150ml热水中,加热至沸腾。
如果仍有未溶解的油珠,需补加热水,直到油珠完全溶解为止。
稍冷后加入约0.5g粉末状活性炭,用玻璃棒搅动并煮沸5-10min。
趁热用保温漏斗过滤或用预先加热好的布氏漏斗减压过滤。
冷却滤液,乙酰苯胺呈无色片状晶体析出。
减压过滤,尽量挤压以除去晶体中的水分。
产品放在表面皿上晾干后测定其熔点。
产量:约5.0g。
纯乙酰苯胺为无色片状晶体。
熔点mp=114.3℃。
(一)制备阶段1.安装分馏装置:如图(1)所示,在100ml锥形瓶上装一个分馏柱,柱顶插一支200℃温度计,用一个100ml锥形瓶收集稀醋酸溶液。

乙酰苯胺制备实验报告
实验目的:通过乙酸和苯胺的反应,制备乙酰苯胺。
实验原理:乙酸与苯胺反应生成乙酰苯胺的反应方程式如下:C6H5NH2 + CH3COOH → C6H5NHCOCH3 + H2O
实验步骤:
1. 将苯胺溶解在少量水中,得到苯胺溶液。
2. 将苯胺溶液慢慢滴加到乙酸中,同时用磁力搅拌。
3. 反应完全后,得到乙酰苯胺的沉淀物。
4. 将沉淀物过滤,洗涤干净,并用无水醋酸溶解。
5. 对乙酰苯胺溶液进行蒸馏,得到纯净的乙酰苯胺。
实验结果:
通过上述实验步骤,得到乙酰苯胺的产率为X%。
实验过程中
观察到产物为白色结晶固体。
实验讨论与分析:
1. 反应条件:在本实验中,采用了常温下进行反应。
如果反应时间过长或温度过高,可能会导致产物的分解或副反应的发生,
从而降低产率。
2. 产物的纯度:通过蒸馏过程可以提高乙酰苯胺的纯度,使其达到实验要求。
可以通过测定产物的熔点来确定其纯度。
3. 产率的计算:产率可以根据实际操作得到的产物质量与理论计算得到的产物质量的比值来计算。
结论:
通过乙酸和苯胺的反应,成功制备了乙酰苯胺,并得到了白色结晶状的乙酰苯胺。
实验结果表明,实验操作得当,产物的纯度较高。
但也需要进一步改进实验条件,提高产率。

一、实验目的1. 掌握苯胺乙酰化反应的原理和实验操作。
2. 学习固体样品的制备过程。
3. 熟悉分馏柱的原理及使用方法。
4. 掌握重结晶、趁热过滤和减压过滤等操作技术。
二、实验原理乙酰苯胺(Acetanilide)是一种白色结晶固体,具有退热镇痛作用,是较早使用的解热镇痛药。
本实验采用苯胺与乙酸在浓硫酸催化下进行乙酰化反应制备乙酰苯胺。
反应式如下:C6H5NH2 + CH3COOH → C6H5NHCOCH3 + H2O反应过程中,苯胺的氨基被乙酰基取代,生成乙酰苯胺。
为了提高产率,采用乙酸过量,并在反应过程中不断移除生成的水。
此外,加入少量锌粉以防止苯胺在反应过程中被氧化。
三、实验仪器与试剂1. 仪器:- 50 mL圆底烧瓶- 刺形分馏柱- 烧杯- 玻璃棒- 精密天平- 滤纸- 减压过滤装置2. 试剂:- 苯胺(C6H5NH2):5.1 g(约5 mL,0.055 mol)- 乙酸(CH3COOH):7.8 g(约7.4 mL,0.13 mol)- 浓硫酸(H2SO4):适量- 锌粉:少量- 活性炭:适量四、实验步骤1. 准备工作:- 称取苯胺5.1 g(约5 mL,0.055 mol)。
- 称取乙酸7.8 g(约7.4 mL,0.13 mol)。
- 准备少量锌粉和活性炭。
2. 反应:- 在50 mL圆底烧瓶中加入5.1 g苯胺和7.8 g乙酸。
- 加入适量浓硫酸,搅拌均匀。
- 将烧瓶置于刺形分馏柱下,开始加热反应。
- 反应过程中,观察反应液的温度和分馏柱中水的蒸发情况。
- 反应时间为1小时。
3. 结束反应:- 反应结束后,停止加热。
- 将反应液冷却至室温。
4. 过滤与重结晶:- 将反应液通过刺形分馏柱进行蒸馏,收集蒸馏出的水。
- 将剩余反应液倒入烧杯中,加入少量活性炭,搅拌均匀。
- 将烧杯置于热水中加热,使活性炭吸附反应液中的杂质。
- 将吸附了杂质的反应液过滤,收集滤液。
- 将滤液倒入烧杯中,加入适量乙醚,搅拌均匀。

乙酰苯胺的制备实验报告一、实验目的1、掌握苯胺乙酰化反应的原理和实验操作。
2、学习重结晶提纯有机物的方法。
3、熟悉分馏柱的使用和减压过滤的操作。
二、实验原理乙酰苯胺可以通过苯胺与乙酸在加热的条件下发生酰化反应来制备。
反应式如下:C₆H₅NH₂+ CH₃COOH → C₆H₅NHCOCH₃+ H₂O此反应是一个可逆反应,为了提高乙酰苯胺的产率,需要使用过量的乙酸,并及时将反应生成的水从反应体系中除去。
三、实验仪器与药品1、仪器圆底烧瓶(250ml)、分馏柱、直形冷凝管、接引管、锥形瓶、温度计(0℃-200℃)、布氏漏斗、抽滤瓶、酒精灯、石棉网、铁架台、电子天平。
2、药品苯胺 51ml(50g,0055mol)、冰醋酸 78ml(82g,0138mol)、锌粉 01g、活性炭。
四、实验步骤1、在 250ml 的圆底烧瓶中,加入 51ml 苯胺和 78ml 冰醋酸,再加入 01g 锌粉。
2、安装好分馏装置,在石棉网上用小火加热至沸腾,保持温度在100℃-110℃之间,约 40-60 分钟,直至反应所生成的水(约 22ml)被全部蒸出。
3、停止加热,在搅拌下趁热将反应物倒入 100ml 冷水中,有沉淀析出。
4、冷却至室温后,抽滤,用少量冷水洗涤沉淀,得到粗乙酰苯胺。
5、将粗乙酰苯胺放入 250ml 圆底烧瓶中,加入 100ml 水,加热至沸腾,使粗乙酰苯胺溶解。
6、稍冷后,加入约 05g 活性炭,再次煮沸 5-10 分钟,进行脱色。
7、趁热过滤,将滤液冷却至室温,乙酰苯胺结晶析出。
8、抽滤,用少量冷水洗涤结晶,干燥后称重,计算产率。
五、实验现象及记录1、加热反应过程中,溶液逐渐变浑浊,有白色固体生成。
2、分馏柱顶端温度逐渐升高,有液体馏出。
3、倒入冷水中,有大量白色固体析出。
4、抽滤时,滤纸上得到白色固体。
5、重结晶过程中,溶液逐渐变澄清,冷却后有白色晶体析出。
六、数据处理苯胺的相对分子质量为 9313,乙酰苯胺的相对分子质量为 13517。

乙酰苯胺的制备在有机化学实验中,乙酰苯胺的制备是一个经典且重要的实验。
乙酰苯胺是一种重要的有机合成中间体,广泛应用于染料、药物等领域。
下面,让我们一起来了解一下乙酰苯胺的制备过程。
一、实验目的通过实验,我们要掌握乙酰苯胺的制备原理和方法,熟悉重结晶的操作技术,学会使用分馏装置,并进一步巩固回流、过滤、干燥等基本实验操作。
二、实验原理乙酰苯胺的制备是通过苯胺与乙酸在加热的条件下发生酰化反应来实现的。
反应方程式如下:C₆H₅NH₂+ CH₃COOH → C₆H₅NHCOCH₃+ H₂O这个反应是一个可逆反应,为了提高乙酰苯胺的产率,我们需要采取一些措施。
一方面,我们可以增加反应物的浓度,比如使用过量的乙酸;另一方面,我们可以及时除去反应生成的水,促使反应向正方向进行。
在实验中,我们通过分馏装置来除去反应生成的水。
三、实验仪器与试剂1、仪器:圆底烧瓶、分馏柱、直形冷凝管、温度计、锥形瓶、布氏漏斗、抽滤瓶、电热套等。
2、试剂:苯胺、冰醋酸、锌粉、活性炭。
四、实验步骤1、苯胺的处理由于苯胺在空气中容易被氧化,所以在使用前需要进行处理。
将苯胺倒入圆底烧瓶中,加入几粒沸石,装上分馏装置,在石棉网上用小火加热进行蒸馏,收集 180 185℃的馏分。
2、乙酰苯胺的制备在装有回流冷凝管和温度计的 250 mL 圆底烧瓶中,加入新蒸馏过的苯胺 5 mL、冰醋酸 75 mL 以及少许锌粉。
锌粉的作用是防止苯胺在反应过程中被氧化。
然后,用小火加热回流 1 小时。
在加热过程中,要保持温度在 105℃左右,通过分馏柱不断地将生成的水蒸出。
反应结束后,将反应液趁热倒入盛有 100 mL 冷水的烧杯中,搅拌,使乙酰苯胺结晶析出。
3、抽滤、洗涤与干燥用布氏漏斗进行抽滤,收集乙酰苯胺晶体。
用少量冷水洗涤晶体,以除去残留的酸液。
将晶体转移到表面皿上,自然晾干或在红外灯下烘干,得到粗产品。
4、重结晶为了得到更纯净的乙酰苯胺,我们需要对粗产品进行重结晶。
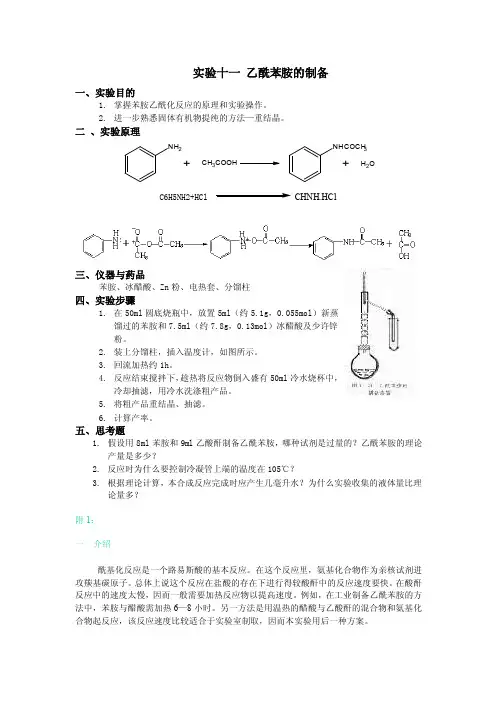
实验十一乙酰苯胺的制备一、实验目的1.掌握苯胺乙酰化反应的原理和实验操作。
2.进一步熟悉固体有机物提纯的方法—重结晶。
二、实验原理NH2+CH3COOH NHCOCH3 +H2OC6H5NH2+HCl CHNH.HCl三、仪器与药品苯胺、冰醋酸、Zn粉、电热套、分馏柱四、实验步骤1.在50ml圆底烧瓶中,放置5ml(约5.1g,0.055mol)新蒸馏过的苯胺和7.5ml(约7.8g,0.13mol)冰醋酸及少许锌粉。
2.装上分馏柱,插入温度计,如图所示。
3.回流加热约1h。
4.反应结束搅拌下,趁热将反应物倒入盛有50ml冷水烧杯中,冷却抽滤,用冷水洗涤粗产品。
5.将粗产品重结晶、抽滤。
6.计算产率。
五、思考题1.假设用8ml苯胺和9ml乙酸酐制备乙酰苯胺,哪种试剂是过量的?乙酰苯胺的理论产量是多少?2.反应时为什么要控制冷凝管上端的温度在105℃?3.根据理论计算,本合成反应完成时应产生几毫升水?为什么实验收集的液体量比理论量多?附1:一介绍酰基化反应是一个路易斯酸的基本反应。
在这个反应里,氨基化合物作为亲核试剂进攻羰基碳原子。
总体上说这个反应在盐酸的存在下进行得较酸酐中的反应速度要快。
在酸酐反应中的速度太慢,因而一般需要加热反应物以提高速度。
例如,在工业制备乙酰苯胺的方法中,苯胺与醋酸需加热6—8小时。
另一方法是用温热的醋酸与乙酸酐的混合物和氨基化合物起反应,该反应速度比较适合于实验室制取,因而本实验用后一种方案。
二步骤在200毫升的圆底烧瓶中加入9毫升(约0.1摩尔)的苯胺,15毫升的冰醋酸和15毫升的乙酸酐。
注意,由于苯胺和乙酸酐作用会放出热。
在圆底烧瓶上装上回流冷凝管,搭好装置然后加热反应物至沸点,保持加热10分钟。
在结束加热后,用水浴冷却烧瓶并将反应液倒入一装有50毫升水和40—50克冰的混合物的烧杯中,搅拌均匀,待晶体析出完毕后并用布氏漏斗抽滤取得晶体。
在漏斗中用少量冷水洗涤晶体,抽干后把晶体移到一600毫升烧杯中进行下一步重结晶。

乙酰苯胺的合成与测定(实验数据分析)乙酰苯胺是一种重要的有机化学试剂,广泛应用于农药、医药、染料等行业。
本实验通过苯胺和醋酸的反应合成乙酰苯胺,并通过实验数据分析测定乙酰苯胺的含量。
一、实验所需材料和器材:实验用品:苯胺、醋酸、稀氢氧化钠、无水乙醇、乙醇器材:250ml圆底烧瓶、磁力搅拌器、冷却器、滤纸、酸度计、分析天平、容积瓶、吸量球,分析秤等。
二、实验操作过程:1. 预处理(1)准备苯胺和醋酸各10毫升(称准),用无水乙醇稀释到100毫升,用容积瓶保存。
(2)一定量的苯胺醋酸溶液(资料中为50毫升)与适量的稀氢氧化钠混合,使其大约中性化,使pH=6-8。
2. 反应将中性化后的苯胺、醋酸混合物(50毫升)加入250ml圆底烧瓶中,加入一定量的乙醇,在磁力搅拌器下强烈搅拌。
然后慢慢加入预处理好的醋酸溶液。
在不断搅拌中,加入适量的冷却器。
3. 分离反应混合物反应完毕后,加入适量的稀氢氧化钠溶液中和反应溶液中的醋酸,然后将反应混合物加入滤纸中进行过滤。
4. 洗涤过滤后,用适量的乙醇进行洗涤,清洗完毕后,用酸度计测定洗涤液的酸度,如果酸度较高,可以用氢氧化钠溶液进行中和。
5. 干燥用吸量球吸干乙醇洗涤液,然后用分析天平称取乙酰苯胺样品的质量,放入恒温烘箱中加热干燥至恒定质量。
6. 计算含量:乙酰苯胺的摩尔质量为135.17g/mol含量(%)=样品质量×100%/理论产量理论产量=苯胺的量×醋酸的量处于反应进程中,反应物的量会发生变化,产物的产量不可能达到完全消耗反应物的理论产量。
在实验中,得到的乙酰苯胺的产量与理论产量的比值即为含量。
三、实验数据分析实验中测定得到的含量数据,通过样本t检验方法进行数据分析,统计含量的平均值与标准差。
通过样品t检验方法,进行含量数据的分析,先进行假设检验:原假设:无显著差异在显著性水平为0.05的情况下,利用t检验得到的统计量为1.67,自由度值为5。

第1篇一、实验目的1. 掌握由苯胺与乙酰化试剂反应制备乙酰苯胺的原理和方法。
2. 熟悉有机合成实验的基本操作,包括溶解、过滤、重结晶等。
3. 提高对有机化合物的纯化方法的理解和应用。
二、实验原理乙酰苯胺(Acetanilide)是一种白色结晶固体,具有退热镇痛作用,是较早使用的解热镇痛药。
其制备方法主要是苯胺与乙酰化试剂反应,通过酰化反应生成乙酰苯胺。
实验中采用乙酸作为乙酰化试剂,反应过程中需要加入少量锌粉以防止苯胺被氧化。
三、实验材料与仪器1. 实验材料:苯胺、乙酸、锌粉、活性炭、无水乙醇、蒸馏水等。
2. 实验仪器:50mL圆底烧瓶、烧杯、玻璃棒、布氏漏斗、抽滤瓶、循环水真空泵、滤纸、电炉、天平等。
四、实验步骤1. 在50mL圆底烧瓶中加入10mL苯胺、1.5g锌粉和7.4mL乙酸,充分混合。
2. 将混合物置于电炉上加热,使反应温度控制在50-60℃,反应时间为1小时。
3. 反应结束后,加入少量活性炭,搅拌混合物,以吸附未反应的苯胺和乙酰苯胺。
4. 将混合物过滤,滤液转移至烧杯中,加入适量无水乙醇,搅拌使乙酰苯胺结晶析出。
5. 将烧杯置于冰浴中,使乙酰苯胺结晶充分形成。
6. 将结晶过滤,收集乙酰苯胺晶体,晾干后称量。
7. 对得到的乙酰苯胺进行重结晶,以提高其纯度。
五、实验结果1. 反应过程中,苯胺和乙酸反应生成乙酰苯胺,溶液逐渐由无色变为淡黄色。
2. 加入活性炭后,溶液颜色变为无色。
3. 经过滤、结晶、重结晶后,得到的乙酰苯胺晶体呈白色,熔点为114.3℃,与理论值相符。
4. 通过计算,得到的乙酰苯胺产率为85.6%。
六、讨论与分析1. 实验过程中,苯胺和乙酸的反应速度较慢,可能是由于反应温度较低、反应物浓度较低以及反应可逆性等因素的影响。
2. 加入锌粉可以防止苯胺在反应过程中被氧化,提高乙酰苯胺的产率。
3. 活性炭的加入可以吸附未反应的苯胺和乙酰苯胺,提高产品的纯度。
4. 通过重结晶,可以进一步提高乙酰苯胺的纯度,使其达到药用要求。
⼄酰苯胺的制备
⼄酰苯胺的制备
⼀、实验⽬的
1、了解和掌握⼄酰保护anji4的⽅法和应⽤。
2、掌握分馏柱除⽔的原理和⽅法。
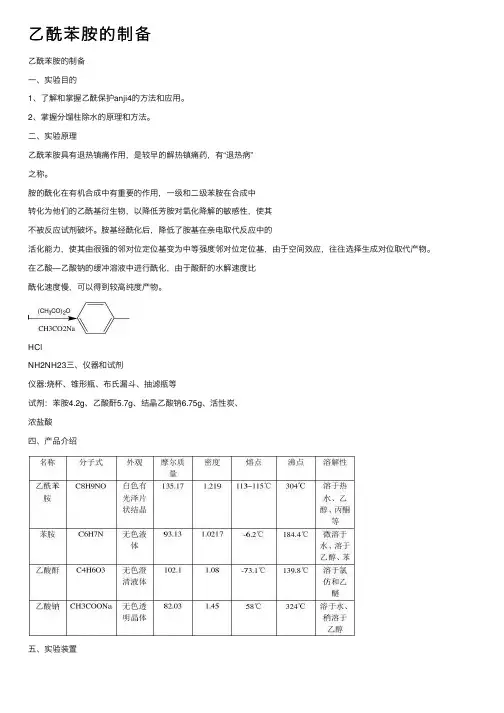
⼆、实验原理
⼄酰苯胺具有退热镇痛作⽤,是较早的解热镇痛药,有“退热病”
之称。
胺的酰化在有机合成中有重要的作⽤,⼀级和⼆级苯胺在合成中
转化为他们的⼄酰基衍⽣物,以降低芳胺对氧化降解的敏感性,使其
不被反应试剂破坏。
胺基经酰化后,降低了胺基在亲电取代反应中的
活化能⼒,使其由很强的邻对位定位基变为中等强度邻对位定位基,由于空间效应,往往选择⽣成对位取代产物。
在⼄酸—⼄酸钠的缓冲溶液中进⾏酰化,由于酸酐的⽔解速度⽐
酰化速度慢,可以得到较⾼纯度产物。
HCl
NH2NH23三、仪器和试剂
仪器:烧杯、锥形瓶、布⽒漏⽃、抽滤瓶等
试剂:苯胺4.2g、⼄酸酐5.7g、结晶⼄酸钠6.75g、活性炭、
浓盐酸
四、产品介绍
五、实验装置
六、实验流程
3.8mL 浓盐酸的3.9mL 苯胺得⽩⾊⽚状固体称重,计算产率
七、实验步骤
⼋、数据处理
由⼀摩尔苯胺⽣成⼀摩尔⼄酰苯胺。
理论产率n=0.045mol的⼄酰苯胺
理论质量m=0.045*135.17=6.08265g
产率w=4.97/6.08265=81.71%
九、思考题
1、⼄酸酐和⼄酸的优缺点?还有那些⼄酰化试剂?
答:⼄酸酐反应时间短,但价格较⾼。
⼄酸相对便宜,但反应时间长。
还有⼄酸酯、酰卤。
2、加盐酸和⼄酸钠的⽬的?
答:加盐酸会⽣成胺盐,使反应平缓。
加⼄酸钠调节pH,促进反应。

乙酰苯胺的制备实验报告乙酰苯胺的制备实验报告一、引言乙酰苯胺,也称为N-乙酰苯胺,是一种常见的有机化合物。
它具有苯胺分子结构中的一个氢原子被乙酰基取代的特点。
乙酰苯胺广泛应用于医药、染料、涂料等领域,因此其制备方法备受关注。
本实验旨在通过一种简单的合成方法制备乙酰苯胺,并对其产率进行评估。
二、实验原理乙酰苯胺的制备方法主要有两种:酰胺化反应和酰化反应。
本实验采用酰胺化反应,即苯胺与酢酸反应生成乙酰苯胺。
三、实验步骤1. 实验前准备:准备苯胺、醋酸、浓硫酸和冷却剂。
2. 反应装置:将苯胺溶解在少量水中,加入浓硫酸稀释至苯胺溶液的浓度为2mol/L。
将醋酸倒入冰水中制成醋酸冰浴。
3. 反应操作:将苯胺溶液加入反应瓶中,然后缓慢滴加醋酸冰浴,同时搅拌反应瓶。
反应结束后,将反应液倒入冷却剂中。
4. 结晶纯化:将产物过滤并用冷水洗涤,然后用冷乙酸乙酯洗涤,最后用醋酸乙酯洗涤。
将产物晾干,称量并计算产率。
四、实验结果与讨论根据实验操作,我们成功合成了乙酰苯胺。
通过过滤、洗涤和晾干,得到了纯净的产物。
我们称量了产物的质量,并计算了产率。
在实验过程中,我们注意到苯胺与醋酸反应时会放热,因此需要控制反应温度。
此外,由于苯胺是一种有毒物质,实验操作时要注意安全。
通过实验结果的分析,我们可以得出以下结论:1. 乙酰苯胺的合成方法简单,易于操作,适用于中小规模生产。
2. 实验中的产率可以通过改变反应条件进行优化。
例如,可以调整反应温度、反应时间和反应物的比例等。
3. 乙酰苯胺是一种重要的有机化合物,在医药和化工领域有广泛的应用前景。
五、结论通过本实验,我们成功合成了乙酰苯胺,并对其产率进行了评估。
实验结果表明,该合成方法简单可行,并具有一定的产率。
乙酰苯胺作为一种重要的有机化合物,在医药和化工领域具有广泛的应用前景。
本实验为乙酰苯胺的制备提供了一种有效的方法,并为进一步研究和应用提供了基础。
乙酰苯胺的制备一.实验目的1.以乙酸和苯胺为原料合成乙酰苯胺。
2.乙酰苯胺粗品用水重结晶法得到纯品。
3.掌握分馏柱除水的原理及方法。
二.实验原理乙酰苯胺为无色晶体,具有退热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称。
乙酰苯胺可由苯胺与乙酰化试剂如:乙酰氯、乙酐或乙酸等直接作用来制备。
反应活性是乙酰氯>乙酐>乙酸。
由于乙酰氯和乙酐的价格较贵,本实验选用乙酸作为乙酰化试剂。
反应如下:乙酸与苯胺的反应速率较慢,且反应是可逆的,为了提高乙酰苯胺的产率,一般采用冰乙酸过量的方法,同时利用分馏柱将反应中生成的水从平衡中移去。
由于苯胺易氧化,加入少量锌粉,防止苯胺在反应过程中氧化。
乙酰苯胺本身是重要的药物,而且是磺胺类药物合成中重要的中间体。
本实验除了在合成上的意义外,还有保护芳环上氨基的作用。
由于芳环上的氨基易氧化,通常先将其乙酰化,然后再在芳环上接上所需基团,再利用酰胺能水解成胺的性质,恢复氨基。
三.实验装置刺型分馏柱四.试剂与器材1、反应圆底烧瓶中,加入5ml苯胺,7.5ml冰醋酸,0.1g 锌粉。
装上刺型分馏柱,柱口装蒸馏头,温度计,蒸馏头出口安装接液管。
加热至反应物微沸10分钟,逐渐升高温度到100℃。
蒸馏头有水馏出,用量筒承接。
维持反应温度100~110℃之间1小时。
水馏出约4ml。
温度计读数下降。
表示反应完成。
2、结晶抽滤反应液搅拌下倒入100ml冷水中。
冷却后抽滤。
粗品晾干。
3、精制粗品用水重结晶。
抽滤,产品晾干称重。
计算产率。
六.注意事项1.反应所用玻璃仪器必须干燥。
2.久置的苯胺因为氧化而颜色较深,最好使用新蒸馏过的苯胺。
3.冰乙酸在室温较低时凝结成冰状固体(凝固点C),可将试剂瓶置于热水浴中加热熔化后量取。
4.锌粉的作用是防止苯胺氧化,只要少量即可。
加得过多,会出现不溶于水的氢氧化锌。
5.反应时间至少30min。
否则反应可能不完全而影响产率。
6.反应时分馏温度不能太高,以免大量乙酸蒸出而降低产率。
§实验一、多步反应制备乙酰苯胺的制备及其红外测定实验目的:1、学习实验室以硝基化合物为原料制备胺、由醋酐和苯胺合成乙酰苯胺的方法和原理;2、学习回流、洗涤、萃取、盐析、高沸点蒸馏和沸点测定等基本操作。
3、巩固水蒸气蒸馏、重结晶、熔点测定、红外光谱测定基本操作。
实验原理:一、苯胺的制备1、反应方程式:4C 6H 5NO 2 + 9Fe + 4H 2O4C 6H 5NH 2 +3Fe 3O 42、可能的副反应NONHOHH 2O NH N N++NO+H 2O+二、乙酰苯胺的制备NH 2Ac 2ONHCOCH 3+CH 3CCOH实验仪器和药品:圆底烧瓶,回流冷凝管,水蒸汽蒸馏装置,分液漏斗,蒸馏烧瓶,空气冷凝管,硝基苯,铁粉,水,盐酸,碳酸钠,乙醚,氯化钠,氢氧化钠,烧杯,布氏漏斗,苯胺,醋酐 实验装置图:图1. 苯胺的制备 图2. 苯胺的分离图3. 苯胺的提纯实验内容:一、苯胺的制备在一个250 mL圆底烧瓶中,放置20 g的铁粉,20 mL水和1 mL的浓盐酸和1 mL 醋酸,用力摇晃,使其混合均匀,微微加热煮沸几分钟,稍冷后加入10.5 g的硝基苯,装上回流冷凝管,小火加热回流1 h,在回流过程中经常用力摇晃使反应化合物均匀,反应完毕后,加入碳酸钠使反应体系呈碱性。
进行水蒸气蒸馏直到馏出液澄清为止,将馏出液放入分液漏斗中分出苯胺。
水层加入氯化钠使溶液饱和,分出有机层,用块状的氢氧化钠干燥,空气冷凝管,蒸馏收集180~185 °C 馏分,称重计算产量、产率和测定苯胺的折光率。
二、乙酰苯胺的制备250 mL烧杯中,放置新蒸馏的2.3 mL苯胺,2.3 mL盐酸,65 mL水加热到50 °C,加入13 mL含3.8 g醋酸钠的水溶液,迅速加入2.3 mL醋酐,冷却搅拌。
过滤后固体加入50 mL水加热溶解,冷却结晶,过滤,干燥,称量、计算产率、测量熔点和测量红外光谱。
实验流程图图4. 苯胺制备实验流程图, 30 mins 水蒸气蒸馏水层有机层残液过滤图5. 乙酰苯胺制备流程图2.3mL 苯胺65 mL H O过滤母液(弃之)重结晶实验注意事项1、本实验的搅拌非常关键,在反应回流过程中,要不断用力摇晃,使反应物充分混合,反应充分,因为该实验不是均相反应。
乙酰苯胺的制备实验报告实验目的:通过对苯胺和乙酸酐的反应,制备乙酰苯胺,并对其产率进行测定。
实验原理:乙酰苯胺的制备反应为苯胺和乙酸酐在酸性条件下的酰化反应,反应方程式如下:C6H5NH2 + (CH3CO)2O → C6H5NHCOCH3 + CH3COOH。
其中,苯胺与乙酸酐在酸性条件下发生缩合反应,生成乙酰苯胺和乙酸。
实验步骤:1. 在干燥管中装入苯胺(10mmol)、乙酸酐(12mmol),加入少量氯化钙干燥剂。
2. 将干燥管加热至60-70℃反应2小时。
3. 反应结束后,冷却至室温,用乙酸酐洗涤产物,过滤得到沉淀。
4. 用冷水洗涤沉淀,得到乙酰苯胺。
5. 对产物进行干燥和称重,计算产率。
实验结果:实验中得到的乙酰苯胺产物质量为2.5g,摩尔质量为135.17g/mol,因此产率为:产率 = (实际产物质量 / 理论产物质量) × 100% = (2.5g / 135.17g) × 100% ≈1.85%。
实验结论:本实验成功制备了乙酰苯胺,并通过产率计算得到了反应的效率。
实验结果表明,乙酰苯胺的制备反应在实验条件下具有一定的可行性,但产率较低,可能受到反应条件和操作技巧的影响。
在今后的实验中,可以通过优化反应条件和改进操作技术,提高乙酰苯胺的产率。
实验注意事项:1. 实验中应注意安全,避免接触到有毒或腐蚀性物质。
2. 反应过程中应控制温度和反应时间,避免产物的不必要损失。
3. 实验结束后,应妥善处理产物和废弃物,保持实验室清洁整洁。
实验存在的问题和改进方向:1. 产率较低,可能是由于实验条件不够理想或操作技巧不够熟练所致,可以通过改进反应条件和加强操作技巧来提高产率。
2. 实验中可能存在其他影响产率的因素,可以通过进一步分析和实验验证来寻找并解决问题。
参考文献:[1] 陈启华, 高等有机化学实验, 化学工业出版社, 2008.[2] 张三, 有机合成实验, 化学工业出版社, 2010.。
乙酰苯胺的制备实验乙酰苯胺(N-乙酰苯胺)是一种重要的有机化合物,在医药、染料和涂料等领域有广泛的应用。
本文将详细介绍乙酰苯胺的制备实验方法,希望对化学实验研究者有所帮助。
实验材料及设备:1. 苯胺(50 mL)2. 乙酸酐(30 mL)3. 硫酸(浓度为98%)(20 mL)4. 冰醋酸(50 mL)5. 饱和氯化钠溶液(10 mL)6. 氢氧化钠溶液(5%)(20 mL)7. 蒸馏水(适量)8. 250 mL圆底烧瓶9. 温度控制装置,磁力搅拌器10. 羊毛滤纸11. 烧杯、滴定管、试管及玻璃棒等常用实验器材实验步骤:1. 预准备a. 准备250 mL圆底烧瓶,加入苯胺(50 mL)和冰醋酸(50 mL)。
b. 在温度控制装置上固定圆底烧瓶,将烧瓶放入温水槽中,温度设定为10°C。
c. 开启磁力搅拌器,以适度的速度搅拌苯胺和冰醋酸混合液。
2. 添加乙酸酐a. 用滴定管逐渐向溶液中滴加乙酸酐(30 mL),同时保持搅拌。
b. 滴加完毕后,继续搅拌混合液10分钟。
3. 加入硫酸催化剂a. 将硫酸(20 mL)缓慢地加入反应混合液,注意避免溅出。
b. 加入硫酸后,继续搅拌混合物1小时。
4. 分离产物a. 将反应混合物转移到烧杯中。
b. 将烧杯中的产物加入饱和氯化钠溶液(10 mL),搅拌均匀。
c. 使用羊毛滤纸过滤产物,将滤液收集在干净的容器中。
5. 精炼产物a. 将收集到的滤液转移至250 mL圆底烧瓶中。
b. 加入氢氧化钠溶液(5%)(20 mL),轻轻搅拌。
c. 将烧瓶放入冰水槽中冷却,使其结晶沉淀。
d. 用玻璃棒挑出结晶沉淀,放在过滤纸上晾干。
实验结果与讨论:通过以上实验步骤,我们成功合成了乙酰苯胺。
实验中,苯胺与乙酸酐在催化剂硫酸的作用下发生酰化反应,生成目标产物。
乙酰苯胺在室温下为白色结晶固体,可以用于有机合成的中间体和染料的合成等许多领域。
此实验中的制备方法简单、方便,具有一定的实用性。