氨基酸含量计算公式(氨基酸占鲜样、干样、蛋白、蛋白氮的比例计算公式)
- 格式:ppt
- 大小:63.50 KB
- 文档页数:6

氨基酸(amino acid,AA)含量测定试剂盒使用说明分光光度法注意:正式测定之前选择2-3个预期差异大的样本做预测定。
货号:BC1570规格:50T/48S产品内容:试剂一:液体×1瓶,4℃保存。
试剂二:液体×1瓶,4℃保存。
试剂三:粉剂×1瓶(棕色),4℃避光保存。
临用前加入2mL无水乙醇,盖紧后充分混匀,再加入28mL蒸馏水混匀,避光保存。
试剂四:粉剂×1管,4℃避光保存。
临用前加10mL蒸馏水,充分溶解。
标准品:液体×1支,1μmol/mL标准液,4℃避光保存。
产品说明:动物肝脏、肾脏是氨基酸代谢的主要器官,故尿中氨基酸的变化最能反应肝、肾的生理状态。
另外,氨基酸还能反应灼伤、伤寒等方面情况。
植物体内氨基酸含量对研究植物在不同条件下及不同生长发育时期氮代谢变化、植物对氮素的吸收、运输、同化及营养状况等有重要意义。
氨基酸的α-氨基可与水合茚三酮反应,产生蓝紫色化合物,在570nm有特征吸收峰;通过测定570nm吸光度,来计算氨基酸含量。
自备仪器及用品:台式离心机、水浴锅、紫外分光光度计、1ml玻璃比色皿、可调式移液枪、研钵、无水乙醇、冰和蒸馏水。
操作步骤:一、样品中AA提取:1.按照组织质量(g):试剂一体积(mL)为1:5~10的比例(建议称取约0.1g组织,加入1mL试剂一)进行室温匀浆,然后转移到1.5mL EP管中,盖紧后(防止水分散失)置于沸水浴提取15min;自来水冷却后,8000g,,4℃离心10min,上清液置冰上待测。
2.细菌或培养细胞:先收集细菌或细胞到离心管内,离心后弃上清;按照细菌或细胞数量(104个):试剂一体积(mL)为500~1000:1的比例(建议500万细菌或细胞加入1mL试剂一),超声波破碎细菌或细胞(冰浴,功率20%或200W,超声3s,间隔10s,重复30次);8000g,4℃离心10min,取上清,置冰上待测。

氨基酸含量的测定标准曲线绘制准确吸取200ug/ml的氨基酸标准溶液0.0,0.6,0.8,1.0,1.2,1.5,2.0 ml,分别置于25ml容量瓶或比色管中,各加水补充至溶剂为4.0ml,然后加入茚三酮和磷酸缓冲溶液各1ml,混合均匀,于水浴上加热15min,取出迅速冷至室温,再摇匀,加水至标线25ml,摇匀。
静置15min后,在570nm波长下,以试剂空白为参比液夨订其余各溶液的吸光度A。
以氨基酸的微克数为横坐标,吸光度A为纵坐标,绘制标准曲线。
样品的测定:将虾研磨冷却过滤后稀释10倍,吸取澄清的样品溶液1.5ml,平行三次,按标准曲线制作步骤,在相同条件下测定吸光度A 值,用测得的A值在标准曲线上即可查得氨基酸的微克数。
公式:氨基酸总量(ug/100g)=(c/m*1000)*100*10式中c是指从标准曲线上查得的氨基酸的ug数;M是指测定的样品溶液相当于样品的质量g;PH计酸度计测量ph的方法:(1)拿下笔帽(2)按on/off键,机器显示运作(3)将ph计放入待测液中(4)轻轻晃动ph计,保证内气泡逸出,使之于溶液充分接触,勿碰撞杯壁(5)ph计会立即显示数值,将笔置入待测液待数值稳定,30秒内将显示正确数值,(特:ph计数值上下浮动或不稳定是正常现象)(6)按hold键锁定数值,可在待测溶液外记录读取,继续按hold键解除锁定(7)按on/off键关闭ph计(8)轻甩PH计测试笔上多于的水,用蒸馏水或脱离子水冲洗,盖上笔帽测量温度方法在测试模式下,温度数值与ph数值同步显示在液晶面板上,但在校准模式下不显示,数值默认为摄氏温度。
(一)挥发性盐基氮(TVB-N)的测定半微量定氮法(1)原理:蛋白质在酶和细菌的作用下分解后产生碱性含氮物质,有氨、伯胺、仲胺等,此类物质具有挥发性,可在碱性溶液中被蒸馏出来,用标准酸滴定,计算含量。
(2)试剂①氧化镁混悬液(10g/L) 称取1.0g氧化镁,加100ml水,振摇成混悬液。

蛋白质元素氮含量计算公式在生物化学和营养学领域,蛋白质是一种重要的营养物质,它是构成生物体的重要组成部分,也是维持生命活动所必需的。
蛋白质的基本单位是氨基酸,每个氨基酸分子中都含有一个或多个氮原子。
因此,蛋白质中的氮元素含量可以作为蛋白质含量的一个重要指标。
本文将介绍蛋白质元素氮含量的计算公式及其应用。
蛋白质元素氮含量的计算公式如下:蛋白质含量(g)= 氮元素含量(g)/ 6.25。
在这个公式中,蛋白质含量以克(g)为单位,氮元素含量也以克(g)为单位。
6.25是一个常数,它是根据蛋白质中氮元素的平均含量来确定的。
根据这个公式,只要知道了蛋白质中氮元素的含量,就可以通过简单的计算得到蛋白质的含量。
蛋白质元素氮含量的计算公式的应用非常广泛。
在食品科学和营养学领域,研究人员经常使用这个公式来测定不同食品中蛋白质的含量。
他们首先测定食品样品中氮元素的含量,然后通过上述公式计算出蛋白质的含量。
这种方法简单、快捷,而且准确度较高,因此得到了广泛的应用。
除了在食品科学和营养学领域,蛋白质元素氮含量的计算公式还被广泛应用于生物化学和生物医学研究中。
研究人员经常需要测定细胞或生物体中蛋白质的含量,以了解其生理功能和代谢过程。
他们可以通过测定样品中氮元素的含量,然后利用上述公式计算蛋白质的含量,从而得到他们所需要的数据。
需要指出的是,蛋白质元素氮含量的计算公式虽然简单易用,但在实际应用中也存在一些限制和注意事项。
首先,这个公式是根据蛋白质中氮元素的平均含量来确定的,因此在不同类型的蛋白质中可能存在一定的误差。
其次,样品的制备和测定方法也会对结果产生影响,需要严格控制实验条件以确保结果的准确性。
总之,蛋白质元素氮含量的计算公式是一个简单而实用的工具,它在食品科学、营养学、生物化学和生物医学研究中得到了广泛的应用。
通过测定样品中氮元素的含量,然后利用上述公式计算蛋白质的含量,研究人员可以快速、准确地获得所需的数据,为他们的研究工作提供有力支持。

氨基酸评分计算公式氨基酸评分是一种用来衡量蛋白质品质的方法,它通过分析蛋白质中各种氨基酸的含量和比例来评估其在人体内的营养功能。
根据氨基酸评分,我们可以更好地了解食物中的蛋白质质量,从而指导我们的膳食选择。
首先,我们需要了解什么是氨基酸。
氨基酸是构成蛋白质的基本组成部分,共有20种不同的氨基酸。
其中,有9种被称为“必需氨基酸”,因为人体无法自身合成,必须从食物中摄入。
这9种必需氨基酸包括赖氨酸、异亮氨酸、亮氨酸、苯丙氨酸、色氨酸、甲硫氨酸、苏氨酸、缬氨酸和苏氨酸。
氨基酸评分是通过比较蛋白质中各种必需氨基酸的含量和人体所需的理想比例来进行的。
理想的氨基酸比例是根据人体需要的营养素和生理机能来确定的。
如果某种食物中的氨基酸含量和比例与理想比例相似,那么它的氨基酸评分就会很高。
所以,如何计算氨基酸评分呢?通常,我们会将食物中各种必需氨基酸的含量与理想比例进行比较,并将它们进行百分比蛋白质完备度计算。
百分比蛋白质完备度指的是蛋白质中包含的必需氨基酸的百分比。
例如,如果某种蛋白质中的赖氨酸含量是理想比例的90%,那么它的百分比蛋白质完备度就是90%。
然而,单纯的氨基酸评分并不能完全反映蛋白质的品质,因为它只考虑了必需氨基酸的含量和比例,而忽略了其他非必需氨基酸的贡献。
因此,我们在评估蛋白质质量时还需要综合考虑其他因素,例如消化吸收率、生物活性等。
除了了解氨基酸评分的计算方法外,我们还可以根据不同的个体需求和健康目标来选择合适的蛋白质食物。
对于素食主义者来说,他们需要通过搭配不同的植物蛋白来源来获得全面的必需氨基酸。
对于运动员和健身爱好者来说,他们可以选择富含氨基酸的动物蛋白质,以支持肌肉生长和修复。
综上所述,氨基酸评分是评估蛋白质品质的重要指标之一,它能帮助我们了解食物中蛋白质的营养价值,并为我们的膳食选择提供指导。
然而,我们需要综合考虑其他因素,如消化吸收率和生物活性,以全面评估蛋白质的质量。
通过选择适合自己需求的蛋白质食物,我们可以保证获得足够的必需氨基酸,维持身体健康和功能。
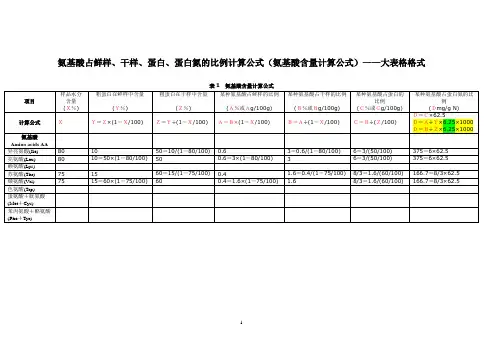
氨基酸占鲜样、干样、蛋白、蛋白氮的比例计算公式(氨基酸含量计算公式)——大表格格式表1 氨基酸含量计算公式氨基酸占鲜样、干样、蛋白、蛋白氮的比例计算公式(氨基酸含量计算公式)——小表格格式表1 氨基酸含量计算公式Ⅰ氨基酸占鲜样、干样、蛋白、蛋白氮的比例计算公式(氨基酸含量计算公式)——WORD格式样品某种氨基酸含量(鲜样)氨基酸含量/(mg/g N)=—————————————×6.25×1000样品粗蛋白含量(鲜样)样品某种氨基酸含量(干样)氨基酸含量/(mg/g N)=—————————————×6.25×1000样品粗蛋白含量(干样)某种氨基酸占鲜样的比例(A%或Ag/100g)↑ ∣A=B×(1-X/100)∣ ∣B=A÷(1-X/100)←——————样品水分含量(X%)∣ ↓某种氨基酸占干样的比例(B%或Bg/100g) 粗蛋白在鲜样中含量(Y%)↑ ∣ ↑ ∣∣ ∣ Y=Z×(1-X/100)∣ ∣Z=Y÷(1-X/100)∣ ∣ ∣ ↓B=C×(Z/100)∣ ∣C=B÷(Z/100)←———————粗蛋白在干样中含量(Z%)∣ ↓某种氨基酸占蛋白的比例(C%或Cg/100g)↑ ∣D=C×62.5C=D÷62.5∣ ∣D=A÷Y×6.25×1000∣ ↓D=B÷Z×6.25×1000某种氨基酸占蛋白氮的比例(Dmg/g N)必须知道样品水分含量;粗蛋白在鲜样中含量、粗蛋白在干样中含量,二者必须知道其一;某种氨基酸占鲜样的比例、某种氨基酸占干样的比例、某种氨基酸占蛋白的比例、某种氨基酸占蛋白氮的比例,四者必须知道其一。
氨基酸占鲜样、干样、蛋白、蛋白氮的比例计算公式(氨基酸含量计算公式)——图片格式样品某种氨基酸含量(鲜样)氨基酸含量/(mg/g N)=—————————————×6.25×1000样品粗蛋白含量(鲜样)样品某种氨基酸含量(干样)氨基酸含量/(mg/g N)=—————————————×6.25×1000样品粗蛋白含量(干样)某种氨基酸占鲜样的比例(A%或Ag/100g)↑∣A=B×(1-X/100)∣∣B=A÷(1-X/100)………样品水分含量(X%)∣↓某种氨基酸占干样的比例(B%或Bg/100g) 粗蛋白在鲜样中含量(Y%)↑∣↑∣∣∣Y=Z×(1-X/100)∣∣Z=Y÷(1-X/100)∣∣∣↓B=C×(Z/100)∣∣C=B÷(Z/100)……………粗蛋白在干样中含量(Z%)∣↓某种氨基酸占蛋白的比例(C%或Cg/100g)↑∣D=C×62.5C=D÷62.5∣∣D=A÷Y×6.25×1000∣↓D=B÷Z×6.25×1000某种氨基酸占蛋白氮的比例(Dmg/g N)必须知道样品水分含量;粗蛋白在鲜样中含量、粗蛋白在干样中含量,二者必须知道其一;某种氨基酸占鲜样的比例、某种氨基酸占干样的比例、某种氨基酸占蛋白的比例、某种氨基酸占蛋白氮的比例,四者必须知道其一。

有关氨基酸、蛋白质的相关计算(1)一个氨基酸中的各原子的数目计算:C原子数=R 基团中的C原子数+2,H原子数=R基团中的H原子数+4,O原子数=R基团中的O原子数+2,N原子数=R基团中的N原子数+1 (2)肽链中氨基酸数目、肽键数目和肽链数目之间的关系:若有n个氨基酸分子缩合成m条肽链,则可形成(n-m)个肽键,脱去(n-m)个水分子,至少有-NH2和-COOH各m个。
(3)氨基酸的平均分子量与蛋白质的分子量之间的关系:n个氨基酸形成m条肽链,每个氨基酸的平均分子量为a,那么由此形成的蛋白质的分子量为:n•a-(n-m)•18 (其中n-m为失去的水分子数,18为水的分子量);该蛋白质的分子量比组成其氨基酸的分子量之和减少了(n-m)•18。
(4)在R基上无N元素存在的情况下,N原子的数目与氨基酸的数目相等。
2.有关碱基互补配对原则的应用:(1)互补的碱基相等,即A=T,G=C。
(2)不互补的两种碱基之和与另两种碱基之和相等,且等于50%。
(3)和之比在双链DNA分子中:●能够互补的两种碱基之和与另两种碱基之和的比同两条互补链中的该比值相等,即:(A+T)/(G+C)=(A1+T1)/(G1+C1)=(A2+T2)/(G2+C2);●不互补的两种碱基之和与另两种碱基之和的比等于1,且在其两条互补链中该比值互为倒数,即:(A+G)/(T+C)=1;(A1+G1)/(T1+C1)=(T2+C2)/(A2+G2)(4)双链DNA分子中某种碱基的含量等于两条互补链中该碱基含量和的一半,即A=(A1+A2)/2(G、T、C同理)。
(一)有关蛋白质和核酸计算:[注:肽链数(m);氨基酸总数(n);氨基酸平均分子量(a);氨基酸平均分子量(b);核苷酸总数(c);核苷酸平均分子量(d)]。
1.蛋白质(和多肽):氨基酸经脱水缩合形成多肽,各种元素的质量守恒,其中H、O参与脱水。
每个氨基酸至少1个氨基和1个羧基,多余的氨基和羧基来自R基。

氨基酸态氮含量公式以氨基酸态氮含量公式为标题的文章:氨基酸是构成蛋白质的基本单位,也是人体所需的重要营养素之一。
氨基酸的态氮含量是评价蛋白质质量的指标之一,它可以反映出蛋白质中的氮元素含量。
本文将介绍氨基酸态氮含量的计算公式以及其意义。
氨基酸态氮含量的计算公式如下:态氮含量(g/kg)= 氨基酸含量(g/100g)× 100 ÷ 14.01其中,氨基酸含量是指100克食物中所含氨基酸的重量,14.01是氮元素的相对原子质量。
氨基酸态氮含量的计算公式是通过测定氨基酸含量和相对原子质量的比值来估计蛋白质中的氮元素含量。
由于氨基酸是构成蛋白质的基本组成部分,蛋白质中的氮元素主要来自于氨基酸。
因此,通过测定氨基酸含量并转化为态氮含量,可以较为准确地评估蛋白质的质量。
氨基酸态氮含量的意义在于可以帮助人们评价蛋白质的营养价值和消化利用率。
蛋白质是人体生长发育和维持正常生理功能所必需的营养素,而氨基酸是蛋白质的构成单元。
通过测定蛋白质中氨基酸的态氮含量,可以了解蛋白质中氮元素的含量,从而评估蛋白质的质量和营养价值。
不同食物中的氨基酸态氮含量有所差异,一般来说,动物性食物中的氨基酸态氮含量较高,植物性食物中的氨基酸态氮含量较低。
这是因为动物性食物中含有较多的优质蛋白质,而植物性食物中的蛋白质质量较差。
因此,通过测定氨基酸态氮含量,可以评估不同食物中蛋白质的质量和营养价值,为人们合理搭配膳食提供参考依据。
氨基酸态氮含量还可以用于评估蛋白质消化利用率。
蛋白质在人体内经过消化吸收后,氨基酸会被利用于合成新的蛋白质,或者被氨基酸氧化代谢产生能量。
通过测定蛋白质中氨基酸的态氮含量,可以了解蛋白质在消化过程中的损失情况,从而评估蛋白质的消化利用率。
氨基酸态氮含量是评价蛋白质质量和营养价值的重要指标之一。
通过测定氨基酸含量并转化为态氮含量,可以评估蛋白质的质量和消化利用率,为人们合理搭配膳食提供科学依据。
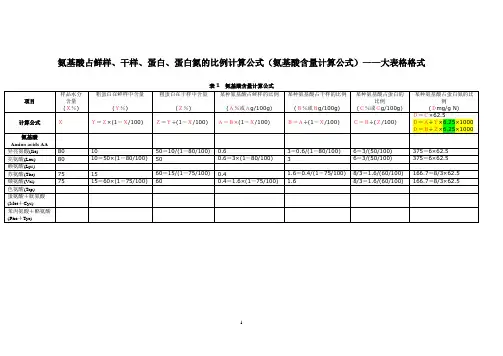
氨基酸占鲜样、干样、蛋白、蛋白氮的比例计算公式(氨基酸含量计算公式)——大表格格式表1 氨基酸含量计算公式氨基酸占鲜样、干样、蛋白、蛋白氮的比例计算公式(氨基酸含量计算公式)——小表格格式表1 氨基酸含量计算公式Ⅰ氨基酸占鲜样、干样、蛋白、蛋白氮的比例计算公式(氨基酸含量计算公式)——WORD格式样品某种氨基酸含量(鲜样)氨基酸含量/(mg/g N)=—————————————×6.25×1000样品粗蛋白含量(鲜样)样品某种氨基酸含量(干样)氨基酸含量/(mg/g N)=—————————————×6.25×1000样品粗蛋白含量(干样)某种氨基酸占鲜样的比例(A%或Ag/100g)↑ ∣A=B×(1-X/100)∣ ∣B=A÷(1-X/100)←——————样品水分含量(X%)∣ ↓某种氨基酸占干样的比例(B%或Bg/100g) 粗蛋白在鲜样中含量(Y%)↑ ∣ ↑ ∣∣ ∣ Y=Z×(1-X/100)∣ ∣Z=Y÷(1-X/100)∣ ∣ ∣ ↓B=C×(Z/100)∣ ∣C=B÷(Z/100)←———————粗蛋白在干样中含量(Z%)∣ ↓某种氨基酸占蛋白的比例(C%或Cg/100g)↑ ∣D=C×62.5C=D÷62.5∣ ∣D=A÷Y×6.25×1000∣ ↓D=B÷Z×6.25×1000某种氨基酸占蛋白氮的比例(Dmg/g N)必须知道样品水分含量;粗蛋白在鲜样中含量、粗蛋白在干样中含量,二者必须知道其一;某种氨基酸占鲜样的比例、某种氨基酸占干样的比例、某种氨基酸占蛋白的比例、某种氨基酸占蛋白氮的比例,四者必须知道其一。
氨基酸占鲜样、干样、蛋白、蛋白氮的比例计算公式(氨基酸含量计算公式)——图片格式样品某种氨基酸含量(鲜样)氨基酸含量/(mg/g N)=—————————————×6.25×1000样品粗蛋白含量(鲜样)样品某种氨基酸含量(干样)氨基酸含量/(mg/g N)=—————————————×6.25×1000样品粗蛋白含量(干样)某种氨基酸占鲜样的比例(A%或Ag/100g)↑∣A=B×(1-X/100)∣∣B=A÷(1-X/100)………样品水分含量(X%)∣↓某种氨基酸占干样的比例(B%或Bg/100g) 粗蛋白在鲜样中含量(Y%)↑∣↑∣∣∣Y=Z×(1-X/100)∣∣Z=Y÷(1-X/100)∣∣∣↓B=C×(Z/100)∣∣C=B÷(Z/100)……………粗蛋白在干样中含量(Z%)∣↓某种氨基酸占蛋白的比例(C%或Cg/100g)↑∣D=C×62.5C=D÷62.5∣∣D=A÷Y×6.25×1000∣↓D=B÷Z×6.25×1000某种氨基酸占蛋白氮的比例(Dmg/g N)必须知道样品水分含量;粗蛋白在鲜样中含量、粗蛋白在干样中含量,二者必须知道其一;某种氨基酸占鲜样的比例、某种氨基酸占干样的比例、某种氨基酸占蛋白的比例、某种氨基酸占蛋白氮的比例,四者必须知道其一。

凯氏定氮法测定蛋白质含量公式
1 凯氏定氮法
凯氏定氮法是一种常用的测定蛋白质含量的方法,由凯氏于1883
年提出。
它的原理是:将样品中的蛋白质氨基酸氧化分解为氨态水,
测定样品中氨态氮的含量,用凯氏定氮法公式计算蛋白质的实际含量。
2 凯氏定氮法的基本原理
凯氏定氮法的基本原理是将蛋白质氨基酸浓度通过离子交换树脂
提取,然后将氨基酸氧化分解为氨态水,再测定样品中氨态氮的含量,用凯氏定氮法公式计算蛋白质的实际含量,凯氏定氮法公式如下:
3 凯氏定氮法公式
蛋白质的实际含量=样品内的氨态氮的总量(毫克)÷6.25
其中6.25是认为蛋白质中的结构基元氨基酸的比例为1:6.25,也就是说,100毫克蛋白质中含有16毫克氨基酸,以此类推。
4 凯氏定氮法的优势
凯氏定氮法具有准确、快速、重现性好等特点,在实时测定立即
分析模式中,仍是最常用的技术。
从实验时间上看,凯氏定氮法比其
他定氮方式更加快捷,且准确率较高,受其实验程序简单、复杂材料
分离容易使用的优势受到广大研究人员的青睐。
5 凯氏定氮法的应用
凯氏定氮法大多用于测定含氨基酸的蛋白质,应用范围很广,一般应用在动物、植物的分子的氨基酸的分析,主要用于衡量蛋白质含量,便于计算组分,如果其他物质也能被氧化,也可以用它进行测定计算。
另外,凯氏定氮法也可以用于研究病毒、细菌等非蛋白质有机物的含氮量。

含氮量与蛋白质含量换算公式
含氮量与蛋白质含量是密切相关的,因为蛋白质是由氨基酸组成的,而氨基酸中含有氮元素。
因此,测定食品中的含氮量可以推算出其中的蛋白质含量。
下面介绍一些相关的公式和计算方法。
1. 总氮量与蛋白质含量的转换
在食品中,总氮量通常用Kjeldahl法测定。
这种方法是将样品加入硫酸和碱性钾高锰酸盐溶液中加热,使其中的有机氮转化为无机氮,再用氢氧化钠溶液将硫酸中的氮化合物中和。
最终,通过滴定测定氢氧化钠的用量,计算出样品中的总氮量。
总氮量(g)×6.25=蛋白质含量(g)
其中,6.25是蛋白质的氮含量,因此将总氮量乘以6.25即可得到蛋白质含量的估算值。
这个方法可以用于大部分食品,包括动物性食品和植物性食品。
2. 牛奶中蛋白质含量的计算
牛奶是富含蛋白质的营养食品,其中90%的蛋白质为酪蛋白,其余为乳清蛋白、β-球蛋白和α-乳白蛋白等。
在牛奶中,蛋白质含量的计算方法如下。
牛奶中的总氮量(g)×0.68=酪蛋白含量(g)
牛奶中的总氮量(g)×0.09=乳清蛋白含量(g)
其中,0.68和0.09是对各自种类蛋白质的氮含量进行的乘数修正。
3. 大豆中蛋白质含量的计算
大豆是一种富含蛋白质的植物性食品,其蛋白质质量分数约为40%。
大豆中的蛋白质含量计算方法如下。
大豆中的总氮量(g)×6.25×0.4=蛋白质含量(g)
其中,6.25仍然是蛋白质的氮含量,0.4是大豆中蛋白质质量分数。
在实际生产和食品检测中,以上公式和方法仅供参考,具体还需要结合各种因素进行修正和调整。

氨基酸含量的测定标准曲线绘制准确吸取200ug/ml的氨基酸标准溶液0.0,0.6,0.8,1.0,1.2,1.5,2.0 ml,分别置于25ml容量瓶或比色管中,各加水补充至溶剂为4.0ml,然后加入茚三酮和磷酸缓冲溶液各1ml,混合均匀,于水浴上加热15min,取出迅速冷至室温,再摇匀,加水至标线25ml,摇匀。
静置15min后,在570nm波长下,以试剂空白为参比液夨订其余各溶液的吸光度A。
以氨基酸的微克数为横坐标,吸光度A为纵坐标,绘制标准曲线。
样品的测定:将虾研磨冷却过滤后稀释10倍,吸取澄清的样品溶液1.5ml,平行三次,按标准曲线制作步骤,在相同条件下测定吸光度A 值,用测得的A值在标准曲线上即可查得氨基酸的微克数。
公式:氨基酸总量(ug/100g)=(c/m*1000)*100*10式中c是指从标准曲线上查得的氨基酸的ug数;M是指测定的样品溶液相当于样品的质量g;PH计酸度计测量ph的方法:(1)拿下笔帽(2)按on/off键,机器显示运作(3)将ph计放入待测液中(4)轻轻晃动ph计,保证内气泡逸出,使之于溶液充分接触,勿碰撞杯壁(5)ph计会立即显示数值,将笔置入待测液待数值稳定,30秒内将显示正确数值,(特:ph计数值上下浮动或不稳定是正常现象)(6)按hold键锁定数值,可在待测溶液外记录读取,继续按hold键解除锁定(7)按on/off键关闭ph计(8)轻甩PH计测试笔上多于的水,用蒸馏水或脱离子水冲洗,盖上笔帽测量温度方法在测试模式下,温度数值与ph数值同步显示在液晶面板上,但在校准模式下不显示,数值默认为摄氏温度。
(一)挥发性盐基氮(TVB-N)的测定半微量定氮法(1)原理:蛋白质在酶和细菌的作用下分解后产生碱性含氮物质,有氨、伯胺、仲胺等,此类物质具有挥发性,可在碱性溶液中被蒸馏出来,用标准酸滴定,计算含量。
(2)试剂①氧化镁混悬液(10g/L) 称取1.0g氧化镁,加100ml水,振摇成混悬液。
氨基酸与氮的换算关系概述说明以及解释1. 引言1.1 概述氨基酸是构成蛋白质的基本组成单元,其中氮元素在氨基酸分子中占据重要地位。
在研究和应用过程中,需要将氨基酸含量转化为氮含量或将氮含量换算为相应的氨基酸含量。
因此,深入了解和探讨氨基酸与氮的换算关系具有重要意义。
1.2 文章结构本文将从以下几个方面对氨基酸与氮的换算关系进行概述说明。
首先,我们将简要介绍本文的目的和研究背景,然后详细介绍氨基酸的组成和功能以及其内部所含的氮元素。
随后,我们将重点探讨氨基酸与氮的换算关系,并强调其在研究和实际应用中的重要性。
在第三部分中,我们将介绍一些常用的换算公式和方法,并对不同类型氨基酸的换算因子进行分析。
同时,我们还会提及实际应用中需要注意的事项和常见误区。
接下来,在第四部分中,我们将结合实验数据来验证换算关系的准确性,并结合具体案例分析可能存在的偏差因素。
最后,在第五部分中,我们将总结研究成果并对未来发展方向进行展望和建议。
1.3 目的本文旨在全面了解和解释氨基酸与氮的换算关系,并提供实验验证和案例分析以支持所介绍的相关理论。
通过深入研究这一主题,我们可以更好地理解氨基酸及其与氮的相互关系,为相关领域的进一步研究和应用提供指导。
2. 氨基酸与氮的换算关系2.1 氨基酸的组成和功能氨基酸是生物体内构成蛋白质的基本组成单元,它由氢、碳、氧和氮元素组成。
在细胞中,氨基酸通过连接形成多肽链,并进一步折叠为特定的三维结构,从而实现不同功能的蛋白质合成。
不同种类的氨基酸具有各自特定的化学性质和生物学功能。
2.2 氨基酸中的氮元素在氨基酸分子中,每个氨基(–NH2)部分都含有一个或多个能够与其他化合物反应形成化学键的游离电子对。
这些游离电子对往往与其他原子共享电子,其中包括碳、氢、以及最重要的一项——氮。
作为蛋白质主要组成部分之一的氮元素,在维持人体正常代谢过程中发挥着重要角色。
2.3 探讨氨基酸与氮的换算关系及其重要性确定蛋白质含量和评估蛋白供给状况是许多科研领域的重要任务。
含氮量与蛋白质含量换算公式
含氮量与蛋白质含量有着密切的关系,因此在食品科学领域中经常需要进行相互转换。
下面介绍一下含氮量与蛋白质含量的换算公式: 1. 含氮量与蛋白质含量的关系
蛋白质是由氨基酸组成的大分子化合物。
因此,蛋白质含量与含有的氮元素数量之间具有明确的关系。
通常情况下,蛋白质含量可以通过含氮量进行计算。
2. 含氮量与蛋白质含量的换算公式
通常采用的换算公式是:蛋白质含量(%)=含氮量(%)× 6.25。
其中,6.25是蛋白质中平均每个氨基酸所含氮元素的数量。
该公式
适用于大部分蛋白质。
例如,一种食品中含有1%的氮元素,那么该食品中的蛋白质含
量为1% × 6.25 = 6.25%。
需要注意的是,该公式仅适用于未受到氧化或其他化学反应影响的蛋白质。
对于已经发生变化的蛋白质,这个公式将不再适用。
以上就是含氮量与蛋白质含量的换算公式。
在实际应用中,需要注意选择正确的方法进行分析,以确保分析结果的可靠性。
- 1 -。
生物氨基酸计算公式一、引言生物氨基酸是构成生物体内蛋白质的基本组成单位,其结构由氨基(NH2)基团、羧基(COOH)团和侧链组成。
在生物学研究中,计算生物氨基酸的含量和比例是十分重要的。
本文将介绍一种常用的生物氨基酸计算公式,并探讨其应用。
二、计算公式生物氨基酸的计算公式通常采用氨基酸残基的摩尔吸光系数和氨基酸溶液的吸光度来计算。
公式如下:C(氨基酸含量,单位:mol/L)= A(吸光度)/ ε(摩尔吸光系数) * d(溶液浓度)其中,吸光度(A)是指氨基酸溶液在特定波长下的吸光度值,摩尔吸光系数(ε)是指氨基酸在特定波长下的摩尔吸光系数,溶液浓度(d)是指氨基酸溶液的摩尔浓度。
三、实际应用生物氨基酸计算公式的应用范围十分广泛,下面将以两个具体的应用例子来说明。
1. 蛋白质含量测定蛋白质是由多个氨基酸残基组成的大分子,通过测定氨基酸溶液的吸光度可以间接测定蛋白质的含量。
首先,将待测样品与酸性溶液混合,使蛋白质水解成氨基酸。
然后,根据公式计算氨基酸的含量,从而得到蛋白质的含量。
2. 蛋白质组成分析蛋白质的组成可以通过氨基酸的含量和比例来分析。
通过测定不同氨基酸溶液的吸光度,可以计算出各个氨基酸的含量。
进一步,可以根据氨基酸的比例推断蛋白质的类型和结构。
四、注意事项在使用生物氨基酸计算公式时,需要注意以下几点:1. 选择适当的波长和摩尔吸光系数,以确保计算结果的准确性。
2. 确保溶液浓度的准确测量,避免浓度误差对计算结果的影响。
3. 对于含有多个氨基酸的样品,需要进行分离和纯化,以确保吸光度的准确测量。
4. 在进行实验前,需要校准仪器和标定吸光度的参考物质,以确保实验的准确性和可重复性。
五、结论生物氨基酸计算公式是一种常用的计算方法,可以用于测定蛋白质的含量和分析蛋白质的组成。
通过合理应用该公式,可以为生物学研究提供重要的数据支持。
在实际应用中,需要注意实验操作的准确性和仪器的校准,以确保结果的可靠性。
氨基酸计算公式氨基酸是构成蛋白质的基本单元,它们通过特定的化学结构和功能发挥着重要的生物学作用。
氨基酸的计算公式是指通过一系列化学计算来确定氨基酸的结构和特性。
计算公式的第一步是确定氨基酸的化学结构。
氨基酸由一个氨基(NH2)、一个羧基(COOH)、一个侧链和一个中心碳原子组成。
中心碳原子与氨基、羧基和侧链分别连接。
在计算氨基酸的结构时,需要考虑侧链的不同,因为氨基酸的侧链决定了其特性和功能。
侧链可以是疏水的、亲水的、带电的或具有特定功能的。
根据侧链的不同,氨基酸可以分为极性氨基酸和非极性氨基酸。
极性氨基酸的侧链在水中具有亲水性,可以与水分子形成氢键。
它们在蛋白质中起到调节蛋白质溶解度和稳定性的作用。
常见的极性氨基酸有丝氨酸、苏氨酸、谷氨酸和天冬氨酸等。
非极性氨基酸的侧链在水中具有疏水性,无法与水分子形成氢键。
它们在蛋白质中起到构建蛋白质结构和保持蛋白质稳定性的作用。
常见的非极性氨基酸有甘氨酸、丙氨酸、异亮氨酸和苯丙氨酸等。
通过计算公式,可以确定氨基酸的分子量和化学式。
氨基酸的分子量是指其分子中所有原子的质量之和。
氨基酸的化学式是指其分子中原子的种类和数量。
根据不同的氨基酸,其分子量和化学式也会有所不同。
通过计算公式还可以确定氨基酸的等电点和pH值。
氨基酸的等电点是指在该pH值下,氨基酸带有的正电荷和负电荷相互抵消,呈电中性的状态。
而氨基酸的pH值则是指溶液中氨基酸分子的质子化程度。
根据氨基酸的结构和侧链性质,可以通过计算公式来确定氨基酸的等电点和pH值。
在生物学研究和医学领域中,氨基酸的计算公式被广泛运用。
通过计算公式,可以预测蛋白质的结构和功能,设计新的药物分子,并研究氨基酸在人体中的代谢和生理过程。
此外,计算公式还可以用于鉴定和定量氨基酸的含量,以及检测蛋白质的降解和合成速率。
氨基酸计算公式是一种重要的化学工具,用于确定氨基酸的结构、特性和功能。
通过计算公式,可以深入理解氨基酸在生物体内的重要作用,为生物学和医学研究提供有力支持。
氨基酸的计算公式氨基酸是构成蛋白质的基本组成单位,它们在生物体内具有重要的生理功能。
氨基酸的计算公式可以用来确定氨基酸的分子式和分子量。
下面将介绍氨基酸的计算公式及其相关内容。
一、氨基酸的分子式氨基酸的分子式通常由三部分组成:氨基基团(NH2)、羧基基团(COOH)和侧链基团。
在不同的氨基酸中,侧链基团的结构不同,导致氨基酸具有不同的性质和功能。
二、氨基酸的分子量氨基酸的分子量是指一个氨基酸分子中所有原子的质量之和。
氨基酸的分子量可以通过化学计算公式来确定。
以脯氨酸为例,其分子式为C5H9NO3,可以根据元素的相对原子质量计算出分子量。
氨基酸的计算公式可以用来确定氨基酸的分子式和分子量。
例如,以甘氨酸为例,其分子式为C6H13NO2,可以根据元素的相对原子质量计算出分子量。
四、氨基酸的分类根据侧链基团的不同,氨基酸可以分为极性氨基酸和非极性氨基酸。
极性氨基酸具有极性侧链基团,能够与其他分子进行氢键和其他相互作用,例如谷氨酸和赖氨酸。
非极性氨基酸则没有极性侧链基团,不能与其他分子进行氢键和其他相互作用,例如丙氨酸和丝氨酸。
五、氨基酸的生理功能氨基酸在生物体内具有多种重要的生理功能。
首先,氨基酸是构成蛋白质的基本组成单位,参与蛋白质的合成和修复。
其次,氨基酸还参与能量代谢和物质转运,例如谷氨酸和丙氨酸参与三羧酸循环和尿素循环。
此外,氨基酸还参与生物体的免疫反应和信号传导等生理过程。
六、氨基酸的补充与保健人体无法自行合成某些氨基酸,需要从食物中获取。
因此,适量补充氨基酸对维持人体健康非常重要。
某些特定氨基酸,例如谷氨酸和精氨酸,还可以作为营养补充剂使用,具有一定的保健功能。
氨基酸的计算公式可以用来确定氨基酸的分子式和分子量。
氨基酸在生物体内具有重要的生理功能,适量补充氨基酸对维持人体健康非常重要。
希望通过本文的介绍,能够加深对氨基酸的认识和理解。
氨基酸大小计算摘要:1.氨基酸的定义和基本组成2.氨基酸大小计算的方法和意义3.不同方法计算氨基酸大小的比较4.氨基酸大小计算在生物学和化学领域的应用5.总结与展望正文:氨基酸是生物体内构成蛋白质的基本组成单位,是一类含有氨基(-NH2)和羧基(-COOH)的有机化合物。
在生物体内,氨基酸通过脱水缩合反应形成肽键(-CO-NH-),从而连接成多肽链,进一步折叠成蛋白质。
氨基酸大小计算在生物学和化学领域具有重要意义。
氨基酸大小计算的方法主要有两种:一种是根据氨基酸的分子量进行计算;另一种是根据氨基酸的氢原子数量进行计算。
其中,根据分子量计算的方法较为常用,其计算公式为:氨基酸大小(单位:Dalton)= 氨基酸分子量(单位:g/mol)× 1.8。
根据氢原子数量计算的方法较为简单,其计算公式为:氨基酸大小= 氨基酸分子中氢原子数量× 1.008。
虽然两种方法都可以计算氨基酸大小,但它们在实际应用中存在一定的误差。
例如,对于分子量较小的氨基酸,如甘氨酸(Gly),由于氢原子数量较少,根据氢原子数量计算的方法得到的氨基酸大小与实际值相差较大。
而对于分子量较大的氨基酸,如酪氨酸(Tyr)和组氨酸(His),两种方法的计算结果较为接近。
氨基酸大小计算在生物学和化学领域具有广泛的应用。
在生物学中,氨基酸大小对于蛋白质的折叠和功能具有重要影响。
通过计算氨基酸大小,可以推测蛋白质的折叠方式和功能。
此外,在化学领域,氨基酸大小计算对于药物设计和筛选具有重要意义。
通过比较药物分子与氨基酸的大小,可以推测药物与生物分子的相互作用,从而为药物设计提供依据。
总之,氨基酸大小计算在生物学和化学领域具有重要意义。
通过掌握不同计算方法的特点和适用范围,可以为我们研究生物大分子和药物设计提供有力支持。