第九章 化学动力学基本原理
- 格式:ppt
- 大小:2.18 MB
- 文档页数:76


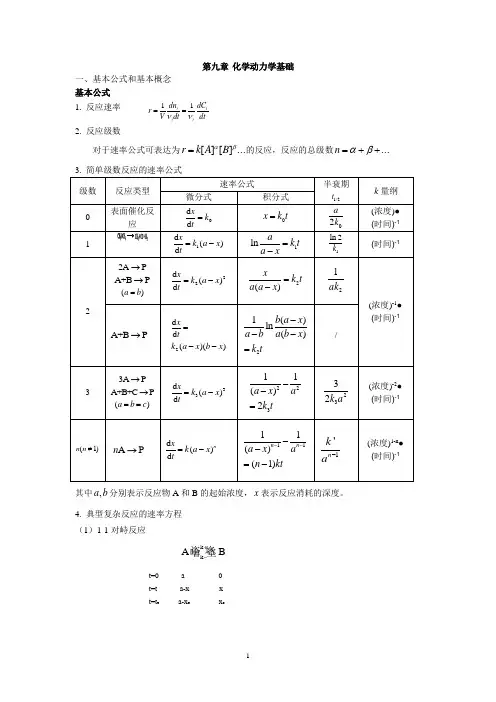
第九章 化学动力学基础一、基本公式和基本概念 基本公式 1. 反应速率 11i ii i dn dC r V dtdtνν==2. 反应级数对于速率公式可表达为...][][βαB A k r =的反应,反应的总级数...++=βαn 3. 简单级数反应的速率公式 级数 反应类型 速率公式半衰期 1/2tk 量纲微分式积分式0 表面催化反应0d d x k t =0x k t = 02a k (浓度)● (时间)-1 11d ()d x k a x t=-1lna k t a x=-1ln 2k(时间)-122A P→A +B P →()a b =22d ()d x k a x t=-2()x k t a a x =-21ak(浓度)-1●(时间)-1A +B P →2d d ()()xtk a x b x =--21()ln()b a x a b a b x k t---=/33A P→A +B +C P→()a b c ==33d ()d x k a x t=-22311()2a x a k t --=2332k a(浓度)-2● (时间)-1(1)n n ≠A P n →d ()d nx k a x t=-1111()(1)n n a x an kt----=-1'n k a-(浓度)1-n ● (时间)-1其中,a b 分别表示反应物A 和B 的起始浓度,x 表示反应消耗的深度。
4. 典型复杂反应的速率方程 (1)1-1对峙反应k k A B +-t=0 a 0 t=t a-x x t=t e a-x e x e速率方程: ()kk te e x x x e +--+-=(2)平行反应最简单的平行反应是由两个一级基元反应组成的平行反应:x=x 1+x 2速率方程:tk k aex a )(21+-=-产物B 和C 的浓度比由竞争反应的速率决定:2121k k x x = (3)连续反应最简单的连续反应是两个单向连续的一级反应:C B A kk −→−−→−21t=0 a 0 0 t=t x y z 速率方程:1k tx ae-=)(21121tk tk eek k a k y ----=]1[21121122tk tk ek k k ek k k a z ---+--=中间产物B 的浓度在反应过程中出现极大值:122)(21k k k m k k a y -=,出现极大值的时间为:2121)ln(k k k k tm-=5. 温度对反应速率的影响 (1)阿累尼乌斯经验公式2ln RTE dTk d a =阿累尼乌斯公式的指数函数式: RTE a Aek -=k 1k 2A a-xCx 2 B x 1(2)阿累尼乌斯活化能基元反应的活化能是活化分子的平均能量与所有分子平均能量之差。


第九章化学动力学基本原理一、填空题1、设物质A 可发生两个平行的一级反应:(a )C B A Ea ka +−−→−,(b )E D A Ebkb +−−→−, 式中,B 和C 是需要的产品,D 和E 为副产物。
设两反应的频率因子相等且与温度无关,E a >E b ,则反应(a)和反应(b)相比,速率较大的反应是 ,升高温度对 更有利。
2、硝酸异丙烷在水溶液中被碱中和,其反应速率常数可表示为lgk=11.899-3163/T ,该反应的表观活化能为 。
3、今将某物质A 放入一反应器内,反应了3600s ,消耗掉75%,设反应分别为一级,二级,零级反应。
则反应进行了7200s 时,对于各级反应,A 物质的剩余量分别为 、 和 。
4、某化合物的分解反应是一级反应,设反应的活化能E=14.43×104J ·mol -1,已知557K 时该反应的速率常数k=3.3×10-2s -1,现要控制反应在10min 内转化率达到90%,则应控制该反应的温度为 。
5、比较两相同类型的反应I 和II ,发现活化能E I >E II ,速率常数k I >k II ,其原因在于 。
6、在T ,V 恒定时,反应A(g)+B(g)→D(g)t=0时,P A,0=800kPa ,t 1=30s 时,P A,1=400kPa ,t 2=60s 时P A,2=200kPa ,t 3=90s 时,P A,3=100kPa 时此反应的半衰期t 1/2= ,反应级数n= ,反应的速率常数k= 。
.7、阿累尼乌斯活化能是 。
.8、气相有效分子碰撞理论的基本观点是 。
.9、根据活化络合物理论,液相分子重排反应的活化能E a 和活化焓△r H m 之间的关系是 。
.10、由经验规则“温度每增加10K ,反应速率增加二倍”可知,在T 1=298K 时和T 2=308K 时符合这规律的活化能值E a = 。




第九章 化学动力学基本原理一、填空题1、设物质A 可发生两个平行的一级反应:(a )C B A Ea ka +−−→−, (b )E D A Ebkb +−−→−, 式中,B 和C 是需要的产品,D 和E 为副产物。
设两反应的频率因子相等且与温度无关,E a >E b ,则反应(a)和反应(b)相比,速率较大的反应是 ,升高温度对 更有利。
2、硝酸异丙烷在水溶液中被碱中和,其反应速率常数可表示为lgk=11.899-3163/T ,该反应的表观活化能为 。
3、今将某物质A 放入一反应器内,反应了3600s ,消耗掉75%,设反应分别为一级,二级,零级反应。
则反应进行了7200s 时,对于各级反应,A 物质的剩余量分别为 、 和 。
4、某化合物的分解反应是一级反应,设反应的活化能E=14.43×104J ·mol -1,已知557K 时该反应的速率常数k=3.3×10-2s -1,现要控制反应在10min 内转化率达到90%,则应控制该反应的温度为 。
5、比较两相同类型的反应I 和II ,发现活化能E I >E II ,速率常数k I >k II ,其原因在于 。
6、在T ,V 恒定时,反应A(g)+B(g)→D(g) t=0时,P A,0=800kPa ,t 1=30s 时,P A,1=400kPa ,t 2=60s 时P A,2=200kPa ,t 3=90s 时,P A,3=100kPa 时此反应的半衰期t 1/2= ,反应级数n= ,反应的速率常数k= 。
.7、阿累尼乌斯活化能是 。
.8、气相有效分子碰撞理论的基本观点是 。
.9、根据活化络合物理论,液相分子重排反应的活化能E a 和活化焓△r H m 之间的关系是 。
.10、由经验规则“温度每增加10K ,反应速率增加二倍”可知,在T 1=298K 时和T 2=308K 时符合这规律的活化能值E a = 。

第九章化学动力学基本原理第九章化学动力学基本原理§9.3简单级数反应的动力学规律凡是反应速率只与反应物浓度有关,而且反应级数,无论是?、?、…或n都只是零或正整数的反应,泛称为“直观级数反应”。
简单反应都是简单级数反应,但简单级数反应不一定就是简单反应,前已述及的hi气相合成反应就是一例。
具有相同级数的简单级数反应的速率遵循某些简单规律,本节将分析这类反应速率公式的微分形式、积分形式及其特征。
(1)一级反应反应速率与反应物浓度的一次方成正比的反应称为一级反应。
其速率公式可表示为dc??k1cdt(9.7)dc式中c为t时刻的反应物浓度。
将上式改写成??k1dt的形式,积分可得clnc??k1t?b(9.8)b为分数常数,其值可以由t=0时反应物初始浓度c0确认:b=lnc0。
故一级反应速率公式分数形式可以则表示为cln0?k1tc(9.9)c1k1?ln0tc(9.10)或k1tcce0或(9.11)采用这些公式纡算是速率常数k1的数值,只要晓得了k1和c0的值,即可求算任意t时刻反应物的浓度。
从(9.8)式可看出,以lnc对t作图应得一直线,其斜率即为?k1。
如图9.2所示。
反应物浓度由c0消耗至c=c0/2所需的反应时间,称作反应的半衰期,以t1/2则表示。
由(9.9)式所述,一级反应的t1/2表示式为图9.2一级反应的lnc对t图10.6932t1/2?ln2?k1k1(9.12)可以窥见,一级反应的半衰期与反应物初始浓度c0毫无关系。
许多分子的重排反应和热分解反应属一级反应。
还有些反应例如蔗糖水解c12h22o11?h2o?c6h12o6(葡萄糖)?c6h12o6(果糖)实际上就是二级反应,但由于水溶液中反应物之一h2o大大过量,其浓度在整个反应过程中可以视作常数,故表观上整体表现为一级反应,这类反应称作“科东俄一级反应”。
例题130℃时n2o5在ccl4中的水解反应n2o5n2o4+2o212no2为一级反应,由于n2o4和no2均溶ccl4中,只有o2能够逸出,用量气管测量相同时刻逸出o2的体积存有以下数据:t/sv(o2)/cm300240015.65480027.65720037.70960045.851200052.671440058.301680063. 001920066.85?84.85戊日和此反应的速率常数k1和半衰期t1/2。

第九章化学动力学基本原理化学动力学是研究化学反应速度和反应机理的学科。
了解反应速率和反应机理对于理解和控制化学反应过程至关重要。
本章将介绍化学动力学基本原理,包括反应速率的定义和测定、速率定律方程、反应级数和速率常数等概念。
1.反应速率反应速率指的是单位时间内反应物消失或生成物产生的物质量。
以一般的反应方程式表示为:aA+bB→cC+dD反应速率可以用消失反应物或生成物的物质量的减少或增加来表示。
根据反应物或生成物浓度随时间的变化关系,可以得到反应速率的数学表示。
2.速率定律方程速率定律方程描述了反应物浓度与反应速率之间的关系。
一般的速率定律方程可以表示为:v=k[A]^m[B]^n其中,v为反应速率,k为速率常数,[A]和[B]为反应物的浓度,m 和n分别为反应物A和B的反应级数。
3.反应级数反应级数指的是反应物在速率定律方程中的指数。
根据反应级数的不同,反应可以分为一级反应、二级反应和零级反应。
-一级反应:速率与一个反应物的浓度的一次幂成正比,二级反应:速率与一个反应物的浓度的二次幂成正比-零级反应:速率与一个反应物的浓度无关4.速率常数速率常数是衡量反应速率快慢的物理量,其数值与反应机理、反应温度等因素有关。
速率常数的大小与活化能有关,活化能越低,速率常数越大,反应速率越快。
5.反应速率的测定测定反应速率的方法有多种,包括观察物质变化、测量反应物浓度的变化、测量生成物浓度的变化等。
6.反应速率与温度的关系根据阿伦尼乌斯方程,反应速率与温度之间存在正比关系。
提高温度可以提高反应活性,增加反应速率。
并且,根据阿伦尼乌斯方程,温度每升高10摄氏度,反应速率大约增加一倍。
总结:化学动力学是研究化学反应速率和反应机理的学科。
了解反应速率和反应机理对于理解和控制化学反应过程至关重要。
本章介绍了化学动力学基本原理,包括反应速率的定义和测定、速率定律方程、反应级数和速率常数等概念。
另外,还介绍了反应速率与温度的关系,即温度越高,反应速率越快。
第九章 化学动力学基本原理质量作用定律r = k[A]a [B]b ;质量作用定律只适用于基元反应。
(简单反应和复合反应中的各基元反应)简单反应都是简单级数反应,但是简单级数反应不一定是简单反应一级反应:xx a a c c t k -=-==11lnln ln01;c c k t 01ln 1= 1)k1单位:s-12)半衰期t1/2:当c=1/2c0时所需时间110012/16932.02ln 2/ln 1k k c c k t ===;t ½ 与起始浓度c0无关。
阿累尼乌斯公式⎪⎪⎭⎫ ⎝⎛-=⎪⎪⎭⎫ ⎝⎛-=1212211211)()(ln T T T T R E T T R E T k T k a a ; 26.20/106.12ln ln 3+⨯-=+-=KT A RT E k aEa =12.6 ×10^3×R=104.8kJ · mol-1 lnA=20.26A = e^20.26 = 6.29 ×10^8 mol-1·dm3·s-1第八章 表面现象与分散系统 表面张力σ 单位:N/m物理意义:表面紧缩力定义:在相表面的切面上,垂直作用于表面任意单位长度上的紧缩力。
影响表面张力的因素:1. 物质的种类及共存相的种类(性质);2. 温度影响:前者<0,即温度升高,表面张力变小拉普拉斯公式:rp σ2=∆ r :曲率半径。
r 越大,Δp 越小;平面时r 趋近于无穷大,Δp=01.不管是凸液面,还是凹液面,附加压力的方向总是指向球心,即球内的压力一定大于球外的压力;2. 液膜(肥皂泡)Δp=4σ/rKelvin 公式:(液相) P'=P+2σ/r ;(气相) pr 凹(液中气泡):r 取负值,pr < p ;凸(小液滴):r 取正值,pr > p人工降雨(过饱和蒸气)高空中没有灰尘,水蒸汽可达到相当高的过饱和程度而不致凝结成水。
第九章 《化学动力学基本原理》第十章 《复合反应动力学》一、选择题1.在TK时,对于某一简单级数反应的半衰期与反应物起始浓度的关系,正确的是( )。
A. 对一级反应为反比;B. 对二级反应为正比;C. 对零级反应为正比;D. 无明确关系。
2.某反应的反应物消耗3/4所需时间是消耗1/2所需时间的二倍,则反应级数为( )。
A. 零级;B. 一级;C. 二级;D. 三级。
3.基元反应的反应级数( )反应分子数。
A. 总大于;B. 总小于;C. 总等于;D. 等于或小于。
4.某放射性同位素的半衰期为5天,则经15天后所剩的同位素的物质的量是原来同位素的物质的量的( )。
A. 1/3;B. 1/4;C. 1/8;D. 1/16。
5.某反应的速率常数k = 2×10-2 dm3· mol-1 · s-1,当反应物初始浓度为1.0 mol · dm-3时,反应的半衰期为( )。
A. 50 s ;B. 15 s ;C. 30 s ;D. 21.65 s 。
6.反应速率常数随温度变化的阿仑尼乌斯经验式适用于( )。
A. 基元反应; B. 基元反应和大部分非基元反应;C. 非基元反应;D. 所有化学反应。
7.反应物A进行由两个一级反应组成的平行反应: 步骤⑴的速率常数为k1,步骤⑵的速率常数为k2。
已知k1> k2,若两步骤的指前因子相近且与温度无关, 则( )。
A. 升温对⑴和⑵的影响相同;B. 升温对⑴有利;C. 升温对⑵有利;D. 降温对⑵有利。
8.某物质A与水反应,在水溶液中,若A起始浓度为1mol/kg,1h后,浓度为0.5 mol/kg,2h后, 浓度为0.25mol/kg, 则对A来说,此反应的级数为( )。
A. 零级;B. 一级;C. 二级;D. 三级。
9.在Tk时,某一反应的速率常数为0.0693min-1,反应物起始浓度0.1mol/L, 则半衰期为()。