分析化学6 配位滴定法2学时
- 格式:ppt
- 大小:1.18 MB
- 文档页数:12
![分析化学第六章--配位滴定法[精编文档]](https://uimg.taocdn.com/34d081a4ba0d4a7302763a96.webp)




《分析化学》课程标准课程名称:分析化学课时安排:136教时课程性质和任务:分析化学是化学学科的一个重要分支,它是一门研究物质化学分析方法及有关理论重要课程,担负着鉴定物质组成成分、测定其相对含量的两个任务。
一.设计思路及目标:以掌握分析基本类型及操作为目标,以分析操作过程的学习为主线。
1.掌握化学分析的基本原理和基础知识。
2.准确树立“量”的概念。
3.学会对各种物质的测定方法。
4.正确掌握化学分析实验的基本操作,养成良好的实验习惯。
5.培养严谨求实的科学态度和观察判断问题的能力,提高分析问题、解决问题的能力,为学习后续课程和以后从事专业技术工作打下良好的基础。
二.课程内容及要求:序号工作任务模块课程内容教学要求理论参考课时实验参考课时1 绪论1.分析化学的任务和作用2.分析化学的分类3.分析化学的进展概况4.分析化学课程要求和学习方法简介1.了解分析化学的对象、任务及它所包括的重要分支,明确其重要性。
2.了解分析化学的分类、联系和区别3.对分析化学的发展趋势有概括性的了解理论:2教时2 定量分析概述1.误差及其表示方法2.误差产生的原因及其分类3.减少误差提高分析结果准确度的方法4.分析数据的处理1.了解误差的概念、误差来源及消除方法2.运用误差理论对分析结果进行处理3.明确有效数字的定义及运算规则理论:6教时实验:4教时1.天平的使用2教时2.移液管、5.有效数字及其运算规则4.掌握天平的使用滴定管校正。
2学时3 滴定分析概述1.滴定分析的过程2.滴定分析方法的分类3.标准溶液的配制及标定4.标准溶液浓度的表示方法5.滴定分析计算1.了解滴定分析法的过程、分类2.掌握标准溶液的配制和浓度标定的各种方法及有关计算3.掌握滴定分析结果的计算方法理论:8教时实验:6学时标淮溶液的配制1.直接法22.间接法23.标定24 水溶液中的酸碱平衡1.温度和湿度系数的概念2.酸碱质子理论3.酸碱平衡有关浓度的计算4.缓冲溶液1.理解酸碱质子理论的概念2.掌握酸碱平衡体系中PH值的计算方法3.通过实验掌握缓冲溶液的作用原理、配制方法及其应用理论:8教时实验:6学时1.缓冲液配制。



第五章配位滴定法1.基本概念稳定常数:为一定温度时金属离子与EDTA配合物的形成常数,以KMY表示,此值越大,配合物越稳定。
逐级稳定常数和累积稳定常数:逐级稳定常数是指金属离子与其它配位剂L逐级形成MLn型配位化合物的各级形成常数。
将逐级稳定常数相乘,得到累积稳定常数。
副反应系数:表示各种型体的总浓度与能参加主反应的平衡浓度之比。
它是分布系数的倒数。
配位剂的副反应系数主要表现为酸效应系数αY(H)和共存离子效应αY(N)系数。
金属离子的副反应系数以αM表示,主要是溶液中除EDTA外的其他配位剂和羟基的影响。
金属指示剂:一种能与金属离子生成有色配合物的有机染料显色剂,来指示滴定过程中金属离子浓度的变化。
金属指示剂必须具备的条件:金属指示剂与金属离子生成的配合物颜色应与指示剂本身的颜色有明显区别。
金属指示剂与金属配合物(MIn)的稳定性应比金属-EDTA配合物(MY)的稳定性低。
一般要求K MY'>K MIn'>102。
最高酸度:在配位滴定的条件下,溶液酸度的最高限度。
最低酸度:金属离子发生水解的酸度。
封闭现象:某些金属离子与指示剂生成极稳定的配合物,过量的EDTA不能将其从MIn中夺取出来,以致于在计量点附近指示剂也不变色或变色不敏锐的现象。
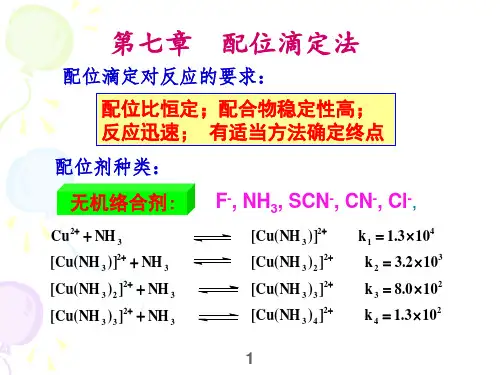
2.基本原理(1)配位滴定法:EDTA与大多数金属离子能形成稳定配位化合物,此类配合物不仅稳定性高,且反应速度快,一般情况下,其配位比为1:1,配合物多为无色。
所以目前常用的配位滴定法就是EDTA滴定,常被用于金属离子的定量分析。
(2)准确滴定的条件:在配位滴定中,若化学计量点和指示剂的变色点ΔpM'=±0.2,将lgC×K MY'≥6 或C×K MY'≥106作为能进行准确滴定的条件,此时的终点误差在0.1%左右。
(3)酸度的控制:在配位滴定中,由于酸度对金属离子、EDTA和指示剂都可能产生影响,所以必须控制溶液的酸度,需要考虑的有:满足条件稳定常数38时的最高酸度;金属离子水解最低酸度;指示剂所处的最佳酸度等。

《化学分析技术》课程标准课程代码: B0302216, B0302319 课程类别:专业技术课授课系(部):药品与环境工程学院学分学时:8.5 142.5一、课程定位与作用1.课程的定位:本课程是工业分析技术专业的专业基础课程,是学习化学检验必备专业基础知识和技能的一门课程。
2.课程的作用:化学分析技术课程重点培养学生掌握化学分析法的误差来源和消除方法,分析数据记录、处理与评价;掌握酸碱滴定、配位滴定、氧化还原滴定、沉淀滴定、称量分析定量分析方法的基础知识、基本理论、基本计算和基本操作技能。
通过化学分析的学习,能针对不同的化学分析方法要求进行样品预处理,能根据具体方法正确地对样品进行分析检验和分析处理测定数据,准确表述和评价分析结果,能正确地分析和解决化学分析过程中出现的问题,具备选择和拟定常用化学分析方法的能力。
从而达到培养学生对组成简单的试样进行化学分析的岗位操作技能的目的。
使学生开始树立“量”的概念,培养学生规范操作、记录和处理数据、完成检验报告,正确评价分析结果的能力,以及严谨认真、实事求是的职业素质。
3.与其他课程的关系:本课程是在学习了无机化学、有机化学后,为后续专业核心课程工业分析技术、药物分析技术、食品分析与检测技术、环境监测技术打下牢固的技能基础和理论基础的一门专业基础课。
二、课程目标1.知识目标(1)掌握化学分析过程中产生的误差原因及消除方法;(2)掌握有效数字进行数据记录、处理和评价实验结果的方法;(3)掌握各种典型化学分析方法的基本原理、特点和使用注意事项;(4)正确理解相关分析检验标准并制定适合的实验方案;(5)掌握选择合适的分析方法的原则;(6)掌握解决化学分析过程中出现各种问题的方法和知识。
2.能力目标(1)独立学习、获取新知识技能的能力;(2)独立寻找解决问题途径的能力;(3)能正确、规范、熟练使用化学分析中所使用的各种仪器的能力;(4)能根据分析任务制定相应的实施方案的能力;(5)能正确配制化学分析中所用的各种标准溶液和辅助试剂的能力;(6)能选择合理的方法消除化学分析过程中产生的干扰的能力;(7)能独立完成对简单试样的化学分析并给出报告的能力;(8)能撰写报告和解释所得结果和信息的能力。
《无机及分析化学》课程标准课程代码:B0301301 课程类别:专业基础课授课系(部):制药与环境工程系学分学时: 6学时/周一、课程定位与作用1.课程的定位:《无机及分析化学》是研究物质的组成、结构、性质、应用、组分分析方法和实验技术的一门应用学科,是药品生产技术专业的一门重要专业基础课。
本课程包括理论课和实践课两大教学内容,教学内容是根据专业特点选定的。
理论课以化学基础理论知识和分析方法的应用为主线进行课程设计,主要包括溶液及其浓度的表示、电解质溶液和沉淀—溶解平衡、原子结构、共价键和分子间作用力、化学反应速度和化学平衡、氧化还原反应和电极电势、误差和分析数据处理、滴定分析法概论、酸碱滴定法、沉淀滴定法和重量分析法、配位滴定法、氧化还原滴定法等。
实践课以化学基本操作技术、滴定分析操作技术为主线进行课程设计,根据专业需要开设实验,所开实验包括化学基本操作、溶液的配制和标定、物质含量测定等。
2.课程的作用:通过本课程的教学,要求学生掌握与专业相关的化学基础理论知识和基本操作技术、从事分析检验工作必需的基本知识和操作技能,确立正确的“量”的理念,提高学生分析和解决问题的能力,培养实事求是的科学态度和认真细致的工作作风,为学习后续课程或实际工作打下良好的基础,为今后到各类相关企业工作或从事产品质量检验和控制工作打下良好的基础。
3.与其他课程的关系:本课程是一门承上启下的课程,承接中学化学,为后续的《药用基础化学》、《仪器分析》、《药物化学》等课程打下基础。
二、课程目标本课程以培养学生掌握化学理论基础知识和基本操作技术,掌握从事分析检验工作必需的基本知识和操作技能,确立正确的“量”的理念,具有较强的分析解决问题的能力和实事求是的科学态度为教学目标。
1.知识目标(1)掌握气体溶液、物质结构、化学平衡的基本理论知识(2)掌握分析化学中误差及数据处理;(3)掌握酸碱滴定法、配位滴定法、氧化还原滴定法、配位滴定法的基本原理和操作技能。