结构化学 第六章-1..
- 格式:ppt
- 大小:1.65 MB
- 文档页数:25




第六章配位化合物的结构和性质教学目的:通过学习,使学生对配位化合物的三大化学键理论(价键理论、晶体场理论、分子轨道理论)有所了解,并能够运用合适的理论对常见配合物的结构和性质进行理论分析和解释。
教学重点:1.晶体场理论;2.姜-泰勒效应;3.分子轨道理论。
引言:配位化合物简称配合物,又叫络合物,是一类含有中心金属原子(离子)(M)和若干配体(L) 的化合物(MLn)。
中心原子通常是过渡金属元素的原子或离子,具有空的价轨道;而配体则有一对或多对孤对电子。
在广泛的化学实践和量子化学巨大发展的基础上,提出了各种解释中心原子和配体之间化学键本质的理论,主要有价键理论、晶体场理论和分子轨道理论第一节价键理论1928年Pauling把杂化轨道理论应用到配合物中,提出了配合物的价键理论。
一、理论要点:配体的配位原子提供孤对电子进入中心原子(或离子)的空的杂化轨道形成配位键;配位键可分为电价配键和共价配键两种,相应的配合物叫做电价配合物和共价配合物。
二、杂化轨道与空间构型三、电价配键和共价配键1、电价配合物中心离子的电子层结构和自由离子的一样,它与配体是以静电作用力结合在一起,常采用spd外轨道杂化,形成高自旋配合物。
电价配合物特点:配体往往电负性大,不易给出孤电子对,中心离子的结构不发生变化。
配合物中配位键共价性较弱,离子性较强;键能小,不稳定,在水中易分解简单粒子;2、共价配合物中心离子腾出内层能量较低的空d轨道,进行dsp内轨道杂化,接受配体的孤对电子,形成低自旋共价配合物。
共价配合物特点:配体往往电负性较小,较易给出孤电子对,对中心离子的影响较大,使其结构发生变化。
配合物中配位键共价性较强,离子性较弱;由于(n-1)d轨道比nd轨道能量低,所以一般共价配合物比电价配合物稳定,在水溶液中不易解离为简单离子。
3.实验测定:通过测定络合物的磁化率,可判断中央离子与配体间化学键性质kTN x A 32μμ=, )()(反顺O M x x x +=μ磁矩cn ehn n e B B πμμμ4,)2(=+=(玻尔磁子) n 未成对电子数有摩尔磁化率X m 可计算络合物的磁矩μ,由μ可估算出n(未成对电子数),从而可判断此络合物是电价配键,或共价配键。

第六章配位化合物的结构和性质
一.基本概念:
1.配合物、中心原子、配体、单核配合物、多核配合物
2.电价配合物、共价配合物、高自旋配合物和低自旋配合物
3.分子磁矩与未成对电子数的关系
4.晶体场、分裂能、成对能、光谱化学序、强场、弱场、晶体场稳定化能5.姜太勒效应和络合物畸变
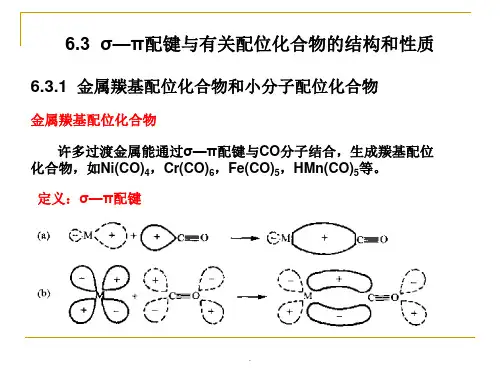
6. M中σ型轨道和π型轨道
7. M-L之间的σ键及能级次序
8.羰基配合物中的σ-π键
9.π络合物中的σ-π键
10.电子规则和9n-l规则
二.基本计算和应用:
1.VBT与CFT理论对配合物的结构与性质的解释
2.d电子的排布、影响分裂能的因素
3.稳定化能的计算及应用
4.姜太勒效应
5.过渡金属络合物的颜色
6.络合物的几何构型
7.用分子轨道理论说明配合物的成键情况
8.σ-π型配键
三.重点内容
1.晶体场理论,d电子的排布、影响分裂能的因素,稳定化能的计算及应用2.配位场理论,八面体场的分裂,配位场稳定化能及对化合物性质的影响3.姜太勒效应
4.σ-π型配键及配位化合物的结构
四.自学引导
1.由静电作用模型引出晶体场理论,通过d电子轨道分裂引出分裂能、稳定化能及对配合物的结构与性质的解释
2.由分子轨道理论引出配位场理论,通过八面体场的分裂引出配位场稳定化能、姜太勒效应及对化合物性质的解释
3.通过σ-π型配键引出对过渡金属的配位化合物的结构、性质的解释。
五.作业
6.3,6.4,6.5,6.7,6.12,6.14,6.15,6.20, 6.23。

《结构化学》第六章习题答案6001分裂成两组, d22yx 和2zd处于高能级,d xy,d yz,d xz处于低能级。
6002X-为弱场配体,CN-为强场配体, NH3介于两者之间。
6003(A)6004否6005(C)6006-2△06007此结论仅在O h场中,中心离子 d 电子数n=4--7 时才成立。
6008-0.4△0×6 =-2.4△06009假设填T d空隙LFSE(Td)=[4×(-0.267△)+4×0.178△] = -0.356△假设填O h空隙LFSE(Oh)=[6×(-0.4△)+2×0.6△] = -1.2△Ni2+倾向填入稳定化能大的空隙中,所以NiAl2O4为反尖晶石。
6010小 6011参看《结构化学基础》 (周公度编著) p.2756012(1) t 2g 4 e g 2(2) - 0.4△ (3) │M s │=6π2h(4) μ= 26μβ6013(D) 6014能级次序: d 22y x -最高, 2d z 次之,d xy 再次之,d yz ,d xz 最低。
理由:①因z 方向拉长,相应xy 平面上的 4 个L 靠近,所以d 22y x -能级升高,d z2能级下降; ②因为 d xy 在xy 平面内,受L 的影响大,所以d xy 能级上升,而d yz , d xz 受xy 平面上的 4 个L 排斥小,所以能级下降。
③但因z 方向上方还有 1 个L,加之2z d 的"小环"在xy 平面上,可受到L 的直接作用,所以2d z 能级高于 d xy 能级。
6015O h 点群,说明Jahn-Teller 效应为 0,按强场排:( t 2g )6(e g )0LFSE =-2.4△06016(B), (D)6017否6018(B)6019(1) [Fe(CN)6]3-: μ= [n(n+2)]1/2μβ; n1= 1[FeF6]3-: n2= 5(2) 中心离子Fe3+为d5结构,配位场为八面体场。



《结构化学》第六章习题6001 试述正八面体场中,中心离子 d 轨道的分裂方式。
6002 试用分子轨道理论阐明 X -,NH 3 和 CN -的配体场强弱的次序。
6003 按配位场理论,在 O h 场中没有高低自旋络合物之分的组态是:---------------- ( )(A) d 3 (B) d 4 (C) d 5 (D) d 6 (E) d 76004 凡是中心离子电子组态为d 6的八面体络合物,其 LFSE 都是相等的,这一说法是否正确?6005 络合物的中心离子的 d 轨道在正方形场中,将分裂成几个能级:---------------- ( )(A) 2 (B) 3 (C) 4 (D) 56006 Fe(CN)63-的 LFSE=________________。
6007 凡是在弱场配位体作用下,中心离子 d 电子一定取高自旋态;凡是在强场配位体作用下,中心离子 d 电子一定取低自旋态。
这一结论是否正确?6008 Fe(CN)64-中,CN -是强场配位体,Fe 2+的电子排布为6g 2t ,故 LFSE 为_____________。
6009 尖晶石的一般表示式为 AB 2O 4, 其中氧离子为密堆积,当金属离子A 占据正四面体T d 空隙时,称为正常尖晶石,而当A 占据O h 空隙时,称为反尖晶石, 试从晶体场稳定化能计算说明 NiAl 2O 4 晶体是什么型尖晶石结构( Ni 2+为d 8结构)。
6010 在 Fe(CN)64-中的 Fe 2+离子半径比 Fe(H 2O)62+中的 Fe 2+离子半径大还是小?为什么?6011 作图证明 CO 是个强配位体。
6012 CoF 63-的成对能为 21000 cm -1,分裂能为 13000 cm -1,试写出:(1) d 电子排布 (2) LFSE 值 (3) 电子自旋角动量 (4) 磁矩6013 已知 ML 6络合物中(M 3+为d 6),f =1,g = 20000 cm -1,P = 25000 cm -1,它的LFSE 绝对值等于多少?------------------------------------ ( )(A) 0 (B) 25000 cm -1 (C) 54000 cm -1 (D) 8000 cm -16014 四角方锥可认为是正八面体从z 方向拉长,且下端没有配体 L 的情况。