AYL-S7-352 药物敏感性试验标准操作规程
- 格式:doc
- 大小:68.00 KB
- 文档页数:3
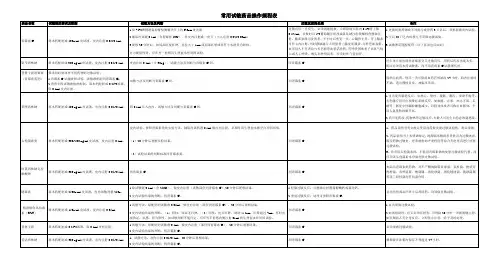
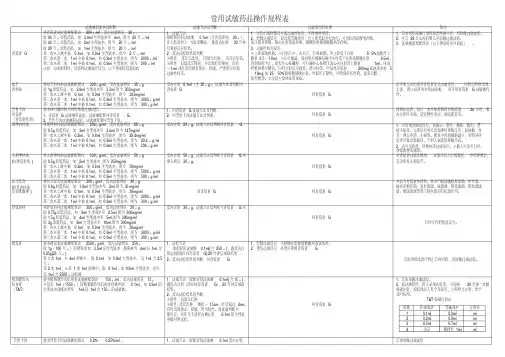

微生物检验实验室药物敏感性试验标准操作规程1.目的规范药物敏感性试验标准操作规程,确保药敏结果准确。
2.原理将含有定量抗菌药物的纸片贴在已接种待检菌的琼脂平板上,纸片中所含的药物吸取琼脂中的水分溶解后会不断的向纸片周围区域扩散,形成递减的浓度梯度,在纸片周围抑菌浓度范围内待检菌的生长被抑制,从而产生透明的抑菌圈。
抑菌圈的大小反映检测菌对测定药物的敏感程度,并与该待检菌的最低抑菌浓度(MIC)呈负相关,即抑菌圈愈大,MIC愈小。
3.试剂M-H培养基、无菌生理盐水、药敏纸片、无菌棉签、35℃孵育箱、标准比浊管或比浊仪。
4.质控4.1 常用细菌药敏质控标准菌株参见CLSI规定。
4.2 质控菌株每日随临床标本一起进行药敏试验,测定质控菌株的抑菌环。
质控菌株的抑菌环在允许范围之内,说明结果可信。
4.3 质控的频率由于纸片法药敏试验是很稳定的,在不失控的时候,可以每周作1~2次质控菌株的测定。
如果发现有失控的情况,就必须每日做1次,寻找失控的原因并予以纠正。
如果连续30日失控<3次的,可以恢复每周1次。
5.操作步骤5.1 挑取4~5个纯培养菌落,接种于3~5ml M-H肉汤(0.5麦氏单位)中,经35℃培养6~8h。
5.2 用无菌生理盐水或M-H肉汤校正菌液浊度,使其与标准比浊管的浓度相同。
5.3 用无菌棉拭蘸取校正过的菌液,在试管壁上挤压几次,压去多余的菌液,涂布整个M-H平板表面,再重复两次,每次旋转平板60°,使整个平板涂布均匀,最后用棉拭涂布平板四周缘一圈。
5.4 涂布菌液的平板于室温中干燥3~5分钟后,用纸片分配器或无菌镊子取药敏纸片,贴于平板表面,并用镊尖轻压一下纸片,使其贴平。
每张纸片的间距不小于24mm,纸片的中心距平板的边缘不小于15mm,直径90mm的平板宜贴6张药敏纸片。
5.5 将贴好纸片的平板置35℃孵育18~24小时后,用卡尺量取抑菌圈直径。
个别菌孵育温度,时间及条件应按照CLSI规定。

基础护理操作规程-药物试验法(一)青霉素过敏试验1.目的鉴别青霉素过敏者。
2.方法皮内注射青霉素皮试液0.1ml,使局部成皮丘。
注射后20分钟观察反应结果。
3.结果判断①阴性:皮丘局部无红肿,无自觉症状,可以用药。
②阳性:皮丘局部隆起,并出现红晕、硬块,直径大于1cm或红晕周围有伪足,痒感,严重时全身出现皮疹或过敏性休克反应。
阳性者表示对该药过敏,不可使用。
③假阳性:由于稀释液的刺激,也可出现假阳性反应,皮丘不大,红晕直径小于1cm,应在另一侧前臂做生理盐水对照试验。
④迟缓反应:有些病人过敏试验虽阴性,但在注射药物数小时或数日后,出现发热、皮疹,出现过敏性休克,应立即停药及处理。
4.注意事项①做皮肤过敏试验前,应详细询问用药过敏史及家族史,有过敏者严禁做过敏试验。
②凡首次使用青霉素或停药3天以上或用药中途更改批号者,应需重新做皮试。
阴性者可用药。
③长效青霉素在每次注射前均应做皮试。
④注入皮内试验药液应正确,针头不宜过深,以免刺入皮下引起出血。
拔针后勿按压局部,以免影响效果。
⑤试验药液现用现配。
⑥认真判断反应结果,严格掌握时间。
⑦为了判断是否假阳性,应同时在另一侧前臂以生理盐水做对照试验。
⑧观察结果应记录在医嘱单上。
阴性注“(-)”,阳性注“(+)”。
禁用青霉素者同时在护理记录单、病历上做醒目标记,并告诉病人及家属。
⑨应备好抢救药品及物品,如肾上腺素、地塞米松等,以备发生过敏性休克抢救时应用。
注射后应观察半小时。
(二)链霉素过敏试验1.目的鉴别对链霉素过敏者。
2.方法皮内注射链霉素皮试液0.1ml,20分钟后观察结果。
3.结果判断同青霉素过敏试验。
4.注意事项①使用链霉素前详细询问过敏史,有过敏史者严禁做过敏试验;②注入皮内药液应正确,针头不宜过深,以免影响观察效果;③认真判断结果,做记录,有标记;④如出现过敏反应,急救时可静脉推注10%葡萄糖酸钙溶液,其他与青霉素过敏处理相同。
(三)普鲁卡因过敏试验1.目的鉴别普鲁卡因过敏者。

克州人民医院药物过敏试验操作办法总则1、临床医生、护士和药师要高度重视药物过敏试验相关事宜。
熟悉使用前需要进行过敏试验的药品品种。
严格掌握需要进行过敏试验和严禁做过敏试验的情形。
2、用药前应询问药物过敏史,严格掌握药品说明书规定的禁忌证,在病历中做好必要的记录。
3、药品说明书是法律文书,因此,对于药品说明书中要求或建议用药前进行过敏试验的品种,用药前必须进行过敏试验。
4、药物过敏试验是一些药品安全使用的重要保障。
但需要强调的是,过敏试验本身也可导致严重过敏反应。
药物过敏试验阴性结果也存在给药过程中发生过敏反应的可能性。
因此,给药前需要做必要的患者风险告知和抢救准备,给药后仍应注意密切观察。
一旦出现过敏反应,及时停药,实施救治,对输液器、注射器和残存的药液进行封存,在病历中作相应记录,并呈报药品不良反应。
5、对于用药前需要进行药物过敏试验的药品,以下情形需知晓:(1)国家卫生行政部门、药监部门、现版中国药典以及药品说明书中均没有要求“不同批号的同一产品(生产厂家、通用名、规格、商品名均相同)交替使用时需要重新做皮试”。
(2)在连续治疗过程中,原则上不应更换为“相同通用名但生产厂家不同”的其他品种,除非有证据证明后者对治疗更有利。
若临床确需更换,则需要慎重。
若替代药品的说明书明确要求用药前进行过敏试验,则更换时需要重新进行药物过敏试验。
关于附表的说明:附表所列的药物名称、皮试药液浓度及给药方法与剂量,来自《中国国家处方集》2010年版。
附表:克州人民医院常用药物必做或应做皮肤敏感试验的药液浓度和给药方法与剂量备注:1、苯唑西林钠、氯唑西林钠、氨苄西林钠、阿莫西林、羧苄西林钠、哌拉西林钠、磺苄西林钠注射剂等皮试药液浓度和给药剂量同青霉素。
2、①凡头孢菌素规格(每瓶)为0.5g、0.75g、1g的先依次应用0.9%氯化钠注射液10ml、15ml、20ml稀释原药后,抽取0.1ml,再用0.9%氯化钠注射液稀释至10ml,抽取0.1ml做皮试。


药品检验仪器操作规程1.仪器自检规程1.净化工作台和净化空调器2.半自动青霉素电位滴定仪3.四道生理记录仪2.仪器操作规程1.高压消毒锅2.AE-240电子天平3.AEL-200电子天平4.ZRS-6型智能溶出试验仪5.ZRS-4型智能溶出试验仪6.BP-9300高分子杂质分析仪7.ZY-300A型抑菌圈测量仪8.AD-2.5型电子体重秤9.LDZ4-0.8型自动平稳微型离心机10.ZRY-2智能热原仪11.MS-302多媒体化生物信号记录分析系统12.ZYT-1型自动永停滴定仪13.智能崩解试验仪ZBS-6B型14.Waters 高效液相色谱仪15.501/486/U6K/746 HPLC仪16、DL?熔点测定仪17.pHS-3C型酸度计18.旋转式粘度计19.紫外分光光度计UV-2401PC20.紫外分光光度计UV-16021.天平的操作规程与爱护保养22.折光计23.韦氏比重秤24.TLC操作规程25.TLC照相操作规程26.显微镜的使用规程及日常爱护27. DWNER`SMANUAL 纯水器一、仪器自检规程1、净化工作台和净化空调器1.1 技术指标:1)净化工作台的操作台面空间的尘粒数和沉降菌应符合GMP100级的规定2)净化空调器的空间的尘粒数和沉降菌应符合GMP10000级的规定1.2 检定方法1)检定前仪器应先打开20~30分钟使平稳2)用尘粒计数器测定空间的尘粒数(0.5μ和5μ),做好记录3)用平皿计数法测定30分钟的沉降菌,做好记录1.3 以上二项若达不到规定要求,应及时进行处理(清洗过滤无纺布或清洁无菌室等)1.4 检定周期1)净化工作台:必要时或半年2)净化空调器:必要时或每次抽样时2、半自动青霉素电位滴定仪本仪器为配合中国药典一九九五年版硝酸汞电位滴定法的实施测定青霉素类抗生素电位滴定的专用仪器。
2.1 要紧技术规格电源电压:220V±10%,50Hz工作条件:环境温度0-40℃相对湿度:80%(20℃)电位值输入范畴:0±1000MV测量精度:0.25%2.2 检定方法取经110℃干燥至恒重的基准氯化钠约15mg,周密称定,加水50ml使溶解,以下按照本仪器"使用说明书"四项"操作与使用"测得硝酸汞滴定液(0.02mol/l)的浓度;滴定的同时按照中国药典记录一九九五年版电位滴定法(附录VIIA),详细记录硝酸汞滴定液(0.02mol/l)的消耗体积和电位,依照硝酸汞滴定液(0.02mol/l)的消耗量和氯化钠的取用量,算出硝酸汞滴定液(0.02mol/l)的浓度.两种方法误差不得过0.5%.2.3 检定周期二年.3、四道生理记录仪3.1 生物电放大器1)阻尼校验方法连续打下数个l毫伏标准电压后按以下判定:如升降线差不多陡直,横线差不多平直既为阻尼正常。

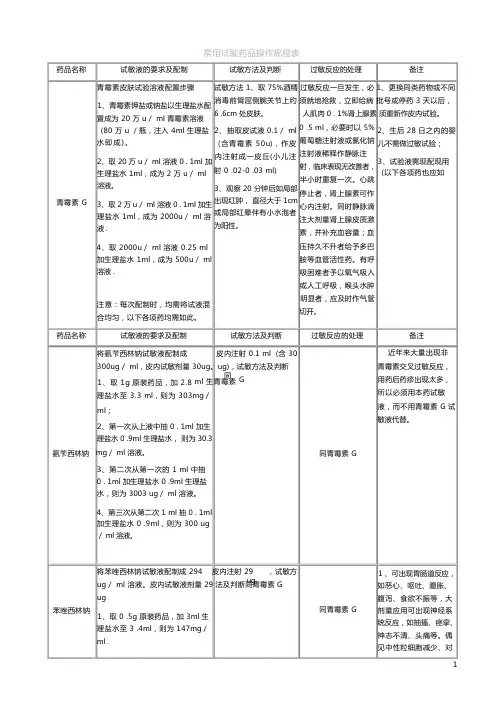
常用试敏药品操作规程表药品名称青霉素 G试敏液的要求及配制青霉素皮肤试验溶液配置步骤1、青霉素钾盐或钠盐以生理盐水配置成为 20 万 u/ ml 青霉素溶液(80 万 u /瓶,注入 4ml 生理盐水即成)。
2、取 20 万 u/ ml 溶液 0 . 1ml 加生理盐水 1ml,成为 2 万 u/ ml溶液。
3、取 2 万 u/ ml 溶液 0 . 1ml 加生理盐水 1ml,成为 2000u/ ml 溶液 .4、取 2000u/ ml 溶液 0.25 ml加生理盐水 1ml,成为 500u/ ml溶液 .注意:每次配制时,均需将试液混合均匀,以下各项药均需如此。
试敏方法及判断过敏反应的处理备注试敏方法 1、取 75%酒精过敏反应一旦发生,必 1、更换同类药物或不同消毒前臂屈侧腕关节上约须就地抢救,立即给病批号或停药 3 天以后,6 .6cm 处皮肤。
人肌肉 0 . 1%肾上腺素须重新作皮内试验。
2、抽取皮试液 0.1/ ml 0 .5 ml,必要时以 5% 2、生后 28 日之内的婴(含青霉素 50u),作皮内注射成一皮丘(小儿注射 0 .02-0 .03 ml)3、观察 20 分钟后如局部出现红肿,直径大于 1cm或局部红晕伴有小水泡者为阳性。
葡萄糖注射液或氯化钠注射液稀释作静脉注射,临床表现无改善者,半小时重复一次。
心跳停止者,肾上腺素可作心内注射。
同时静脉滴注大剂量肾上腺皮质激素,并补充血容量;血压持久不升者给予多巴胺等血管活性药。
有呼吸困难者予以氧气吸入或人工呼吸,喉头水肿明显者,应及时作气管切开。
儿不需做过敏试验;3、试验液需现配现用(以下各项药也应如药品名称试敏液的要求及配制试敏方法及判断将氨苄西林钠试敏液配制成皮内注射 0.1 ml (含 30300ug/ ml,皮内试敏剂量 30ug。
ug),试敏方法及判断同理盐水至 3.3 ml,则为 303mg/ml;2、第一次从上液中抽 0 . 1ml 加生理盐水 0 .9ml 生理盐水,则为 30.3氨苄西林钠mg/ ml 溶液。
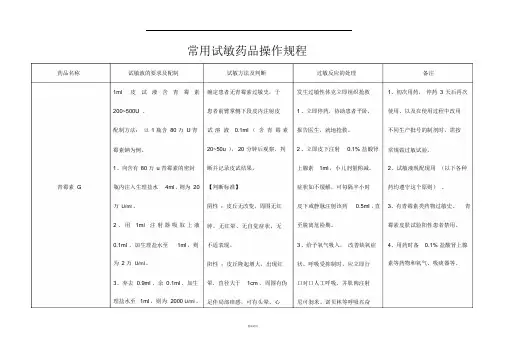
常用试敏药品操作规程药品名称试敏液的要求及配制试敏方法及判断过敏反应的处理备注1ml 皮试液含青霉素200~500U 。
配制方法:以1 瓶含80 万U 青霉素钠为例。
1、向含有80 万u 青霉素的密封确定患者无青霉素过敏史,于患者前臂掌侧下段皮内注射皮试溶液0.1ml (含青霉素20~50u ),20 分钟后观察、判断并记录皮试结果。
发生过敏性休克立即组织抢救1 、立即停药,协助患者平卧,报告医生,就地抢救。
2 、立即皮下注射0.1% 盐酸肾上腺素1ml ,小儿剂量酌减。
1、初次用药,停药3 天后再次使用、以及在使用过程中改用不同生产批号的制剂时,需按常规做过敏试验。
2、试敏液现配现用(以下各种青霉素G 瓶内注入生理盐水4ml ,则为20万U/ml 。
2 、用1ml 注射器吸取上液0.1ml ,加生理盐水至1ml ,则为 2 万U/ml 。
3、弃去0.9ml ,余0.1ml ,加生理盐水至1ml ,则为2000 U/ml 。
【判断标准】阴性:皮丘无改变,周围无红肿,无红晕、无自觉症状,无不适表现。
阳性;皮丘隆起增大,出现红晕,直径大于1cm ,周围有伪足伴局部痒感,可有头晕、心症状如不缓解,可每隔半小时皮下或静脉注射该药0.5ml ,直至脱离危险期。
3 、给予氧气吸入,改善缺氧症状。
呼吸受抑制时,应立即行口对口人工呼吸,并肌肉注射尼可刹米、诺贝林等呼吸兴奋药均遵守这个原则)。
3、有青霉素类药物过敏史、青霉素皮肤试验阳性患者禁用。
4、用药时备0.1% 盐酸肾上腺素等药物和氧气、吸痰器等。
4、再弃去0.9 ml ,余0.1ml (或弃去0.75ml ,余0.25ml )加生理盐水至1ml ,则1ml 内含青霉素200u (或500u )。
注意:每次配置时,均需将试液混合均匀,以下各项药均需如此。
慌、恶心,甚至发生过敏性休克。
药。
有条件者可插入气管导管,借助人工呼吸机辅助或控制呼吸。
喉头水肿导致窒息时,应尽快施行气管切开。

药物过敏试验操作流程步骤及评分下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的实用资料,如教育随笔、日记赏析、句子摘抄、古诗大全、经典美文、话题作文、工作总结、词语解析、文案摘录、其他资料等等,想了解不同资料格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, this shop provides you with various types of practical materials, such as educational essays, diary appreciation, sentence excerpts, ancient poems, classic articles, topic composition, work summary, word parsing, copy excerpts, other materials and so on, want to know different data formats and writing methods, please pay attention!药物过敏试验是一种常见的临床操作,用于确定患者对某种药物的过敏反应。
抗菌药物敏感试验标准操作规程肠杆菌科纸片扩散法药物敏感试验标准操作规程 (235)假单胞菌纸片扩散法药物敏感试验标准操作规程 (238)不动杆菌属纸片扩散法药物敏感试验标准操作规程 (240)嗜麦芽窄食单胞菌纸片扩散法药物敏感试验标准操作规程 (242)洋葱伯克霍尔德菌纸片扩散法药物敏感试验标准操作规程 (244)葡萄球菌属纸片扩散法药物敏感试验标准操作规程 (246)肠球菌属纸片扩散法药物敏感试验标准操作规程 (249)链球菌属纸片扩散法药物敏感试验标准操作规程 (251)超广谱β-内酰胺酶测定标准操作规程 (253)深部真菌药物敏感试验标准操作规程 (256)参考文献[1]CLSI.Performance Standards for Antimicrobial Susceptibility Testing;Nineteenth Informational Supplement. CLSI document M100-S19.Wayne,PA:Clinical and Laboratory Standards Institute,2009[2]叶应妩,王毓三,申子瑜主编.全国临床检验操作规程.第三版.南京:东南大学出版社,20068.1抑菌圈直径量取的范围为包括药敏纸片在内的被药物完全抑制的区域(肉眼判断)。
药敏平板应置于无反光的黑色背景下,用反射光源肉眼观测。
测量区域应为肉眼观察无明显可见菌落生长区域,忽略只有用放大镜才能观察到的位于抑菌圈外缘的细菌菌落。
8.2 分离自囊性纤维化病人的铜绿假单胞菌的纸片扩散法药敏试验结果可靠,但药敏平板一定要孵育24小时方可报告。
8.3 铜绿假单胞菌在抗感染治疗期间对药物会产生耐药性,因此初分离到的敏感菌在抗感染治疗3~4日后应重复进行药物敏感试验。
9.结果解释对青霉素类药物,敏感的试验结果提示在临床治疗铜绿假单胞菌严重感染时应使用高剂量的治疗方案。
单剂治疗可能会失败,这时应考虑联合使用其他菌株对其敏感的抗感染药物,如氟喹诺酮类或氨基糖苷类。
药物Ⅱ、Ⅲ期临床试验标准操作规程1.过程详述1.1试验启动阶段1.1.1 项目交接市场部、项目管理部与临床中心项目部签署正式项目交接文件,同时交接临床前研究综述资料和已有的临床研究资料,必要时还应提供相应的药学研究资料和药理毒理研究资料。
项目交接单包括:项目名称、客户信息、客户经理、合同风险、项目预算、完成时限、项目经理职责、厂家提供资料清单等内容。
相关人员签字确认。
由厂家提供研究者手册,或者项目经理撰写研究者手册,该手册包括:药物理化性质、药理、药效、毒理以及已有的临床研究资料。
研究者手册是临床试验开始前的资料汇编。
研究者手册的内容一般包括:目录、序言、化学和物理性质、临床前研究、药理学研究、药代动力学研究、毒理学研究、已有临床资料、药品使用信息等。
1.1.2 项目时间计划项目正式交接后,要求项目经理在三个工作日内完成整个临床试验工作的时间计划。
1.1.3 基地和研究者筛选详见:CRD-SOP003临床试验基地筛选流程。
另:基地筛选必须充分发挥当地监查员的作用,把详细情况和条件要求发给当地监查员,由他们筛选全部或者部分合适的试验基地。
1.1.4试验方案初稿等资料的准备在试验负责单位和主要研究者确定以后,即可与申办单位和主要研究者拟定试验方案、知情同意书、病例报告表等资料,以供首次研究者会议—方案讨论会使用。
设计并准备临床试验中所用的其他各种文件和记录表格。
1.1.5首次研究者会议-方案讨论与试验布置会详见CRD-SOP005 临床试验首研会规程。
1.1.6报伦理委员会审批根据首研会讨论的结果,修改试验方案、知情同意书等资料。
按照GCP的要求,所有临床试验必须得到伦理委员会的批准。
在实际进行临床试验时,首先必须取得牵头单位伦理委员会的批准,其他参加单位是否要过伦理根据各家单位的具体要求而定。
项目负责人按照CRD-SOP 008 临床试验过伦理资料准备规程准备过伦理资料。
伦理委员会将对临床试验批准文件、试验方案、知情同意书、药检报告、研究者手册、、病例报告表进行审批。
编写者:沈继录审核者:批准人:
生效日期:2012.1.1
文件发放范围:微生物组
文件年度审核
审核者:审核者:审核者:审核者:
日期:日期:日期:日期:
1. 目的
规范药物敏感性试验标准操作程序,确保药敏结果准确。
2.原理
将含有定量抗菌药物的纸片贴在已接种待检菌的琼脂平板上,纸片中所含的药物吸取琼脂中的水分溶解后会不断地向纸片周围区域扩散,形成递减的梯度浓度,在纸片周围抑菌浓度范围内待检菌的生长被抑制,从而产生透明的抑菌圈。
抑菌圈的大小反映检测菌对测定药物的敏感程度,并与该药对待检菌的最低抑菌浓度(MIC)呈负相关,即抑菌圈愈大,MIC愈小。
3.试剂
M-H培养基、无菌生理盐水、药敏纸片、无菌棉签、35℃孵育箱、标准比浊管或比浊仪。
4.质控
4.1 常用细菌药敏质控标准菌株参见CLSI规定。
4.2 质控菌株每日随临床标本一起进行药敏试验,测定质控菌株的抑菌环。
质控菌株的抑菌环在允许范围之内,说明结果可信。
4.3 质控的频率由于纸片法药敏试验是很稳定的,在不失控的时候,可以每周作1~2次质控菌株的测定。
如果发现有失控的情况,就必须每日作1次,寻找失控的原因并予以纠正。
如果连续30日失控<3次的,可以恢复每周1次。
5.操作步骤
5.1 挑取4~5个纯培养菌落,接种于3~5mlM-H肉汤(0.5麦氏单位)中,经35℃培养6~8 h。
5.2 用无菌生理盐水或M-H肉汤校正菌液浊度,使其与标准比浊管的浓度相同。
5.3 用无菌棉拭蘸取校正过的菌液,在试管壁上挤压几次,压去多余的菌液,涂布整个M-H平板表面,再重复两次,每次旋转平板60°,使整个平板涂布均匀,最后用
棉拭涂布平板四周边缘一圈。
5.4 涂布菌液的平板于室温中干燥3~5分钟后,用纸片分配器或无菌镊子取药敏纸片,贴于平板表面,并用镊尖轻压一下纸片,使其贴平。
每张纸片的间距不小于24 mm,纸片的中心距平扳的边缘不小于15 mm,直径90 mm的平板宜贴6张药敏纸片。
5.5 将贴好纸片的平板置35℃孵育18~24小时后,用卡尺量取抑菌圈直径。
个别菌孵育温度、时间及条件应按照CLSI规定。
6.结果判断
根据CLSIMl00最新标准将所测抑菌圈的大小,报告为敏感(S)、中介/中敏(I)或耐药(R)。
7.注意事项
8.1 测试链球菌时应测量生长受抑制区域而不是溶血受抑制区域。
8.2 如抑菌圈内有独立生长的菌落,则提示可能有杂菌,需要重新分离鉴定和药敏实验。
此菌落也可能为高频突变耐药株。
8.3 某些细菌的黄胺类药抑菌圈内有微量的细菌生长,可忽略不计,应以外圈为准。
8. 临床意义
测定细菌对药物的敏感程度,指导临床合理选用抗菌药物。
文件更改记录
修改后版本更改概述批准人生效日期
3.0 增加“文件更改记录”2012.1.1。