简单蒸馏与闪蒸
- 格式:docx
- 大小:40.14 KB
- 文档页数:3

常减压蒸馏一、蒸馏的形式蒸馏有多种形式,可归纳为闪蒸(平衡气化或一次气化)、简单蒸馏(渐次气化)和精馏三种方式。
简单蒸馏常用于实验室或小型装置上,如恩氏蒸馏。
而闪蒸和精馏是在工业上常用的两种蒸馏方式,前者如闪蒸塔、蒸发塔或精馏塔的气化段等,精馏过程通常是在精馏塔中进行的。
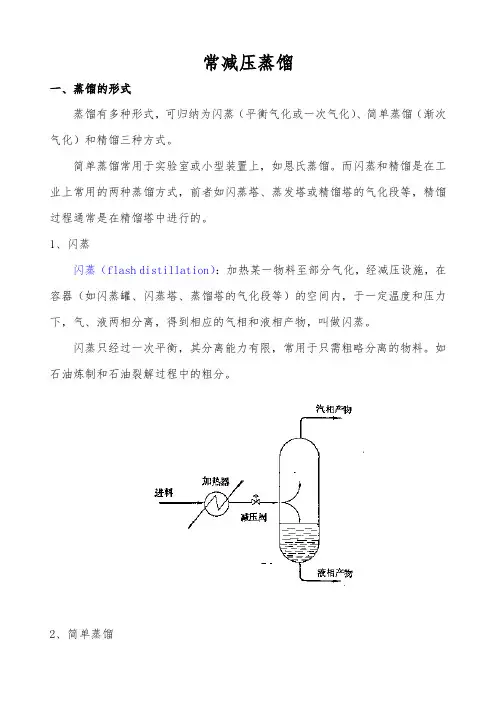
1、闪蒸闪蒸(flash distillation):加热某一物料至部分气化,经减压设施,在容器(如闪蒸罐、闪蒸塔、蒸馏塔的气化段等)的空间内,于一定温度和压力下,气、液两相分离,得到相应的气相和液相产物,叫做闪蒸。
闪蒸只经过一次平衡,其分离能力有限,常用于只需粗略分离的物料。
如石油炼制和石油裂解过程中的粗分。
2、简单蒸馏简单蒸馏(simple distillation):作为原料的液体混合物被放置在蒸馏釜中加热。
在一定的压力下,当被加热到某一温度时,液体开始气化,生成了微量的蒸气,即开始形成第一个汽泡。
此时的温度,即为该液相的泡点温度,液体温合物到达了泡点状态。
生成的气体当即被引出,随即冷凝,如此不断升温,不断冷凝,直到所需要的程度为止。
这种蒸馏方式称为简单蒸馏。
在整个简单蒸馏过程中,所产生的一系列微量蒸气的组成是不断变化的。
从本质上看,简单蒸馏过程是由无数次平衡汽化所组成的,是渐次气化过程。
简单蒸馏是一种间歇过程,基本上无精馏效果,分离程度也还不高,一般只是在实验室中使用。
3、精馏精馏(rectification)是分离液相混合物的有效手段,它是在多次部分气化和多次部分冷凝过程的基础上发展起来的一种蒸馏方式。
炼油厂中大部分的石油精馏塔,如原油精馏塔、催化裂化和焦化产品的分馏塔、催化重整原料的预分馏塔以及一些工艺过程中的溶剂回收塔等,都是通过精馏这种蒸馏方式进行操作的。
由于塔顶液相回流和塔底气相回流的作用,沿精馏塔高度建立了两个梯度:自塔底至塔顶逐级下降的温度梯度;气、液相中轻组分自塔底至塔顶逐级增大的浓度梯度。
精馏塔内沿塔高的温度梯度和浓度梯度的建立及接触设施的存在是精馏过程得以进行的必要条件。




第六章蒸馏第一节概述一、蒸馏分离依据---利用液体混合物中各组分具有不同的挥发度而进行分离的操作;----即利用在相同温度下各组分的蒸汽压不同。
易挥发组分(轻组分)A难挥发组分(重组分)B例如:酒精(A)与水(B)溶液,沸腾部分汽化,y A>x A同理,蒸汽部分冷凝,x B>y B∴蒸馏----使液体混合物部分汽化,利用其挥发度差异实现初步分离的一种传质操作精馏---利用多次部分汽化,多次部分冷凝,使汽相得到较纯的轻组分,液相得到较纯的重组分的操作二、蒸馏操作分类简单蒸馏(微分蒸馏)与平衡蒸馏(闪蒸)常压蒸馏、加压蒸馏与减压蒸馏连续蒸馏与间歇蒸馏普通蒸馏与特殊蒸馏三、蒸馏分离推动力与分离极限蒸馏是汽液两相间的传质过程蒸馏分离推动力——两相浓度偏离平衡的程度蒸馏分离极限——汽液两相达到相平衡(动态平衡)第二节 双组分溶液的汽液相平衡一、相组成表示法1.质量分率 iAA G G a ∑=该相的总质量一相中某组分质量可见:a <1, a A +a B …+ a N =1 2.摩尔分率 x A ,x B , y A ,y B 3.两者关系 )/(/)/(/i i AA i i A A i A A M a M a M G M G n n x ∑=∑=∑=对两元溶液:B B A A AA A M a M a M a x ///+=BB A A AA A M x M x M x a +=二、溶液的蒸汽压与Raoult 定律1.蒸汽压:汽液相平衡是一种动态平衡纯溶液----在达到汽液动态平衡时,逸出的A 分子数=回到液相的A 分子数,此时汽相中A 的压强=该温度下A 的饱和蒸汽压0A P混合液(A 、B 互溶)----在达到平衡时,由于A 、B 分子间相互作用,使B p <0B P , p A <0A P溶液存在三种分子间的作用力:AA f ,BB f ,AB f (1) 理想溶液:AB BB AA f f f ==显示无容积效应,无热效应如:苯-甲苯,甲醇-乙醇,烃类同系物溶液 (2)非理想溶液(实际溶液);AB BB AA f f f ≠≠2.Roult 定律:实验证明,在一定温度下,理想溶液的汽相中,任一组分的分压等于:A A A P x p =, 00)1(B A B B B P x P x p -==00000)()1(B B A A B A A A B A P P P x P x P x p p P +-=-+=+=00BA B A P P P P x --=∴ 非理想溶液不符合Roult 定律,汽液平衡关系主要靠实验数据。

蒸 馏蒸馏操作是分离液体混合物或液态气体混合物的常用单元操作。
它是以液体混合中各组分在相同操作条件下沸点(挥发度)的不同为依据,通过加入热量或取出热量的方法,使混合物形成气、液两相系统,气、液两相在相互接触中进行热量、质量传递,使易挥发组分在气相中增浓,难挥发组分在液相中增浓,从而实现互溶液体混合物分离的方法称为蒸馏。
蒸馏操作的依据:液体混合物中各组分沸点(挥发度)的差异;分离的条件:必须造成气、液两相系统。
轻组分(易挥发组分):液体混合物中沸点较低的组分容易汽化,称为轻组分。
重组分(难挥发组分):沸点较高的组分不易汽化,称为重组分。
馏出液:蒸馏所得到的蒸气冷凝后生成的液体称为馏出液。
馏出液中,轻组分的浓度较高。
残液(釜液):残留的液体称为残液。
残液中,重组分的浓度较高。
例如:在常压下,苯的沸点是80.1℃,甲苯的沸点是106℃,将苯和甲苯的混合液进行蒸馏时,苯是易挥发组分或轻组分,甲苯是难挥发组分或重组分,馏出液中:含高浓度的苯;残液中:含高浓度甲苯使苯和甲苯的混合液得以分离。
根据蒸馏操作的不同特点,蒸馏可以有不同的分类方法。
① 按蒸馏操作方式分类:可分为简单蒸馏、精馏和特殊精馏。
简单蒸馏适用于易分离物系或对分离要求不高的场合;精馏适用于难分离物系或对分离要求较高的场合;特殊蒸馏包括水蒸气蒸馏,恒沸蒸馏,萃取蒸馏,特殊精馏适用于普通精馏难以分离或无法分离的物系。
工业生产中以精馏的应用最为广泛。
② 按操作流程分类:可分为间歇蒸馏和连续蒸馏。
间歇蒸馏多应用于小规模生产或某些有特殊要求的场合。
工业生产中多处理大批量物料,通常采用连续蒸馏。
③ 按物系中组分的数目分类:可分为双组分蒸馏和多组分蒸馏。
工业生产以多组分蒸馏最为常见。
④ 按操作压强分类:可分为常压蒸馏、减压蒸馏和加压蒸馏。
工业生产中一般多采用常压蒸馏。
对在常压下物系沸点较高或在高温下易发生分解、聚合等 易变质的物系,常采用减压蒸馏。
对常压下物系的沸点在室温以下的混合物或气态混合物,则采用加压蒸馏。

第一章蒸馏在化工生产过程中,常常需要将原料、中间产物或粗产品中的组成部分进行分离,如将原油分成气油、煤油、柴油及重油等馏分作为产品又如聚氯乙烯在聚合前要求单体氯乙烯纯度不低于99.99%(也即将杂质分离掉),这些物质大都是均相混合物。
对于均相物系的分离,必须造成一个两相物系,,实现传质与分离操作。
常见的传质与分离过程有蒸馏、吸收、萃取与干燥等。
其中蒸馏是分离均相液态溶液的最常用的方法。
蒸馏是利用溶液中各组分蒸气压(或沸点、挥发度)的差异使各组分得到分离。
,由于苯的挥发性能比甲苯强,(即苯的沸点比甲苯低),气化出来的蒸气中苯的组成(即浓度)必然比原来液体的要高。
当气液达到平衡后,从容器中将蒸气抽出并使之冷凝,则可得到苯含量高的冷凝液。
显然,遗留下的残液中苯的组成要比原来溶液低,即甲苯组成要比原来溶液高,这样溶液就得到初步分离。
图1为常采用的连续精馏装置流程图,其主要设备为精馏塔,是由若干层塔板组成的板式塔,有时也用充满填料的填料塔。
溶液经预热后由塔的中部引入,因为原料组分的沸点不同,沸点低的组分较易气化而向上升,最后在冷凝器中冷凝成易挥发组分含量高的液体,一部分作为塔顶产品(又称馏出液),余下的送回塔内作为回流(称为回流液)。
沸点高的组分则从蒸气中不断地冷凝到沿各板下流的回流液中,最后从塔底排出的釜液中难挥发组分含量较高,釜液的一部分被引出作为塔底产品,余下的再送入再沸器(或者蒸馏釜),被加热气化后再返回塔中,具体内容第二节介绍。
蒸馏按操作方式可分为简单蒸馏、平衡蒸馏(闪蒸)、精馏和特殊精馏;按原图1:连续精馏流程图料中所含组分数目可分成双组分精馏及多组分精馏;按操作压力则可分为常压蒸馏、加压蒸馏及减压(真空)蒸馏;按操作是否连续又可分为连续蒸馏和间歇蒸馏。
本章将重点讨论常压下双组分连续精馏。
平衡关系是指溶液与其上方蒸气达到相平衡时,气、液两相间组成的关系。
它是分析蒸馏原理和进行蒸馏设备计算的依据。


蒸馏化工生产中经常要处理由若干组分所组成的混合物,其中大部分是均相物系。
生产中为了满足贮存、运输、加工和使用的要求,时常需要将这些混合物分离成为较纯净或几乎纯态的物质或组分。
蒸馏是分离液体混合物的典型单元操作。
这种操作是将液体混合物部分气化,利用其中各组分挥发度不同的特性以实现分离的目的。
它是通过液相和气相间的质量传递来实现的。
蒸馏过程可以按不同方法分类。
按照操作方式可分为间歇和连续蒸馏。
按蒸馏方法可分为简单蒸馏、平衡蒸馏(闪蒸)、精馏和特殊精馏等。
当一般较易分离的物系或对分离要求不高时,可采用简单蒸馏或闪蒸,较难分离的可采用精馏,很难分离的或用普通精馏不能分离的可采用特殊精馏。
工业中以精馏的应用最为广泛。
按操作压强可分为常压、加压和减压精馏。
按待分离混合物中组分的数目可以分为两(双)组分和多组分精馏。
因两组分精馏计算较为简单,故常以两组分溶液的精馏原理为计算基础,然后引申用于多组分精馏的计算中。
在本章中将着重讨论常压下两组分连续精馏。
蒸馏在化学工业中应用十分广泛,其历史也最为悠久,因此它是分离(传质)过程中最重要的单元操作之一。
在前面我们已经知道,蒸馏是气液两相间的传质过程,因此常用组分在两相中的浓度(组成)偏离平衡的程度来衡量传质推动力的大小。
传质过程是以两相达到相平衡为极限的。
由此可见,气液相平衡关系是分析蒸馏原理和进行设备计算的理论基础,故在讨论精馏过程的计算前,首先简述相平衡关系。
相平衡是《物理化学》课程的基本内容,本章侧重于论述其在化学工程中的应用,且讨论的只限于两组分理想溶液。
本节包含四个部分的内容:拉乌尔定律相律相图相对挥发度。
拉乌尔定律根据溶液中同分子间的与异分子间的作用力的差异,可将溶液分为理想溶液和非理想溶液两种。
实验表明,理想溶液的气液平衡关系遵循拉乌尔定律(Raoult's Law),即:式中溶液上方组分的平衡分压,Pa;同温度下纯组分的饱和蒸气压,Pa;溶液中组分的摩尔分率。

三、平衡蒸馏与简单蒸馏平衡蒸馏(闪蒸)是液体的一次部分气化的蒸馏操作。
1、流程2. 原理:将原料液加热到泡点温度以上,再经节流阀减压后进入闪蒸室,因压力下降原料液变为过热而使液体发生部分气化,形成气液两相,气化耗热使得液体温度下降,最后气、液两相温度趋于一致,两相组成趋于平衡。
简单蒸馏也称微分蒸馏,在蒸馏过程中系统的温度和气液相组成均随时间而改变,属于间歇非定态操作。
闪蒸罐塔顶产品yAxA加热器原料液塔底产品Q减压阀1. 流程2. 原理:原料液一次加入釜中,将其加热至泡点,使之不断的气化,产生的蒸气由釜顶连续引入冷凝器得馏出液产品。
釜内任一时刻的气液两相组成互成平衡。
由于 y ,随着蒸气的不断引出,釜液中易挥发组分的组成不断减少,泡点逐渐升高,与之相应的气化蒸气中的易挥发组分的含量也不断降低,故常设有几个接受器,按时间的先后,分别得到不同组成的馏出液。
四、精馏精馏:把液体混合物进行多次部分气化,同时把产生的蒸气多次部分冷凝,使混合物分离为所要求组分的操作过程称为精馏 1. 精馏流程y原料液x蒸气xD1xD2xD3冷凝器预热到一定温度的原料液送入精馏塔的进料板,在每层塔板上, 回流液体与上升蒸气互相接触, 进行热和质的传递.塔顶冷凝器的作用: 获得塔顶产品及保证有适宜的液相回流。
再沸器的作用: 提供一定量的上升蒸蒸气。
精馏段:加料板以上的塔段.上升气相中重组分向液相传递,液相中轻组分向气相传递,完成上升蒸气轻组分精制。
提馏段:加料板及其以下的塔段.下降液体中轻组分向气相传递,气相中重组分向液相传递,完成下降液体重组分提浓。
2. 精馏原理任意第n 块塔板上的精馏过程混合蒸汽多次部分冷凝,蒸汽组成沿 t-x(y) 相图的露点线变化,可得到易挥发组分含量很高而难挥发组分含量很低的蒸汽。
混合液体多次部分汽化,釜液组成沿 t-x(y) 相图的泡点线变化,可得难挥发组分含量很高而易挥发组分含量很低的釜液。
简单蒸馏与闪蒸
一、简单蒸馏
简单蒸馏是一种间歇操作,其设备流程如图10—14所示。
原料液直接加入蒸馏釜至一定量后停止,蒸馏釜内料液在恒压下以间接蒸汽加热至沸腾汽化,所产生的蒸汽从釜顶引出至冷凝器全部冷凝作为塔顶产品送入产品贮罐,由蒸馏原理知,其中易挥发组分的浓度将相对增加。
当釜中溶液浓度下降至规定要求时,即停止加热,将釜中残液排出后,再将新料液加入釜中重复上述蒸馏过程。
随着蒸馏过程的进行,釜内溶液中易挥发组分含量愈来愈低,随之产生的蒸汽中易挥发组分含量也愈来愈低。
生产中往往要求得到不同浓度范围的产品,可用不同的贮槽收集不同时间的产品。
二、闪蒸
闪蒸亦称为平衡蒸馏,其流程如图10—15所示。
混合液通过加热器升温(未沸腾)后,经节流阀减压至预定压强送人分离室,由于压强的突然降低,使得由加热器来的过热液体在减压情况下大量自蒸发,最终产生相互平衡的气液两相。
气相中易挥发组分浓度较高,与之呈平衡的液相中易挥发组分浓度较低,在分离室内气、液两相分离后,气相经冷凝成为顶部产品,液相则作为底部产品。
闪蒸和简单蒸馏都是直接运用蒸馏原理进行初步组分分离的一种操作,分离程度不高,可作为精馏的预处理步骤。
这两种蒸馏过程的流程、设备和操作控制都比较简单,但因其分离程度很低,不能满足
高纯度的分离要求。
因此,主要用来分离沸点相差较大或分离要求不高的场合。
要实现混合液的高纯度分离,需采用精馏操作。
一、蒸馏的基本概念和原理1、基本概念1.1饱和蒸汽压任何物质(气态、液态和固态)的分子都在不停的运动,都具有向周围挥发逃逸的本领,液体表面的分子由于挥发,由液态变为气态的现象,我们称之为蒸发。
挥发到周围空间的气相分子由于分子间的作用力以及分子与容器壁之间的作用,使一部分气体分子又返回到液体中,这种现象称之为冷凝.在某一温度下,当液体的挥发量与它的蒸气冷凝量在同一时间内相等时,那么液体与它液面上的蒸气就建立了一种动态平衡,这种动态平衡称为气液相平衡。
当气液相达到平衡时,液面上的蒸气称为饱和蒸汽,而由此蒸气所产生的压力称为饱和蒸汽压,简称为蒸汽压.蒸气压的高低表明了液体中的分子离开液面气化或蒸发的能力,蒸气压越高,就说明液体越容易气化.在炼油工艺中,根据油品的蒸气压数据,可以用来计算平衡状态下烃类气相和液相组成,也可以根据蒸气压进行烃类及其混合物在不同压力下的沸点换算、计算烃类液化条件等。
1.2气液相平衡处于密闭容器中的液体,在一定温度和压力下,当从液面挥发到空间的分子数目与同一时间内从空间返回液体的分子数目相等时,就与液面上的蒸气建立了一种动态平衡,称为气液平衡。
气液平衡是两相传质的极限状态。
气液两相不平衡到平衡的原理,是气化和冷凝、吸收和解吸过程的基础。
例如,蒸馏的最基本过程,就是气液两相充分接触,通过两相组分浓度差和温度差进行传质传热,使系统趋近于动平衡,这样,经过塔板多级接触,就能达到混合物组分的最大限度分离。
2、蒸馏方式在炼油厂生产过程中,有多种形式蒸馏操作,但基本类型归纳起来主要有三种,即闪蒸、简单蒸馏和精馏2。
1闪蒸(平衡汽化)加热液体混合物,达到一定的温度和压力,在一个容器的空间内,使之气化,气液两相迅速分离,得到相应的气相和液相产物,此过程称为闪蒸.当气液两相有足够的接触时间,达到了汽液平衡状态,则这种气液方式称为平衡汽化.2.2简单蒸馏(渐次汽化) 液体混合物在蒸馏釜中被加热,在一定压力下,当温度达到混合物的泡点温度时,液体即开始气化,生成微量蒸气,生成的蒸气当即被引出并经冷凝冷却后收集起来,同时液体继续加热,继续生成蒸气并被引出.这种蒸馏方式称为简单蒸馏或微分蒸馏,借助于简单蒸馏,可以使原料中的轻、重组分得到一定程度的分离。
编号:SM-ZD-28579 简单蒸馏与闪蒸
Organize enterprise safety management planning, guidance, inspection and decision-making, ensure the safety status, and unify the overall plan objectives
编制:____________________
审核:____________________
时间:____________________
本文档下载后可任意修改
简单蒸馏与闪蒸
简介:该安全管理资料适用于安全管理工作中组织实施企业安全管理规划、指导、检查
和决策等事项,保证生产中的人、物、环境因素处于最佳安全状态,从而使整体计划目
标统一,行动协调,过程有条不紊。
文档可直接下载或修改,使用时请详细阅读内容。
一、简单蒸馏
简单蒸馏是一种间歇操作,其设备流程如图10—14所示。
原料液直接加入蒸馏釜至一定量后停止,蒸馏釜内料液在恒压下以间接蒸汽加热至沸腾汽化,所产生的蒸汽从釜顶引出至冷凝器全部冷凝作为塔顶产品送入产品贮罐,由蒸馏原理知,其中易挥发组分的浓度将相对增加。
当釜中溶液浓度下降至规定要求时,即停止加热,将釜中残液排出后,再将新料液加入釜中重复上述蒸馏过程。
随着蒸馏过程的进行,釜内溶液中易挥发组分含量愈来愈低,随之产生的蒸汽中易挥发组分含量也愈来愈低。
生产中往往要求得到不同浓度范围的产品,可用不同的贮槽收集不同时间的产品。
二、闪蒸
闪蒸亦称为平衡蒸馏,其流程如图10—15所示。
混合液通过加热器升温(未沸腾)后,经节流阀减压至预定压强送人分离室,由于压强的突然降低,使得由加热器来的过热液
体在减压情况下大量自蒸发,最终产生相互平衡的气液两相。
气相中易挥发组分浓度较高,与之呈平衡的液相中易挥发组分浓度较低,在分离室内气、液两相分离后,气相经冷凝成为顶部产品,液相则作为底部产品。
闪蒸和简单蒸馏都是直接运用蒸馏原理进行初步组分分离的一种操作,分离程度不高,可作为精馏的预处理步骤。
这两种蒸馏过程的流程、设备和操作控制都比较简单,但因其分离程度很低,不能满足高纯度的分离要求。
因此,主要用来分离沸点相差较大或分离要求不高的场合。
要实现混合液的高纯度分离,需采用精馏操作。
这里填写您的企业名字
Name of an enterprise。