聚合物的玻璃化转变
- 格式:doc
- 大小:217.50 KB
- 文档页数:6

下列聚合物中玻璃化转变温度聚合物材料在化学、材料工程和生物医学等领域中扮演着重要角色。
而玻璃化转变温度是评估聚合物材料性能的重要指标之一。
本文将深入探讨下列聚合物中玻璃化转变温度这一主题,并着重分析其在材料科学领域的重要性。
一、概念解释什么是玻璃化转变温度?玻璃化转变温度是指在聚合物材料中,由蠕变态转变为弹性态所需的温度。
简单来说,当聚合物材料在加热过程中,温度达到玻璃化转变温度时,材料的物理性质会发生明显的变化,从而影响其力学性能和形状稳定性。
二、玻璃化转变温度的影响因素1. 聚合物分子结构:聚合物的分子结构对其玻璃化转变温度有着重要影响。
通常来说,分子链越长、交联结构越多的聚合物材料,其玻璃化转变温度会相对较高。
2. 添加剂和填料:在一些特殊的应用中,通过添加剂和填料来改变聚合物材料的玻璃化转变温度,以使其更适合特定的工程和应用需求。
3. 加工过程和历史:加工过程和历史会对聚合物材料的分子结构和排列产生影响,从而改变其玻璃化转变温度。
三、玻璃化转变温度的应用1. 材料选型和设计:了解聚合物材料的玻璃化转变温度有助于工程师和设计师选择适合的材料,并进行合理的构件设计。
2. 功能性材料的开发:在一些特殊领域,如智能材料和微电子器件等,需要研究和开发具有特定玻璃化转变温度的功能性材料。
3. 材料性能评价:玻璃化转变温度是评估聚合物材料热稳定性、抗老化性能和应力松弛性能的重要指标之一。
四、个人观点和理解玻璃化转变温度是聚合物材料中至关重要的指标之一,它不仅影响着材料的力学性能和形状稳定性,也对材料的加工和应用提出了挑战。
未来,我希望能够进一步深入研究和应用玻璃化转变温度这一指标,为材料科学领域的发展做出更多的贡献。
总结回顾通过本文的阐述,我们对下列聚合物中玻璃化转变温度这一重要主题有了更全面、深刻和灵活的理解。
我们了解了玻璃化转变温度的概念和影响因素,以及它在材料科学领域的应用和重要性。
我们也分享了个人的观点和理解。
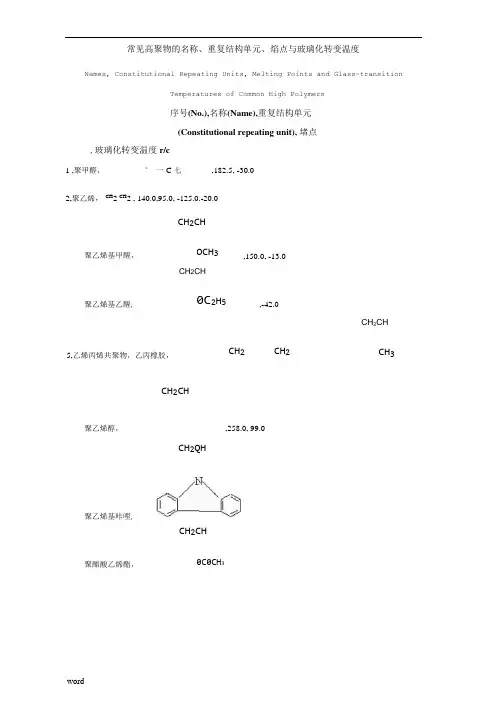
常见高聚物的名称、重复结构单元、焰点与玻璃化转变温度Names, Constitutional Repeating Units, Melting Points and Glass-transitionTemperatures of Common High Polymers序号(No.),名称(Name),重复结构单元 (Constitutional repeating unit), 堵点,玻璃化转变温度r/c1 ,聚甲醛,° 一C 七,182.5, -30.02,聚乙烯, CH 2 CH 2 , 140.0,95.0, -125.0.-20.0CH 2CHCH 2CHCH 2CHCH 2CH聚乙烯基甲醒,OCH 3,150.0, -13.0聚乙烯基乙醒,0C 2H 5,-42.05,乙烯丙烯共聚物,乙丙橡胶, CH 2 CH 2CH 3聚乙烯醇,CH 2CH,258.0, 99.0CH 2QH聚乙烯基咔哩,聚醋酸乙烯酯,0C0CH 39,聚氟乙烯, F , 200.0,-10,聚四氟乙烯(Teflon), CF2 , 327.0 , 130.011 ,聚偏二氯乙烯,如2 OF? , 171.0, 39.012,偏二氟乙烯与六氟丙烯共聚物(Viton), CH2 CF2 —------- CF2------------ CF ------------E ,一,-55.0------------- CH2CH ------------13 ,聚氯乙烯(PVC), C1 , 78.0-81.014,聚偏二氯乙烯,CH2 CCI2 , 210.0, -18.0--- C H2CH----15 ,聚丙烯,CH3 , 183.0,130.0, 26.0,-35.0-- CH2CH ---16,聚丙烯酸,cboH , 106.0--------- CH2C(CH3) ---------17,聚甲基丙烯酸甲酯,有机玻璃,C00CH3 , 160.0, 105.0-- CH2CH ----18,聚丙烯酸乙酯,C00CH2CH3)_22.0C00C4Hg-- C H2C ---19,聚(】■腊基丙烯酸丁酯),CN 85.020,聚丙烯酰胺, C0NH 2 ,・,165.0-- CH 2CH ---21 ,聚丙烯腊, CN , 317.0, 85.022,聚异丁烯基橡胶,CH 2qCH3)2 , 1.5 , -70.0------- CH 2C =^CHCH2——C1, 43.0, -45.0-CH 2C: CHCH 2 ----II28,聚亚癸基甲酰胺,尼龙・11 , NH (CH 2)W G , 198.0, 46.00 0.II.. II29,聚己二酰己二胺,尼龙-66,NH I CH 2)6NHC(CH 2)4C, 267 0 ? 45.00 0.IIII30,聚癸二酰己二胺,尼龙-610,NH(CH 2)5NHC(CH 2)5C, ]65.O , 50.023,聚氯代丁二烯,氯丁橡胶, 24,聚顺式.1.4.异戊二烯,天然橡胶CH 3,36.0, -70.025,聚反式.1.4.异戊二烯,古塔橡胶,26,苯乙烯和丁二烯共聚物,丁苯橡胶,CH 2CHCHCH 227,聚己内酰胺,尼龙.6, 0IINH(CH 2)5CCH 2CCHCH 2,74.0, -68.0CH 2CHCH 2CHCH=CH-56.0CH 3-0—(^-^一C(CH 3)2——一oc 一34, 聚碳酸酯,, 267.0, 150.035,聚环氧乙烷,—。


聚合物的玻璃化转变高宇(华东理工大学材料科学与工程学院,200237)【摘要】玻璃化转变是高聚物的一种普遍现象,研究玻璃化转变现象,有着重要的理论和实际意义。
本文先综述了玻璃化转变过程中的一些现象,然后简要介绍了玻璃化转变的三种主要理论:自由体积理论、热力学理论和动力学理论。
【关键词】玻璃化转变自由体积理论热力学理论动力学理论聚合物试样上施加恒定载荷,在一定范围内改变温度,试样的形变将随温度变化,以形变或相对形变对温度作图,所得到的曲线,通常称为温度-形变曲线或热机械曲线。
根据试样的力学性质随温度变化的特征,可以把非晶态聚合物按温度区域不同划为三种力学状态——玻璃态、高弹态和粘流态。
玻璃态与高弹态之间的转变,称为玻璃化转变,对应的转变温度即玻璃化转变温度。
1. 玻璃化转变现象玻璃化转变是聚合物的玻璃态与高弹态之间的转变,对应于含20~50 个链节的链段的微布朗运动的“冻结”和“解冻”的临界状态。
由于非晶态结构在聚合物中是普遍存在的,因此玻璃化转变是聚合物的一种普遍现象。
在玻璃化转变前后,聚合物的体积性质、热力学性质、力学性质、电学性质等都将发生明显变化。
跟踪这些性质随温度的变化,可确定玻璃化转变温度。
聚合物的玻璃化转变是链段运动随温度的升高被激发或随温度的降低被冻结造成的现象。
也可以从另一个角度来理解玻璃化转变行为,分子运动具有时间依赖性,在较低温度下,链段的运动速度十分缓慢,在实验限定的观察时间尺度下觉察不到它的运动现象,随着温度的升高,运动速度加快,当链段的运动速度同检测时间标尺相匹配时,玻璃化转变行为就表现出来了。
玻璃化转变本质上讲是分子运动方式的改变。
通过改变温度可以改变分子的运动方式,在温度恒定的前提下,也可改变其他因素以实现分子运动方式的变化,使材料处于不同的力学状态。
这种可通过多种因素导致玻璃化转变的现象称为玻璃化转变的多维性。
在玻璃化转变时,聚合物材料的力学性质的变化相当显著。

聚合物的玻璃化转变温度姓名:罗新杰学号:20101648 班级:高分子材料与工程一班摘要:在高分子科学中,聚合物的玻璃化转变是一个非常重要的现象,玻璃化转变是非晶态高分子材料固有的性质,是高分子运动形式转变的宏观体现,它直接影响到材料的使用性能和工艺性能,因此长期以来它都是高分子物理研究的主要内容。
本文主要简单地介绍玻璃化转变温度的相关知识和理论。
前言:玻璃化转变温度(Tg)是非晶态聚合物的一个重要的物理性质,也是凝聚态物理基础理论中的一个重要问题和难题,是涉及动力学和热力学的众多前沿问题。
玻璃转变的理论一直在不断的发展和更新。
从20世纪50年代出现的自由体积理论到现在还在不断完善的模态祸合理论及其他众多理论,都只能解决玻璃转变中的某些问题。
一个完整的玻璃转变理论仍需要人们作艰苦的努力。
对于非晶聚物,对它施加恒定的力,观察它发生的形变与温度的关系,通常特称为温度-形变曲线或热机械曲线。
非晶聚物有四种力学状态,它们是玻璃态、粘弹态、高弹态和粘流态。
在温度较低时,材料为刚性固体状,与玻璃相似,在外力作用下只会发生非常小的形变,此状态即为玻璃态,当温度继续升高到一定范围后,材料的形变明显地增加,并在随后的一定温度区间形变相对稳定,此状态即为高弹态,温度继续升高形变量又逐渐增大,材料逐渐变成粘性的流体,此时形变不可能恢复,此状态即为粘流态。
我们通常把玻璃态与高弹态之间的转变,称为玻璃化转变,它所对应的转变温度即是玻璃化转变温度,或是玻璃化温度。
高分子材料玻璃化转变的表征可提供丰富的信息,例如固化程度、热历史、材料的最高服役温度,共聚、共混物组分的相容性和相分离,组分的定性和定量等等,因此长期以来它都是高分子物理研究的主要内容。
所以我们得研究和掌握不同高分子玻璃化转变温度的测试方法,并比较不同测试方法的优缺点。
通过对玻璃化转变温度的不断研究,人们逐渐了解了影响玻璃化转变温度的不同因素,从而能更加灵活的处理和运用聚合物的玻璃化转变温度。

聚合物的玻璃态和玻璃化转变
1.名词解释
玻璃化温度:
粘流温度:
自由体积:
次级转变:
松弛时间:
2.试说明下列橡胶Tg不同的原因:
如果橡胶的结构已定,要想进一步提高其耐寒性,应采取什么措施?
3.分别画出无定形、半结晶、交联和增塑聚合物的形变-温度曲线和模量-温度
曲线。
4.将聚甲基丙烯酸甲酯从77K(液氮温度)加热到423K(粘流温度),共经历了哪些松弛转变?
各是什么分子运动机理?转变前后聚合物的力学性能发生了什么变化?
5. 请解释下列现象:
(1) 聚合物的g T 开始时随分子量增大而升高,当分子量达到一定值之后,g T 变为与分子量
无关的常数;
(2) 聚合物中加入单体、溶剂、增塑剂等低分子物时导致g T 下降。
6. 现在具有下列化学结构单元的几组聚合物,估计各组聚合物的Tg 高低顺序,写出其结构式并说理由:
(1) PE <PP< PVC< PAN
(2) 聚己二酸己二酯 尼龙66 聚对苯二甲酰已二胺
(3) 聚辛二酸丁二酯 聚对苯醚戊二酸 聚对苯二乙酸对苯二甲醇酯。




01什么是玻璃化转变?非晶态高聚物的温度–形变曲线玻璃化转变是非晶聚合物特有的性质,是由于温度的升高,大分子链段开始解冻到完全解冻的一个温度区域。
在这个转折区域有一个重要的特征温度就是玻璃化转变温度,是聚合物由玻璃态向高弹态转变的转变温度,也是链段冻结或解冻的温度。
是无定型聚合物大分子链段自由运动的最低温度,通常用Tg表示。
在此温度以上,高聚物表现出弹性;在此温度以下,高聚物表现出脆性。
02高聚物的三种力学状态玻璃态:是聚合物在玻璃化转变温度Tg以下的一种力学状态,由于温度较低,链段处于冻结状态,仅有分子键长、键角变化。
因此该状态下聚合物类似玻璃,常为脆性的,形变量很小,为可逆的普弹形变,应力应变可用虎克弹性定律来描述,具有普弹性。
比如塑料就是常温下处于玻璃态的聚合物。
高弹态:聚合物在Tg~Tf 之间的一种力学状态,温度升高,使链段运动能力增大,形变量随之增大,另一方面是大分子链柔顺性增大,链蜷曲程度随之增大,两种因素共同作用的结果是,形变不随温度而改变,出现平台区。
此状态下聚合物的形变与时间有关,具有松驰特性,表现为可逆的高弹形变,形变量很大,为高弹形变,模量进一步降低,聚合物表现为橡胶行为。
粘流态:是聚合物在Tf~Td (分解气化温度)之间的一种力学状态,此状态下大分子链受外力作用时发生位移,且无法回复。
聚合物表现出与小分子液体类似的流动行为,只是粘度较小分子液体大出很多。
一般高分子的熔融加工都是在此温度区间进行。
03影响玻璃化转变温度的因素一、链结构(1)主链:主链上引入苯基、联苯基、共轭双键等刚性基团,链的刚性会增大,而Tg、Tm和Tf均升高;主链上引入醚键、孤立双键等,链会变得柔顺,Tg、Tm和Tf均降低。
(2)侧基:侧基为刚性基团时,随着侧基体积的增大,链的柔顺性降低,Tg、Tm和Tf均升高;侧基(或侧链)为柔性基团(或柔性链)时,侧基(链)越大,柔性越好,则整个分子链的柔顺性越好,Tg、Tm和Tf均降低。

聚合物的玻璃化转变高宇(华东理工大学材料科学与工程学院,200237)【摘要】玻璃化转变是高聚物的一种普遍现象,研究玻璃化转变现象,有着重要的理论和实际意义。
本文先综述了玻璃化转变过程中的一些现象,然后简要介绍了玻璃化转变的三种主要理论:自由体积理论、热力学理论和动力学理论。
【关键词】玻璃化转变自由体积理论热力学理论动力学理论聚合物试样上施加恒定载荷,在一定范围内改变温度,试样的形变将随温度变化,以形变或相对形变对温度作图,所得到的曲线,通常称为温度-形变曲线或热机械曲线。
根据试样的力学性质随温度变化的特征,可以把非晶态聚合物按温度区域不同划为三种力学状态——玻璃态、高弹态和粘流态。
玻璃态与高弹态之间的转变,称为玻璃化转变,对应的转变温度即玻璃化转变温度。
1. 玻璃化转变现象玻璃化转变是聚合物的玻璃态与高弹态之间的转变,对应于含20~50个链节的链段的微布朗运动的“冻结”和“解冻”的临界状态。
由于非晶态结构在聚合物中是普遍存在的,因此玻璃化转变是聚合物的一种普遍现象。
在玻璃化转变前后,聚合物的体积性质、热力学性质、力学性质、电学性质等都将发生明显变化。
跟踪这些性质随温度的变化,可确定玻璃化转变温度。
聚合物的玻璃化转变是链段运动随温度的升高被激发或随温度的降低被冻结造成的现象。
也可以从另一个角度来理解玻璃化转变行为,分子运动具有时间依赖性,在较低温度下,链段的运动速度十分缓慢,在实验限定的观察时间尺度下觉察不到它的运动现象,随着温度的升高,运动速度加快,当链段的运动速度同检测时间标尺相匹配时,玻璃化转变行为就表现出来了。
玻璃化转变本质上讲是分子运动方式的改变。
通过改变温度可以改变分子的运动方式,在温度恒定的前提下,也可改变其他因素以实现分子运动方式的变化,使材料处于不同的力学状态。
这种可通过多种因素导致玻璃化转变的现象称为玻璃化转变的多维性。
在玻璃化转变时,聚合物材料的力学性质的变化相当显著。
在只有几度的转变温度区前后,材料的模量可改变三到四个数量级。
在玻璃态,材料是坚硬的固体,而在橡胶态,材料为具有较大变形性的柔软的弹性体。
作为塑料使用的无定形聚合物,当温度升高到发生玻璃化转变时,便失去了塑料的性能,变成了橡胶;反之,橡胶材料在温度降低到Tg以下时,便失去了橡胶弹性,变成了坚硬的塑料。
因此,玻璃化温度是非晶态热塑性塑料使用温度的上限,是橡胶使用温度的下限。
因此,玻璃化转变是高聚物的一个非常重要的性质。
研究玻璃化转变现象,有着重要的理论和实际意义。
2. 玻璃化转变理论玻璃化转变有多种理论,主要有三种:Fox和Flory提出的自由体积理论;根据玻璃态的熵函数的热力学理论和根据与玻璃化转变同时发生的松弛现象的动力学理论。
2.1 自由体积理论自由体积理论最初由Fox和Flory提出,认为液体乃至固体的宏观体积可分成两个部分:其主要部分是分子的占有体积,另一部分时分子堆砌形成的空隙,称为自由体积,它以“空穴”的形式分散在物质中。
自由体积的存在提供了分子运动的余地,使分子能够进行构象重排和移动。
在玻璃态,链段的运动被冻结,自由体积也处于冻结状态,自由体积的“空穴”尺寸和分布基本上保持固定。
聚合物的玻璃化温度为自由体积降至最低值的临界温度,在此温度以下,自由体积提供的空间已不足够允许聚合物分子链发生构象调整。
在玻璃态时聚合物的宏观体积随温度的升高发生的膨胀来源于分子占有体积的膨胀,包括分子振动幅度的增加和键长的变化等。
当温度升高到玻璃化转变点以后,自由体积开始膨胀,为链段运动提供了空间保证,分子热运动能量已足够高。
链段由冻结状态进入运动状态,聚合物进入高弹态。
在高弹态,聚合物试样的体积膨胀是由分子占有体积和自由体积的膨胀共同贡献的,所以体积随温度的变化率比玻璃态来得大,从而导致比容—温度关系在Tg 处发生转折,热膨胀系数则发生突变。
非晶聚合物的体积膨胀情况可用图2.1来描述,如果聚合物在绝对零度的分子实占体积为0V ,在玻璃态,自由体积为,f g V ,聚合物的膨胀率即分子实占体积的膨胀率为(/)g dV dT ,则在玻璃态聚合物的宏观体积g V 随温度的变化可表示为:,0()()g f g g g dV V V V T T T dT =++≤当温度为g T 时,宏观体积以Tg V 表示,则:,0()Tg f g g g dV V V V T dT=++ 在高弹态,聚合物的体积膨胀率为(/)r dV dT ,它是实占体积膨胀和自由体积膨胀的综合效果,宏观体积与温度的关系可表示为:()()()r Tg r g g dV V V T T T T dT =+->自由体积的膨胀率为聚合物在高弹态与玻璃态的体积膨胀率之差。
在高弹态的自由体积f V 同温度的关系为:,[()()]()f f g r g g dV dV V V T T dT dT=+-- 定义单位体积德膨胀率为膨胀系数。
在玻璃化温度附近,处于玻璃态和高弹态的聚合物的膨胀系数分别为:1()g g Tg dV V dTα= 1()r r Tg dV V dT α=自由体积德膨胀系数为两者之差:f rg αααα=-=∆在玻璃态的自由体积分数g f 为一固定值:,f g g Tg V f V =在高弹态的自由体积分数r f 为:()r g f g f f T T α=+-自由体积理论对玻璃化转变现象的描述基本上是成功的,但也存在一些不足。
g T 的数值同冷却速度有关,不同的冷却速度对应于不同的g T 值,在g T 时的比容也各不相同,因而自由体积分数也各不相等。
这种现象不能用自由体积理论予以说明。
如图2.1,把聚醋酸乙烯酯淬火后恒温放置,发现其体积不断减小,就是说,自由体积并没有完全冻结,而仅仅能冻结一部分。
2.2 热力学理论热力学研究指出相转变过程中自由能是连续的,而与自由能的导数有关的性质发生不连续的变化。
以温度和压力作为变量,与自由能相应的一阶导数有关的性质如体积、熵及焓在晶体熔融和液体蒸发过程中发生突变,这类相转变称为一级相转变。
而对自由能的二阶导数有关的性质如压缩系数K ,膨胀系数α及比热p c 出现不连续变化的热力学转变成为二级相转变。
在玻璃化转变时,高聚物的K 、α、p c 恰恰都有不连续,所以通常把玻璃化转变看作是二级转变。
其实这是并没有达到热力学平衡,因而也不是真正的二级转变。
但是如果冷却速率无限缓慢,允许构象重排达到平衡,便有可能观察到真正的二级转变。
W .Kauzmann 发现将简单玻璃状物质的熵外推到低温,在温度到达绝对零度前,熵已经变为零,而当外推至0K 时,便会得到负熵,见图2.2,这在物理学上是没有意义的。
J .H .Gibbs 和E .A .DiMarzio 重新解释了该现象,指出在构象熵变为零时将发生热力学二级转变,对应的温度为二级相转变点2T 。
在2T 以下构象熵不再改变,恒等于零。
具体地说,在高温下,高分子链可实现的构象数目是很大的,每种构象都同一定的能量相对应。
随着温度的降低,高分子链发生构象重排,高能量的构象数目越来越少,构象熵越来越低。
温度降至2T 时,所有分子链都调整到能量最低状态的那种构象,构象熵为零。
温度在2T 以下,链构象不再发生变化。
在转变温度2T 所对应的转变是分子链由众多的构象状态通过重排调整到能量最低的统一的构象状态的变化。
在该点熵变是连续的,但自由能的二阶导数发生不连续变化。
高分子链的构象调整需要一定的时间。
随着温度的降低,构象重排运动难度增大,所需时间越来越长。
在没有达到转变点2T 之前,分子链的构象重排所需时间已足够长,在实验规定的时间尺度下已难以觉察到这种分子运动,从而发生玻璃化转变现象。
就是说,实验上观察到的玻璃化转变现象同二级转变的分子运动机理是等同的,都是构象熵随温度的下降而减少的过程。
只是因为分子运动需要一定的时间,在有限的时间标尺下构象熵降不到零,从而只能观测到具有松弛特征的转变点g T ,而不能得到二级相转变点2T 。
为了得到2T ,应在无限缓慢的条件下进行实验。
2T 的数值可由WLF 方程估计。
在T=2T 时,有:12222()()lg ()g g gC T T T T C T T ηη--=+- 此时,构象重排无限慢,对应于黏度趋于无穷大。
欲满足这一条件,上式右端的分母必须为零,于是22g T T C =-因此热力学理论预期在g T 以下的某一2T 处,在无限长的时间里,可以实现所有高分子链都调整到能量最低的构象状态的真正的二级转变。
2C 的平均值为50℃左右,因此2T 应当出现在g T 以下50℃附近。
g T 和2T 是相关的,除了时间标尺以外,其他一些因素对g T 的影响与对2T 的影响具有一定规律。
虽然不能直接用实验证明2T ,但可通过g T 的变化规律对二级转变理论进行评价。
从热力学理论出发,可推论出结构或环境发生变化时2T 的变化趋势,所预言的结果同观察到的这些因素对g T 的影响的实验事实一致,反映了热力学二级转变理论可成功地解释玻璃化转变现象。
该理论成功地预言了g T 随分子量、稀释剂、交联密度及其他变量的变化,但很难说明玻璃化转变时复杂的时间依赖性。
2.3 动力学理论玻璃化转变现象具有明显的动力学性质,g T 与实验的时间标尺(如升降温速度和动态实验时所用的频率等)有关,因此有人指出,玻璃化转变是由动力学方面的原因引起的,如A .J .Kovacs 理论。
在平衡态,体积是温度和压力的函数,温度和压力确定后,体积就具有固定值——平衡态体积。
玻璃态物质在玻璃化转变区,当温度和压力确定后,试样的体积并不能立即达到平衡态体积,它同平衡态体积有偏差,这一偏差的大小同时间有关。
这时,体积不再是温度和压力的唯一函数,可表示为:V=V(T,P,)ξξ称为有序参数,由实际体积与平衡态体积的偏离量决定。
这样就建立了体积与松弛过程时间的联系。
当松弛到平衡态时,ξ只同温度和压力有关,体积又还原为温度和压力的唯一函数。
如果试样在温度为T ,压力为P 时的实际比容为v ,相应的平衡态比容为v ∞,则体积的相对偏差为:v v v δ∞∞-= 随着时间的延长,v 趋近于v ∞,体积偏差越来越小。
根据质量作用定律,δ减小的速度可简单地由下式表示:()d dt δδτδ-=比例常数的倒数τ为推迟时间。
δ减少的快慢同推迟时间有关,τ越大,趋向平衡的过程就越长。
玻璃化转变的自由体积理论没有考虑自由体积的膨胀或收缩的时间依赖性。
热力学理论的出发点是构象在平衡态的变化,同样不涉及时间问题。
动力学理论核心是松弛过程的时间T。
一个完善的玻依赖性,虽然能解释许多玻璃化转变的现象,但无法从分子结构来预示g璃化转变理论还有待于进一步研究。
3 参考文献[1]何曼君等编.高分子物理(修订版).上海:复旦大学出版社,2005.[2]刘凤岐等编.高分子物理(第二版).北京:高等教育出版社,2004.[3]冯新德等编.高分子化学与物理专论.广东:中山大学出版社,1984.。