化工单元操作与控制--知识点汇总(精选)
- 格式:docx
- 大小:16.26 KB
- 文档页数:2

总复习 流体流动重点:柏努利方程∑+++=+++f e E Pu gz W P u gz ρρ2222121122 Kg J /∑+++=+++f e h gPg u z h g P g u z ρρ2222121122 m N J =/压强降)(2222221211f f e p E P u gz W P u gz ∆+++=+++∑ρρρρρρ Pa m J =3/一、位能z/gz/ρgzz 是相对值,是相对于所取水平面的垂直高度。
二、动能(两个知识点:连续性方程,流量计) 1、连续性方程定态流动与非定态流动定态流动时对所有流体有:常数====n n n A u A u A u ρρρ 322111 对不可压缩流体有:常数====n n A u A u A u 2211对圆管有:21222122122144d d d d A A u u ===ππ2、流量计孔板、文丘里、转子三种,利用V=uA 来测量。
孔板、文丘里:A 一定,Δu 与ΔP 根据柏努利方程成一定关系,而ΔP 由压差计测得。
故该两种流量计由孔板或文氏管与压差计相连组成。
V S 增大,Δu 增大,ΔP 增大,A 不变。
转子:fff f A gV gV P ρρ-=∆V S 增大,转子上移,A 增大,Δu 不变,ΔP 不变。
三、静压能(两个知识点:静力学基本方程,密度ρ) 1、静力学基本方程 ①压强单位及换算:O mH mmHg at Pa atm 2533.10760033.110013.11===⨯=②压强表示法表压强=绝对压强-大气压强 真空度=大气压强-绝对压强 真空度= -表压强 ③表达式:gh P P ρ+=0或)(2112z z g P P -+=ρ④等压面:等高、静止、连通、同一流体(分液器) ⑤应用:压强或压差的测量(U 形管)、液位测量、液封高度计算。
解题原理:等压面指示液:与被测液不互溶,颜色好分辨,密度一般大于被测液(倒U 形管除外)gR P B A )(ρρ-=∆(水平放置时)气体为指示液,因液气ρρ≤,可忽略不计,所以gR P ρ=∆(液封时常用) 安全液封:gP g P P h ρρ表=-≤0 溢流液封:g Pg P P h ρρ真=-≥02、密度液体:随温度和压强变化而变化,可通过查表获得数据。

化工单元知识点总结大全化工单元是指利用化学、物理和机械等工艺制备化学产品的生产装置。
化工单元包括各种设备和设施,如反应器、分离器、塔器、泵、管道、阀门、控制系统等等。
化工单元的设计、操作和维护需要掌握丰富的知识和技能,以确保生产过程的安全、稳定和高效。
本文将介绍化工单元的一些重要知识点,包括反应工程、传质传热、分离工程以及过程控制等方面的内容。
一、反应工程反应工程是化工过程中的关键环节,涉及到化学反应的研究、设计和操作。
反应工程的主要任务是确定最佳的反应条件,以实现化学反应的高效、安全和经济运行。
在反应工程中,需要考虑的主要因素包括反应热、反应速率、反应平衡、反应物质的选择和处理、反应条件的控制等等。
1. 反应热反应热是指化学反应过程中释放或吸收的热量。
反应热的大小会影响到反应的热平衡和温度控制。
在设计反应工程时,需要通过实验或计算来确定反应热的值,并选择合适的冷却或加热方式,以保证反应过程的温度在安全范围内。
2. 反应速率反应速率是指化学反应物质转化的快慢程度。
在反应工程中需要确定最佳的反应速率,以提高产品的产量和质量。
影响反应速率的因素包括反应物质的浓度、温度、压力以及催化剂的选择等。
3. 反应平衡反应平衡是指在一定条件下,反应物质和生成物质之间的浓度或压力达到动态平衡的状态。
在设计反应工程时,需要考虑到反应平衡的影响,以确定最佳的反应条件和操作参数。
4. 反应物质的选择和处理在反应工程中,需要根据反应物质的性质和要求,选择合适的原料,并对其进行处理,以确保反应的顺利进行和产品的质量。
5. 反应条件的控制在反应工程中,需要通过控制温度、压力、pH值、搅拌速度等参数,来实现反应条件的控制,以保证反应的稳定和高效。
二、传质传热传质传热是化工过程中的另一个重要环节,涉及到物质和热量的传递、分离和转化。
传质传热的主要任务是提高产量、提高质量、降低能耗和保证生产过程的安全稳定。
1. 传质传质是指物质在不同系统之间的传递。

化工单元操作知识嘿,朋友们!咱今儿来聊聊化工单元操作这档子事儿。
化工单元操作,就好比是一场奇妙的大冒险!你想想看,各种物质在不同的操作下发生奇妙的变化,多有意思呀!比如说蒸馏,那就像是一场分离的魔术。
把混合物放进蒸馏塔这个大魔术箱里,通过温度的变化,让不同的成分乖乖地分开,各走各的路。
这不就像我们整理房间,把不同的东西归置到不同的地方嘛!再说说吸收,它就像一个贪吃的小怪兽,把有用的气体大口大口地吃进去。
这多神奇呀,能把那些在空气中飘来飘去的气体给抓住。
还有过滤呢,简直就是个超级大筛子,把杂质统统筛掉,只留下纯净的宝贝。
这就像是我们淘米,把那些不好的米粒筛出去,留下白白净净的好米。
萃取呢,就像是个聪明的小侦探,能从一堆乱七八糟的东西里精准地找到它想要的那个宝贝成分,然后把它带走。
在化工单元操作里,每个环节都至关重要啊!要是哪个地方出了岔子,那可不得了。
就好像一辆汽车,一个零件坏了,整个车都跑不起来啦!你说,这些操作是不是特别神奇?它们能把普普通通的原料变成我们需要的各种宝贝。
而且呀,这可不是随随便便就能做好的,得靠我们的技术和经验呢。
就拿温度控制来说吧,高一点不行,低一点也不行,就得恰到好处。
这就像做饭,火候掌握不好,那菜的味道可就差远了。
还有压力呢,也得控制得稳稳当当的。
压力大了可能会爆炸,压力小了又达不到效果,你说难不难?化工单元操作可不只是在工厂里有用哦,它和我们的生活息息相关呢。
我们用的好多东西,都是通过这些操作生产出来的。
没有它们,我们的生活可就没那么丰富多彩啦!所以啊,朋友们,可别小看了化工单元操作。
它就像一个默默奉献的英雄,在背后为我们的生活添砖加瓦呢!我们要好好了解它,掌握它,让它为我们创造更多的美好呀!这就是化工单元操作,神奇又重要,不是吗?。

化工单元操作相关知识1.什么是化工单元操作?一个化工产品的生产是通过若干个物理操作与若干个化学反应实现的。
尽管化工产品千差万别,生产工艺多种多样,但这些产品的生产过程所包含的物理过程并不是很多,而且是相似的。
比如,流体输送不论用来输送何种物料,其目的都是将流体从一个设备输送至另一个设备;加热与冷却的目的都是得到需要的操作温度;分离提纯的目的都是得到指定浓度的混合物等。
因此把这些包含在不同化工产品生产过程中,发生同样物理变化,遵循共同的物理学规律,使用相似设备,具有相同功能的基本物理操作,称为单元操作。
2.单元操作按其遵循的基本规律分类:(1)遵循流体动力学基本规律的单元操作:包括流体输送、沉降、过滤、固体流态化等;(2)遵循热量传递基本规律的单元操作:包括加热、冷却、冷凝、蒸发等;(3)遵循质量传递基本规律的单元操作:包括蒸馏、吸收、萃取、结晶、干燥等;(物质从物体或空间的某一部分转移到另一部分的现象)3.流体输送单元操作的相关知识3.1什么叫流体输送?流体输送指的是流体以一定流量沿着管道(或明渠)由一处送到另一处.3。
2流体输送在化工生产中的作用?化工生产处理的物料多数为流体,按工艺要求在各化工设备和机器之间输送这些物料,是实现化工生产的重要环节。
化工生产中物料的种类很多,被输送流体的性质如密度、粘度、毒性、腐蚀性、易燃性与易爆性等各不相同,而且流体的,压力从高真空到高压,每小时的输送量从0。
01m³到100m³以上,所以输送流体所用的流体输送机械有多种形式,制作材料也是多种多样的.3。
3化工生产中常用的流体输送机械有哪些?常用的有离心泵、往复泵、高油压泵、旋转泵等。
3。
4化工生产中常用流体输送机械的制作材料主要有哪些?化工生产中,流体大都用密闭的管道输送。
为调节流量,改变流向以及实现流体的分流或合流,管道中装有阀门、弯头和三通等管件。
管道和管件由碳钢、铸铁、不锈钢、铜、铝和铅等金属材料或塑料、陶瓷、玻璃和石墨等非金属材料制成,其中以碳钢和铸铁应用最广。


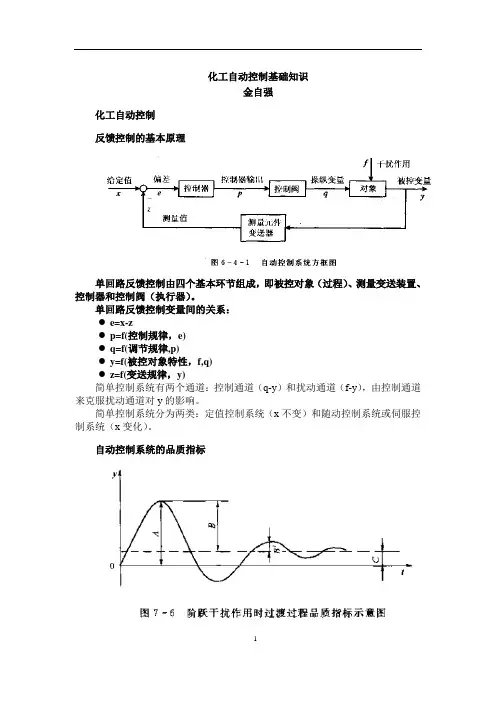
化工自动控制基础知识金自强化工自动控制反馈控制的基本原理单回路反馈控制由四个基本环节组成,即被控对象(过程)、测量变送装置、控制器和控制阀(执行器)。
单回路反馈控制变量间的关系:●e=x-z●p=f(控制规律,e)●q=f(调节规律,p)●y=f(被控对象特性,f,q)●z=f(变送规律,y)简单控制系统有两个通道:控制通道(q-y)和扰动通道(f-y),由控制通道来克服扰动通道对y的影响。
简单控制系统分为两类:定值控制系统(x不变)和随动控制系统或伺服控制系统(x变化)。
自动控制系统的品质指标余差C最大偏差A衰减比B:B’,(4:1)过渡时间Ts,(5%)被控对象特性参数放大系数K=Δ输入/Δ输出,(应该使控制K大,干扰K小)滞后时间τ=纯滞后τo+容量滞后τn时间常数Tc,63.2%化工自动控制元件传感器、变送器控制器执行器基本控制规律双位控制PID控制复杂控制以下以液位控制系统为例加以说明。
8串级控制如果系统中不止采用一个控制器,而且控制器间相互串联,主控制器的输出作为串级控制器的给定值,这样的系统称为串级控制系统。
串级控制系统的特点:1、主回路为定值系统,副回路为随动系统2、副回路包含了主要的干扰,具有超前作用,有效地克服了时间滞后,改善了主控制器的被控对象特征。
3、有利于克服副回路内执行机构等的非线性在本单元中罐V101的液位是由液位调节器LIC101(主控制器)和流量调节器FIC102(副控制器)串级控制。
主控制器LIC101的输出作为副控制器FIC102的给定值。
即正常工况下LIC101投自动,FIC102投串级。
具体来讲,LIC101的百分比输出OP(例如50%)对应一个流量(例如20000Kg/H),该流量随LIC101的输出而变,且作为FIC102的给定值SP,FIC102投串级时,可见该SP值不断变化,FIC102的PV值因泵的流量波动而出现较大波动,但LIC101的PV值却波动较小,可见改善了主控制器的被控对象特征。

(完整版)化工原理各章节知识点总结第一章流体流动质点含有大量分子的流体微团,其尺寸远小于设备尺寸,但比起分子自由程却要大得多。
连续性假定假定流体是由大量质点组成的、彼此间没有间隙、完全充满所占空间的连续介质。
拉格朗日法选定一个流体质点,对其跟踪观察,描述其运动参数(如位移、速度等)与时间的关系。
欧拉法在固定空间位置上观察流体质点的运动情况,如空间各点的速度、压强、密度等,即直接描述各有关运动参数在空间各点的分布情况和随时间的变化。
定态流动流场中各点流体的速度u 、压强p 不随时间而变化。
轨线与流线轨线是同一流体质点在不同时间的位置连线,是拉格朗日法考察的结果。
流线是同一瞬间不同质点在速度方向上的连线,是欧拉法考察的结果。
系统与控制体系统是采用拉格朗日法考察流体的。
控制体是采用欧拉法考察流体的。
理想流体与实际流体的区别理想流体粘度为零,而实际流体粘度不为零。
粘性的物理本质分子间的引力和分子的热运动。
通常液体的粘度随温度增加而减小,因为液体分子间距离较小,以分子间的引力为主。
气体的粘度随温度上升而增大,因为气体分子间距离较大,以分子的热运动为主。
总势能流体的压强能与位能之和。
可压缩流体与不可压缩流体的区别流体的密度是否与压强有关。
有关的称为可压缩流体,无关的称为不可压缩流体。
伯努利方程的物理意义流体流动中的位能、压强能、动能之和保持不变。
平均流速流体的平均流速是以体积流量相同为原则的。
动能校正因子实际动能之平均值与平均速度之动能的比值。
均匀分布同一横截面上流体速度相同。
均匀流段各流线都是平行的直线并与截面垂直,在定态流动条件下该截面上的流体没有加速度, 故沿该截面势能分布应服从静力学原理。
层流与湍流的本质区别是否存在流体速度u、压强p的脉动性,即是否存在流体质点的脉动性。
稳定性与定态性稳定性是指系统对外界扰动的反应。
定态性是指有关运动参数随时间的变化情况。
边界层流动流体受固体壁面阻滞而造成速度梯度的区域。

常用化工单元操作基本知识一、水浴加热、蒸汽直接加热如何进行操作, 答:根据工艺要求使反应罐处于蒸馏或回流及其其他加热状态,在夹套控制阀关闭位置下: 1、水浴加热操作步骤: (1) 开“水浴排”阀门。
(2) 开“循环水进”阀门,使水体装满夹层,自“水浴排”溢出。
(3) 关“循环水进”阀门。
(4) 缓慢开启“蒸汽下进”阀门,控制蒸汽压力,使罐内温度升至工艺要求。
(5) 升温至工艺要求后,关“蒸汽下进”阀或保护适当进汽,稳定罐内温度。
(6) 水浴加热结束,关“蒸汽下进”阀和“水浴排”阀,视情况是否排空夹层。
2、蒸汽直接加热步骤: (1) 开罐底“冷凝水”阀和“旁通阀” ,排空夹套内的水。
(2) 缓慢开“蒸汽上进”阀,控制蒸汽压力?0.4Mpa。
(3) 待排水管道发烫或排出较多蒸汽时,关旁通阀,开疏水器前后阀门。
(4) 注意调节蒸汽压力,时常观察罐内情况,如有大量冒泡要马上关闭“蒸汽上进”阀,甚至停止搅拌,防止冲料。
(5) 升温将至釜内物料温度低于釜内溶剂沸点 510?时(注:此时极,易冲料) 应减小或关闭蒸汽,观察几分钟,视罐内情况供给蒸汽,使温度稳定在工艺要求范围内。
(6) 蒸汽加热结束,关“蒸汽上进”和“冷凝水”阀。
二、减压蒸馏如何操作, 答:减压蒸馏操作步骤:1、检查水、电、汽和真空系统是否正常。
2、检查反应罐、接受罐等设备是否正常,及其所有相连的阀门处于关闭位置,开启搅拌正常。
3、打开升气管蒸馏阀,接受罐进口阀。
、、、4、依次开各级冷凝器“循环水出”“循环水进”“冰盐水出”“冰盐水进”阀门,观察视盅是否有漏水现象,冷却有效。
5、开接受罐“真空”阀,按工艺要求控制真空度。
6、按工艺要求进行蒸汽直接加热或则水浴加热,正确操作,升温至工艺控制要求,进行减压蒸馏。
7、减压蒸馏过程中,要密切关注真空是否稳定,如有波动要及时调节罐内真空,防止冲料。
8、要观察接受罐液位,严禁满罐被真空抽走。

化工单元操作总复习化工单元操作是指在化工生产过程中进行的各种操作,包括原料的加工处理、反应操作、分离和纯化等步骤。
化工单元操作对于保证生产过程的顺利进行,以及产品质量的稳定提高具有重要意义。
本文将对化工单元操作的相关知识进行总结和复习。
首先,化工单元操作的第一步是原料的加工处理。
原料加工处理主要包括物料的粉碎、过滤、浸提、溶解等操作。
物料的粉碎可以使用粉碎机等设备,将大颗粒物料破碎成适当大小的颗粒。
过滤则是在液-固或液-液分离过程中,通过过滤装置或过滤器,将悬浮固体分离出来。
浸提是指通过溶剂将有机物或无机物从固体物料中提取出来。
溶解是将固体物质溶解于溶剂中,形成溶液。
其次,化工单元操作的核心部分是反应操作。
反应操作主要包括原料混合、反应过程控制、反应时间等操作。
原料混合是将各种原料按照一定比例混合,形成反应物。
反应过程控制主要是控制反应的温度、压力、pH 值等参数,以确保反应得到预期的产物。
反应时间是指反应过程中所需的时间,根据反应的速度和程度可以确定。
常用的反应设备包括反应釜、搅拌器、加热装置等。
第三,化工单元操作的最后一步是分离和纯化。
分离和纯化操作主要是将反应产物中的各种组分进行分离和提纯。
分离操作包括蒸馏、萃取、结晶、过滤等。
蒸馏是将液体混合物根据其沸点差异进行分离,通过不同的升温和冷却方式实现。
萃取是通过溶剂选择性地提取目标组分,实现分离纯化。
结晶是通过溶解物质后再使其结晶,以得到纯度较高的晶体。
纯化操作是通过化学或物理方法,将产物中杂质去除,提高产物的纯度。
除了以上的基本操作,化工单元操作还需要关注安全和环保等问题。
在化工过程中,需要使用各种安全设备,确保操作人员的安全。
同时,需要严格遵守环保法规,避免对环境的污染。
综上所述,化工单元操作是化工生产过程中的核心环节之一、通过加工处理、反应操作、分离和纯化等步骤,实现了原料的加工转化和产物的提纯。
化工单元操作的复习对于提高化工生产的效率和产品质量具有重要意义。
化工单元操作技术知识点习题解答GE GROUP system office room 【GEIHUA16H-GEIHUA GEIHUA8Q8-《化工单元操作技术》知识点、习题解答一、填空题1. 粘度的物理意义是促使流体流动产生单位速度梯度的剪应力。
解答:该题目主要考核流体粘度的物理意义。
液体在流动时,在其分子间产生内摩擦的性质,称为液体的黏性,粘性的大小用黏度表示,是用来表征液体性质相关的阻力因子。
粘度的物理意义是促使流体流动产生单位速度梯度的剪应力。
2.在完全湍流区,摩擦系数λ与 Re 无关,与ε/d 有关。
在完全湍流区则λ与雷诺系数的关系线趋近于水平线。
解答:该题目主要考核对莫狄图的理解。
其中在此图中完全湍流区的特点为:摩擦系数λ与 Re 无关,与ε/d 有关,且λ与雷诺系数的关系线趋近于水平线。
3.在间壁式换热器中,间壁两边流体都变温时,两流体的流动方向有并流、逆流、错流、和折流四种。
解答:该题目主要考核间壁式换热器中两流体流动的四种方式:并流、逆流、错流、和折流。
4.某化工厂,用河水在一间壁式换热器内冷凝有机蒸汽,经过一段时间运行后,发现换热器的传热效果明显下降,分析主要原因是传热壁面上形成污垢,产生附加热阻,使K 值下降。
解答:该题目主要考核影响热量传递的因素,主要为污垢热阻的增大使得K 值下降。
5.离心泵启动前应关闭出口阀;旋涡泵启动前应打开出口阀。
解答:该题目主要考核离心泵及旋涡泵的正确开启方法。
6.离心泵通常采用出口阀门调节流量;往复泵采用旁路调节流量。
解答:该题目主要考核离心泵和往复泵常用的流量调节方法。
7.降尘室内,颗粒可被分离的必要条件是气体在室内的停留时间θ应≥颗粒的沉降时间t θ。
解答:该题目主要考核降尘室中颗粒可被分离的必要条件。
8.过滤操作有恒压过滤和恒速过滤两种典型方式。
解答:该题目主要考核过滤操作的两种方式:恒压过滤和恒速过滤。
9.精馏塔的作用是提供气液接触进行传热和传质的场所。
化工原理知识绪论1、单元操作:(Unit Operations):用来为化学反应过程创造适宜的条件或将反应物分离制成纯净品,在化工生产中共有的过程称为单元操作(12)。
单元操作特点:①所有的单元操作都是物理性操作,不改变化学性质。
②单元操作是化工生产过程中共有的操作。
③单元操作作用于不同的化工过程时,基本原理相同,所用设备也是通用的。
单元操作理论基础:(11、12)质量守恒定律:输入=输出+积存能量守恒定律:对于稳定的过,程输入=输出动量守恒定律:动量的输入=动量的输出+动量的积存2、研究方法:实验研究方法(经验法):用量纲分析和相似论为指导,依靠实验来确定过程变量之间的关系,通常用无量纲数群(或称准数)构成的关系来表达。
数学模型法(半经验半理论方法):通过分析,在抓住过程本质的前提下,对过程做出合理的简化,得出能基本反映过程机理的物理模型。
(04)3、因次分析法与数学模型法的区别:(08B)数学模型法(半经验半理论)因次论指导下的实验研究法实验:寻找函数形式,决定参数第二章:流体输送机械一、概念题1、离心泵的压头(或扬程):离心泵的压头(或扬程):泵向单位重量的液体提供的机械能。
以H 表示,单位为m 。
2、离心泵的理论压头:理论压头:离心泵的叶轮叶片无限多,液体完全沿着叶片弯曲的表面流动而无任何其他的流动,液体为粘性等于零的理想流体,泵在这种理想状态下产生的压头称为理论压头。
实际压头:离心泵的实际压头与理论压头有较大的差异,原因在于流体在通过泵的过程中存在着压头损失,它主要包括:1)叶片间的环流,2)流体的阻力损失,3)冲击损失。
3、气缚现象及其防止:气缚现象:离心泵开动时如果泵壳内和吸入管内没有充满液体,它便没有抽吸液体的能力,这是因为气体的密度比液体的密度小的多,随叶轮旋转产生的离心力不足以造成吸上液体所需要的真空度。
像这种泵壳内因为存在气体而导致吸不上液的现象称为气缚。
防止:在吸入管底部装上止逆阀,使启动前泵内充满液体。
化工单元操作复习总结-流体流动第一章:流体输送第一节流体静力学(一)流体的主要物理量密度、比容、压强(表压=绝对压强-大气压强真空度=大气压强-绝对压强)(二)流体静力学方程定义:描述静止流体内部的压力随高度变化的数学表达式第二节流体动力学(一)流量与流速1.流量:单位时间内流过管道任一截面的流体数量①体积流量:单位时间内流体流经管道任一截面的体积。
用v或vs表示,单位m/s②质量流量:单位时间内流体流经管道任一截面的质量。
用ms表示,单位kg/s体积流量和质量流量之间的关系式为:ms=v/p2.流速①平均流速:单位时间内流体质点在流动方向上所流经的距离。
用u 表示,单位m/s②质量流速:单位时间内流体流经单位管道截面的质量。
(用于气体)用w表示,单位kg/(m:s)③管道直径的估算:以d表示管道内径,由(二)定态流动和非定态流动1.定态流动:流动系统中各物理量的大小仅随位置变化、不随时间变化。
化工厂中流体的流动情况大多视为定态流动(稳定流动)2.非定态流动:若流动系统中各物理量的大小不紧随位置变化、而且随时间变化。
(三) 连续性方程:ms1=ms2、u1/u2=a1/a2= 反映的是在稳定流动中,任一截面流速的变化规律与管路安排无关。
(四)伯努利方程式及应用1:流动系统的能量:机械能、内能、功、热、损失能量①流动流体本身所具有的机械能⑴位能:流体因受重力作用而具有的能量⑵动能:流动着的流体因为有速度而具有的能量⑶静压能:静止流体内部任一位置都具有相应的静压能,流动着的流体内部任一位置上也有静压强2: 实际流体的伯努利方程式①以1kg流体为衡量基准:gz1+1/2u1+p1/p=gz2+1/2u2+p2/p(反映的是流体在流动过程中机械能的变化规律)②以1N流体为衡量基准:z1+u1/2g+p1pg+He=z2+uz/2g+p2/pg+hf 3.伯努利方程的应用步骤:①选取计算截面、②选取基准水平面、③确定各项的物理量、④列伯努利方程求解第三节流动阻力(一)流体的粘性粘度u。
常用化工单元操作基本知识一、水浴加热、蒸汽直接加热如何进行操作, 答:根据工艺要求使反应罐处于蒸馏或回流及其其他加热状态,在夹套控制阀关闭位置下: 1、水浴加热操作步骤: (1) 开“水浴排”阀门。
(2) 开“循环水进”阀门,使水体装满夹层,自“水浴排”溢出。
(3) 关“循环水进”阀门。
(4) 缓慢开启“蒸汽下进”阀门,控制蒸汽压力,使罐内温度升至工艺要求。
(5) 升温至工艺要求后,关“蒸汽下进”阀或保护适当进汽,稳定罐内温度。
(6) 水浴加热结束,关“蒸汽下进”阀和“水浴排”阀,视情况是否排空夹层。
2、蒸汽直接加热步骤: (1) 开罐底“冷凝水”阀和“旁通阀” ,排空夹套内的水。
(2) 缓慢开“蒸汽上进”阀,控制蒸汽压力?0.4Mpa。
(3) 待排水管道发烫或排出较多蒸汽时,关旁通阀,开疏水器前后阀门。
(4) 注意调节蒸汽压力,时常观察罐内情况,如有大量冒泡要马上关闭“蒸汽上进”阀,甚至停止搅拌,防止冲料。
(5) 升温将至釜内物料温度低于釜内溶剂沸点 510?时(注:此时极,易冲料) 应减小或关闭蒸汽,观察几分钟,视罐内情况供给蒸汽,使温度稳定在工艺要求范围内。
(6) 蒸汽加热结束,关“蒸汽上进”和“冷凝水”阀。
二、减压蒸馏如何操作, 答:减压蒸馏操作步骤:1、检查水、电、汽和真空系统是否正常。
2、检查反应罐、接受罐等设备是否正常,及其所有相连的阀门处于关闭位置,开启搅拌正常。
3、打开升气管蒸馏阀,接受罐进口阀。
、、、4、依次开各级冷凝器“循环水出”“循环水进”“冰盐水出”“冰盐水进”阀门,观察视盅是否有漏水现象,冷却有效。
5、开接受罐“真空”阀,按工艺要求控制真空度。
6、按工艺要求进行蒸汽直接加热或则水浴加热,正确操作,升温至工艺控制要求,进行减压蒸馏。
7、减压蒸馏过程中,要密切关注真空是否稳定,如有波动要及时调节罐内真空,防止冲料。
8、要观察接受罐液位,严禁满罐被真空抽走。
《化工单元操作技术》知识点、习题解答一、填空题1. 粘度的物理意义是促使流体流动产生单位速度梯度的剪应力。
解答:该题目主要考核流体粘度的物理意义。
液体在流动时,在其分子间产生内摩擦的性质,称为液体的黏性,粘性的大小用黏度表示,是用来表征液体性质相关的阻力因子。
粘度的物理意义是促使流体流动产生单位速度梯度的剪应力。
2.在完全湍流区,摩擦系数λ与 Re 无关,与ε/d 有关。
在完全湍流区则λ与雷诺系数的关系线趋近于水平线。
解答:该题目主要考核对莫狄图的理解。
其中在此图中完全湍流区的特点为:摩擦系数λ与 Re 无关,与ε/d 有关,且λ与雷诺系数的关系线趋近于水平线。
3.在间壁式换热器中,间壁两边流体都变温时,两流体的流动方向有并流、逆流、错流、和折流四种。
解答:该题目主要考核间壁式换热器中两流体流动的四种方式:并流、逆流、错流、和折流。
4.某化工厂,用河水在一间壁式换热器内冷凝有机蒸汽,经过一段时间运行后,发现换热器的传热效果明显下降,分析主要原因是传热壁面上形成污垢,产生附加热阻,使K 值下降。
解答:该题目主要考核影响热量传递的因素,主要为污垢热阻的增大使得K 值下降。
5.离心泵启动前应关闭出口阀;旋涡泵启动前应打开出口阀。
解答:该题目主要考核离心泵及旋涡泵的正确开启方法。
6.离心泵通常采用出口阀门调节流量;往复泵采用旁路调节流量。
解答:该题目主要考核离心泵和往复泵常用的流量调节方法。
7.降尘室内,颗粒可被分离的必要条件是气体在室内的停留时间θ应≥颗粒的沉降时间t θ。
解答:该题目主要考核降尘室中颗粒可被分离的必要条件。
8.过滤操作有恒压过滤和恒速过滤两种典型方式。
解答:该题目主要考核过滤操作的两种方式:恒压过滤和恒速过滤。
9.精馏塔的作用是提供气液接触进行传热和传质的场所。
解答:该题目主要考核精馏塔的作用:提供气液接触进行传热和传质的场所。
10.空气进入干燥器之前一般都要进行了预热,其目的是提高空气干球温度,而降低空气的相对湿度。
化工单元操作章节总结化工单元操作是化学工程中的基础课程,主要介绍了各种化工生产过程中所涉及的基本操作单元,如流体输送、传热、蒸馏、吸收、萃取、干燥等。
以下是化工单元操作的章节总结:1. 绪论:介绍化工单元操作的定义、分类、研究方法以及其在化工生产中的应用和重要性。
2. 流体输送:介绍流体输送的基本原理、流体静力学和动力学的基本概念和计算方法,以及各种流体输送设备如泵、压缩机、鼓风机等的结构、工作原理和使用特点。
3. 传热:介绍热量传递的基本原理、传热过程的基本计算方法和各种传热设备如换热器、加热炉等的结构、工作原理和使用特点。
4. 蒸发:介绍蒸发的基本原理、蒸发过程的基本计算方法和各种蒸发设备如蒸发器、结晶器的结构、工作原理和使用特点。
5. 蒸馏:介绍蒸馏的基本原理、蒸馏过程的基本计算方法和各种蒸馏设备如精馏塔、分馏塔等的结构、工作原理和使用特点。
6. 吸收:介绍吸收的基本原理、吸收过程的基本计算方法和各种吸收设备如吸收塔、解吸塔等的结构、工作原理和使用特点。
7. 萃取:介绍萃取的基本原理、萃取过程的基本计算方法和各种萃取设备如萃取塔等的结构、工作原理和使用特点。
8. 干燥:介绍干燥的基本原理、干燥过程的基本计算方法和各种干燥设备如干燥器等的结构、工作原理和使用特点。
9. 膜分离:介绍膜分离的基本原理、膜分离过程的基本计算方法和各种膜分离设备如反渗透膜等的结构、工作原理和使用特点。
10. 实验与数据处理:介绍实验设计、实验数据的采集与处理以及实验结果的分析方法,并通过实验验证化工单元操作的基本原理和计算方法。
通过以上章节的学习,学生可以掌握化工单元操作的基本原理和计算方法,了解各种化工设备的结构和工作原理,为后续的化工专业课程学习和实际工作打下基础。
离心泵,往复泵,旋涡泵的开车步骤
离心泵:先开前阀,再开泵,然后开后阀。
往复泵:先把前后阀门打开,再启动泵。
旋涡泵:先开进口阀,再开旁路阀门,然后开泵,最后开出口阀。
静力学方程
1.表压力=绝对压力-当地环境大气压力
2.真空度=当地环境大气压力-绝对压力
3.静力学方程:P
1/密度+Z
1
g=P
2
/密度+Z
2
g(适用于在重力场中静止、连续的同种
不可压缩流体)
在静止的、连续的同种液体内,处于同一水平面上各点的压力处处相等。
雷诺数
4.雷诺数Re(没有单位):Re=duρ/μ当Re<=2000时,此区为层流区,当
Re>=4000时,此区为湍流区,当2000<Re<4000时,流动可能是层流,也可能是湍流。
换热知识点
5.传热的三种基本方式:热传导、热对流和热辐射。
温度差是传热根本原因。
热传导需要介质。
热对流分为强制对流和自然对流。
6.换热器有间壁式换热器、直接接触式换热器、蓄热式换热器、中间载热体换热器
10. 测定热量方式:显热法、潜热法、焓差法
11. 对流传热膜系数越大,说明对流强度越大,对流传热热阻越小。
12. 水的沸腾曲线分为自然对流、泡核沸腾、膜状沸腾三个区域。
过滤知识点
13. 恒压过滤的特点是过滤操作的总压差恒定,随着过滤时间的延长,滤饼厚度
增大,过滤阻力增加,过滤速率降低。
测定湿度,相对湿度
利用以下知识点的工式 1.湿度 2.相对湿度 3.湿空气中的比容 4.湿空气中的比热容 5.湿空气中的焓 6.露点 7.绝热饱和温度
精馏知识点
15. 精馏就是多次蒸馏,利用挥发度和沸点不同,实现分离。
精馏塔主要包括塔体,全凝器和再沸器。
塔板是进行气液交换的场所。
精馏分为常压、加压和真空精馏三种。
16. 露点方程:表示平衡物系的温度与气相组成的关系。
泡点方程:表示平衡物系的温度与液相组成的关系。
17. t-x-y相图,根据泡点线和露点线将图像分为三个区域:液相区、气相区和气液共存区
18. t-x相图中,相平衡线离对角线越远,表示该溶液越容易分离。
19. 加料板以上为精馏段,加料板及加料板以下为提馏段。
20. 回流比是回流液量与塔顶馏出产品量的比值。
21. 塔底蒸汽气回流和塔顶液体回流是精馏操作过程连续进行的必要条件。
22. 全回流:塔顶上升蒸气经冷凝后全部流回塔内。
全回流时回流比趋向无穷大。
装置调试、操作过程异常、开车或短期停料时多采用全回流。
23. 操作线离平衡线的距离越远,完成一定的分离任务所需的理论塔板数最少,称为最少理论板数。
24. 操作线方程是精馏塔内任意板下降液相组成Xn及由其下一层板上升的蒸汽组成Yn+1之间的函数关系。
25. 对于难分离体系,相对挥发度接近1,应采用较大的回流比,以降低塔高并保证产品的浓度;对于易分离体系,相对挥发度较大,可采用较小的回流比,以减少加热蒸气消耗量,降低操作费用。
26. 五种进料状况:冷液体进料、饱和液体进料、气液混合物进料、饱和蒸气进料、过热蒸气进料
吸收与解析知识点
27. 吸收:利用混合气中各组分在某液体中的溶解度不同,气体中易溶的一个或几个组分便溶解于吸收剂,不能溶解的组分则保留在气相中,从而达到分离操作。
解吸:溶解于液体中的气体释放出来的操作
28. 低温、高压有利于吸收;高温、低压有利于解吸。