九年级化学溶液浓稀的表示
- 格式:pdf
- 大小:1.42 MB
- 文档页数:9



第2课时配制一定溶质质量分数的溶液探究点一配制一定溶质质量分数的溶液[情景展示]配制50 g质量分数为5%的氯化钠溶液。
[问题探究]配制一定溶质质量分数的溶液时,应如何操作?[思考交流]_________________________________________________________________________________________________________________________________________ [归纳提升]1.计算。
2.称量(量取):用天平称量时应“左物右码”,称量固体化学品时,两托盘应放上质量相等的称量纸,调整节天平零点准备进行称量。
若试剂具有腐蚀性,则需将试剂置于小烧杯等玻璃皿中称量。
用量筒量取液体的体积,读数时视线与液体凹液面的最低处相平。
若俯视读数,读数偏大,实际量取的液体偏少;若仰视读数,则读数偏小,实际量取的液体量偏多。
3.溶解:用玻璃棒搅拌加速溶解。
4.装入试剂瓶贴标签:将配好的溶液装入贴有试剂名称和溶质质量分数标签的试剂瓶中,盖好瓶塞,放到指定的液体试剂柜中。
[课堂速记]______________________________________________________________ ___________________________________________________________________________ 探究点二配制一定溶质质量分数的溶液的实验误差分析[情景展示]配制溶液时,用量筒量取一定量的液体,俯视读数。
[问题探究]不规范的操作会引起哪些误差呢?[思考交流]______________________________________________________________ ______________________________________________________________________________ [归纳提升]量筒读数时俯视读数,会使测量值偏大,所取液体量偏小,导致配制的溶液溶质质量分数偏大。

初中化学溶液的稀释计算及浓度的表示方法溶液的稀释是化学实验中常见的操作,它是将一定体积的浓溶液加入适量的溶剂,使其体积增大而浓度降低的过程。
溶液的浓度决定着其中溶质的含量,对于化学反应的进行和实验的准确性具有重要影响。
本文将介绍溶液的稀释计算方法和常见的浓度表示方法。
一、溶液的稀释计算方法溶液的稀释计算需要使用到稀释定律,即初始溶液的浓度与最终溶液的浓度及体积之间的关系。
稀释定律的数学表达式为:C1V1 = C2V2其中,C1为初始溶液的浓度,V1为初始溶液的体积,C2为最终溶液的浓度,V2为最终溶液的体积。
通过这个公式,我们可以推导出浓度和体积的关系:V2 = (C1V1) / C2这个公式表明,最终溶液的体积等于初始溶液的浓度乘以初始溶液的体积,再除以最终溶液的浓度。
以一个具体的例子来说明溶液的稀释计算。
例:某试剂浓度为0.2 mol/L,需制备100 mL浓度为0.05 mol/L的溶液,该如何操作?解:根据稀释定律,可以写出等式:0.2 mol/L × V1 = 0.05 mol/L × 100 mL通过变换单位,将体积V1由升转换为毫升:0.2 mol/L × V1 = 0.05 mol/L × 100 mL0.2 mol/L × V1 = 0.05 mol/L × 0.1 LV1 = (0.05 mol/L × 0.1 L) / 0.2 mol/LV1 = 0.025 L = 25 mL因此,需要取出25 mL试剂加入到适量的溶剂中,制备出100 mL 浓度为0.05 mol/L的溶液。
二、浓度的表示方法浓度表示的是单位体积内的溶质含量。
在化学实验中,常见的浓度表示方法有质量浓度、摩尔浓度和体积浓度。
1. 质量浓度(C):它表示单位体积溶液中溶质质量的多少,其数学表达式为:C = m/V其中,C为质量浓度,m为溶质的质量(单位为克),V为溶液的体积(单位为升)。



溶液浓稀的表示一.教学目标:1.知识与技能目标:(1)了解溶质、溶剂的概念。
(2)能正确区分常见溶液中的溶质和溶剂。
(3)掌握溶液、溶质、溶剂三者之间的质量关系。
(4)掌握用溶质的质量分数表示溶液组成的方法和有关计算。
(5)学会配制一定质量的溶质质量分数的溶液。
2.过程和方法目标:(1)通过课前有关资料收集、课堂表述,使学生初步学会运用归纳、概括等方法对获取的信息进行加工,并能准确表述有关信息。
(2)通过实验探究,初步认识科学探究的意义和基本过程,并进行初步的探究。
(3)通过以小组合作形式的研究性学习的探究过程,使学生能主动与他人进行交流和讨论,清楚地表达自己的观点,形成良好的学习习惯和学习方法。
(4)通过符合认知规律的教学过程,对学生进行科学方法的教育。
3.情感态度与价值观目标:(1)通过收集的资料和研究性学习的有关内容,使学生体会到溶液与生活密切相关。
(2)通过实验探究,增强学生对化学好奇心和探究欲,激发学生的学习兴趣。
(3)通过课前资料收集、小组合作研究性学习,发展学生善于合作、勤于思考、勇于创新和实践的科学精神。
二、重点、难点:1.重点:有关溶液中溶质的质量分数的计算。
2.难点:理解溶液组成的含义;溶质的质量分数的计算中涉及溶液体积的计算。
三、课前准备:1.课前将学生分成小组,分别收集有关溶液在工农业生产、医学等方面的应用等资料,每个小组推选一人在课堂上做简短汇报。
2.做好实验的准备。
3.教师做好有关投影片的制作。
四、教学过程:五.板书设计:§7-3 溶液浓稀的表示一、溶液的组成溶液质量=溶质质量+溶剂质量二、溶液组成的定量表示1.溶质质量分数的概念:2.计算公式:溶质质量溶质的质量分数=——————×100%溶液质量三、有关溶质质量分数的计算1.溶质、溶剂、溶液和溶质质量分数之间的相互换算【例题】(略)2.关于溶液稀释问题的计算原则:稀释前溶质质量=稀释后溶质质量【例1】(投影)解:设需水的质量为x.50克×98%=(x+50克)×20%x=195克答:略。

7.3溶液浓稀的表示学情分析1.本节教材从溶液的浓稀引出浓度的概念,说明日常生活中浓稀的说法不能准确的表明溶液里溶质的含量,生产中必须把溶液的浓稀水准给以数量的含义。
通过溶液的浓度的知识引导学生从定量的方面去理解溶液组成,是溶液知识的深化,也是在溶液、溶质、溶剂、溶解度等概念基础上的又一重要的化学计算,它能协助学生加深相关概念的理解,提升学生的化学计算水平,也为高中学习物质的量浓度做好坚实的基础。
2.我们的学生是农村学生,寒假在家过春节受到村子打工者的各种影响,刚从寒假回校,对学生教学要有耐心,多做思想教育工作,给他们以学习的信心。
教学目标知识与技能目标:1.明确溶液浓度的含义。
2.理解溶解度与溶质分数的区别与联系。
过程与方法目标:1.掌握溶液浓稀的一种定量表示方式——溶质的质量分数,能实行简单的溶质质量分数的计算。
2.初步学会配置一定溶质质量分数的溶液。
3.能实行关于溶质质量分数的简单计算。
情感态度价值观目标:通过溶液涵义的讲解和相关溶质质量分数的计算水平的培养,实行实事求是的科学态度的教育。
教学重点1.溶质质量分数的概念及其计算。
2.配制一定溶质质量分数的溶液。
教学难点溶解度与溶质质量分数的区别与联系。
教学课时3课时教学过程第一课时[板书]7.3溶液浓稀的表示[引言]某一溶液浓或稀到什么水准?用定量的方法表达出来,这就是通常说的“浓度”。
溶液的浓度有很多种表达方式,现在我们学习其中一种———溶质的质量分数。
[实验7-7]引导学生完成实验,比较蓝色的深浅,阅读课文,完成DEF三支试管内相关猜测的计算。
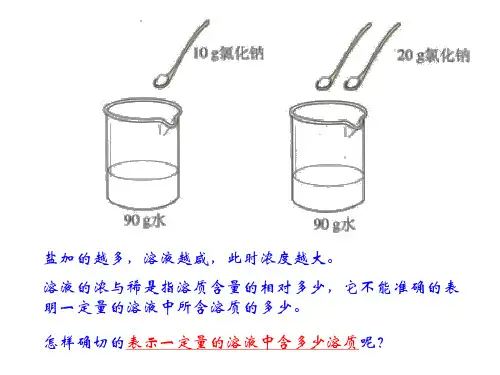
[自学]课文204-205[小组合作思考讨论]1.什么叫溶液的浓度?2.溶质质量分数是溶液浓度的一种方式,它是怎么样表示的?3.溶液的溶质质量分数有物理量单位吗?它能单独表明溶质的溶解量是多少吗?[讨 论]溶解度与溶质的质量分数有何区别?在常温下能否配制35%的氯化钠溶液?为什么?(实行小组讨论P206“讨论与交流”的两道题)[板 书]一.溶液的浓度1. 溶液浓稀水准(浓度)是指溶质质量所占溶液质量的相对多少。


溶液浓稀的表示方法有以下三种:
向原溶液中添加溶质:设原溶液质量为Ag,溶质的质量分数为a%,加溶质Bg后变成溶质质量分数为b%溶液,则Ag×a%+Bg=(Ag+Bg)×b%。
将原溶液蒸发掉部分溶剂:因为溶液蒸发溶剂前后,溶质的质量不变。
所以若设原溶液质量为Ag,溶质的质量分数为a%,蒸发Bg 水后变成溶质质量分数为b%溶液,则Ag×a%=(Ag-Bg)×b%。
与浓溶液混合:因为混合物溶液的总质量等于两混合组分溶液的质量之和。
混合后的溶液中溶质的质量等于两混合组分的溶质质量之和。
所以设原溶液质量为Ag,溶质的质量分数为a%,浓溶液的质量为Bg,溶质质量分数为b%,两溶液混合后得到溶质的质量分数为c%的溶液,则Ag×a%+Bg×b%=(Ag+Bg)×c%。
以上信息仅供参考,建议咨询专业人士获取更准确的信息。
溶质质量分数计算中的十字交叉法在浓溶液里加入水将它稀释为稀溶液,称为溶液的稀释。
在浓溶液里加入含有相同溶质的稀溶液,称为溶液的混合。
在溶液稀释与溶液混合的过程中,溶液中溶质的质量分数变了,但稀释前浓溶液里所含溶质的质量与稀释后稀溶液里所含溶质的质量相等;混合溶液中溶质的质量等于浓溶液中溶质质量与稀溶液中溶质质量之和。
抓住这一点,就抓住了这类计算的关键。
其实溶液的稀释也可以看作是溶液的混合,即把水看作是溶质质量分数为0%的稀溶液。
这样就可以合并成为一个问题来讨论了。
有关溶液混合的计算公式是:m(浓)×c%(浓)+m(稀)×c%(稀)= m(混)×c%(混),由于m(混)=m(浓)+m(稀),上式也可以写成:m(浓)×c%(浓)+m(稀)×c%(稀)= [m(浓)+m(稀)]×c%(混)此式经整理可得:m(浓)×[c%(浓)-c%(混)]=m(稀)×[c%(混)-c%(稀)]这个计算式也可以写成十字交叉图式,即利用这个十字交叉图式,可以比较简单地进行有关溶液混合的计算。
若进行溶液的稀释时把c(稀)视为水,把c(稀)中溶质的质量分数视为0%即可。
用十字交叉法解题过程可分为以下4步:(l)设出要求的未知数。
(2)把有关数据对号入座。
浓溶液的质量写在c(浓)的左方,稀溶液的质量写在c(稀)的左方,将c(浓)-c(混)、c(混)-c(稀)所得的差写在各自的右方,并用虚线画上方框。
(3)取四角虚线方框内的数值列成比例式。
(4)解比例式。
例如:将52%的KOH溶液与42%的KOH溶液以怎样的质量比混合,才能得到50%的KOH溶液?【解】设需52%的KO H的质量为x,需42%的KOH的质量为y【答】52%的KOH溶液与42%的KOH溶液的质量比为4∶l。